文档内容
课时检测(七十三) 定量分析型综合实验
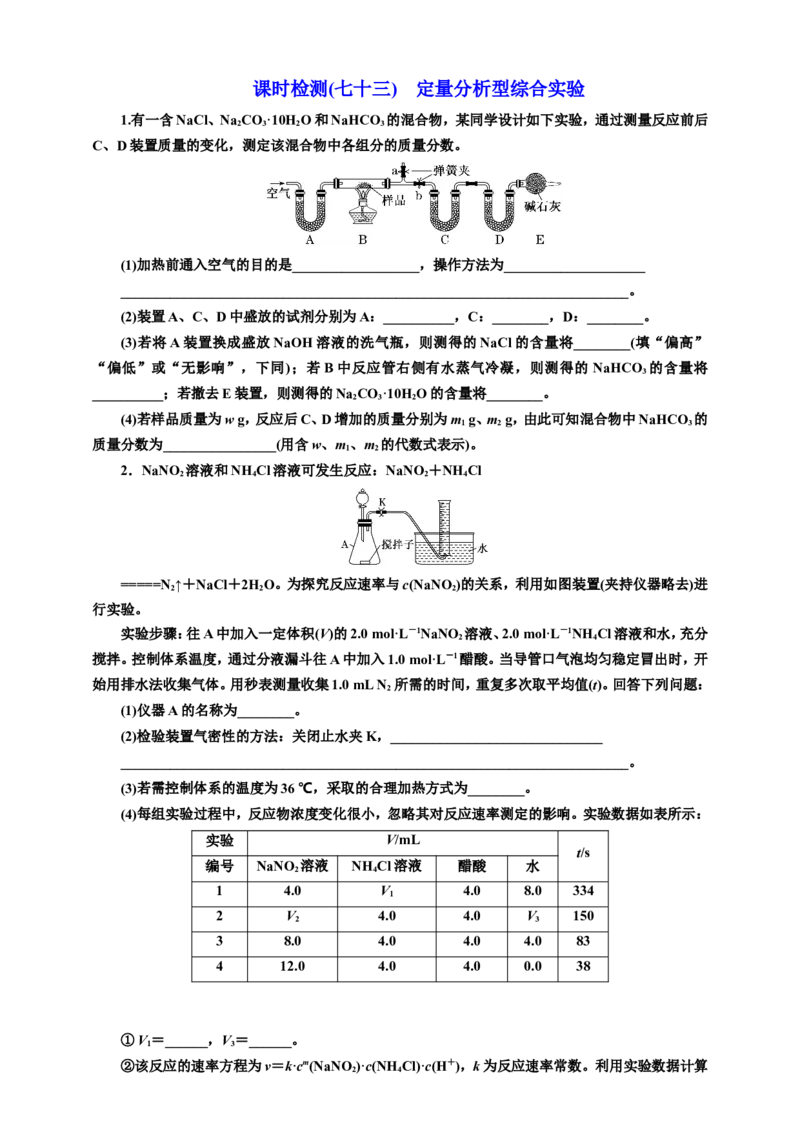
1.有一含NaCl、Na CO ·10HO和NaHCO 的混合物,某同学设计如下实验,通过测量反应前后
2 3 2 3
C、D装置质量的变化,测定该混合物中各组分的质量分数。
(1)加热前通入空气的目的是__________________,操作方法为____________________
________________________________________________________________________。
(2)装置A、C、D中盛放的试剂分别为A:__________,C:________,D:________。
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将________(填“偏高”
“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测得的 NaHCO 的含量将
3
__________;若撤去E装置,则测得的Na CO ·10HO的含量将________。
2 3 2
(4)若样品质量为w g,反应后C、D增加的质量分别为m g、m g,由此可知混合物中NaHCO 的
1 2 3
质量分数为________________(用含w、m、m 的代数式表示)。
1 2
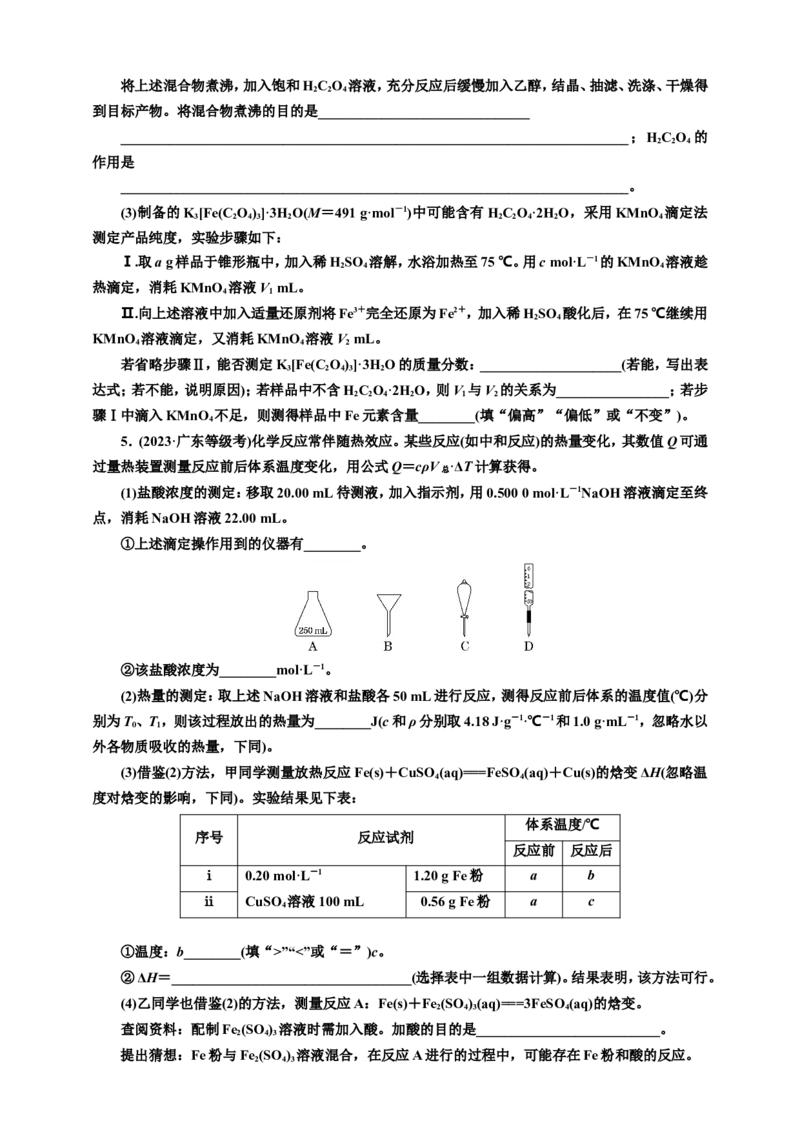
2.NaNO 溶液和NH Cl溶液可发生反应:NaNO +NH Cl
2 4 2 4
=====N↑+NaCl+2HO。为探究反应速率与c(NaNO )的关系,利用如图装置(夹持仪器略去)进
2 2 2
行实验。
实验步骤:往A中加入一定体积(V)的2.0 mol·L-1NaNO 溶液、2.0 mol·L-1NH Cl溶液和水,充分
2 4
搅拌。控制体系温度,通过分液漏斗往A中加入1.0 mol·L-1醋酸。当导管口气泡均匀稳定冒出时,开
始用排水法收集气体。用秒表测量收集1.0 mL N 所需的时间,重复多次取平均值(t)。回答下列问题:
2
(1)仪器A的名称为________。
(2)检验装置气密性的方法:关闭止水夹K,______________________________
________________________________________________________________________。
(3)若需控制体系的温度为36 ℃,采取的合理加热方式为________。
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如表所示:
实验 V/mL
t/s
编号 NaNO 溶液 NH Cl溶液 醋酸 水
2 4
1 4.0 V 4.0 8.0 334
1
2 V 4.0 4.0 V 150
2 3
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
①V =______,V =______。
1 3
②该反应的速率方程为v=k·cm(NaNO )·c(NHCl)·c(H+),k为反应速率常数。利用实验数据计算
2 4得m=_______(填整数)。
③醋酸的作用是_________________________________________________。
3.(2023·重庆等级考)煤的化学活性是评价煤气化或燃烧性能的一项重要指标,可用与焦炭(由煤
样制得)反应的CO 的转化率α来表示。研究小组设计测定α的实验装置如下:
2
(1)装置Ⅰ中,仪器a的名称是______________;b中除去的物质是________(填化学式)。
(2)①将煤样隔绝空气在900 ℃加热1小时得焦炭,该过程称为________________。
②装置Ⅱ中,高温下发生反应的化学方程式为______________________。
(3)装置Ⅲ中,先通入适量的气体X,再通入足量Ar气。若气体X被完全吸收,则可依据d和e中
分别生成的固体质量计算α。
①d中的现象是______________________________________________________。
②e中生成的固体为Ag,发生反应的化学方程式为__________________________。
③d和e的连接顺序颠倒后将造成α__________(填“偏大”“偏小”或“不变”)。
(4)在工业上按照国家标准规定α:将干燥后的CO (含杂质N 的体积分数为n)以一定流量通入装
2 2
置Ⅱ反应,用奥氏气体分析仪测出反应后某时段气体中 CO 的体积分数为m,此时α的表达式为
2
__________________________。
4.K[Fe(C O)]·3H O(三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同
3 2 4 3 2
学利用如图装置制备FeC O·2HO,然后再制备三草酸合铁酸钾。
2 4 2
回答下列问题:
(1)打开K、K 和K,关闭K,制备FeSO。为使生成的FeSO 溶液与HCO 溶液接触,应进行的
1 3 4 2 4 4 2 2 4
操作为_________________________________________________,
B中生成FeC O·2HO沉淀的离子方程式为______________________________________
2 4 2
________________________________________________________________________。
(2)向 FeC O·2HO 中加入过量饱和 KCO 溶液,水浴加热并缓慢滴加 HO 溶液,制得
2 4 2 2 2 4 2 2
K[Fe(C O)],同时有红褐色沉淀生成,该反应的化学方程式为_________________;
3 2 4 3将上述混合物煮沸,加入饱和HCO 溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得
2 2 4
到目标产物。将混合物煮沸的目的是______________________________
________________________________________________________________________;HCO 的
2 2 4
作用是
________________________________________________________________________。
(3)制备的K[Fe(C O)]·3H O(M=491 g·mol-1)中可能含有HCO·2HO,采用KMnO 滴定法
3 2 4 3 2 2 2 4 2 4
测定产品纯度,实验步骤如下:
Ⅰ.取a g样品于锥形瓶中,加入稀HSO 溶解,水浴加热至75 ℃。用c mol·L-1的KMnO 溶液趁
2 4 4
热滴定,消耗KMnO 溶液V mL。
4 1
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀HSO 酸化后,在75 ℃继续用
2 4
KMnO 溶液滴定,又消耗KMnO 溶液V mL。
4 4 2
若省略步骤Ⅱ,能否测定K[Fe(C O)]·3H O的质量分数:____________________(若能,写出表
3 2 4 3 2
达式;若不能,说明原因);若样品中不含HCO·2HO,则V 与V 的关系为________________;若步
2 2 4 2 1 2
骤Ⅰ中滴入KMnO 不足,则测得样品中Fe元素含量________(填“偏高”“偏低”或“不变”)。
4
5.(2023·广东等级考)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通
过量热装置测量反应前后体系温度变化,用公式Q=cρV ·ΔT计算获得。
总
(1)盐酸浓度的测定:移取20.00 mL待测液,加入指示剂,用0.500 0 mol·L-1NaOH溶液滴定至终
点,消耗NaOH溶液22.00 mL。
①上述滴定操作用到的仪器有________。
②该盐酸浓度为________mol·L-1。
(2)热量的测定:取上述NaOH溶液和盐酸各50 mL 进行反应,测得反应前后体系的温度值(℃)分
别为T、T,则该过程放出的热量为________J(c和ρ分别取4.18 J·g-1·℃-1和1.0 g·mL-1,忽略水以
0 1
外各物质吸收的热量,下同)。
(3)借鉴(2)方法,甲同学测量放热反应Fe(s)+CuSO (aq)===FeSO (aq)+Cu(s)的焓变ΔH(忽略温
4 4
度对焓变的影响,下同)。实验结果见下表:
体系温度/℃
序号 反应试剂
反应前 反应后
ⅰ 0.20 mol·L-1 1.20 g Fe粉 a b
ⅱ CuSO 溶液100 mL 0.56 g Fe粉 a c
4
①温度:b________(填“>”“<”或“=”)c。
②ΔH=__________________________________(选择表中一组数据计算)。结果表明,该方法可行。
(4)乙同学也借鉴(2)的方法,测量反应A:Fe(s)+Fe(SO )(aq)===3FeSO (aq)的焓变。
2 4 3 4
查阅资料:配制Fe(SO ) 溶液时需加入酸。加酸的目的是__________________________。
2 4 3
提出猜想:Fe粉与Fe(SO ) 溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
2 4 3验证猜想:用pH试纸测得Fe(SO ) 溶液的pH不大于1;向少量Fe(SO ) 溶液中加入Fe粉,溶
2 4 3 2 4 3
液颜色变浅的同时有气泡冒出,说明存在反应A和___________________(用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实
验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为
_______________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)化学能可转化为热能,写出其在生产或生活中的一种应用:_______________。
课时检测(七十三)
1.解析:(2)A、C、D都是U形管,不能盛液体试剂,只能盛固体试剂。A处试剂必须能同时吸收
CO 和水蒸气,故A处盛的是碱石灰;C、D两处分别吸收水蒸气和CO ,故C处可盛无水CaCl 或
2 2 2
PO ,D处可盛碱石灰。(3)若A装置盛放NaOH溶液,则A装置只吸收CO ,不吸收水蒸气,
2 5 2
Na CO ·10HO和Na CO 的总质量在计算中会增大,因此测得的NaCl的含量将偏低。若B中反应管
2 3 2 2 3
右侧有水蒸气冷凝,则水蒸气总质量减小,Na CO ·10HO和NaHCO 的总质量在计算中会减小,但是
2 3 2 3
NaHCO 的质量是根据CO 的质量进行计算的,所以测得的NaHCO 的含量不受影响。若撤去E装置,
3 2 3
则 D 装置可吸收来自外界空气中的 CO 与水,NaHCO 的质量在计算中会增大,因此测得的
2 3
Na CO ·10HO的含量会偏低。(4)NaHCO 的质量分数为×100%=%。
2 3 2 3
答案:(1)除去装置中的水蒸气和二氧化碳 关闭b,打开a,缓缓通入空气,直至a处出来的空气
不再使澄清石灰水变浑浊为止
(2)碱石灰 无水CaCl 或PO 碱石灰
2 2 5
(3)偏低 无影响 偏低 (4)%
2.解析:(4)①为探究反应速率与c(NaNO )的关系,NH Cl浓度不变,根据实验3和4可知溶液总
2 4
体积为20.0 mL,故V =4.0;根据变量单一可知V =6.0,V =6.0。②浓度增大速率加快,根据1和3组
1 2 3
数据分析,3的c(NaNO )是1的2倍,1和3所用的时间比≈4,根据分析可知速率和浓度的平方成正
2
比,故m=2。③醋酸在反应前后体积未发生改变,作催化剂,作用是加快反应速率。
答案:(1)锥形瓶 (2)通过分液漏斗往A中加水,一段时间后水难以滴入,则气密性良好
(3)水浴加热 (4)①4.0 6.0 ②2 ③加快反应速率
3.解析:(1)装置Ⅰ中,稀盐酸与碳酸钙反应生成二氧化碳、氯化钙和水,由于盐酸易挥发,故制得
的二氧化碳中含有氯化氢气体,碳酸氢钠能与氯化氢反应,故b中除去的物质是HCl。(2)①将煤隔绝
空气加强热使之分解的过程称为煤的干馏。②装置Ⅱ中,高温下CO 和焦炭反应生成CO:C+
2
CO =====2CO。(3)①气体X中含有CO和CO ,则d中CO 和氢氧化钡反应生成碳酸钡沉淀和水,反
2 2 2
应的现象是有白色沉淀生成。②e中生成的固体为Ag,根据氧化还原反应规律分析知CO转变成碳酸
铵,发生反应的化学方程式为CO+2[Ag(NH )]OH===(NH )CO +2Ag↓+2NH 。③CO 是酸性气体,
3 2 4 2 3 3 2能和银氨溶液反应,从而使碳酸钡的生成量减少,计算得到的与焦炭反应的CO 的量增大,则测得的α
2
偏大。(4)设起始通入x mol气体,则CO 为(1-n)x mol,N 为xn mol,
2 2
CO (g)+C(s)=====2CO(g)
2
起始/mol (1-n)x 0
转化/mol (1-n)αx 2(1-n)αx
某时段/mol (1-n)(1-α)x 2(1-n)αx
由某时段气体中CO 的体积分数为m,有m=,解得α=×100%。
2
答案:(1)分液漏斗 HCl (2)①煤的干馏 ② C+CO =====2CO (3)①有白色沉淀生成
2
②CO+2[Ag(NH )]OH===(NH)CO +2Ag↓+2NH ③偏大 (4)×100%
3 2 4 2 3 3
4.解析:(1)铁和稀硫酸反应生成氢气,装置A内压强增大,关闭K,打开K、K,利用压强差将
3 1 2
FeSO 溶液压至装置B中与HCO 溶液反应生成FeC O·2HO沉淀,离子方程式为Fe2++HCO+
4 2 2 4 2 4 2 2 2 4
2HO===FeCO·2HO↓+2H+。(2)FeC O·2HO与KCO 和HO 反应生成K[Fe(C O)]和红褐色
2 2 4 2 2 4 2 2 2 4 2 2 3 2 4 3
沉淀 Fe(OH) ,该反应的化学方程式为 6FeC O·2HO+3HO +6KCO===4K [Fe(C O)]+
3 2 4 2 2 2 2 2 4 3 2 4 3
2Fe(OH) ↓+12HO;HCO 具有还原性,HO 具有氧化性,先将混合物煮沸,目的是除去过量的
3 2 2 2 4 2 2
HO ,防止与饱和HCO 溶液发生反应;加入饱和HCO 溶液发生反应 2Fe(OH) +3HCO +
2 2 2 2 4 2 2 4 3 2 2 4
3KCO===2K [Fe(C O)] + 6HO , 故 HCO 的 作 用 是 将 红 褐 色 沉 淀 Fe(OH) 转 化 为
2 2 4 3 2 4 3 2 2 2 4 3
K[Fe(C O)],提高产率。(3)步骤Ⅰ中加入KMnO 溶液与K[Fe(C O)]·3H O和HCO·2HO发生
3 2 4 3 4 3 2 4 3 2 2 2 4 2
氧化还原反应生成Mn2+和CO ,根据得失电子守恒可得关系式:5CO~2MnO,n(C O)=n(MnO),设
2 2 2
a g 样 品 中 K[Fe(C O)]·3H O 为 x mol , HCO·2HO 为 y mol , 则 491x + 126y = a ,
3 2 4 3 2 2 2 4 2
K[Fe(C O)]·3H O和HCO·2HO中CO的总物质的量为3x+y=×cV ×10-3,联立两个方程式解
3 2 4 3 2 2 2 4 2 2 1
得x=,所以K[Fe(C O)]·3H O的质量分数为×100%,则省略步骤Ⅱ,也能测定其质量分数。
3 2 4 3 2
K[Fe(C O)]中Fe为+3价,加入适量还原剂将Fe3+完全还原为Fe2+,再用KMnO 溶液滴定,反应的
3 2 4 3 4
离子方程式为5Fe2++MnO+8H+===5Fe3++Mn2++4HO,则n(Fe2+)=5n(KMnO )=5cV ×10-3
2 4 2
mol,若样品中不含HCO·2HO,步骤Ⅰ中由Fe元素守恒可得 n(Fe2+)=n{K [Fe(C O)]·3H O}=
2 2 4 2 3 2 4 3 2
××cV ×10-3 mol=×cV ×10-3mol,所以5cV ×10-3 mol=×cV ×10-3 mol,得出V 与V 的关系为V =
1 1 2 1 1 2 1
6V 。若步骤Ⅰ中滴入KMnO 不足,计算HCO·2HO质量偏小,导致 K[Fe(C O)]·3H O质量偏大,
2 4 2 2 4 2 3 2 4 3 2
则测得样品中Fe元素含量偏高。
答案:(1)关闭K,打开K、K
3 1 2
Fe2++HCO+2HO===FeCO·2HO↓+2H+
2 2 4 2 2 4 2
(2)6FeC O·2HO+3HO +6KCO===4K [Fe(C O)]+2Fe(OH) ↓+12HO 除去过量的
2 4 2 2 2 2 2 4 3 2 4 3 3 2
HO ,防止与饱和HCO 溶液发生反应 将红褐色沉淀Fe(OH) 转化为K[Fe(C O)],提高产率
2 2 2 2 4 3 3 2 4 3
(3)×100% V =6V 偏高
1 2
5.解析:(1)①滴定操作时需要用的仪器有锥形瓶、酸式滴定管、碱式滴定管、铁架台等,故选A、
D。②滴定时发生反应HCl+NaOH===NaCl+HO,故c(HCl)===0.550 0 mol·L-1。(2)由Q=cρV
2 总
·ΔT可得Q=4.18 J·g-1·℃-1×1.0 g·mL-1×(50 mL+50 mL)×(T-T)=418(T-T)。(3)①100 mL 0.20
1 0 1 0
mol·L-1CuSO 溶液含有溶质的物质的量为0.02 mol,1.20 g Fe粉和0.56 g Fe粉的物质的量分别为
4
0.021 mol、0.01 mol,实验ⅰ中有0.02 mol CuSO 发生反应,实验ⅱ中有0.01 mol CuSO 发生反应,实
4 4
验ⅰ放出的热量多,则b>c。②若按实验ⅰ进行计算,ΔH=-=-20.9(b-a)kJ·mol-1;若按实验ⅱ进
行计算,ΔH=-=-41.8(c-a)kJ·mol-1。(4)Fe3+易水解,为防止Fe3+水解,在配制Fe(SO ) 溶液时需
2 4 3加入酸;用pH试纸测得Fe(SO ) 溶液的pH不大于1,说明溶液呈强酸性,向少量Fe(SO ) 溶液中加
2 4 3 2 4 3
入Fe粉,溶液颜色变浅的同时有气泡即氢气产生,说明溶液中还存在Fe与酸的反应,其离子方程式
为Fe+2H+===Fe2++H↑;乙同学根据相关原理,重新设计优化的实验方案的重点为如何防止Fe与
2
酸反应产生影响,可以借助盖斯定律,设计分步反应来实现Fe(SO ) 溶液与Fe的反应,故可将一定量
2 4 3
的Cu粉加入一定浓度的Fe(SO ) 溶液中反应,测量反应热,计算得到反应Cu+Fe(SO )===CuSO
2 4 3 2 4 3 4
+2FeSO 的焓变ΔH;根据(3)中实验计算得到反应Fe+CuSO ===Cu+FeSO 的焓变ΔH;根据盖斯
4 1 4 4 2
定律计算得到反应Fe+Fe(SO )===3FeSO 的焓变为ΔH+ΔH。(5)化学能转化为热能在生产、生活
2 4 3 4 1 2
中应用比较广泛,化石燃料的燃烧、炸药开山、发射火箭等都是化学能转化为热能的应用,另外铝热反
应焊接铁轨也是化学能转化为热能的应用。
答案:(1)①AD ②0.550 0 (2)418(T-T) (3)①>
1 0
②-20.9(b-a)kJ·mol-1[或-41.8(c-a)kJ·mol-1]
(4)抑制Fe3+水解 Fe+2H+===Fe2++H↑ 将一定量的Cu粉加入一定浓度的Fe(SO ) 溶液中
2 2 4 3
反应,测量反应热,计算得到反应Cu+Fe(SO )===CuSO +2FeSO 的焓变ΔH;根据(3)中实验计算
2 4 3 4 4 1
得到反应 Fe+CuSO ===Cu+FeSO 的焓变 ΔH ;根据盖斯定律计算得到反应 Fe+
4 4 2
Fe(SO )===3FeSO 的焓变为ΔH+ΔH (5)化石燃料的燃烧(或铝热反应焊接铁轨等)
2 4 3 4 1 2