文档内容
课时检测(十七) 常见的金属材料的基本知能评价
1.(2024年1月·九省联考广西卷)下列广西优秀传统工艺品中,主要由合金材料制成的是( )
A.壮乡铜鼓 B.绣球 C.坭兴陶 D.壮锦
2.《天工开物》中记载:“若造熟铁,则生铁流出时,相连数尺内,低下数寸,筑一方塘,短墙抵之。
其铁流入塘内,数人执持柳木棍排立墙上……众人柳棍疾搅,即时炒成熟铁。”以下说法不正确的是(
)
A.金属冶炼方法由金属活动性决定
B.熟铁比生铁质地更硬,延展性稍差
C.炒铁是为了降低铁水中的碳含量
D.该法与近代往生铁水中吹空气炼钢异曲同工
3.金属的冶炼与生产、生活及国防军事等领域均密切相关。下列有关金属冶炼的原理错误的是(
)
A.用电解法制取金属钠:2NaCl(熔融)=====2Na+Cl ↑
2
B.用Na、Mg等活泼金属为还原剂冶炼Ti:
2Mg+TiCl(熔融)=====Ti+2MgCl
4 2
C.用Al作还原剂冶炼金属V:
3VO+10Al=====6V+5Al O
2 5 2 3
D.用H 作还原剂冶炼金属Ag:
2
Ag O+H=====2Ag+HO
2 2 2
4.西汉东方朔所撰的《申异经·中荒经》:“西北有宫,黄铜为墙,题曰地皇之宫”。文中“黄铜”
主要成分是铜锌,含少量锡、铅等。下列说法错误的是( )
A.铜锈的主要成分为Cu(OH) ,俗称铜绿
2
B.相关金属元素还原性由强到弱的顺序为Zn>Sn>Pb>Cu
C.黄铜制作的高洪太铜锣应保存在干燥处
D.用灼烧法可区别“黄铜”和黄金首饰
5.软锰矿主要成分是MnO ,还含有少量的CaO、MgO、CuO等杂质。用软锰矿生产MnSO 晶体
2 4
的部分工艺流程如图所示。下列说法错误的是(已知:MnF 不溶于水)( )
2
A.可用NaOH溶液检验浸出液中的Fe2+
B.CaCO 的作用是调节溶液pH
3
C.BaS可除去Cu2+
D.“深度除杂”中加入MnF 除去Mg2+和Ca2+
26.氧化亚铜(Cu O)主要用于船底防污。已知CuO经高温灼烧生成Cu O,Cu O与H+发生反应:
2 2 2
Cu O+2H+===Cu+Cu2++HO。现将经高温灼烧后的CuO样品投入足量稀硫酸中得到混合溶液,
2 2
下列有关说法不正确的是( )
A.稳定性:Cu O>CuO
2
B.样品与酸的反应中,Cu O既是氧化剂又是还原剂
2
C.如果溶液中出现蓝色,说明CuO已分解
D.若有14.4 g CuO参加反应,则转移电子数为0.1N
2 A
7.(2023·湖北等级考)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题。
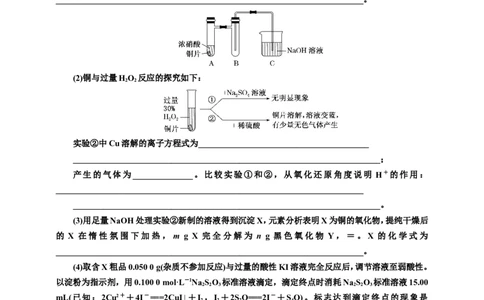
(1)铜与浓硝酸反应的装置如图,仪器 A 的名称为____________,装置 B 的作用为
________________________________________________________________________。
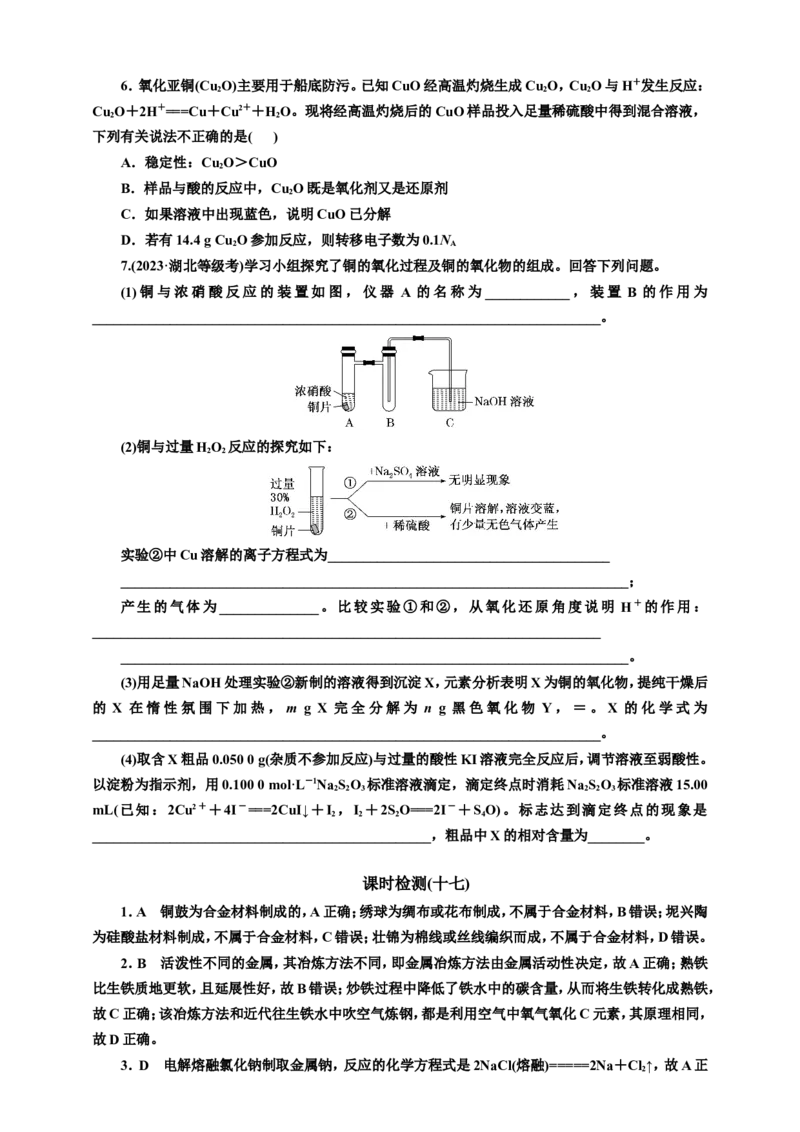
(2)铜与过量HO 反应的探究如下:
2 2
实验②中Cu溶解的离子方程式为________________________________________
________________________________________________________________________;
产生的气体为______________。比较实验①和②,从氧化还原角度说明 H+的作用:
________________________________________________________________________
________________________________________________________________________。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后
的 X 在惰性氛围下加热,m g X 完全分解为 n g 黑色氧化物 Y,=。X 的化学式为
________________________________________________________________________。
(4)取含X粗品0.050 0 g(杂质不参加反应)与过量的酸性KI溶液完全反应后,调节溶液至弱酸性。
以淀粉为指示剂,用0.100 0 mol·L-1Na SO 标准溶液滴定,滴定终点时消耗Na SO 标准溶液15.00
2 2 3 2 2 3
mL(已知:2Cu2++4I-===2CuI↓+I ,I +2SO===2I-+SO)。标志达到滴定终点的现象是
2 2 2 4
________________________________________________,粗品中X的相对含量为________。
课时检测(十七)
1.A 铜鼓为合金材料制成的,A正确;绣球为绸布或花布制成,不属于合金材料,B错误;坭兴陶
为硅酸盐材料制成,不属于合金材料,C错误;壮锦为棉线或丝线编织而成,不属于合金材料,D错误。
2.B 活泼性不同的金属,其冶炼方法不同,即金属冶炼方法由金属活动性决定,故A正确;熟铁
比生铁质地更软,且延展性好,故B错误;炒铁过程中降低了铁水中的碳含量,从而将生铁转化成熟铁,
故C正确;该冶炼方法和近代往生铁水中吹空气炼钢,都是利用空气中氧气氧化C元素,其原理相同,
故D正确。
3.D 电解熔融氯化钠制取金属钠,反应的化学方程式是2NaCl(熔融)=====2Na+Cl ↑,故A正
2确;Na、Mg的活泼性大于Ti,可用Na、Mg等活泼金属为还原剂冶炼Ti,反应的化学方程式是2Mg+
TiCl(熔融)=====Ti+2MgCl ,故B正确;铝的还原性大于钒,用Al作还原剂可以冶炼金属V,反应的
4 2
化学方程式是3VO+10Al=====6V+5Al O,故C正确;银是不活泼金属,一般采用加热Ag O的方
2 5 2 3 2
法冶炼Ag,故D错误。
4.A 潮湿的环境中,Cu和CO 、HO、O 反应生成Cu (OH) CO 而产生铜锈,故A错误;根据金
2 2 2 2 2 3
属活动性顺序表可知,金属活动性:Zn>Sn>Pb>Cu,故B正确;潮湿的环境中,Cu和CO 、HO、O 反
2 2 2
应生成Cu (OH) CO 而产生铜锈,所以用黄铜制作的高洪太铜锣应置于干燥处保存,故C正确;Cu在
2 2 3
加热的条件下和氧气反应生成黑色的CuO,Au在加热条件下和氧气不反应,所以可以采用灼烧的方
法区分黄铜和黄金首饰,故D正确。
5.A 第一步加稀HSO 会使CuO和Fe溶解生成Cu2+、Fe2+,加NaOH溶液,铜离子产生蓝色
2 4
沉淀,亚铁离子产生白色沉淀后变为红褐色,颜色变化不能反映Fe2+是否存在,A项错误;由题图中加
CaCO 沉铁可知此时为调节pH使铁离子转为沉淀,B项正确;加BaS除重金属,溶液中只有Cu2+是
3
重金属离子,故加入BaS可除去Cu2+,C项正确;经前面一系列除杂后剩下的Ca2+和Mg2+为杂质离
子,且CaF 和MgF 均为难溶物,故为不引入新杂质可用MnF 除杂,同时MnF 也为难溶物,不会引
2 2 2 2
入新杂质,D项正确。
6.C CuO经高温灼烧生成Cu O,说明稳定性:Cu O>CuO,故A正确;反应Cu O+2H+===Cu+
2 2 2
Cu2++HO中,部分Cu元素的化合价从+1价升高到+2价,部分降低到0价,则Cu O既是氧化剂
2 2
又是还原剂,故B正确;如果溶液中出现蓝色,不能说明CuO已分解,因为CuO与稀硫酸反应后的溶
液也呈蓝色,故C错误;反应Cu O+2H+===Cu+Cu2++HO中,1 mol 氧化亚铜完全反应转移1 mol
2 2
电子,14.4 g CuO物质的量为=0.1 mol,0.1 mol 氧化亚铜完全反应转移0.1 mol 电子,转移电子数为
2
0.1N ,故D正确。
A
7.解析:(1)仪器A的名称为具支试管;Cu与浓硝酸反应产生的尾气直接用NaOH溶液吸收会引
发溶液倒吸,装置B起到安全瓶的作用,防止倒吸。(2)Cu在稀硫酸作用下,被HO 氧化生成Cu2+和
2 2
HO,溶液变蓝;在Cu2+作用下,HO 会被催化分解生成O。在Na SO 溶液中HO 不能氧化Cu,在
2 2 2 2 2 4 2 2
稀硫酸中HO 能氧化Cu,说明H+使得HO 的氧化性增强。(3)X为铜的氧化物,设X的化学式为
2 2 2 2
CuO ,其在惰性氛围下分解生成的黑色氧化物为CuO:CuO =====CuO+O↑,则=,又=,解得x=
x x 2
2,则X的化学式为CuO 。(4)CuO 在酸性条件下生成Cu2+,Cu2+与KI反应生成I,I 遇淀粉变蓝,用
2 2 2 2
Na SO 标准溶液滴定I,当滴入最后半滴Na SO 标准溶液时,溶液的蓝色褪去,且半分钟内不恢复,
2 2 3 2 2 2 3
表明I 已完全反应,达到滴定终点。CuO 中Cu为+2价、O为-1价,结合已知反应可知,CuO 在酸
2 2 2
性条件下与 KI 发生反应 2CuO +8I-+8H+===2CuI↓+3I +4HO,有关系式:2CuO ~3I ~
2 2 2 2 2
6Na SO,则样品中n(CuO )=n(Na SO),m(CuO )=×96 g=0.048 g,w(CuO )=×100%=96%。
2 2 3 2 2 2 3 2 2
答案:(1)具支试管 安全瓶(或防倒吸) (2)Cu+HO+2H+===Cu2++2HO O 增强HO
2 2 2 2 2 2
的氧化性 (3)CuO
2
(4)当滴入最后半滴Na SO 标准溶液时,溶液蓝色刚好褪去,且半分钟内不恢复 96%
2 2 3