文档内容
镁、铝及其化合物作业题
作业题目难度分为3档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目1-11,14-17,21-23题为三星,12-13,18,24-28为四星,
19-20,29-30为五星
1.铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途.下列关于铝
的说法正确的是( ) ☆☆☆
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.常温下不与任何酸、碱反应
C.铝元素在地壳中的含量高,储量丰富,仅次于铁
D.工业上通常用钠与铝盐溶液反应来制备铝
【解答】
A.铝的表面容易被氧化生成氧化铝,为致密的氧化膜结构,所以抗腐蚀性能好,
故A正确;
B.常温下Al与盐酸、NaOH均反应生成盐和氢气,故B错误;
C.Al为地壳中含量最多的金属元素,则含量高,储量丰富,故 C错误;
D.Al为活泼金属,工业上可以用电解法冶炼铝,即用电解熔融的氧化铝制备Al,
而不是用钠与铝盐溶液反应来制备铝,与氯化铝反应首先是钠与水反应,故 D
错误;
故选A.
2.下列关于铝的性质和用途描述正确的是( ) ☆☆☆
A.铝能与所有的酸和碱反应放出氢气
第1页(共19页)B.用酒精灯外焰加热铝箔,可以看到少量液滴悬而不落,说明铝的熔点比氧化
铝高
C.铝合金质轻,强度大,耐腐蚀,可以用作门窗
D.氢氧化铝能溶于氨水
【解答】
A.铝与酸或强碱溶液反应生成氢气,而与氨水不发生反应,故 A错误;
B.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,
又因三氧化二铝的熔点高于铝的熔点,而三氧化二铝在铝的表面,所以加热铝箔
的时候铝熔化了但是不会滴落,故B错误;
C.铝常温下能与空气中氧气反应,生成一层致密的氧化物保护膜,从而具有抗
腐蚀性,铝合金材料的密度小,用以减轻列车质量,铝合金强度大,所以可用作
门窗,故C正确;
D.氢氧化铝溶于强碱,不溶于弱碱,所以氢氧化铝不能溶于氨水,故 D错误;
故选C.
3.1989年世界卫生组织把铝确定为食品污染源之一,而加以控制使用.铝在下
列应用时应加以控制的是( ) ☆☆☆
①制铝合金 ②制电线 ③制炊具 ④银色漆颜料 ⑤明矾净水
⑥明矾与苏打制食品膨松剂 ⑦易拉罐
⑧用Al(OH) 凝胶制胃舒平药片 ⑨包装糖果和小食品.
3
A.③⑤⑧⑨ B.③⑤⑥⑦⑧⑨ C.③⑤⑨ D.⑥⑧⑨
【解答】
③制炊具⑤明矾净水⑥明矾与苏打制食品膨松剂⑦易拉罐⑧用Al(OH) 凝胶制
3
胃舒平药片⑨包装糖果和小食品,都有可能进入人体,对人体造成危害,都需要
加以控制。
故选B.
第2页(共19页)4.关于铝及其化合物的下列说法不正确的是( ) ☆☆☆
A.Al(OH) 可以用来做胃酸中和剂
3
B.铝与任何酸、碱都能反应放出氢气
C.不宜用铝制品来蒸煮酸性或碱性食物
D.AlO 可以用来制造耐火坩埚、耐火管等实验仪器
2 3
【解答】
A.Al(OH) 可与盐酸反应,胃酸中含盐酸,则 Al(OH) 可以用来做胃酸中和
3 3
剂,故A正确;
B.铝排在H的前边,与酸反应放出氢气,但是只能和强碱反应放出氢气,故 B
错误;
C.Al与酸碱均反应,在盐溶液中可发生电化学腐蚀,则不能用铝制品来蒸煮酸
性、碱性或咸的食物,故C正确;
D.AlO 的熔点较高,则AlO 可以用来制造耐火坩埚、耐火管等实验仪器,故D
2 3 2 3
正确;
故选B.
5.有关Al与NaOH溶液的反应的说法中,正确的是( ) ☆☆☆
A.铝是还原剂,其氧化产物是 Al(OH)
3
B.NaOH是氧化剂,其还原产物是H
2
C.铝是还原剂,HO和NaOH都是氧化剂
2
D.HO是氧化剂,Al被氧化
2
【解答】
A、铝和氢氧化钠溶液反应方程式为:2Al+2HO+2NaOH=2NaAlO+3H↑,实质是金
2 2 2
属铝和水先反应生成氢氧化铝和氢气,再是氢氧化铝和氢氧化钠之间反应生成偏
铝酸钠,铝元素的化合价从 0价升高到+3价,金属铝是还原剂,水是氧化剂,
对应产物NaAlO 是氧化产物,故 A错误;
2
B、氢元素的化合价降低,HO是氧化剂,氢气是还原产物,故B错误;
2
第3页(共19页)C、铝是还原剂,HO是氧化剂,故C错误;
2
D、HO是氧化剂,铝元素的化合价从0价升高到+3价,Al被氧化,故D正确.
2
故选D.
6.欲除去铁粉中的少量铝粉,应选用的试剂是( ) ☆☆☆
A.稀盐酸 B.稀硝酸 C.氨水 D.氢氧化钠溶液
【解答】
铝粉与强碱溶液反应生成溶于水的偏铝酸钠,反应的离子方程式为 2Al+2OH﹣
+2HO=2AlO﹣+3H↑,所以可加入NaOH溶液除去铁粉中的铝粉,盐酸、硝酸和铁
2 2 2
与铝都反应,而氨水与两者都不反应,
故选D.
7.将两粒相同大小的钠,一粒用铝箔包好为甲,另一粒为乙,将甲、乙两粒钠
分别投入足量的水中,收集所得气体,气体的体积大小关系是( ) ☆☆☆
A.乙多 B.甲多 C.一样多 D.无法确定
【解答】
由2Na+2HO═2NaOH+H↑可知,Na相同,则Na与水反应生成的氢气相同,但甲
2 2
中发生2Al+2NaOH+2HO═2NaAlO+3H↑,则甲生成的氢气多,体积大.
2 2 2
故选B.
8.在天平的左右两个托盘上放有两个烧杯,两个烧杯中分别盛有盐酸和氢氧化
钠溶液,天平处于平衡状态,当分别向两烧杯中加入等质量的铝(酸和碱都是足
量的)充分反应后( ) ☆☆☆
A.天平保持平衡 B.左高右低 C.左低右高 D.无法确定
【解答】
第4页(共19页)由2Al+6HCl═2AlCl+3H↑、2Al+2NaOH+2HO═2NaAlO+3H↑可知,酸碱足量,
3 2 2 2 2
生成气体相同,由铝的质量相同,盐酸和氢氧化钠溶液的质量也相同,则反应前
后的质量变化也相同,所以天平仍然保持平衡。
故选:A.
9.在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡.然后将两球
分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如下图所示.下
列说法正确的是( ) ☆☆☆
A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡
B.铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,
溶液蓝色变浅,杠杆右边下沉
C.反应后去掉两烧杯,杠杆仍平衡
D.右边球上出现红色,左边溶液的碱性增强
【解答】
A.左烧杯中发生2Al+2NaOH+2HO=2NaAlO+3H↑,不生成沉淀,故A错误;
2 2 2
B.左烧杯中发生2Al+2NaOH+2HO=2NaAlO+3H↑,右烧杯中发生
2 2 2
Fe+CuSO=Cu+FeSO,观察到铝球表面有气泡产生,溶液澄清,而铁球表面有红色
4 4
物质析出,溶液蓝色变浅,由反应可知左烧杯中Al的质量变小,右烧杯中Fe
球上生成Cu质量变大,杠杆右边下沉,故B正确;
C.由选项B的分析可知,反应后去掉两烧杯,杠杆不能平衡,故 C错误;
D.右边球上生成Cu,则出现红色,而左边溶液中消耗NaOH,则c(OH﹣)减小,
碱性减弱,故D错误;
故选B.
10.实验室中,要使明矾溶液中的Al3+全部沉淀出来,适宜用的试剂是( )
☆☆☆
A.NaOH溶液 B.氨水 C.盐酸 D.Ba(OH) 溶液
2
第5页(共19页)【解答】
Al3+转化为不溶于水的物质是Al(OH),Al(OH) 具有两性,既能和强酸反应
3 3
又能和强碱反应,要使AlCl 溶液中的Al3+完全沉淀,选取试剂时就不能选强碱,
3
只能是弱碱,
A、NaOH溶液是强碱能溶解氢氧化铝沉淀,故A不选;
B、氨水是弱碱,加入过量的氨水能把铝离子完全沉淀,故 B选;
C、盐酸是酸,与Al3+不反应,故C不选;
D、Ba(OH) 溶液是强碱,能溶解氢氧化铝沉淀,故D不选;
2
故选B.
11.将一块镁铝合金溶于盐酸后,再加入过量NaOH溶液,所得的溶液中主要存
在的离子是( ) ☆☆☆
A.AlO﹣、OH﹣、Na+、Cl﹣ B.Na+、OH﹣、Al3+、Cl﹣
2
C.AlO﹣、OH﹣、Mg2+、Cl﹣ D.Na+、Mg2+、Al3+、Cl﹣
2
【解答】
将一块镁铝合金溶于盐酸后,生成氯化镁、氯化铝,再加入过量 NaOH溶液,反
应生成氯化钠、偏铝酸钠、氢氧化镁沉淀,溶液中还有剩余的 NaOH,所得的溶
液中主要存在的离子有:AlO﹣、OH﹣、Na+、Cl﹣
2
故选A.
12.将0.1mol Al投入3mol/L NaOH溶液100mL中,充分反应后再滴加1mol/L
硫酸溶液120mL,最终结果是( ) ☆☆☆☆
A.得到混浊液体 B.得到澄清透明溶液
C.溶液中无NaAlO D.溶液pH=7
2
【解答】
100mL3mol/L的NaOH溶液中n(NaOH)=c×V=3mol/L×0.1L=0.3mol,120mL1mol/L
的HSO 溶液,n(HSO)=c×V=1mol/L×0.12L=0.12mol,0.1mol铝投入100mL
2 4 2 4
第6页(共19页)3mol/L的NaOH溶液中充分反应,发生2Al+2NaOH+2HO=2NaAlO+3H↑,0.1mol
2 2 2
铝消耗0.1mol的NaOH,生成0.1molNaAlO ,有0.2molNaOH剩余,再滴入0.12mol
2
HSO 溶液,发生反应2NaOH+HSO=NaSO+2HO,消耗0.1molHSO,剩余0.02mol
2 4 2 4 2 4 2 2 4
HSO,即0.04molH+,氢离子和偏铝酸根离子先后发生AlO﹣+H++HO=Al(OH)↓,
2 4 2 2 3
H+消耗完全,生成0.04mol Al(OH) 沉淀,由于H+量不足,最终只有沉淀,沉
3
淀不溶解.
A.最终生成0.04mol氢氧化铝沉淀和0.06mol NaAlO 溶液,得到浑浊液体,故
2
A正确;
B.最终生成0.04mol氢氧化铝沉淀,故B错误;
C.最终生成0.04mol氢氧化铝沉淀和0.06mol NaAlO 溶液,故C错误;
2
D.最终生成0.04mol氢氧化铝沉淀和0.06mol NaAlO 溶液,偏氯酸钠为强碱弱
2
酸盐,溶液显碱性,故D错误;
故选A.
13.将4g铝铁合金粉末溶于足量盐酸中,加入过量氢氧化钠溶液,过滤后向滤
液中通入足量二氧化碳,再将沉淀滤出,经洗涤、干燥、灼烧后得到固体粉末的
质量仍为4g,原合金中铁的质量分数最接近( ) ☆☆☆☆
A.30% B.47% C.53% D.70%
【解答】
由铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液,过滤后向滤液中通入足
量二氧化碳,沉淀为氢氧化铝,则经洗涤、干燥、灼烧,得到的固体粉末是氧化
铝,利用组成可知氧化铝中氧元素的质量等于合金中铁的质量,
合金中铁的质量等于氧化铝中氧元素的质量,则合金中铁的质量分数等于氧化铝
中氧的质量分数= =47%,
故选B.
14.质量相同的两份铝粉,第一份中加入足量的NaOH溶液,第二份中加入足量
的盐酸,在同温同压下放出气体的体积比是( ) ☆☆☆
第7页(共19页)A.1:2 B.2:1 C.1:4 D.1:1
【解答】
铝与盐酸反应的方程式为2Al+6HCl=2AlCl+3H↑,
3 2
与烧碱溶液反应的方程式为 2Al+2NaOH+2HO=2NaAlO+3H↑,
2 2 2
由方程式可以看出,反应关系式都为2Al~3H,
2
因酸、碱均足量,则质量相同的 Al,同温同压下放出相同体积的气体,
即同温同压下放出气体的体积比是1:1,
故选D.
15.将足量的两份铝,分别加入到等物质的量的盐酸和氢氧化钠溶液中,放出气
体的物质的量之比为( ) ☆☆☆
A.3:2 B.2:3 C.1:1 D.1:3
【解答】
由2Al+6HCl═2AlCl+3H↑、2Al+2NaOH+2HO═2NaAlO+3H↑,可知,参加反应
3 2 2 2 2
的铝与酸碱与生成的氢气的物质的量关系为:2Al~6HCl~3H,2Al~2NaOH~3H,
2 2
根据n=cv,则盐酸和氢氧化钠溶液物质的量之比为1:1,体积和物质的量浓度
都相等的盐酸和氢氧化钠溶液中投入足量的铝粉,放出的氢气物质的量之比是 :
=1:3
故选D.
16.铝分别与足量的稀硫酸和氢氧化钠溶液反应,当两个反应放出的气体在相同
状况体积相等时,反应中消耗的 HSO 和NaOH物质的量之比为( ) ☆☆☆
2 4
A.1:4 B.2:3 C.3:2 D.4:1
【解答】
令生成的氢气的物质的量为 3mol,则:
2Al+3HSO=Al(SO)+3H↑
2 4 2 4 3 2
第8页(共19页)3mol 3mol
2Al+2NaOH+2HO=2NaAlO+3H↑
2 2 2
2mol 3mol
稀硫酸和氢氧化钠溶液的物质的量浓度相等,所以所取稀硫酸和氢氧化钠溶液的
体积比等于溶质HSO、NaOH的物质的量的之比,即为3mol:2mol=3:2.
2 4
故选C.
17.两份铝屑,一份与过量HCl反应,另一份与过量NaOH溶液反应,产生的H
2
体积比为1:2,则两份铝屑的质量比为( ) ☆☆☆
A.1:1 B.1:2 C.1:3 D.2:1
【解答】
铝屑与过量HCl反应,铝与过量NaOH溶液反应,两份铝产生的H 体积比为1:2,
2
所以两份铝产生H 的物质的量比为 1:2.
2
根据电子转移守恒,所以两份铝提供的电子的物质的量之比为 1:2,
所以两份铝的物质的量之比为 1:2
故选:B.
18.等体积等物质的量浓度的硫酸,氢氧化钠溶液分别放在甲、乙两烧杯中,各
加等质量的铝,生成氢气的体积比为4:5,则甲、乙两烧杯中的反应情况可能
分别是( ) ☆☆☆☆
A.甲、乙中都是铝过量 B.甲中铝过量,乙中碱过量
C.甲中酸过量,乙中铝过量 D.甲中酸过量,乙中碱过量
【解答】
发生反应有:2Al+3HSO═Al(SO)+3H↑、2Al+2NaOH+2HO=2NaAlO+3H↑,
2 4 2 4 3 2 2 2 2
①若等质量的铝都反应完,生成气体为1:1,
②若铝均没有反应完,根据酸和碱的物质的量相等,可得生成气体为 2:3,
第9页(共19页)而题中为4:5,因此所以一个是铝反应完全,一个是铝过量,由于等量的铝消
耗的硫酸的量更多,所以完全反应的一定是硫酸,碱过量,
即甲中铝过量,乙中碱过量。
故选B.
19.甲、乙两烧杯中各盛有200mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中
分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则
加入的铝粉质量为( ) ☆☆☆☆☆
A.10.8g B.7.2g C.2.7g D.1.8g
【解答】
根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,应结束后测得
生成的气体体积比为甲:乙=1:2,由化学反应方程式可知,酸与金属反应时酸
不过量,碱与金属反应时碱过量来计算解答.
盐酸和氢氧化钠溶液中溶质的物质的量均为0.2L×3mol/L=0.6mol,
又两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙
=1:2,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为 x,
则 2Al+6HCl═2AlCl+3H↑
3 2
6 3
0.6mol x
,解得x=0.3mol,
一定条件下,气体的物质的量之比等于体积之比,
则碱与金属铝反应生成的氢气的物质的量为0.3mol×2=0.6mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为 y,
则 2Al+2NaOH+2HO═2NaAlO+3H↑
2 2 2
2 3
y 0.6mol
,解得y=0.4mol,
第10页(共19页)则铝的质量为0.4mol×27g/mol=10.8g,
故选:A.
20.将5.1g镁铝合金,投入500mL 2.0mol•L﹣1盐酸中,金属完全溶解,再加入
4.0mol•L﹣1的NaOH溶液,若要生成的沉淀最多,则加入NaOH溶液的体积是( )
☆☆☆☆☆
A.200mL B.425mL C.250mL D.560mL
【解答】
镁铝合金与盐酸反应,金属完全溶解,发生的反应为:Mg+2HCl=MgCl+H↑、
2 2
2Al+6HCl=2AlCl+3H↑,氯化镁和氯化铝,分别与NaOH溶液反应的方程式为
3 2
AlCl+3NaOH=Al(OH)↓+3NaCl、MgCl +2NaOH=Mg(OH)↓+2NaCl,
3 3 2 2
Mg2+和Al3+全部转化为沉淀,所以溶液中的溶质只有NaCl,
根据氯原子和钠原子守恒可知,n(HCl)=n(NaCl)=n(NaOH)=0.5L×2mol/L=1mol,
则加入NaOH溶液的体积是 =0.25L=250mL。
故选C.
21.向MgSO 和Al(SO) 的混合溶液中,逐滴加入NaOH溶液.下列图象中,
4 2 4 3
能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应
生成沉淀的质量)( ) ☆☆☆
A. B.
C. D.
第11页(共19页)【解答】
因横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量,则向
MgSO 和Al(SO) 的混合溶液中,逐滴加入NaOH溶液,
4 2 4 3
发生Mg2++2OH﹣═Mg(OH)↓、Al3++3OH﹣═Al(OH)↓,则沉淀的质量一直在增
2 3
大,直到最大;然后发生Al(OH)+OH﹣═AlO﹣+2HO,沉淀的质量减少,但氢氧
3 2 2
化镁不与碱反应,则最后沉淀的质量为一定值,显然只有 D符合。
故选D.
22.在MgCl、AlCl 的混合溶液中加入足量的氨水,下列选项各图中能正确表示
2 3
加入氨水的量(x)与生成沉淀的量(y)的关系的是( ) ☆☆☆
A. B. C. D.
【解答】
MgCl 和AlCl 混合溶液中足量的氨水,发生AlCl+3NH•HO=Al(OH)↓+3NHCl、
2 3 3 3 2 3 4
MgCl+2NH•HO=Mg(OH)↓+2NHCl,生成Mg(OH) 和Al(OH) 沉淀,沉淀达
2 3 2 2 4 2 3
最大值,继续足量的氨水,Mg(OH) 和Al(OH) 沉淀都不与氨水反应,沉淀量
2 3
不变,故图象D符合。
故答案为:D.
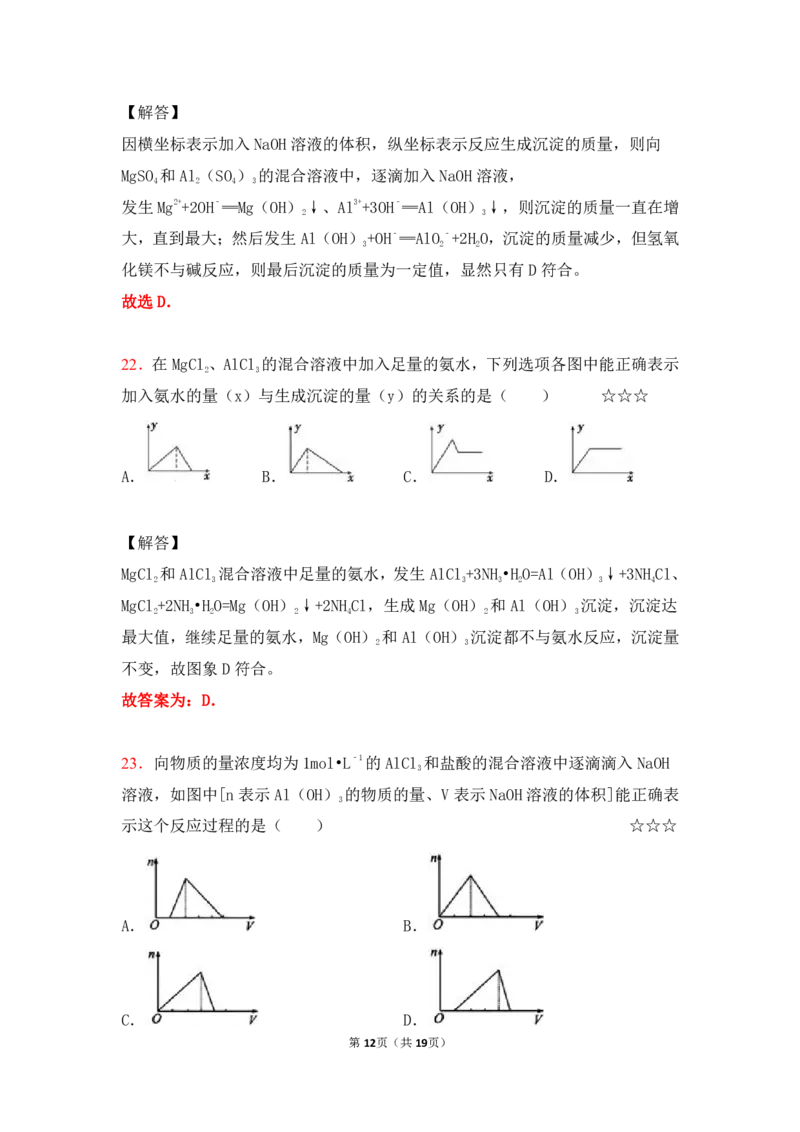
23.向物质的量浓度均为1mol•L﹣1的AlCl 和盐酸的混合溶液中逐滴滴入NaOH
3
溶液,如图中[n表示Al(OH) 的物质的量、V表示NaOH溶液的体积]能正确表
3
示这个反应过程的是( ) ☆☆☆
A. B.
C. D.
第12页(共19页)【解答】
向AlCl 和HCl的混合溶液中滴入 NaOH溶液时,盐酸先和氢氧化钠发生反应:
3
NaOH+HCl=NaCl+HO,没有沉淀生成,再发生3NaOH+AlCl=Al(OH)↓+3NaCl,
2 3 3
最后发生Al(OH)+NaOH=NaAlO+2HO,沉淀溶解,由方程式可以看出产生沉淀
3 2 2
消耗的氢氧化钠是溶解沉淀消耗氢氧化钠的3倍.所以图象应该为D;
故选D.
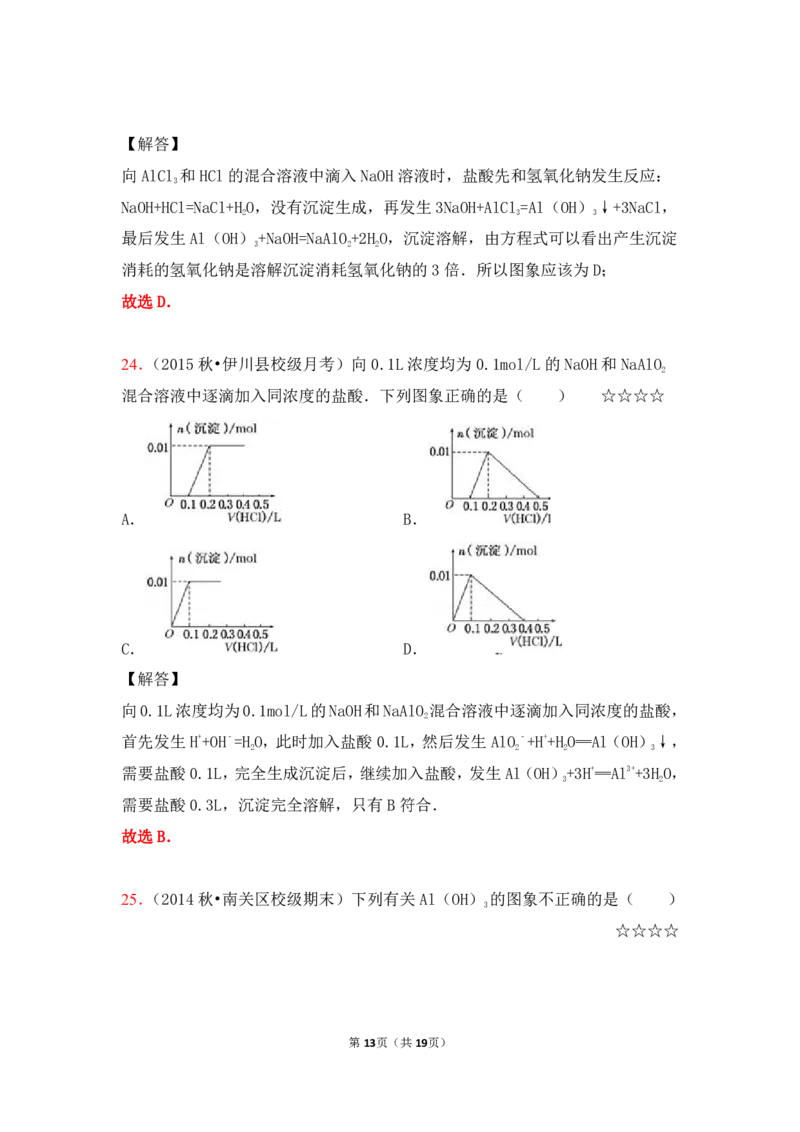
24.(2015秋•伊川县校级月考)向0.1L浓度均为0.1mol/L的NaOH和NaAlO
2
混合溶液中逐滴加入同浓度的盐酸.下列图象正确的是( ) ☆☆☆☆
A. B.
C. D.
【解答】
向0.1L浓度均为0.1mol/L的NaOH和NaAlO 混合溶液中逐滴加入同浓度的盐酸,
2
首先发生H++OH﹣=HO,此时加入盐酸0.1L,然后发生AlO﹣+H++HO═Al(OH)↓,
2 2 2 3
需要盐酸0.1L,完全生成沉淀后,继续加入盐酸,发生Al(OH)+3H+═Al3++3HO,
3 2
需要盐酸0.3L,沉淀完全溶解,只有B符合.
故选B.
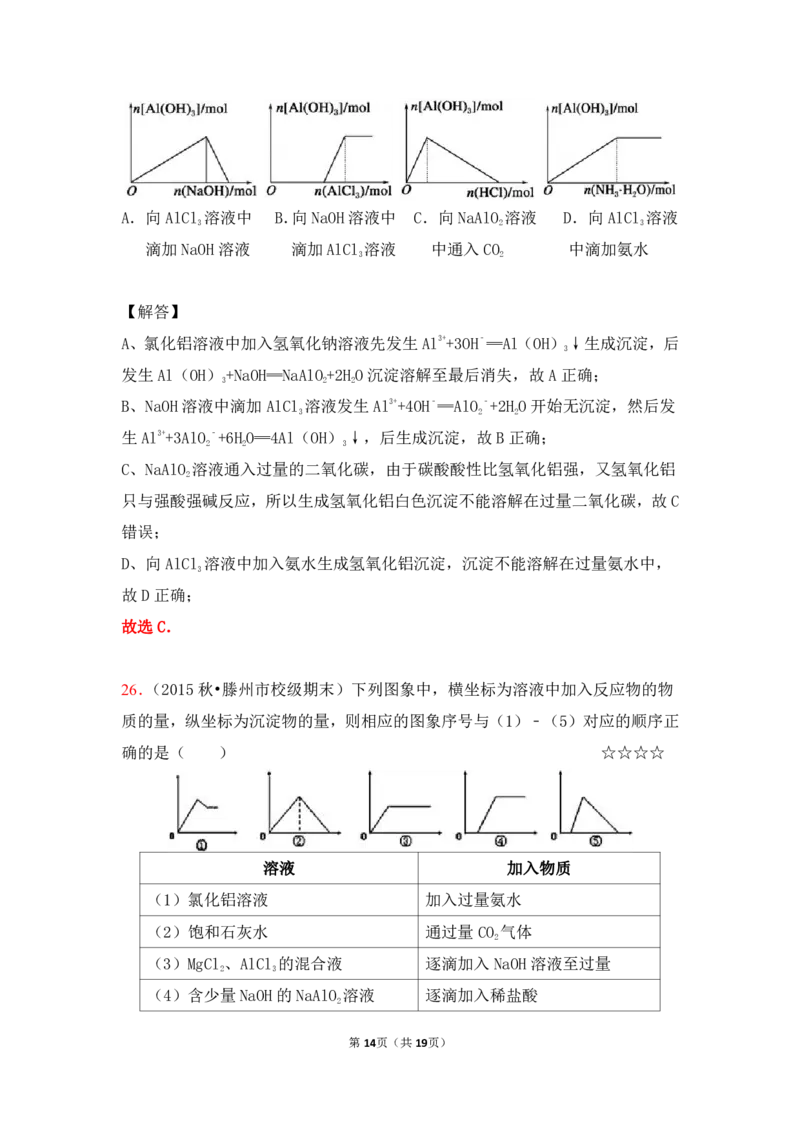
25.(2014秋•南关区校级期末)下列有关Al(OH) 的图象不正确的是( )
3
☆☆☆☆
第13页(共19页)A.向AlCl 溶液中 B.向NaOH溶液中 C.向NaAlO 溶液 D.向AlCl 溶液
3 2 3
滴加NaOH溶液 滴加AlCl 溶液 中通入CO 中滴加氨水
3 2
【解答】
A、氯化铝溶液中加入氢氧化钠溶液先发生Al3++3OH﹣═Al(OH)↓生成沉淀,后
3
发生Al(OH)+NaOH═NaAlO+2HO沉淀溶解至最后消失,故A正确;
3 2 2
B、NaOH溶液中滴加AlCl 溶液发生 Al3++4OH﹣═AlO﹣+2HO开始无沉淀,然后发
3 2 2
生Al3++3AlO﹣+6HO═4Al(OH)↓,后生成沉淀,故B正确;
2 2 3
C、NaAlO 溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,又氢氧化铝
2
只与强酸强碱反应,所以生成氢氧化铝白色沉淀不能溶解在过量二氧化碳,故C
错误;
D、向AlCl 溶液中加入氨水生成氢氧化铝沉淀,沉淀不能溶解在过量氨水中,
3
故D正确;
故选C.
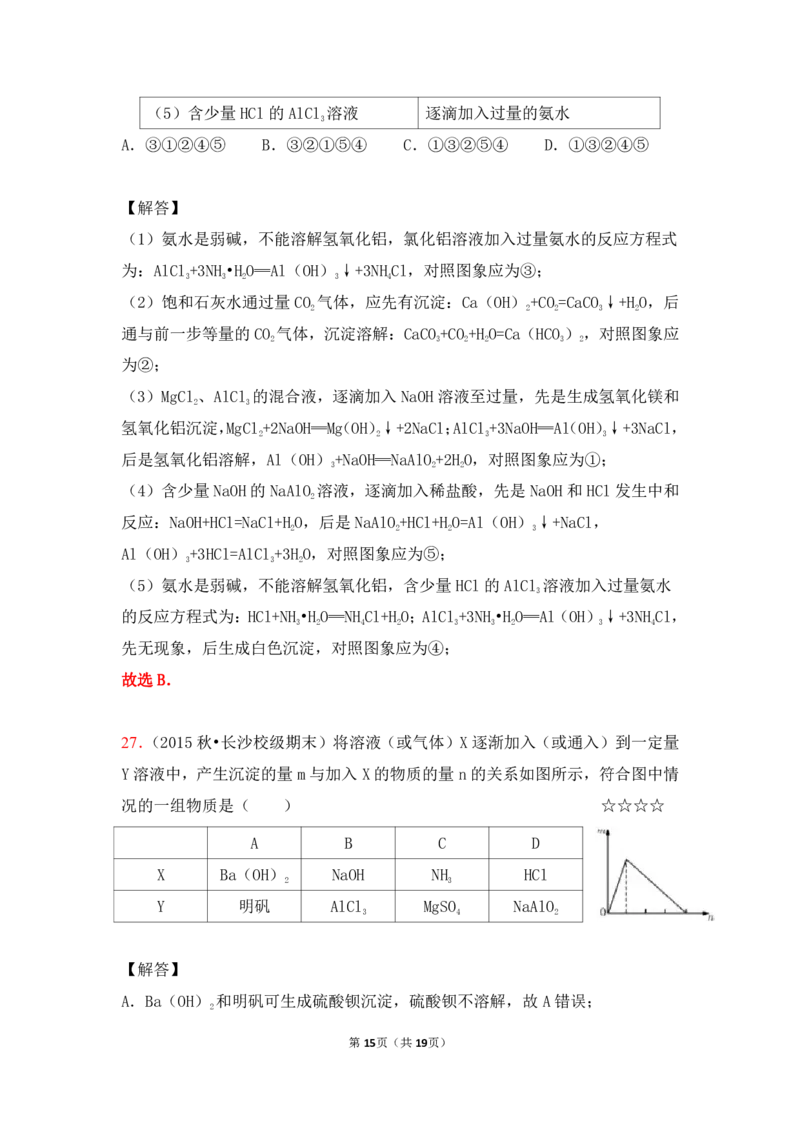
26.(2015秋•滕州市校级期末)下列图象中,横坐标为溶液中加入反应物的物
质的量,纵坐标为沉淀物的量,则相应的图象序号与(1)﹣(5)对应的顺序正
确的是( ) ☆☆☆☆
溶液 加入物质
(1)氯化铝溶液 加入过量氨水
(2)饱和石灰水 通过量CO 气体
2
(3)MgCl、AlCl 的混合液 逐滴加入NaOH溶液至过量
2 3
(4)含少量NaOH的NaAlO 溶液 逐滴加入稀盐酸
2
第14页(共19页)(5)含少量HCl的AlCl 溶液 逐滴加入过量的氨水
3
A.③①②④⑤ B.③②①⑤④ C.①③②⑤④ D.①③②④⑤
【解答】
(1)氨水是弱碱,不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式
为:AlCl+3NH•HO═Al(OH)↓+3NHCl,对照图象应为③;
3 3 2 3 4
(2)饱和石灰水通过量CO 气体,应先有沉淀:Ca(OH)+CO=CaCO↓+HO,后
2 2 2 3 2
通与前一步等量的CO 气体,沉淀溶解:CaCO+CO+HO=Ca(HCO),对照图象应
2 3 2 2 3 2
为②;
(3)MgCl、AlCl 的混合液,逐滴加入NaOH溶液至过量,先是生成氢氧化镁和
2 3
氢氧化铝沉淀,MgCl+2NaOH═Mg(OH)↓+2NaCl;AlCl+3NaOH═Al(OH)↓+3NaCl,
2 2 3 3
后是氢氧化铝溶解,Al(OH)+NaOH═NaAlO+2HO,对照图象应为①;
3 2 2
(4)含少量NaOH的NaAlO 溶液,逐滴加入稀盐酸,先是NaOH和HCl发生中和
2
反应:NaOH+HCl=NaCl+HO,后是NaAlO+HCl+HO=Al(OH)↓+NaCl,
2 2 2 3
Al(OH)+3HCl=AlCl+3HO,对照图象应为⑤;
3 3 2
(5)氨水是弱碱,不能溶解氢氧化铝,含少量HCl的AlCl 溶液加入过量氨水
3
的反应方程式为:HCl+NH•HO═NHCl+HO;AlCl+3NH•HO═Al(OH)↓+3NHCl,
3 2 4 2 3 3 2 3 4
先无现象,后生成白色沉淀,对照图象应为④;
故选B.
27.(2015 秋•长沙校级期末)将溶液(或气体)X逐渐加入(或通入)到一定量
Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情
况的一组物质是( ) ☆☆☆☆
A B C D
X Ba(OH) NaOH NH HCl
2 3
Y 明矾 AlCl MgSO NaAlO
3 4 2
【解答】
A.Ba(OH) 和明矾可生成硫酸钡沉淀,硫酸钡不溶解,故 A错误;
2
第15页(共19页)B.将氢氧化钠酸逐渐加入氯化铝溶液中,先产生沉淀,后沉淀溶解,所用氢氧
化钠溶液体积为3:1,故B错误;
C.硫酸镁和氨水反应生成氢氧化镁沉淀,氢氧化镁不溶解,故 C错误;
D.将稀盐酸逐渐加入偏铝酸钠溶液中,先发生反应:
NaAlO+HCl+HO=Al(OH)↓+NaCl,Al(OH)+3HCl=AlCl+3HO,先产生沉淀,
2 2 3 3 3 2
后沉淀溶解,所用稀盐酸溶液体积为1:3,故D正确.
故选D.
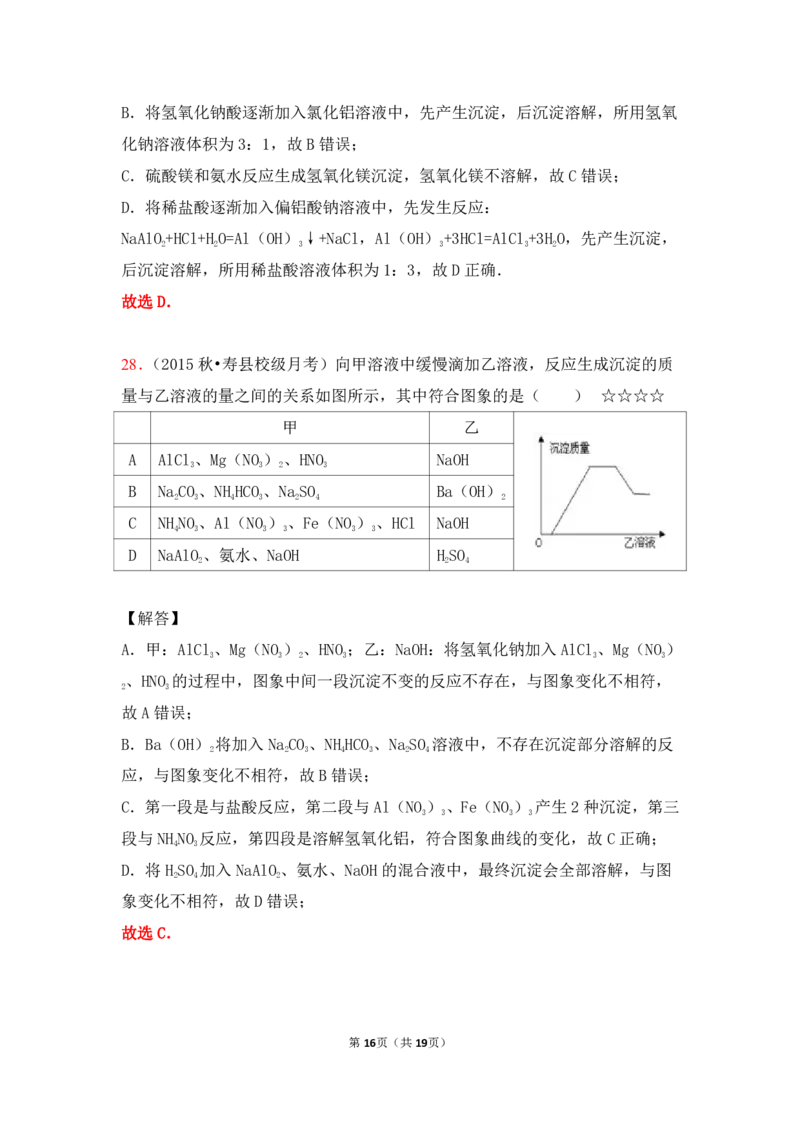
28.(2015秋•寿县校级月考)向甲溶液中缓慢滴加乙溶液,反应生成沉淀的质
量与乙溶液的量之间的关系如图所示,其中符合图象的是( ) ☆☆☆☆
甲 乙
A AlCl、Mg(NO)、HNO NaOH
3 3 2 3
B NaCO、NHHCO、NaSO Ba(OH)
2 3 4 3 2 4 2
C NHNO、Al(NO)、Fe(NO)、HCl NaOH
4 3 3 3 3 3
D NaAlO、氨水、NaOH HSO
2 2 4
【解答】
A.甲:AlCl、Mg(NO)、HNO;乙:NaOH:将氢氧化钠加入AlCl、Mg(NO)
3 3 2 3 3 3
、HNO 的过程中,图象中间一段沉淀不变的反应不存在,与图象变化不相符,
2 3
故A错误;
B.Ba(OH) 将加入NaCO、NH HCO、NaSO 溶液中,不存在沉淀部分溶解的反
2 2 3 4 3 2 4
应,与图象变化不相符,故 B错误;
C.第一段是与盐酸反应,第二段与Al(NO)、Fe(NO) 产生2种沉淀,第三
3 3 3 3
段与NHNO 反应,第四段是溶解氢氧化铝,符合图象曲线的变化,故 C正确;
4 3
D.将HSO 加入NaAlO、氨水、NaOH的混合液中,最终沉淀会全部溶解,与图
2 4 2
象变化不相符,故D错误;
故选C.
第16页(共19页)29.甲、乙两烧杯中各盛有l00ml 3mol•L﹣1的盐酸和氢氧化钠溶液.向烧杯中
分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为
1:2 ☆☆☆☆☆
(1)加入铝粉的质量是 g.
(2)向反应结束后的乙烧杯中逐滴滴加3mol•L﹣1的盐酸,使溶液中的铝元素仅
以Al3+的形式存在.则至少需要滴加3mol•L﹣1的盐酸 mL.
【解答】
盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×3mol/L=0.3mol,又两烧杯中
分别加入等质最的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为 x,
则 2Al+6HCl═2AlCl+3H↑
3 2
6 3
0.3mol x
= ,解得x=0.15mol,
一定条件下,气体的物质的量之比等于体积之比,则碱与金属铝反应生成的氢气
的物质的量为0.15mol×2=0.3mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为 y,
则 2Al+2NaOH+2HO═2NaAlO+3H↑
2 2 2
2 3
y 0.3mol
= ,解得y=0.2mol,
则铝的质量为0.2mol×27g/mol=5.4g,
故答案为:5.4;
(2)乙烧杯中含有0.1mol的NaOH、0.2molNaAlO,设与NaOH反应消耗的盐酸
2
的物质的量为x mol,与NaAlO 反应消耗的盐酸的物质的量为y mol,则
2
NaOH+HCl=NaCl+HO
2
1 1
0.1mol x
第17页(共19页)求得x=0.1mol,
NaAlO +4HCl=AlCl+NaCl+2HO
2 3 2
1 4
0.2mol y
= 求得:y=0.8mol,因此共消耗HCl的物质的量为0.9mol,
至少需要需要滴加的盐酸的体积 V= =0.3L=300ml,
故答案为:300.
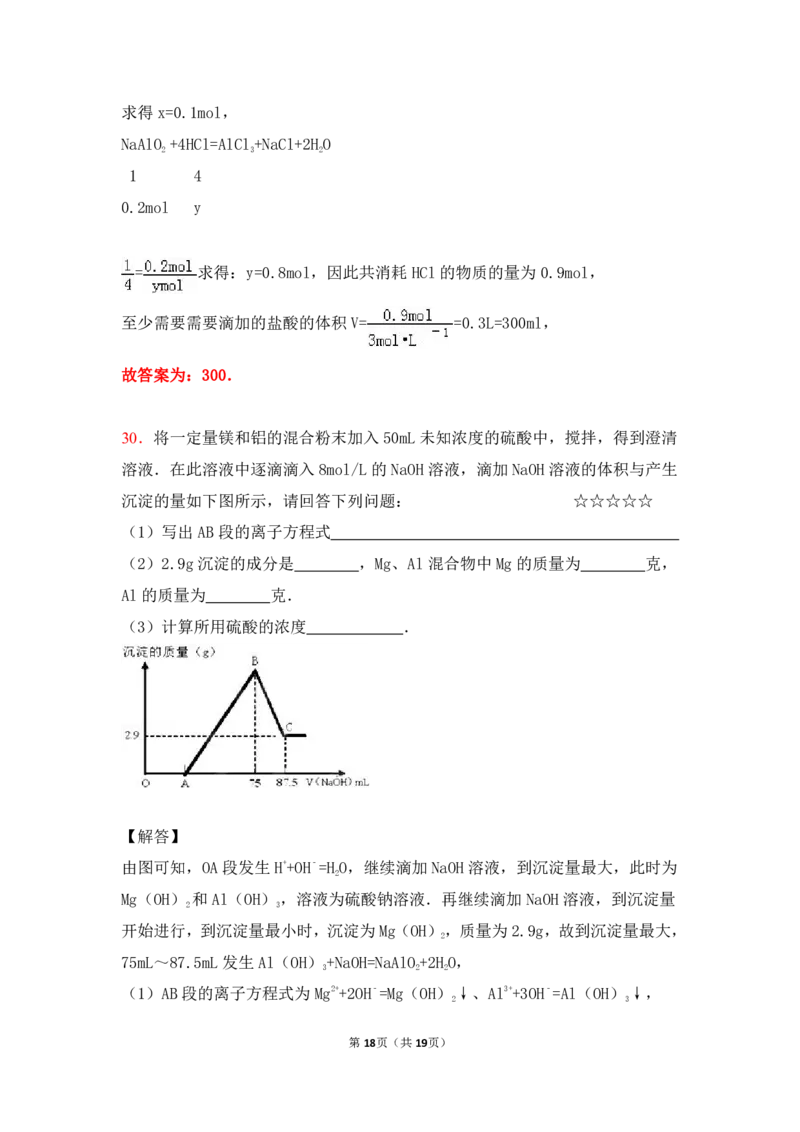
30.将一定量镁和铝的混合粉末加入50mL未知浓度的硫酸中,搅拌,得到澄清
溶液.在此溶液中逐滴滴入 8mol/L的NaOH溶液,滴加NaOH溶液的体积与产生
沉淀的量如下图所示,请回答下列问题: ☆☆☆☆☆
(1)写出AB段的离子方程式
(2)2.9g沉淀的成分是 ,Mg、Al混合物中Mg的质量为 克,
Al的质量为 克.
(3)计算所用硫酸的浓度 .
【解答】
由图可知,OA段发生H++OH﹣=HO,继续滴加NaOH溶液,到沉淀量最大,此时为
2
Mg(OH) 和Al(OH),溶液为硫酸钠溶液.再继续滴加 NaOH溶液,到沉淀量
2 3
开始进行,到沉淀量最小时,沉淀为Mg(OH),质量为2.9g,故到沉淀量最大,
2
75mL~87.5mL发生Al(OH)+NaOH=NaAlO+2HO,
3 2 2
(1)AB段的离子方程式为Mg2++2OH﹣=Mg(OH)↓、Al3++3OH﹣=Al(OH)↓,
2 3
第18页(共19页)故答案为:Mg2++2OH﹣=Mg(OH)↓、Al3++3OH﹣=Al(OH)↓;
2 3
(2)2.9g沉淀的成分是Mg(OH),物质的量为 =0.05mol,Mg的质量
2
为0.05mol×24g/mol=1.2g,75mL~87.5mL发生Al(OH)+NaOH=NaAlO+2HO,n
3 2 2
(Al)=n[Al(OH)]=n(NaOH)=(87.5﹣75)×10﹣3L×8mol/L=0.1mol,Al的
3
质量为0.1mol×27g/mol=2.7g,
故答案为:Mg(OH);1.2;2.7;
2
(3)B点溶液为硫酸钠溶液,n(硫酸)=2n(NaOH),则硫酸的浓度
c= =6mol/L。
故答案为:6mol/L.
第19页(共19页)