文档内容
专练 1 阿伏加德罗常数的应用
1.[2022·全国甲卷]N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.25 ℃,101 kPa下,28 L氢气中质子的数目为2.5N
A
B.2.0 L 1.0 mol·L-1AlCl 溶液中,Al3+的数目为2.0N
3 A
C.0.20 mol苯甲酸完全燃烧,生成CO 的数目为1.4N
2 A
D.电解熔融CuCl ,阴极增重6.4 g,外电路中通过电子的数目为0.10N
2 A
2.[2021·全国甲卷]N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.18 g重水(D O)中含有的质子数为10N
2 A
B.3 mol的NO 与HO完全反应时转移的电子数为4N
2 2 A
C.32 g环状S( )分子中含有的S—S键数为1N
8 A
D.1 L pH=4的0.1 mol·L-1 KCr O 溶液中Cr O离子数为0.1N
2 2 7 2 A
3.[2021·湖南卷]N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.18 g H18O含有的中子数为10N
2 A
B.0.1 mol·L-1HClO 溶液中含有的H+数为0.1N
4 A
C.2 mol NO与1 mol O 在密闭容器中充分反应后的分子数为2N
2 A
D.11.2 L CH 和22.4 L Cl (均为标准状况)在光照下充分反应后的分子数为1.5N
4 2 A
4.[2021·浙江卷1月]设N 为阿伏加德罗常数的值。下列说法正确的是 ( )
A
A.1 mol NH F晶体中含有的共价键数目为3N
4 A
B.CH 和C H 混合气体2.24 L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A
C.向100 mL 0.10 mol·L-1 FeCl 溶液中加入足量 Cu粉充分反应,转移电子数目为
3
0.01N
A
D.0.1 mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目为
3 3 2 3 2 3
0.1N
A
5.[2021·河北卷]N 是阿伏加德罗常数的值。下列说法错误的是( )
A
A.22.4 L(标准状况)氟气所含的质子数为18N
A
B.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73 g,则转移电子数为N
A
D.1 L 1 mol·L-1溴化铵水溶液中NH与H+离子数之和大于N
A
6.[2021·广东卷]设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1 mol CHCl 含有C—Cl键的数目为3N
3 A
B.1 L 1.0 mol·L-1的盐酸含有阴离子总数为2N
A
C.11.2 L NO与11.2 L O 混合后的分子数目为N
2 A
D.23 g Na与足量HO反应生成的H 分子数目为N
2 2 A
7.[2021·浙江卷6月]设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.标准状况下,1.12 L 18O 中含有中子数为N
2 A
B.31 g P(分子结构: )中的共价键数目为1.5N
4 A
C.100 mL 0.1 mol·L-1的NaOH水溶液中含有氧原子数为0.01N
A
D.18.9 g三肽C H NO(相对分子质量:189)中的肽键数目为0.2N
6 11 3 4 A8.[2020·浙江卷1月]设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,
N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.H(g)+O(g)===H O(l) ΔH=-286 kJ·mol-1,则每1 mol生成1 mol[H O(l)]放热
2 2 2 2
286 kJ
B.Cr O+ne-+14H+===2Cr3++7HO,则每生成1 mol Cr3+转移电子数为3N
2 2 A
C.Al3++4OH-===[Al(OH) ]-,说明1 mol Al(OH) 电离出H+数为N
4 3 A
D.1 mol CO 与NaOH溶液完全反应,则n(CO)+n(HCO)+n(H CO)=1 mol
2 2 3
9.[2022·安徽皖南八校联考]N 表示阿伏加德罗常数的值。下列叙述中正确的是( )
A
A.1 mol白磷(P )中所含化学键的数目为4N
4 A
B.1 L 0.1 mol·L-1 KNO 溶液中含O原子的数目为0.3N
3 A
C.2.3 g钠反应生成NaO和NaO 的混合物,转移电子的数目为0.1N
2 2 2 A
D.1 mol H O+和1 mol NH中含质子的数目均为10N
3 A
10.[2022·河南名校模拟]N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.2.24 L水蒸气与足量的NaO 反应,生成氧气的分子数为0.05N
2 2 A
B.常温常压下,3.6 g 18O 所含的中子数为2N
2 A
C.0.1 mol淀粉[(C H O)]完全水解消耗的水分子数为0.1N
6 10 5 n A
D.将0.1 mol CO 溶于水中,所得溶液中CO、HCO、HCO 的粒子总数为0.1N
2 2 3 A
11.
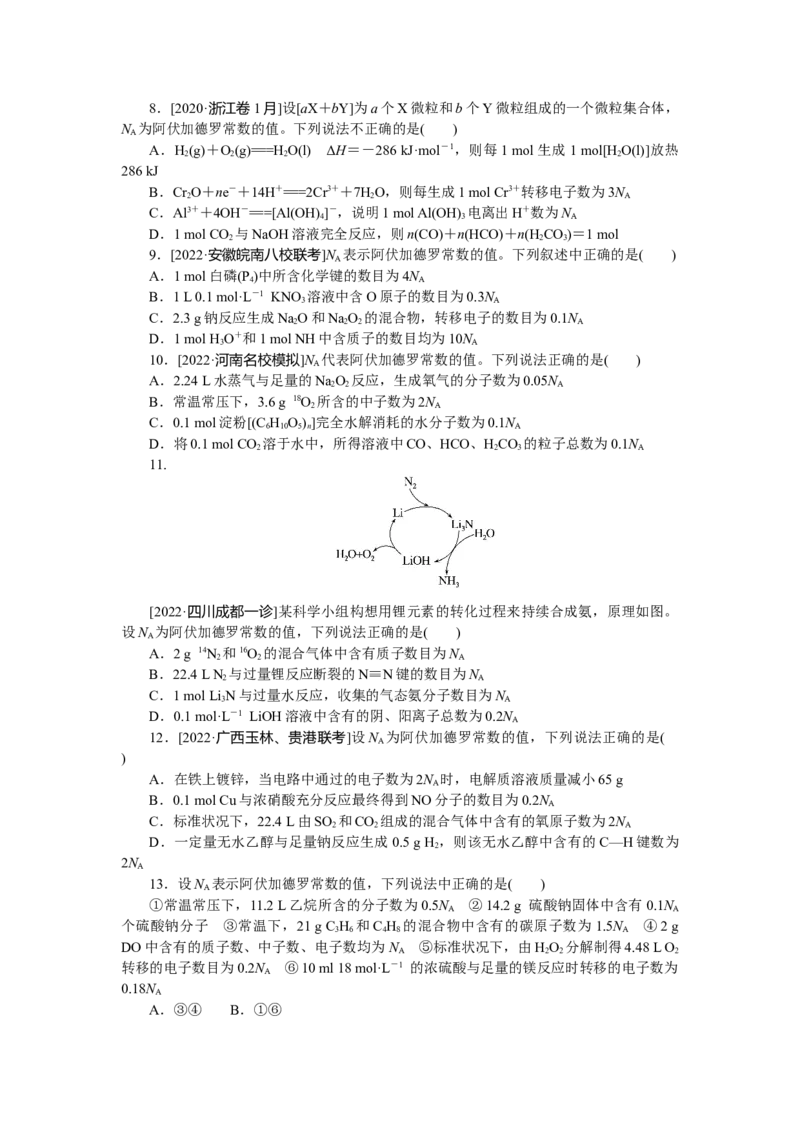
[2022·四川成都一诊]某科学小组构想用锂元素的转化过程来持续合成氨,原理如图。
设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.2 g 14N 和16O 的混合气体中含有质子数目为N
2 2 A
B.22.4 L N 与过量锂反应断裂的N≡N键的数目为N
2 A
C.1 mol Li N与过量水反应,收集的气态氨分子数目为N
3 A
D.0.1 mol·L-1 LiOH溶液中含有的阴、阳离子总数为0.2N
A
12.[2022·广西玉林、贵港联考]设N 为阿伏加德罗常数的值,下列说法正确的是(
A
)
A.在铁上镀锌,当电路中通过的电子数为2N 时,电解质溶液质量减小65 g
A
B.0.1 mol Cu与浓硝酸充分反应最终得到NO分子的数目为0.2N
A
C.标准状况下,22.4 L由SO 和CO 组成的混合气体中含有的氧原子数为2N
2 2 A
D.一定量无水乙醇与足量钠反应生成0.5 g H ,则该无水乙醇中含有的C—H键数为
2
2N
A
13.设N 表示阿伏加德罗常数的值,下列说法中正确的是( )
A
①常温常压下,11.2 L乙烷所含的分子数为0.5N ②14.2 g 硫酸钠固体中含有0.1N
A A
个硫酸钠分子 ③常温下,21 g C H 和C H 的混合物中含有的碳原子数为 1.5N ④2 g
3 6 4 8 A
DO中含有的质子数、中子数、电子数均为N ⑤标准状况下,由HO 分解制得4.48 L O
A 2 2 2
转移的电子数目为0.2N ⑥10 ml 18 mol·L-1 的浓硫酸与足量的镁反应时转移的电子数为
A
0.18N
A
A.③④ B.①⑥C.④⑤⑥ D.①②⑥
14.[2021·海南卷]N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.0.1 mol 27Al3+中含有的电子数为1.3N
A
B.3.9 g Na O 中含有的共价键的数目为0.1N
2 2 A
C.0.1 mol肼(H N——NH)含有的孤电子对数为0.2N
2 2 A
D.CH===CH +H――→CHCH,生成1 mol乙烷时断裂的共价键总数为N
2 2 2 3 3 A
15.[2021·福建卷]设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1.12 L C H 所含极性共价键的数目为0.2N
2 4 A
B.12 g NaHSO 晶体中阴、阳离子总数为0.2N
4 A
C.0.1 mol CH 与足量Cl 反应生成CHCl的分子数为0.1N
4 2 3 A
D.电解熔融MgCl 制2.4 g Mg,电路中通过的电子数为0.1N
2 A