文档内容
第五篇 水溶液中的离子反应与平衡
专项 30 微粒浓度大小比较
从高考命题的变化趋势来看,溶液中离子浓度的大小比较是离子平衡的主流试题,既与弱电解质电离
平衡有关,又与盐的水解有关;不仅偏重考查粒子的浓度大小顺序,且还侧重溶液中各种守恒(电荷守恒、
物料守恒、质子守恒)关系考查,从而使题目具有一定的综合性、灵活性和技巧性。
1.电离理论
(1)弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离,如氨水溶液中:
NH ·H O、NH、OH-浓度的大小关系是c(NH ·H O)>c(OH-)>c(NH)。
3 2 3 2
(2)多元弱酸的电离是分步进行的,其主要是第一级电离(第一级电离程度远大于第二级电离)。如在
HS溶液中:HS、HS-、S2-、H+的浓度大小关系是c(H S)>c(H+)>c(HS-)>c(S2-)。
2 2 2
2.水解理论
(1)弱电解质离子的水解损失是微量的(双水解除外),但由于水的电离,故水解后酸性溶液中c(H+)或碱
性溶液中c(OH-)总是大于水解产生的弱电解质的浓度。如NH Cl溶液中:NH、Cl-、NH ·H O、H+的浓度
4 3 2
大小关系是c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
3 2
(2)多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解,如在 NaCO 溶液中:CO、HCO、
2 3
HCO 的浓度大小关系应是c(CO)>c(HCO)>c(H CO)。
2 3 2 3
3.电荷守恒规律
电解质溶液中,无论存在多少种离子,溶液都呈电中性,即阴离子所带负电荷总数一定等于阳离子所
带正电荷总数。如NaHCO 溶液中存在Na+、H+、HCO、CO、OH-,存在如下关系:c(Na+)+c(H+)=
3
c(HCO)+c(OH-)+2c(CO)。
4.物料守恒规律
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素总是守恒的。如 KS溶液中S2-、HS
2
-都能水解,故S元素以S2-、HS-、HS三种形式存在,它们之间有如下守恒关系:c(K+)=2c(S2-)+
2
2c(HS-)+2c(H S)。
2
5.质子守恒规律
如NaS水溶液中的质子转移情况图示如下:
2由图可得NaS水溶液中质子守恒式可表示:c(H O+)+2c(H S)+c(HS-)=c(OH-)或c(H+)+2c(H S)+
2 3 2 2
c(HS-)=c(OH-)。质子守恒的关系式也可以由电荷守恒式与物料守恒式推导得到。
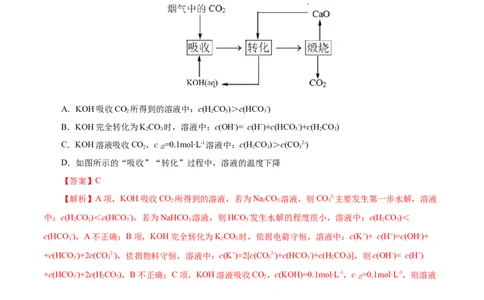
1.(2022•江苏卷)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通
2 2
入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c(HCO - )
2 2 总 2 3 3
+c(CO2-)。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是( )
3 2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c(HCO -)
2 2 3 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c(HCO -)+c(H CO)
2 3 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c(CO2-)
2 总 2 3 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
【答案】C
【解析】A项,KOH吸收CO 所得到的溶液,若为NaCO 溶液,则CO2-主要发生第一步水解,溶液
2 2 3 3
中:c(H CO)<c(HCO -),若为NaHCO 溶液,则HCO -发生水解的程度很小,溶液中:c(H CO)<
2 3 3 3 3 2 3
c(HCO -),A不正确;B项,KOH完全转化为KCO 时,依据电荷守恒,溶液中:c(K+)+ c(H+)=c(OH-)+
3 2 3
+c(HCO -)+2c(CO2-),依据物料守恒,溶液中:c(K+)=2[c(CO2-)+c(HCO -)+c(H CO)],则c(OH-)= c(H+)
3 3 3 3 2 3
+c(HCO -)+2c(H CO),B不正确;C项,KOH溶液吸收CO,c(KOH)=0.1mol∙L-1,c =0.1mol∙L-1,则溶液
3 2 3 2 总
为KHCO 溶液, K = = ≈2.3×10-8>K =4.4×10-11,表明HCO -以水解为主,所以溶液中:
3 h2 a2 3
c(H CO)>c(CO2-),C正确;D项,如图所示的“吸收”“转化”过程中,发生反应为:
2 3 3
CO+2KOH=K CO+H O、KCO+CaO+H O=CaCO ↓+2KOH(若生成KHCO 或KCO 与KHCO 的混合物,
2 2 3 2 2 3 2 3 3 2 3 3
则原理相同),二式相加得:CO+CaO=CaCO ↓,该反应放热,溶液的温度升高,D不正确;故选C。
2 3
2.(2021•天津卷)常温下,下列有关电解质溶液的叙述正确的是( )
A.在0.1mol·L-1HPO 溶液中c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-)
3 4 3 4 2 4 4 4B.在0.1mol·L-1NaC O 溶液中c(Na+)+c(H+)= c(OH―)+c(HC O-)+c(C O2-)
2 2 4 2 4 2 4
C.在0.1mol·L-1NaHCO 溶液中c(H CO)+ c(HCO -)=0.1mol·L-1
3 2 3 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH +)>c(OH―)>c(H+)
4 4
【答案】A
【解析】A项,由于磷酸为多元酸,第一步电离大于第二步电离大于第三步电离,所以在
0.1mol·L-1HPO 溶液中,离子浓度大小为:c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-),故A正确;B项,在
3 4 3 4 2 4 4 4
0.1mol·L-1NaC O 溶液中,根据电荷守恒得到c(Na+)+c(H+)= c(OH―)+c(HC O-)+2c(C O2-),故B错误;C
2 2 4 2 4 2 4
项,在0.1mol·L-1NaHCO 溶液中,根据物料守恒得到c(H CO)+ c(HCO -)+ c(CO2-)=0.1mol·L-1,故C错误;
3 2 3 3 3
D项,氨水和NH Cl溶液混合,形成pH=9的溶液,则c(OH―)>c(H+),根据电荷守恒c(Cl-)
4
+c(OH―)=c(NH +)+c(H+),则c(Cl-)<c(NH +),故D错误;故选A。
4 4
3.(2020•浙江 7 月选考)常温下,用 0.1 mol·L−1氨水滴定 10 mL 浓度均为 0.1 mol·L−1的 HCl 和
CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl−)>c(CHCOO−)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CHCOO−)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH−)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)<c(Cl−)
【答案】D
【解析】A项,未滴定时,溶液溶质为HCl和CHCOOH,且浓度均为0.1mol/L,HCl为强电解质,
3
完全电离,CHCOOH为弱电解质,不完全电离,故,c(Cl-)>c(CHCOO-),A正确;B项,当滴入氨水
3 3
10mL时,n(NH ·H O)=n(CHCOOH),则在同一溶液中c(NH +)+ c(NH ·H O)=c(CHCOOH)+ c(CH COO-),
3 2 3 4 3 2 3 3
B正确;C项,当滴入氨水20mL时,溶液溶质为NH Cl和CHCOONH,质子守恒为c(CHCOOH)+c(H+)=
4 3 4 3
c(NH +)+c(OH-),C正确;D项,当溶液为中性时,电荷守恒为:c(NH +)+c(H+)= c(CHCOO-)+c(Cl-)+
4 4 3
c(OH-),因为溶液为中性,则c(H+)=c(OH-),故c(NH +)>c(Cl-),D不正确;故选D。
4
4.(2020•江苏卷)室温下,将两种浓度均为0.1mol·L-1的溶液等体积混合,若溶液混合引起的体积变化
可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
A.NaHCO -Na CO 混合溶液(pH=10.30):NaHCO 溶液中:c(Na+)>c(HCO)>c(CO2-)>c(OH-)
3 2 3 3 3
B.氨水-NH Cl混合溶液(pH=9.25):c(NH)+ c(H+)= c(NH ∙HO)+c(OH-)
4 3 2
C.CHCOOH - CHCOONa混合溶液(pH=4.76):c(Na+)>c(CHCOOH)>c(CHCOO−)>c(H+)
3 3 3 3
D.HC O-NaHC O 混合溶液(pH=1.68,HC O 为二元弱酸):c(H+)+c(H C O)= c(Na+)+c(OH—)+
2 2 4 2 4 2 2 4 2 2 4
c(C O)
2
【答案】AD【解析】A项,NaHCO 水溶液呈碱性,说明HCO -的水解程度大于其电离程度,等浓度的NaHCO 和
3 3 3
NaCO 水解关系为:CO2->HCO -,溶液中剩余微粒浓度关系为:c(HCO)>c(CO2-),CO2-和HCO -水解程
2 3 3 3 3 3 3
度微弱,生成的OH-浓度较低,由NaHCO 和NaCO 化学式可知,该混合溶液中Na+浓度最大,则混合溶
3 2 3
液中微粒浓度大小关系为:c(Na+)>c(HCO)>c(CO2-)>c(OH-),故A正确;B项,该混合溶液中电荷守恒
3
为:c(NH)+ c(H+)= c(Cl−)+c(OH-),物料守恒为:c(CHCOOH)+c(NH)=2c(Cl−),两式联立消去c(Cl-)可得:
3
c(NH)+2c(H+)= c(NH ∙HO)+2c(OH-),故B错误;C项,若不考虑溶液中相关微粒行为,则
3 2
c(CHCOOH)=c(CHCOO-)=c(Na+),该溶液呈酸性,说明CHCOOH电离程度大于CHCOONa水解程度,
3 3 3 3
则溶液中微粒浓度关系为:c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+),故C错误;D项,该混合溶液中物料
3 3
守恒为:2c(Na+)=c(H C O)+c(HC O-)+c(C O),电荷守恒为:c(H+)+c(Na+)=c(OH—)+c(HC O-)
2 2 4 2 4 2 2 4
+2c(C O),两式相加可得:c(H+)+c(H C O)= c(Na+)+c(OH—)+c(C O),故D正确;故选AD。
2 2 2 4 2
5.(2019•江苏卷)室温下,反应HCO -+H O HCO+OH−的平衡常数K=2.2×10−8。将NH HCO 溶
3 2 2 3 4 3
液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指
定溶液中微粒物质的量浓度关系正确的是( )
A.0.2mol·L−1氨水:c(NH ·H O)>c(NH +)>c(OH−)>c(H+)
3 2 4
B.0.2mol·L−1NH HCO 溶液(pH>7):c(NH +)>c(HCO -)>c(H CO)>c(NH ·H O)
4 3 4 3 2 3 3 2
C.0.2mol·L−1氨水和0.2mol·L−1NH HCO 溶液等体积混合:c(NH +)+c(NH ·H O)=c(H CO)+c(HCO -)
4 3 4 3 2 2 3 3
+c(CO2-)
3
D.0.6mol·L−1氨水和0.2mol·L−1NH HCO 溶液等体积混合:c(NH ·H O)+c(CO2-)
4 3 3 2 3
+c(OH−)=0.3mol·L−1+c(H CO)+c(H+)
2 3
【答案】BD
【解析】A.NH ∙HO 属于弱电解,部分电离,氨水中存在的电离平衡有:NH ∙HO NH +
3 2 3 2 4
+OH-,HO H++OH-,所以c(OH-)>c(NH+),故A错误;B.NH HCO 溶液显碱性,说明HCO -的水
2 4 4 3 3
解程度大于NH +的水解,所以c(NH +)>c(HCO-),HCO -水解:HCO - HCO+OH-,NH +水解:NH +
4 4 3 3 3 2 3 4 4
+H O NH ∙HO+H+,前者水解程度大,则 c(HCO)>c(NH∙HO),故 B 正确;C.由物料守恒,
2 3 2 2 3 3 2
n(N):n(C)=2:1,则有c(NH +)+c(NH∙HO)=2[c(HCO)+c(HCO-)+c(CO 2-)],故C错误;D.由物料守恒,
4 3 2 2 3 3 3
n(N):n(C)=4:1 , 则 有 c(NH +)+c(NH∙HO)=4[c(HCO)+c(HCO-)+c(CO 2-)]① ; 电 荷 守 恒 有 : c(NH +)
4 3 2 2 3 3 3 4
+c(H+)=c(HCO-)+2c(CO 2-)+c(OH-)② ; 结 合 ① ② 消 去 c(NH +) 得 : c(NH ∙HO)+c(OH-)=c(H+)
3 3 4 3 2
+4c(H CO)+3c(HCO-)+2c(CO 2-)③,0.2mol/LNH HCO 与氨水等体积混合后,c(NH HCO )=0.1mol/L,由碳
2 3 3 3 4 3 4 3
守恒有,c(HCO)+c(HCO-)+c(CO 2-)=0.1mol/L④,将③等式两边各加一个 c(CO2-),则有 c(NH ∙HO)
2 3 3 3 3 3 2
+c(OH-)+c(CO 2-)=c(H+)+c(H CO)+3c(H CO)+3c(HCO-)+3c(CO 2-),将④带入③中得,c(NH ∙HO)+c(OH-)
3 2 3 2 3 3 3 3 2+c(CO 2-)=c(H+)+3c(H CO)+0.3mol/L,故D正确;故选BD。
3 2 3
1.解题步骤
2.解题过程
判反应 两溶液混合是否发生反应 弄清真实组成
写平衡 写出溶液中所有平衡(电离平衡、水解平衡)
列等式 根据电荷守恒、物料守恒、质子守恒列式
根据溶液中存在的平衡和题给条件,结合平衡的有关规律,
分主次
分析哪些平衡进行的程度相对大一些,哪些平衡进行的程度
相对小一些,再依此比较出溶液各粒子浓度的大小。
3.比较时紧扣两个微弱
(1)弱电解质(弱酸、弱碱、水)的电离是微弱的,且水的电离能力远远小于弱酸和弱碱的电离能力。如
在稀醋酸溶液中:CHCOOH CHCOO-+H+,HO OH-+H+,在溶液中微粒浓度由大到小的
3 3 2
顺序:c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-)。
3 3
(2)弱酸根离子或弱碱阳离子的水解是微弱的,但水的电离程度远远小于盐的水解程度。如稀的
CHCOONa 溶液中:CHCOONa===CH COO-+Na+,CHCOO-+HO CHCOOH+OH-,HO
3 3 3 3 2 3 2
H++OH-,所以CHCOONa溶液中:c(Na+)>c(CHCOO-)>c(OH-)>c(CHCOOH)>c(H+)。
3 3 3
4.酸式盐与多元弱酸的强碱正盐溶液酸碱性比较
(1)酸式盐溶液的酸碱性主要取决于酸式盐中酸式酸根离子的电离能力和水解能力哪一个更强,如
NaHCO 溶液中HCO的水解能力大于其电离能力,故溶液显碱性。
3
(2)多元弱酸的强碱正盐溶液:多元弱酸根离子水解以第一步为主。例如,NaS溶液中:c(Na+)>c(S2
2
-)>c(OH-)>c(HS-)>c(H+)。
5.质子守恒式可以由电荷守恒式和物料守恒式推导出来
以KHS溶液为例,电荷守恒式为c(K+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)①,物料守恒式为c(K+)=c(HS-)+c(S2-)+c(H S)②,由①-②得质子守恒式,消去没有参与变化的K+等。
2
6.规避等量关系中的2个易失分点
(1)电荷守恒式中不只是各离子浓度的简单相加。如2c(CO)的化学计量数2代表一个CO带2个单位负
电荷,不可漏掉。
(2)物料守恒式中,离子浓度系数不能漏写或颠倒。如NaS溶液中的物料守恒式中,“2”表示c(Na+)
2
是溶液中各种硫元素存在形式的硫原子总浓度的2倍。
1.(2023届·江苏省百校联考高三第一次考试)室温下用0.1mol•L-1NaOH溶液吸收SO ,若通入SO
2 2
所引起的溶液体积变化和HO挥发可忽略,溶液中含硫物种的浓度c =c(H SO )+c(HSO -)+c(SO 2-)。HSO
2 总 2 3 3 3 2 3
电离常数分别为K =1.54×10-2、K =1.00×10-7。下列说法正确的是( )
a1 a2
A.NaOH溶液吸收SO 所得到的溶液中:c(SO 2-)>c(HSO -)>c(H SO )
2 3 3 2 3
B.NaOH完全转化为NaHSO 时,溶液中:c(H+)+c(SO 2-)=c(OH—)+c(H SO )
3 3 2 3
C.NaOH完全转化为NaSO 时,溶液中:c(Na+)>c(SO 2-)>c(OH—)>c(HSO -)
2 3 3 3
D.NaOH溶液吸收SO ,c =0.1mol•L-1溶液中:c(H SO )>c(SO 2-)
2 总 2 3 3
【答案】C
【解析】由电离常数可知,亚硫酸氢根离子的水解常数K = = <K ,说明亚硫酸氢根离
h a2
子在溶液中的电离程度大于水解程度,亚硫酸氢钠溶液呈酸性。A项,氢氧化钠溶液吸收二氧化硫可能得
到亚硫酸氢钠溶液,由分析可知,亚硫酸氢根离子在溶液中的电离程度大于水解程度,溶液中c(HSO -)>
3
c(SO 2-) > c(H SO ),故A错误;B项,亚硫酸氢钠溶液中存在质子守恒关系c(H+)+ c(H SO ) =c(OH—)+
3 2 3 2 3
c(SO 2-),故B错误;C项,亚硫酸钠是强碱弱酸盐,亚硫酸根离子在溶液中分步水解,以一级水解为主,
3
则溶液中离子浓度的大小顺序为c(Na+)>c(SO 2-)>c(OH—)>c(HSO -),故C正确;D项,c =0.1mol•L-1溶液
3 3 总
为亚硫酸氢钠溶液,由分析可知,亚硫酸氢根离子在溶液中的电离程度大于水解程度,溶液中c(SO 2-) >
3
c(H SO ),故D错误;故选C。
2 3
2.(2023届·江苏省包场高级中学高三开学考试)室温下,通过下列实验探究Na HC O (K 为
2 4 h
NaHC O 水解平衡常数、K 为HC O 电离平衡常数)溶液的性质。
2 4 a1 2 2 4
实验 实验操作和现象
1 用试纸测定0.1mol·L-1 NaHC O 溶液的pH,测得约为5.5
2 4
2 向含0.1mol NaHC O 稀溶液中加入0.05molBa(OH) ,产生沉淀
2 4 23 向0.1mol·L-1 NaHC O 溶液中通入过量HCl,无现象
2 4
4 向0.1mol·L-1 NaHC O 溶液中通入一定量NH ,测得溶液pH=7
2 4 3
下列有关说法不正确的是( )
A.实验1的溶液中:
B.实验2反应静置后的上层清液中:
C.实验3得到的溶液中:c(Na+)>c(Cl-)>c(H C O)>c(H+)
2 2 4
D.实验4所得的溶液中:c(NH +)+ c(H C O)=c(C O2-)
4 2 2 4 2 4
【答案】C
【解析】A项,实验1的溶液中: , ,则,
,即 ,A正确;B项,实验2反应静置后的上
层清液中:NaHC O 与Ba(OH) 反应生成BaC O 沉淀,根据溶解平衡, ,
2 4 2 2 4
B正确;C项,实验3得到的溶液中,如果通入的HCl的量过多,使其浓度超过了0.1mol/L,则会使c(Na+)
<c(Cl-),C错误;D项,实验4所得的溶液中:根据电荷守恒,得到(NH +)+c(H+)+ c(Na+)=c(OH-)
4
+c(HC O-)+2c(C O2-),再根据物料守恒得c(Na+)=c(HC O-)+2c(C O2-)+ c(H C O),两者连立得到c(NH +)+
2 4 2 4 2 4 2 4 2 2 4 4
c(H C O)=c(C O2-),D正确;故选C。
2 2 4 2 4
3.下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO)>
3
c(HCO)>c(OH-)
B.20 mL 0.1 mol·L-1 CHCOONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH)+c(OH
-)
D.0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)
3
+c(CHCOOH)
3
【答案】B
【解析】A项,等浓度等体积的NaHCO 与NaOH混合时,两者恰好反应生成NaCO,在该溶液中
3 2 3
CO能进行两级水解:CO+HOHCO+OH-、HCO+HO HCO+OH-,故溶液中c(OH
2 2 2 3-)>c(HCO),该项错误;B项,CHCOONa与HCl混合时反应后生成的溶液中含有等量的CHCOONa、
3 3
CHCOOH、NaCl,因溶液显酸性,故溶液中CHCOOH的电离程度大于CHCOO-的水解程度,该项正确;
3 3 3
C项,在混合前两溶液的pH之和为14,则氨水过量,所得溶液为少量NH Cl和过量NH ·H O的混合溶液,
4 3 2
则c(Cl-)c(H+)>c(NH+)>c(OH-)
4
C.0.1mol/L Na CO 与0.1mol/L NaHCO 溶液等体积混合: 2c(Na+)=3c(CO 2-)+3c(HCO-)+3c(H CO)
2 3 3 3 3 2 3
D.0.1mol/L Na C O 与0.1mol/L 的盐酸等体积混合(H C O 为二元弱酸):2c(C O2-)+c(HC O-)
2 2 4 2 2 4 2 4 2 4
+c(OH-)=c(Na+)+c(H+)
【答案】C
【解析】A项,NaHCO 溶液中:HCO -的水解程度大于其电离程度,所以溶液显碱性,根据质子守恒
3 3
可得c(OH-)=c(H+)+c(H CO),A错误;B项,HCl是一元强酸,完全电离,c(H+)与盐酸的浓度相等,而
2 3
NH ·HO是一元弱碱,只有很少一部分电离,在溶液中存在电离平衡,所以c(NH ·HO)>c(OH-),室温下,
3 2 3 2
将pH=2的盐酸与pH=12的氨水等体积混合,电离产生的OH-恰好与H+中和,但c(NH ·HO)> c(OH-),电
3 2
解质分子进一步电离产生OH-和NH +,因此溶液显碱性,所得溶液中:c(NH +)>c(Cl-),c(OH-)>c(H+),盐
4 4
电离产生的离子浓度远大于弱碱电离产生的离子浓度所以微粒浓度关系为c(NH +) >c(Cl-)>c(OH-) >c(H+),
4
B错误;C项,0.1mol/L Na CO 与0.1mol/L NaHCO 溶液等体积混合,根据物料守恒可得: 2c(Na+)
2 3 3
=3c(CO 2-)+3c(HCO-)+3c(H CO),C正确;D项,0.1mol/L Na C O 与0.1mol/L 的盐酸等体积混合(H C O
3 3 2 3 2 2 4 2 2 4
为二元弱酸,二者发生反应:NaC O+HCl=NaCl+NaHC O,根据电荷守恒可得2c(C O2-)+c(HC O-)+
2 2 4 2 4 2 4 2 4
c(OH-)+c(Cl-)=c(Na+)+c(H+),D错误。
5.(2022·上海市洋泾中学高三模拟)H C O 为二元弱酸,K (H C O)=5.4×10-2,K (H C O)=5.4×10-5,
2 2 4 a1 2 2 4 a2 2 2 4
NaHC O 溶液显酸性。设HC O 溶液中c(总)=c(H C O)+c(HC O-)+c(C O2-)。室温下用NaOH溶液滴定
2 4 2 2 4 2 2 4 2 4 2 4
25.00mL0.1000mol·L-1HC O 溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的
2 2 4
是( )
A.0.1000mol·L-1HC O 溶液:c(H+)=0.1000mol·L-1+c(C O2-)+c(OH-)+c(H C O)
2 2 4 2 4 2 2 4
B.c(Na+)=c(总)的溶液:c(Na+)>c(H C O)>c(H+)>c(C O2-)
2 2 4 2 4
C.pH=7的溶液:c(Na+)=0.1000mol·L-1+c(C O2-)-c(HC O)
2 4 2 2 4
D.c(Na+)=2c(总)的溶液:c(OH-)-c(H+)=2c(H C O)+c(HC O-)
2 2 4 2 4【答案】D
【解析】A项,0.1000mol·L-1HC O 溶液中c(HC O)+c(HC O-)+c(C O2-)=0.1 mol·L-1,根据电荷守恒
2 2 4 2 2 4 2 4 2 4
c(HC O-)+2c(C O2-)+c(OH-)= c(H+),所以c(H+)=0.1000mol·L-1+c(C O2-)+c(OH-)-c(HC O),故A错误;B项,
2 4 2 4 2 4 2 2 4
根据物料守恒,c(Na+)=c(总)的溶液中溶质为NaHC O,HC O-的电离常数为5.4×10-5、水解常数为
2 4 2 4
,HC O-电离大于水解,c(C O2-)>c(H C O),故B错误;C项,加入一定体积的氢氧
2 4 2 4 2 2 4
化钠溶液,c(HC O)+c(HC O-)+c(C O2-)<0.1 mol·L-1,根据电荷守恒,pH=7的溶液c(HC O-)
2 2 4 2 4 2 4 2 4
+2c(C O2-)=c(Na+),c(Na+)>0.1000mol·L-1+c(C O2-)-c(HC O),故C正确;D项,根据物料守恒
2 4 2 4 2 2 4
c(Na+)=2c(总)的溶液中溶质为NaC O,根据物料守恒c(Na+)=2[c(HC O)+c(HC O-)+c(C O2-)],根据电
2 2 4 2 2 4 2 4 2 4
荷守恒c(HC O-)+2c(C O2-)+c(OH-)=c(Na+)+ c(H+),所以c(OH-)-c(H+)=2c(H C O)+c(HC O-),故D正确;故
2 4 2 4 2 2 4 2 4
选D。
6.(2022·上海市高三二模)室温下,通过下列实验探究0.1mol·L-1NaHS溶液的性质。
实验 实验操作和现象
① 滴加几滴酚酞试液,溶液变红
② 加入等体积0.1molL-1NaOH溶液充分混合,无明显现象
③ 加入少量CuSO 溶⋅液,产生黑色沉淀
4
④ 加入适量NaClO溶液,有淡黄色沉淀产生
下列有关说法正确的是( )
A.实验①溶液中:c(S2-)>c(H S)
2
B.实验②所得溶液中:c(OH-)=c(H+)+c(HS-)+2c(H S)
2
C.实验③中反应的离子方程式:Cu2++HS-→CuS↓+H+
D.实验④中反应的离子方程式:2HS-+ClO-→2S↓+Cl-+H O
2
【答案】B
【解析】A项,实验①:滴加几滴酚酞试液,溶液变红,表明溶液显碱性,则HS-的水解程度大于电
离程度,所以溶液中:c(S2-)<c(H S),A不正确;B项,实验②中,NaHS与NaOH正好完全反应,所得溶
2
液为NaS溶液,溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),物料守恒:c(Na+)=2c(HS-)
2
+2c(S2-)+2c(H S),从而得出c(OH-)=c(H+)+c(HS-)+2c(H S),B正确;C项,实验③中,HS-与Cu2+反应,生
2 2
成CuS沉淀和H+,H+再与HS-结合为HS,反应的离子方程式:Cu2++2HS-→CuS↓+HS↑,C不正确;D项,
2 2
实验④中,HS-与ClO-发生氧化还原反应,生成S、Cl-和OH-,OH-再与HS-反应生成S2-和HO,反应的离
2子方程式:2HS-+ClO-→S↓+Cl-+S2-+H O,D不正确;故选B。
2
7.(2022·江苏省平潮高级中学模拟预测)室温下,通过下列实验探究NaCO 溶液的性质。用K 、K
2 3 a1 a2
分别表示HCO 的第一步和第二步电离常数。
2 3
实验 实验操作和现象
1 用pH试纸测定0.1mol·L-1NaCO 溶液的pH,测得pH约为12
2 3
2 向0.1mol·L-1NaCO 溶液中加入过量0.2mol·L-1CaCl 溶液,产生白色沉淀
2 3 2
3 向0.1mol·L-1NaCO 溶液中通入过量CO,测得溶液pH约为8
2 3 2
4 向含有酚酞的0.1mol·L-1NaCO 中滴加几滴0.2mol·L-1NaOH,红色加深
2 3
下列有关说法不正确的是( )
A.0.1mol·L-1NaCO 溶液中存在c(OH-)=c(H+)+2c(H CO)+c(HCO-)
2 3 2 3 3
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO2-)=K (CaCO)
3 sp 3
C.实验3得到的溶液中有c(HCO -)>c(HCO)>c(CO2-),且K K <K
3 2 3 3 a1 a2 w
D.实验4中滴加的NaOH抑制了CO2-的水解, 的值变小
3
【答案】D
【解析】A项,NaCO 溶液中,根据电荷守恒可得c(OH-)+c(HCO-)+2c(CO 2-)=c(H+)+c(Na+),又根据
2 3 3 3
物料守恒可得c(Na+)=2[c(HCO-)+c(CO 2-)+c(H CO)],两式联立可得c(OH-)=c(H+)+2c(H CO)+c(HCO-),故
3 3 2 3 2 3 3
A正确;B项,NaCO 溶液中加入过量CaCl 溶液生成碳酸钙沉淀,上层清液为饱和碳酸钙溶液,故有
2 3 2
c(Ca2+)·c(CO2-)=K (CaCO),故B正确;C项,NaCO 溶液中通入过量CO,测得溶液pH约为8,即为碳
3 sp 3 2 3 2
酸氢钠溶液,溶液显碱性,水解大于电离,故有c(HCO -)>c(HCO)>c(CO2-),且水解常数大于电离常数,
3 2 3 3
故有K= >K ,故K K <K ,故C正确;D项,CO2-的水解平衡为CO2-+H O HCO -+OH-,水
h a2 a1 a2 w 3 3 2 3
解常数K= ,K 大小随温度变化而变化,故滴加NaOH平衡移动,但 不变,
h h
故D错误;故选D。
8.(2022·江苏省南通市新高考基地学校高三第二次联考)室温下,通过下列实验探究
0.100mol·L-1KC O 溶液的性质。已知:25℃时HC O 的K =10-1.22,K =10-4.19。
2 2 4 2 2 4 a1 a2
序号 实验① 准确量取10.00mL0.100mol·L-1KC O 溶液,测得pH=8.4
2 2 4
② 向①中加入2滴0.100mol·L-1HCl盐酸,测得pH=7.0
③ 向①准确加入10.00mL0.100mol·L-1HCl溶液,pH=3.52
④ 向①中加入20.00mL0.100mol·L-1CaCl 溶液,出现白色沉淀
2
下列说法正确的是( )
A.实验①溶液中: =10-4.21
B.实验②反应所得溶液中:c(K+)=2c(C O2-)+c(HC O-)
2 4 2 4
C.实验③反应所得溶液中:c(C O2-)K (CaSO),D错误;故选C。
3 sp 3
11.(2022·浙江省宁波市鄞州中学高三考前测试)室温下,向100 mL 0.2 mol·L-1的NH ·H O中缓慢
3 2
通入HCl,随着HCl通入量的不同,下列溶液中微粒对应关系(不考虑溶液体积变化)正确的是( )
选项 n(HCl)/mol 溶液中各微粒的物质的量浓度关系
A 0 c(NH ·H O)>c(NH +)>c(OH-)>c(H+)
3 2 4
B 0.005 c(NH ·H O)+4c(OH-)=3c(NH +)+4c(H+)
3 2 4
C 0.01 c(NH ·H O)+c(NH +)=c(Cl-)+c(OH-)
3 2 4
D 0.02 c(Cl-)>c(NH ·H O)>c(NH +)>c(OH-)
3 2 4
【答案】B
【解析】在100 mL 0.2 mol·L-1的NH ·H O中含有溶质的物质的量n(NH ·H O)=0.2 mol/L×0.1 L=0.02
3 2 3 2
mol,通入HCl气体时发生反应:NH ·H O+HCl=NH Cl+H O,然后根据通入的HCl的物质的量,结合反应
3 2 4 2
消耗关系,确定混合溶液的成分,发现溶液中各种微粒的浓度大小关系。A项,通入HCl的物质的量是0
mol时,溶液的溶质为NH ·H O,由于NH ·H O是弱电解质,主要以电解质分子存在,电离产生的NH +、
3 2 3 2 4
OH-的浓度远小于电解质分子的浓度,溶液中除NH ·H O电离产生OH-外,还存在HO电离产生OH-,故
3 2 2
溶液中离子浓度大小关系为:c(NH ·H O)>c(OH-)>c(NH +)>c(H+),A错误;B项,溶液中
3 2 4
n(NH ·H O)=0.2 mol/L×0.1 L=0.02 mol,当通入HCl的物质的量n(HCl)=0.005 mol<0.02 mol,二者发生反
3 2
应:NH ·H O+HCl=NH Cl+H O,二者反应的物质的量的比是1:1,n(NH ·H O) =0.02 mol-0.005
3 2 4 2 3 2 过量
mol=0.015 mol,反应后混合溶液中n(NH ·H O):n(NH Cl)=0.015 mol:0.005 mol=3:1,根据电荷守恒可得:
3 2 4
c(NH +)+c(H+)=c(OH-)+c(Cl-),根据物料守恒可得c(NH ·H O)+c(NH +)=4c(Cl-),将两个式子联立可得
4 3 2 4
c(NH ·H O)+4c(OH-)=3c(NH +)+4c(H+),B正确;C项,当通入HCl的物质的量是0.01 mol时,反应产生
3 2 4
NH Cl的物质的量是0.01 mol,剩余NH ·H O的物质的量是0.01 mol,溶液为等物质的量的NH Cl、
4 3 2 4
NH ·H O的混合溶液,根据电荷守恒可得c(NH +)+c(H+)=c(OH-)+c(Cl-),根据电荷守恒可知c(NH ·H O)
3 2 4 3 2
+c(NH +)=2c(Cl-),将两式联立可得c(NH +)+2c(H+)=c(NH ·H O)+2c(OH-),C错误;D项,当通入HCl的物
4 4 3 2
质的量是0.02 mol时,二者恰好反应产生NH Cl,其物质的量是0.02 mol。该盐是强酸弱碱盐,NH +发生
4 4水解反应产生NH ·H O、H+,导致NH +的物质的量比Cl-小,所以c(Cl-)>c(NH +),但盐水解程度是微弱的,
3 2 4 4
盐电离产生的离子浓度远大于弱电解质产生的离子浓度,盐水解产生的NH ·H O的浓度远小于NH +的浓度,
3 2 4
因此c(NH +)>c(NH ·H O),D错误;故选B。
4 3 2