文档内容
专题 06 化学反应速率与平衡
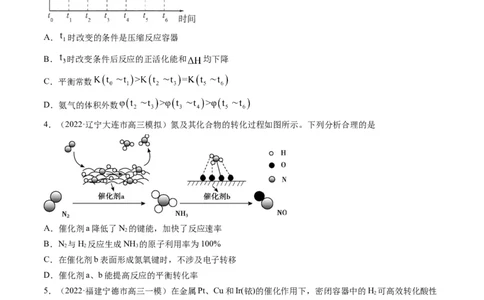
1.(2022·河北衡水中学高三调研) 催化加氢能生成乙烯和 ,按 投
料,保持压强为 ,反应达到平衡时,四种气体组分的物质的量分数 随温度 的变化如图所示。
下列说法正确的是( )
A.表示 变化的曲线是
B. 催化加氢合成 和 反应的 大于0
C.当反应达到平衡时,若增大压强,则 变小
D.图中点 对应的平衡常数 为
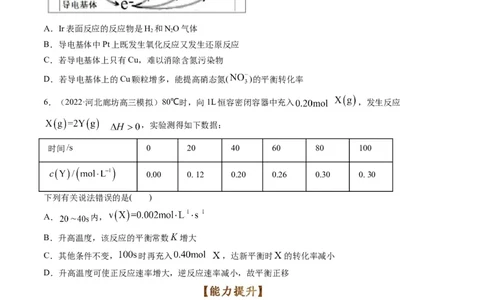
2.(2022·广东茂名高三模拟)如图表示使用不同催化剂( 和 )时 催化转化为 过程中的能量变
化。下列说法错误的是( )
(注:其中吸附在催化剂表面的物种用“· ”表示)
A.在 催化剂催化过程中,· 是最稳定的中间产物
B.· 转化为 的过程吸热
C.吸附在 表面的同种中间产物的能量高于吸附在 表面的
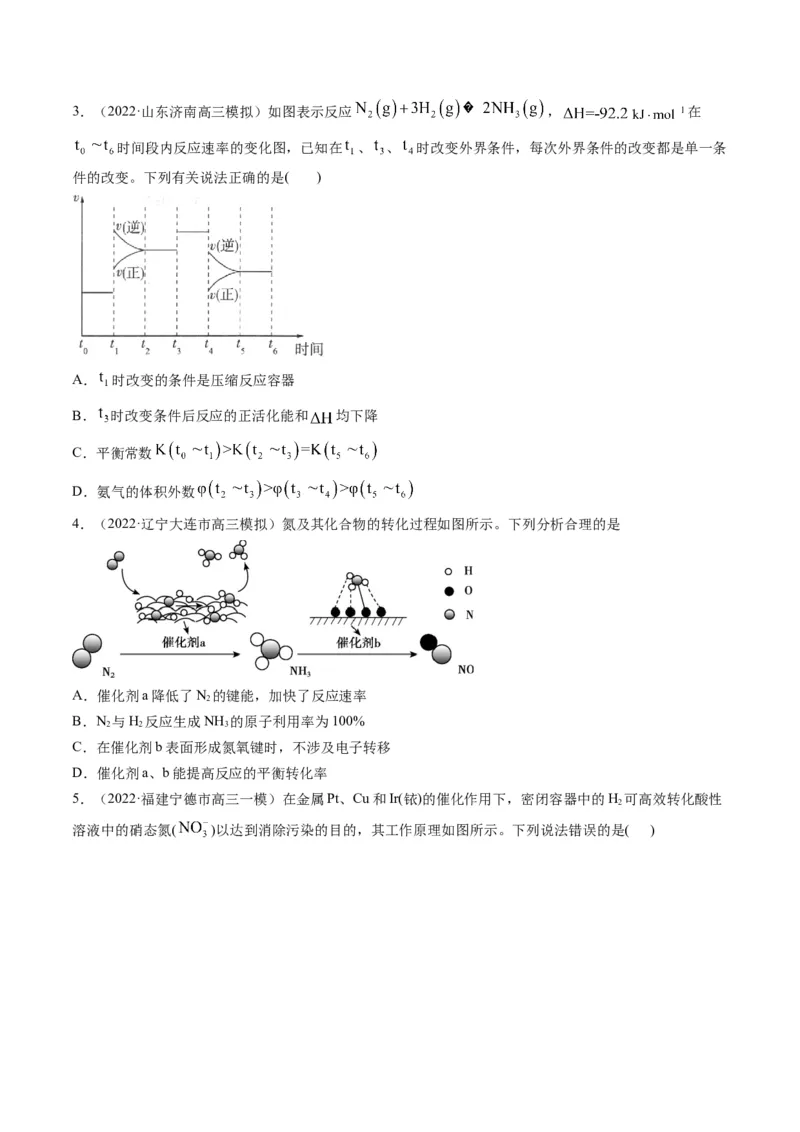
D.其他条件相同时,分别使用 、 两种催化剂, 转化为 ,其转化率相同3.(2022·山东济南高三模拟)如图表示反应 , 在
时间段内反应速率的变化图,已知在 、 、 时改变外界条件,每次外界条件的改变都是单一条
件的改变。下列有关说法正确的是( )
A. 时改变的条件是压缩反应容器
B. 时改变条件后反应的正活化能和 均下降
C.平衡常数
D.氨气的体积外数
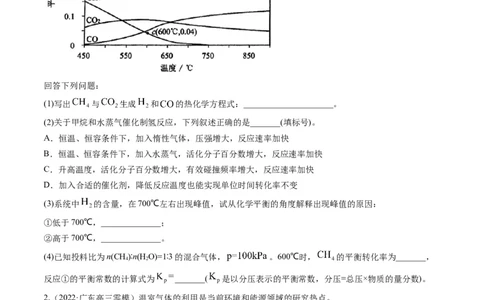
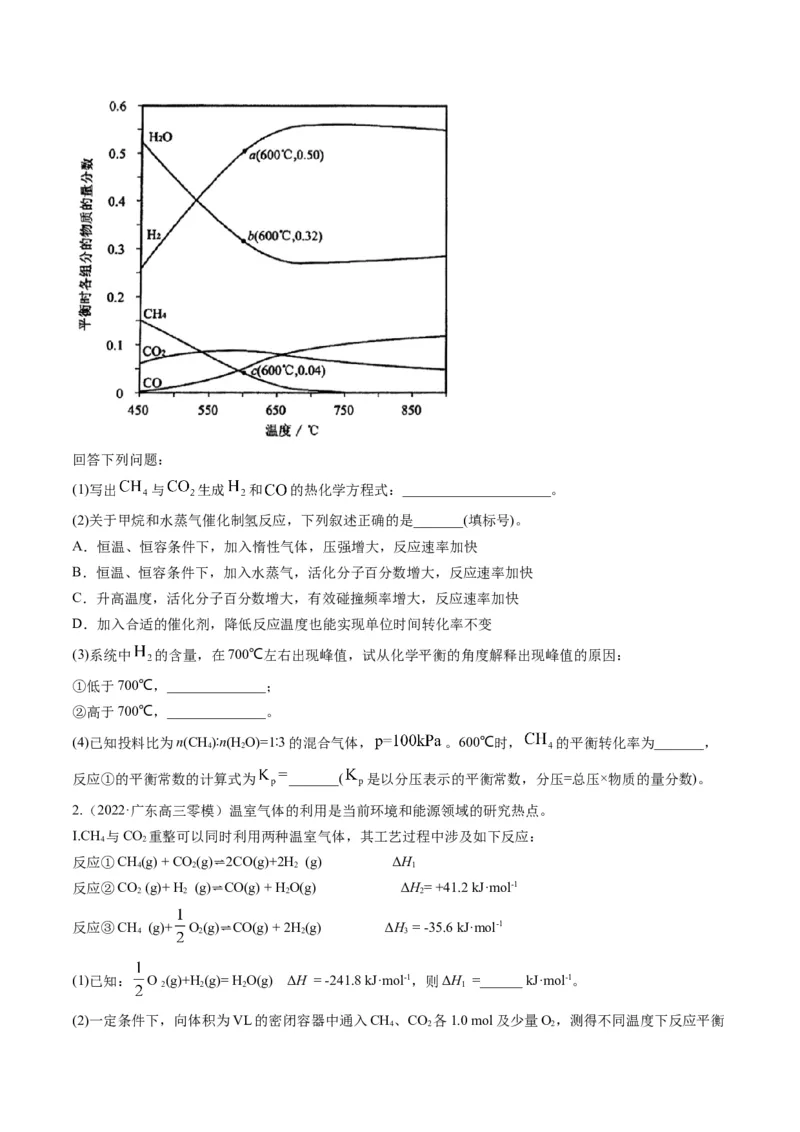
4.(2022·辽宁大连市高三模拟)氮及其化合物的转化过程如图所示。下列分析合理的是
A.催化剂a降低了N 的键能,加快了反应速率
2
B.N 与H 反应生成NH 的原子利用率为100%
2 2 3
C.在催化剂b表面形成氮氧键时,不涉及电子转移
D.催化剂a、b能提高反应的平衡转化率
5.(2022·福建宁德市高三一模)在金属Pt、Cu和Ir(铱)的催化作用下,密闭容器中的H 可高效转化酸性
2
溶液中的硝态氮( )以达到消除污染的目的,其工作原理如图所示。下列说法错误的是( )A.Ir表面反应的反应物是H 和NO气体
2 2
B.导电基体中Pt上既发生氧化反应又发生还原反应
C.若导电基体上只有Cu,难以消除含氮污染物
D.若导电基体上的Cu颗粒增多,能提高硝态氮( )的平衡转化率
6.(2022·河北廊坊高三模拟)80℃时,向1L恒容密闭容器中充入 ,发生反应
,实验测得如下数据:
时间 0 20 40 60 80 100
0.00 0. 12 0.20 0.26 0.30 0. 30
下列有关说法错误的是( )
A. 内,
B.升高温度,该反应的平衡常数 增大
C.其他条件不变, 时再充入 ,达新平衡时 的转化率减小
D.升高温度可使正反应速率增大,逆反应速率减小,故平衡正移
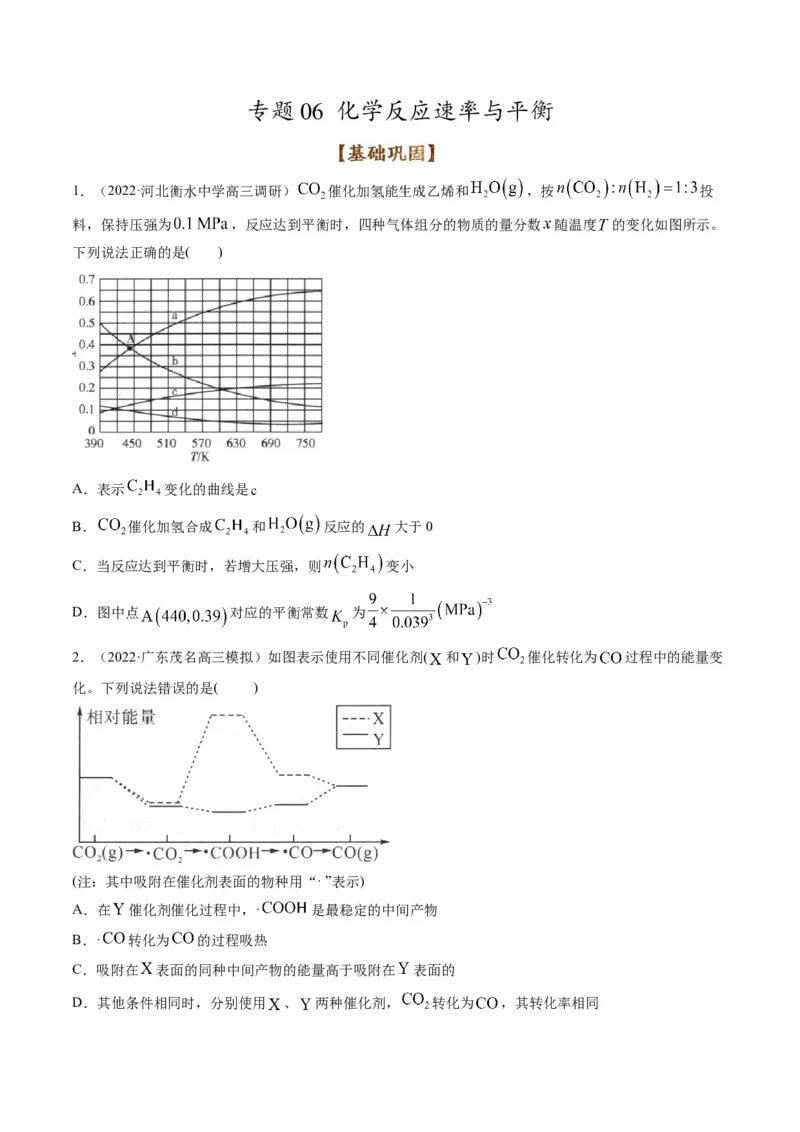
1.(2022·湖北高三零模)甲烷和水蒸气催化制氢主要有如下两个反应:
① ΔH=+206kJ/mol
② ΔH=-41kJ/mol
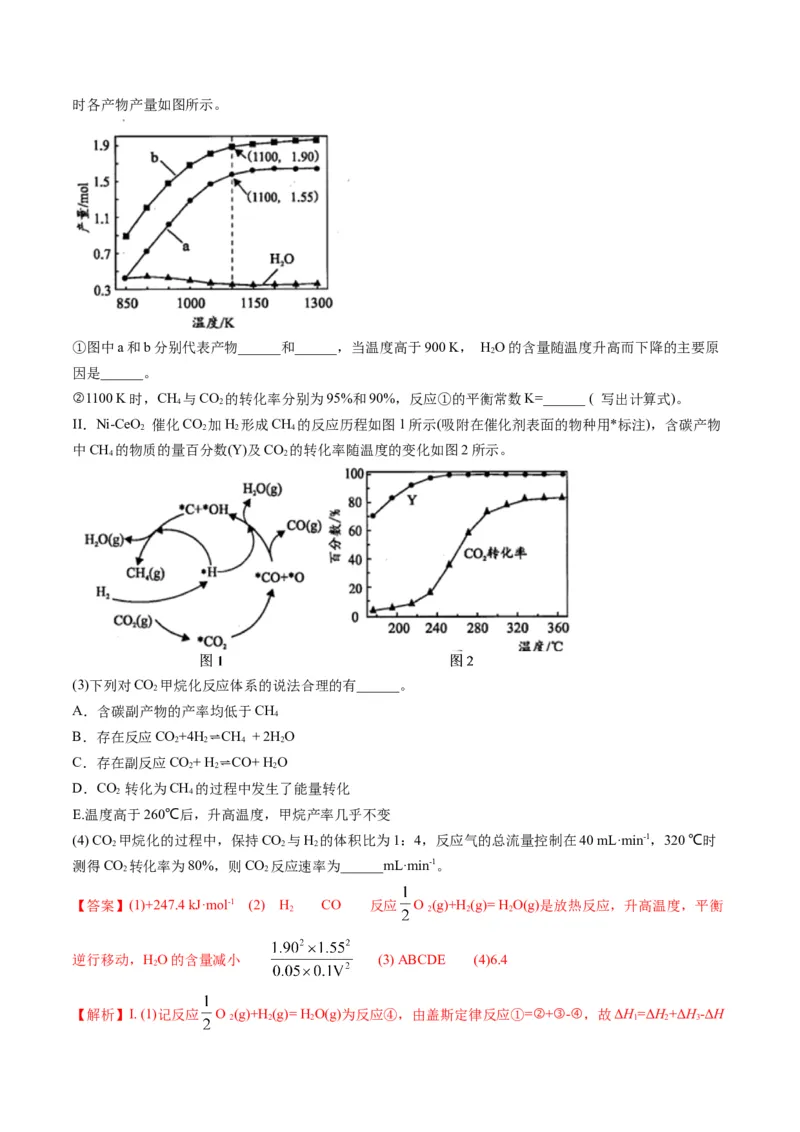
恒定压强为 时,将n(CH)∶n(H O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数
4 2
与温度的关系如图所示。回答下列问题:
(1)写出 与 生成 和 的热化学方程式:_____________________。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是_______(填标号)。
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现单位时间转化率不变
(3)系统中 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
①低于700℃,______________;
②高于700℃,______________。
(4)已知投料比为n(CH)∶n(H O)=1∶3的混合气体, 。600℃时, 的平衡转化率为_______,
4 2
反应①的平衡常数的计算式为 _______( 是以分压表示的平衡常数,分压=总压×物质的量分数)。
2.(2022·广东高三零模)温室气体的利用是当前环境和能源领域的研究热点。
I.CH 与CO 重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
4 2
反应①CH
4
(g) + CO
2
(g)⇌2CO(g)+2H
2
(g) ΔH
1
反应②CO
2
(g)+ H
2
(g)⇌CO(g) + H
2
O(g) ΔH
2
= +41.2 kJ·mol-1
反应③CH
4
(g)+ O
2
(g)⇌CO(g) + 2H
2
(g) ΔH
3
= -35.6 kJ·mol-1
(1)已知: O (g)+H(g)= H O(g) ΔH = -241.8 kJ·mol-1,则ΔH =______ kJ·mol-1。
2 2 2 1
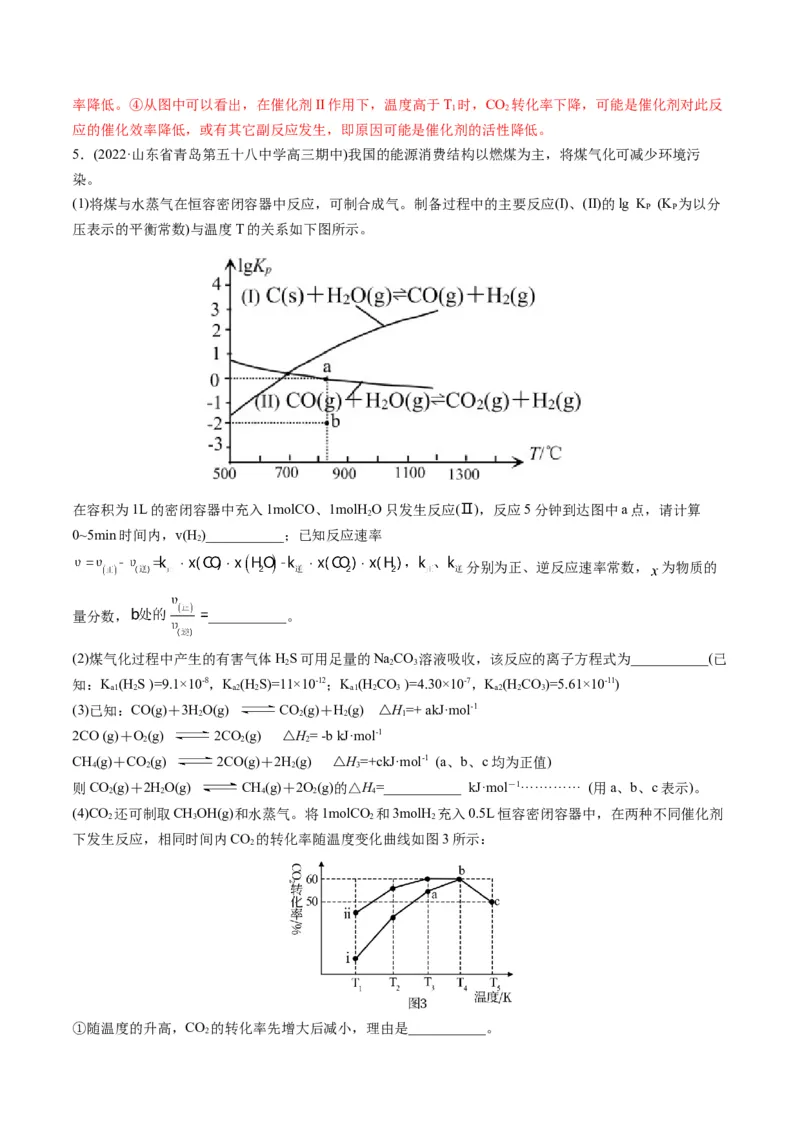
(2)一定条件下,向体积为VL的密闭容器中通入CH、CO 各1.0 mol及少量O,测得不同温度下反应平衡
4 2 2时各产物产量如图所示。
①图中a和b分别代表产物______和______,当温度高于900 K, HO的含量随温度升高而下降的主要原
2
因是______。
②1100 K时,CH 与CO 的转化率分别为95%和90%,反应①的平衡常数K=______ ( 写出计算式)。
4 2
II.Ni-CeO 催化CO 加H 形成CH 的反应历程如图1所示(吸附在催化剂表面的物种用*标注),含碳产物
2 2 2 4
中CH 的物质的量百分数(Y)及CO 的转化率随温度的变化如图2所示。
4 2
(3)下列对CO 甲烷化反应体系的说法合理的有______。
2
A.含碳副产物的产率均低于CH
4
B.存在反应CO
2
+4H 2⇌CH
4
+ 2H
2
O
C.存在副反应CO
2
+ H 2⇌CO+ H
2
O
D.CO 转化为CH 的过程中发生了能量转化
2 4
E.温度高于260℃后,升高温度,甲烷产率几乎不变
(4) CO 甲烷化的过程中,保持CO 与H 的体积比为1:4,反应气的总流量控制在40 mL·min-1,320 ℃时
2 2 2
测得CO 转化率为80%,则CO 反应速率为______mL·min-1。
2 2
【答案】(1)+247.4 kJ·mol-1 (2) H CO 反应 O (g)+H(g)= H O(g)是放热反应,升高温度,平衡
2 2 2 2
逆行移动,HO的含量减小 (3) ABCDE (4)6.4
2
【解析】I. (1)记反应 O (g)+H(g)= H O(g)为反应④,由盖斯定律反应①=②+③-④,故ΔH=ΔH+ΔH-ΔH
2 2 2 1 2 3=41.2-35.6+241.8= +247.4 kJ·mol-1
(2) ①由反应①②③可知,反应产物有CO、H 和HO,生成的H 会在反应②中与CO 反应生成CO,CO
2 2 2 2
的产量高于H,故a曲线表示产物H,b曲线表示CO;反应②是吸热反应,升高温度,有利于反应的正
2 2
向进行,HO的含量增大,但反应 O (g)+H(g)= H O(g)为放热反应,升高温度,不利于反应的正向进
2 2 2 2
行,HO的含量减小;
2
②1100 K时,CH 与CO 的转化率分别为95%、 90%,则计算得平衡时c(CH)= =
4 2 4
mol/L,c(CO)= = mol/L,由图可知,c(H )= mol/L,c(CO)= mol/L,则
2 2
反应①的平衡常数K= = = ;
II.(3)由图可知,含碳产物中CH 的物质的量百分数Y 70%,则含碳副产物的产率 30%,故含碳副产物
4
的产率均低于CH
4
,A正确;由题意及图Ni-CeO
2
催化CO
2
加H
2
形成CH
4
,故存在反应CO
2
+4H 2⇌CH
4
+
2HO,B正确;由图可知,存在CO 和 H 反应生成CO+和HO,C正确;化学反应伴随着物质变化和能
2 2 2 2
量变化,D正确;由图2可知,当温度高于260℃时,CO2的转化率还在增大,但CH 的百分含量几乎不
4
在变化,则继续升高温度甲烷产率几乎不变,E正确,故答案为ABCDE;
(4) CO 甲烷化的过程中,CO 与H 的体积比为1:4,反应气的总流量为40 mL·min-1,则1min内初始时
2 2 2
CO 的体积为40× mL=8 mL,320 ℃时CO 转化率为80%,则CO 反应速率为v = mL·min-1=6.4
2 2 2
mL·min-1。
3.(2022·上海市控江中学高三月考)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环
保、节能减排等目的。汽车尾气脱硝脱碳的主要原理为:
2NO(g)+2CO(g) N(g)+2CO (g)+Q (Q>0)。
2 2
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s 0 1 2 3 4 5
c(NO)/mol·L-1 1.00 ×10-3 4.50 × 10-4 2.50 × 10-4 1.50 × 10-4 1.00 × 10-4 1.00 ×10-4
c(CO)/mol·L-1 3.60 × 10-3 3.05 ×10-3 2.85 × 10-3 2.75 ×10-3 2.70 ×10-3 2.70 × 10-3
(1)根据表格中数据计算该反应的平衡常数K=___________。
(2)前2s内的平均反应速率 (N ) =___________ ; 达到平衡时, CO的转化率为___________。
2
(3)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO 和NO ,获得(NH )SO 的稀溶液。
2 x 4 2 4
①检验溶液中阳离子的方法是___________。②往(NH )SO 溶液中再加入少量(NH )SO 固体, 的值将___________(填“变大”、“不变”或
4 2 4 4 2 4
“变小”)
用NaOH溶液吸收SO ,并用CaO使NaOH再生:NaOH溶液 NaSO 溶液
2 2 3
(4)写出过程①的离子方程式:___________。
(5)CaO在水中存在如下转化: CaO(s)+ H O(1) →Ca(OH) (s) Ca2+ (aq)+ 2OH-(aq) 从平衡移动的角
2 2
度,简述过程②)NaOH再生的原理___________。
(6)如图是NaSO 溶液中各离子浓度的相对大小关系示意图,其中,③是___________ ( 填微粒符号)。
2 3
【答案】(1)5000 (2)1.88×10-4 25%
(3)取少量溶液于一小试管,滴加氢氧化钠溶液,微热,用湿润的红色石蕊试纸放在试管口,如果变蓝,则
证明滤液中含有铵根离子 变大
(4)2OH-+SO=SO2-+H O
2 3 2
(5)SO 2-与Ca2+生成CaSO 沉淀,平衡向正向移动,有NaOH生成
3 3
(6)OH-
【解析】(1)根据表中数据可知,三段式分析为:
故平衡常数为:K= = =5000;(2)前2s内的平均反应速率 (N )=
2
(CO)= × =1.88×10-4mol/(L•s),CO的平衡转化率=
×100%=25%;(3)①检验溶液中阳离子即H+的方法是取少量溶液于一小
4
试管,滴加氢氧化钠溶液,微热,用湿润的红色石蕊试纸放在试管口,如果变蓝,则证明滤液中含有铵根
离子;②在(NH
4
)
2
SO
4
溶液中存在水解反应,2NH
4
++H
2
O⇌NH
3
•H
2
O+H+,往(NH
4
)
2
SO
4
溶液中再加入少量 (
NH )SO 固体,水解平衡向正方向进行,但铵根的水解率减小,所以 的值将变大;(4)用NaOH
4 2 4溶液吸收SO ,并用CaO使NaOH再生:NaOH溶液 NaSO 溶液,故过程①即NaOH吸收SO 生成
2 2 3 2
NaSO 和HO,该反应的离子方程式为:2OH-+SO= SO 2-+H O;(5)过程②加入CaO,存在CaO(s)+H O
2 3 2 2 3 2 2
(l)═Ca(OH)
2
(s)⇌Ca2+(aq)+2OH-(aq),因SO
3
2-与Ca2+生成CaSO
3
沉淀,平衡向正向移动,有NaOH生成;
(6)Na SO 溶液中由于SO 2-+H O HSO -+OH-,HSO -+H O HSO +OH-,溶液显碱性,故
2 3 3 2 3 3 2 2 3
NaSO 溶液中各离子浓度的相对大小关系为:c(Na+)>c(SO 2-)>c(OH-)>c(HSO -)>c(H+),故图中③是OH-
2 3 3 3
-。
4.(2022·重庆市高三第四次质量检测考试)国家主席习近平指出,为推动实现碳达峰碳中和目标,我国将陆
续发布重点领域和行业碳达峰实施方案和一系列支撑保障措施,构建起碳达峰、碳中和“ ”政策体
系。二氧化碳加氢可转化为二甲醚,既可以降低二氧化碳排放量,也可以得到性能优良的汽车燃料。
回答下列问题:
(1)制取二甲醚的热化学方程式为:2CO(g)+6H(g) CHOCH (g)+3HO(g) ∆H,则
2 2 3 3 2
∆H=___________。
已知:①CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49.0kJ∙mol-1
2 2 3 2 1
②2CHOH(g) CHOCH (g)+HO(g) ∆H=-23.5kJ∙mol-1
3 3 3 2 2
(2)往一容积为 的恒容密闭容器中通入2molCO和6molH ,一定温度下发生反应::2CO(g)+6H(g)
2 2 2
CHOCH (g)+3HO(g),起始总压为p,20 min时达到化学平衡状态,测得CHOCH 的物质的量分
3 3 2 0 3 3
数为12.5%。
①达到化学平衡状态时,下列有关叙述正确的是___________(填字母序号)。
a.容器内气体压强不再发生改变
b.正、逆反应速率相等且均为零
c.向容器内再通入1molCO和3molH ,重新达平衡后CHOCH 体积分数增大
2 3 3
d.向容器内通入少量氦气,则平衡向正反应方向移动
②0-20 min内,用H 表示的平均反应速率v(H ) =___________,CO 的平衡转化率α(CO)=___________;
2 2 2 2
该温度下,反应的平衡常数K =___________(用含p 的式子表达,用平衡分压代替平衡浓度计算,分压=总
P 0
压×物质的量分数)。
③升高温度,二甲醚的平衡产率___________(填“增大”、“减小”或“不变”),简述理由:
___________。
④工业上,CO 与H 混合气体以一定的比例和一定流速分别通过填充有催化剂I、II的反应器,CO 转化率
2 2 2
与温度的关系如下图。在催化剂II作用下,温度高于T 时,CO 转化率下降的原因可能是_______。
1 2【答案】(1)-121.5kJ∙mol-1
(2)ac 0.1 mol·L-1·min-1 66.7% 减小 二甲醚的合成反应为放热反应,升高温度,平
衡逆向移动,二甲醚产率降低 催化剂的活性降低
【解析】(1)①CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49.0kJ∙mol-1
2 2 3 2 1
②2CHOH(g) CHOCH (g)+HO(g) ∆H=-23.5kJ∙mol-1
3 3 3 2 2
利用盖斯定律,将反应①+反应②,即得2CO(g)+6H(g) CHOCH (g)+
2 2 3 3
3HO(g)∆H=2×∆H+∆H=2×(-49.0kJ∙mol-1)+( -23.5kJ∙mol-1)= -121.5kJ∙mol-1;(2)①对于反应2CO(g)+6H(g)
2 1 2 2 2
CHOCH (g)+3HO(g),达到化学平衡状态时:a项,容器内各气体的物质的量不变,容器的体积不
3 3 2
变,压强不变,a正确;b项,达平衡时,各物质的量不变,正、逆反应速率相等但都大于零,b不正确;
c项,向容器内再通入1molCO和3molH ,相当于加压,平衡正向移动,重新达平衡后CHOCH 体积分数
2 3 3
增大,c正确;d项,向容器内通入少量氦气,反应混合气体的浓度不变,平衡不发生移动,d不正确;故
选ac;②往一容积为2L的恒容密闭容器中通入2molCO和6molH ,一定温度下发生反应:2CO(g)+
2 2
6H(g) CHOCH (g)+3HO(g),起始总压为p,20 min时达到化学平衡状态,测得CHOCH 的物
2 3 3 2 0 3 3
质的量分数为12.5%。设参加反应的CO 的物质的量为x,则可建立如下三段式:
2
则 ,x= mol。0-20 min内,用H 表示的平均反应速率v(H ) = =
2 2
,CO 的平衡转化率 ≈66.7%;达平衡时,总压强为 = ,该温度下,反应的
2
平衡常数K = = 。③依据平衡移动原理,对于放热反应,升高温度,平衡逆向移
P
动,二甲醚的平衡产率减小,理由:二甲醚的合成反应为放热反应,升高温度,平衡逆向移动,二甲醚产率降低。④从图中可以看出,在催化剂II作用下,温度高于T 时,CO 转化率下降,可能是催化剂对此反
1 2
应的催化效率降低,或有其它副反应发生,即原因可能是催化剂的活性降低。
5.(2022·山东省青岛第五十八中学高三期中)我国的能源消费结构以燃煤为主,将煤气化可减少环境污
染。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(I)、(II)的lg K (K 为以分
P P
压表示的平衡常数)与温度T的关系如下图所示。
在容积为1L的密闭容器中充入1molCO、1molH O只发生反应(Ⅱ),反应5分钟到达图中a点,请计算
2
0~5min时间内,v(H )___________;已知反应速率
2
分别为正、逆反应速率常数, 为物质的
量分数, ___________。
(2)煤气化过程中产生的有害气体HS可用足量的NaCO 溶液吸收,该反应的离子方程式为___________(已
2 2 3
知:K (H S)=9.1×10-8,K (H S)=11×10-12;K (H CO )=4.30×10-7,K (H CO)=5.61×10-11)
a1 2 a2 2 a1 2 3 a2 2 3
(3)已知:CO(g)+3HO(g) CO(g)+H(g) △H=+ akJ·mol-1
2 2 2 1
2CO (g)+O(g) 2CO(g) △H= -b kJ·mol-1
2 2 2
CH(g)+CO(g) 2CO(g)+2H(g) △H=+ckJ·mol-1 (a、b、c均为正值)
4 2 2 3
则CO(g)+2HO(g) CH(g)+2O(g)的△H=___________ kJ·mol-1············· (用a、b、c表示)。
2 2 4 2 4
(4)CO 还可制取CHOH(g)和水蒸气。将1molCO 和3molH 充入0.5L恒容密闭容器中,在两种不同催化剂
2 3 2 2
下发生反应,相同时间内CO 的转化率随温度变化曲线如图3所示:
2
①随温度的升高,CO 的转化率先增大后减小,理由是___________。
2②已知c点容器内压强为P,在T 温度反应的平衡常数K 为___________(用含P的关系式表示)
5 p
【答案】(1)0.1mol·L-1·min-1 100 (2)CO 2-+H S=HCO -+HS-
3 2 3
(3)(2a+2b-c)kJ∙mol-1
(4)b点前,反应未达平衡,随温度升高,反应速率加快,CO 转化率增大;b点后,反应已达平衡,随温度
2
升高,平衡左移,CO 转化率降低
2
【解析】(1)在容积为1L的密闭容器中充入1molCO、1molH O只发生反应(II),反应5分钟到达图中a点此
2
时lgKp=0,Kp=1。 根据化学反应速率与物质反应关系,由于加入1molCO、1molH O,反应是按1: 1物质
2
的量关系进行,剩余的CO、HO也是1: 1物质的量的关系,则反应产生的CO、H 物质的量相等,则每种
2 2 2
气体的物质的量及浓度都相同,此时n(CO)=0.5mol,c(CO)=c(H )=c(CO)=c(H O)=0.5mol/L,所以0~5min
2 2 2
时间内,v(H )= =0.1mol/(L·min);由于反应速率v=v -v =
2 (正) (逆)
,反应达到平衡时v =v ,所以K= =1 10-2,
(正) (逆)
b处的lgKp=-2,Kp=1 10-2,由于反应时c(CO)=c(H O)=1mol/L, c(CO )=c(H )=0;假设反应产生的
2 2 2
c(CO)=c(H )=bmol/L ,则平衡时c(CO)=c(H O)=(1-b)mol/L,c(CO)=c(H )=bmol/L,该反应前后体积不变,
2 2 2 2 2
则Kp= =1 10-2, 解得b= mol/L,c (CO) =c (H O)= mol/L,根据图像所知,此温度下达到平
2
衡时Kp=1,所以b处的 = =100;(2)已知:
,所以HS与 足量的NaCO 反应生成HCO -和HS-,则其离子方
2 2 3 3
程式为:CO2-+H S=HCO -+HS-;(3)已知:①CO(g)+3HO(g) CO(g)+H(g) △H=+ akJ·mol-1
3 2 3 2 2 2 1
②2CO (g)+O(g) 2CO(g) △H= -b kJ·mol-1
2 2 2
③ CH(g)+CO(g) 2CO(g)+2H(g) △H=+ckJ·mol-1 (a、b、c均为正值)
4 2 2 3
根据盖斯定律,由2 ①-2 ②-③得反应CO(g)+2HO(g) CH(g)+2O(g) △H= (2a+2b-c)kJ∙mol-1;
2 2 4 2 4
(4)①b点前,反应未达平衡,随温度升高,反应速率加快,CO 转化率增大; b点后,反应已达平衡,随
2
温度升高,平衡左移,CO 转化率降低;随温度的升高,CO 的转化率先增大后减小;②c点时容器内的压
2 2
强为P,二氧化碳的转化率为50%,列出三段式:
平衡时各物质的物质的总量为0.5mol+1.5mol+0.5mol+0.5mol=3mol,在T 温度下该反应的平衡常数K为
5。