文档内容
专题 12 综合实验设计与评价
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
1.(2023·浙江省部分校高三选考模拟考试)下列说法正确的是( )
A.甲烷中混有乙烯,可通过溴的CCl 溶液洗气
4
B.除去碱式滴定管胶管内的气泡时,将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出
C.在萃取操作中往往因为振摇而使得分液漏斗中出现大量气体,可以通过打开旋塞来放气
D.配制一定物质的量浓度溶液时,第一次转移溶液后玻璃棒应放在洁净的表面皿上
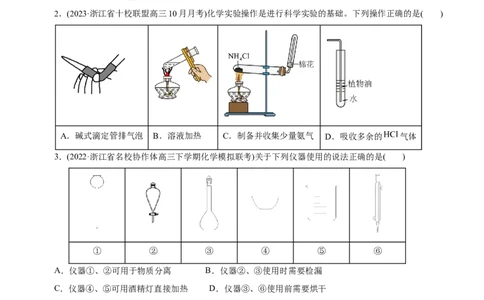
2.(2023·浙江省十校联盟高三10月月考)化学实验操作是进行科学实验的基础。下列操作正确的是( )
A.碱式滴定管排气泡 B.溶液加热 C.制备并收集少量氨气 D.吸收多余的 气体
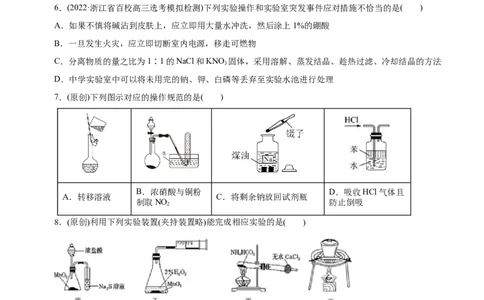
3.(2022·浙江省名校协作体高三下学期化学模拟联考)关于下列仪器使用的说法正确的是( )
① ② ③ ④ ⑤ ⑥
A.仪器①、②可用于物质分离 B.仪器②、③使用时需要检漏
C.仪器④、⑤可用酒精灯直接加热 D.仪器③、⑥使用前需要烘干
4.(2022·山东省学情高三质量检测)为完成下列各组实验,所选玻璃仪器(不考虑存放试剂的容器)和试剂
均准确、完整的是( )
实验目的 玻璃仪器 试剂
粗盐(含SO 2-、Mg2+、 烧杯、玻璃棒、普通漏
A 4 粗盐、BaCl、NaCO、NaOH、稀盐酸
Ca2+)的精制 斗 2 2 3
B 除去CuSO 溶液中Fe2+ 试管、烧杯、玻璃棒 双氧水、Cu (OH) CO、稀硫酸
4 2 2 3
C 测定稀硫酸浓度 烧杯、锥形瓶、胶头滴 待测稀硫酸、已知浓度的NaOH溶液、管、酸式滴定管、碱式
石蕊试剂
滴定管
蒸馏烧瓶、酒精灯、冷
D 石油分馏 经脱水、脱盐处理的原油、沸石
凝管、锥形瓶、牛角管
5.(2022·广东省高考研究会高考测评研究院高三阶段性调研)实验中需1.0mol·L-1的NaCO 溶液450mL,
2 3
配制时应选用的容量瓶的规格、称取NaCO 的质量和操作均最合理的是( )
2 3
A.任意规格,47.7g,一次完成 B.50mL,2.39g、重复9次完成
C.500mL,53.0g,一次完成 D.1000mL,106.0g,一次完成
6.(2022·浙江省百校高三选考模拟检测)下列实验操作和实验室突发事件应对措施不恰当的是( )
A.如果不慎将碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸
B.一旦发生火灾,应立即切断室内电源,移走可燃物
C.分离物质的量之比为1∶1的NaCl和KNO 固体,采用溶解、蒸发结晶、趁热过滤、冷却结晶的方法
3
D.中学实验室中可以将未用完的钠、钾、白磷等丢弃至实验水池进行处理
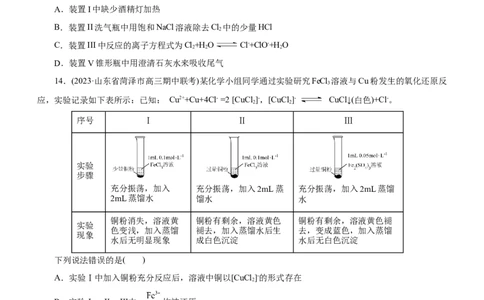
7.(原创)下列图示对应的操作规范的是( )
B.浓硝酸与铜粉 D.吸收HCl气体且
A.转移溶液 C.将剩余钠放回试剂瓶
制取NO 防止倒吸
2
8.(原创)利用下列实验装置(夹持装置略)能完成相应实验的是( )
A.装置甲比较MnO 、Cl、S的氧化性 B.装置乙(秒表未画出)测定化学反应速率
2 2
C.装置丙制备纯净的NH D.从水溶液中提取NaHSO
3 4
9.(2023·浙江省嘉兴市高三上学期联考)关于下列各装置图的叙述正确的是( )A.图①钠会先沉在试管底部,表面有气泡产生,上方的火焰呈淡蓝色
B.图②测定盐酸的浓度
C.图③用于实验室制备并收集NO
2
D.图④制备乙酸乙酯时应先加浓硫酸,再加乙醇,最后加乙酸
10.(2022•浙江省Z20联盟高三第二次联考联考)下列由实验现象所得结论不正确的是( )
A.浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
B.酸性KMnO 溶液中加入Fe O,紫色褪去,证明Fe O 在H+作用下产生Fe2+
4 3 4 3 4
C.NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解
D.NaHSO 溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO -具有氧化性
3 3
11.(2022·江苏省如皋中学高三模拟)侯德榜将氨碱法制取碳酸钠和合成氨联合起来,将制碱技术发展到新
的水平。氨碱法的反应原理为NaCl+NH +CO +H O=NaHCO ↓+NHCl,过滤所得NaHCO 可用于制纯碱。现对
3 2 2 3 4 3
过滤所得滤液进行如下实验,所得结论正确的是( )
A.用铂丝蘸取少量滤液进行焰色反应,观察到火焰呈黄色,说明滤液中含有Na+
B.取少量滤液于试管中,加热试管,将湿润的红色石蕊试纸置于试管口,试纸未变蓝,说明滤液中不含
NH +
4
C.取少量滤液,向其中加入足量稀盐酸,再加入硝酸银溶液,观察到有白色沉淀生成,说明滤液中含有
Cl-
D.取少量滤液,向其中加入适量澄清石灰水,观察到有白色沉淀生成,说明滤液中含有CO2-
3
12.(2022•浙江省普通高中强基联盟高三统一测试)下列有关实验的说法不正确的是( )
A.取5mL0.1mol•L-1KI溶液,加入1mL0.1mol•L-1FeCl 溶液,萃取分离出碘单质后,向溶液中滴加5~6滴
3
15%KSCN溶液变红,说明Fe3+并未完全转化为Fe2+
B.向淀粉溶液中加入硫酸溶液并加热4~5min得到水解液,冷却后加入少量新制氢氧化铜悬浊液,加热
至沸腾,未观察到砖红色沉淀,说明淀粉没有水解
C.氯气和甲烷体积比为4∶1的混合气体,光照一段时间后发现瓶壁上有油状液滴附着
D.实验时不慎受溴腐蚀致伤应先用苯或甘油洗伤口,再用水洗
13.(2023·江苏省苏州市八校联盟、南京市第一中学、中华中学高三联考)氯的含氧酸盐广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置制备KClO 和NaClO。下列说法正确的是( )
3
A.装置I中缺少酒精灯加热
B.装置II洗气瓶中用饱和NaCl溶液除去Cl 中的少量HCl
2
C.装置III中反应的离子方程式为Cl+H O Cl-+ClO-+H O
2 2 2
D.装置V锥形瓶中用澄清石灰水来吸收尾气
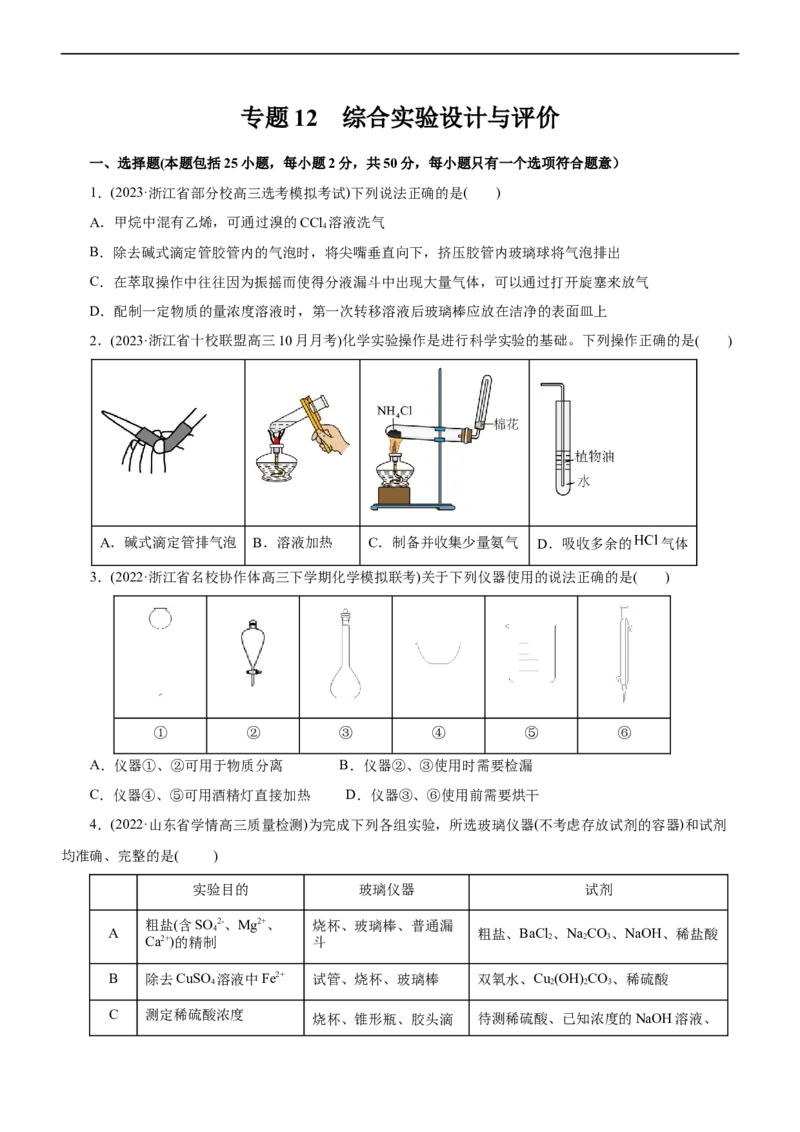
14.(2023·山东省菏泽市高三期中联考)某化学小组同学通过实验研究FeCl 溶液与Cu粉发生的氧化还原反
3
应,实验记录如下表所示:已知: Cu2++Cu+4Cl- =2 [CuCl ]-,[CuCl ]- CuCl↓(白色)+Cl-。
2 2
序号 Ⅰ Ⅱ Ⅲ
实验
步骤
充分振荡,加入 充分振荡,加入2mL蒸 充分振荡,加入2mL蒸馏
2mL蒸馏水 馏水 水
铜粉消失,溶液黄 铜粉有剩余,溶液黄色 铜粉有剩余,溶液黄色褪
实验
色变浅,加入蒸馏 褪去,加入蒸馏水后生 去,变成蓝色,加入蒸馏
现象
水后无明显现象 成白色沉淀 水后无白色沉淀
下列说法错误的是( )
A.实验Ⅰ中加入铜粉充分反应后,溶液中铜以[CuCl ]-的形式存在
2
B.实验Ⅰ、Ⅱ、Ⅲ中, 均被还原
C.实验Ⅱ中所得白色沉淀能溶于饱和NaCl溶液
D.向实验Ⅱ反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
15.(2022·山东省学情高三质量检测)硫酰氯(SO Cl)常用于制造医药品、染料等,某实验小组拟用干燥的
2 2
氯气和二氧化硫在活性炭催化下制取硫酰氯,装置如图所示:已知:SO Cl 的沸点为69℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是( )
2 2
A.装置①中,为了提高浓盐酸的利用率,可控制分液漏斗缓慢逐滴滴加
B.装置②中试剂是饱和食盐水,装置③中试剂是浓硫酸
C.装置④需要热水浴,控制温度不超69℃,装置⑤需要冰水浴
D.“尾气处理”时需在装置⑤后接装有碱石灰的干燥管
16.(2022·江苏省连云港市高三期中调研)硫代硫酸钠(Na SO),又名大苏打、海波,可以看成是硫酸钠中
2 2 3
一个氧原子被硫原子取代的产物(SO 2-结构如图所示),易溶于水。 硫代硫酸钠(Na SO)可作为照相业的定影
4 2 2 3
剂,反应原理为AgBr+2Na SO=Na [Ag(S O)]+ NaBr。
2 2 3 3 2 3 2
下图是实验室模拟工业制备NaSO 的装置示意图,下列说法不正确的是( )
2 2 3
A.不能用98.3%硫酸来代替75%硫酸
B.装置乙和装置丁都有防止倒吸的作用
C.装置丙中发生的离子方程式为: 4SO + 2OH— + 2S2—=3 S O2-+ H O
2 2 3 2
D.反应结束后将K 上端连接导管通入NaOH溶液中,然后关闭K 打开K
1 2 117.(原创)下列实验方案设计、现象和结论都正确的是( )
编号 目的 方案设计 现象和结论
探究NaClO溶液的酸 把NaClO溶液滴到pH试纸上 pH=10,则NaClO溶液水解显碱
A
碱性 性
分别在20℃、30℃下,取0.1
探究反应速率与温度 mol·L-1KI溶液,向其中先加入 30℃下出现蓝色的时间短,则温
B
的关系 0.1 mol·L-1的硫酸,再加入淀粉 度越高反应速率越快
溶液
向酸性KMnO 和HC O 的混合 若生成气体的速率加快,溶液迅
探究MnSO 有催化作 4 2 2 4
C 4 液中加入一小块MnSO 速褪色,则MnSO 可能是该反应
用 4 4
的催化剂
两支试管各盛0.1mol/L4mL酸
加入0.2mol/L草酸溶液试管中,
探究反应速率与浓度 性高锰酸钾溶液,分别加入
D 高锰酸钾溶液褪色更快,则反应
的关系 0.1mol/L2mL草酸溶液和
物浓度越大,反应速率越快
0.2mol/L2mL草酸溶液
18.(2022·浙江省高三下学期高考选考科目联考)下列方案设计、现象和结论都正确的是( )
选项 目的 方案设计 现象和结论
鉴别同为白色粉末 分别取少量晶体于试管中,加入足量 若试纸不变蓝色,说明
状晶体的尿素 浓NaOH溶液加热,在试管口放置湿 该晶体为尿素,若试纸
A
[CO(NH)]和氯化 润的红色石蕊试纸,观察试纸是否变 变蓝色,说明该晶体为
2 2
铵(NH Cl) 色 氯化铵
4
若加热时试管口出现小
检验钠盐试剂柜中 取少量晶体于试管中,加热,观察现
水珠,加盐酸后产生无
某瓶标签残破的纯 象;冷却后加入足量盐酸,观察是否
B 色无味气体,且能使石
净白色晶体是不是 产生无色无味气体,并通入澄清石灰
灰水变浑浊,则该试剂
NaHCO 水
3 为NaHCO
3
探究人体汗液中是
若溶液呈现紫色,则汗
否含有氨基酸 取1mL汗液,加入5滴0.1%茚三酮溶
C 液中可能含有氨基酸,
液加热至沸腾,观察现象
但也可能是含有蛋白质
在试管甲中加入1mL0.01mol·L-1高锰
酸钾溶液和2mL蒸馏水,试管乙中加 若试管乙中溶液紫色先
验证反应物浓度增
D 入2mL0.01mol·L-1高锰酸钾溶液和 褪去,则反应物浓度增
大可加快反应速率
1mL蒸馏水,再同时向两试管加入 大时,反应速率增大
1mL0.1mol·L-1草酸溶液,观察现象
19.(2022·浙江省百校高三选考模拟检测)下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
检验溶液中是 取少量该溶液于试管中,通入足量
A 若有白色沉淀产生,则该溶液中含有Ca2+
否含有Ca2+ CO
2比较HCl与HI 将AgCl固体加入水中,再向其中滴
B 若固体由白色变为黄色,则HI酸性强
的酸性强弱 入几滴HI
AlCl 溶液的烧杯中出现白色沉淀后不溶
比较Al与Cu 将足量氨水分别滴入盛有AlCl 溶 3
C 3 解,CuCl 溶液的烧杯中出现蓝色沉淀后
的金属性强弱 液、CuCl 溶液的烧杯中,观察现象 2
2 溶解,金属性强弱:Al>Cu
苯和液溴在FeBr 催化下发生反应,
验证苯和液溴 3 若紫色石蕊试液变红,则苯和液溴发生取
D 将得到的气体通过足量CCl 后通入
发生取代反应 4 代反应
紫色石蕊试液中
20.(2022·浙江省金丽衢十二校、七彩联盟高三阶段性联考)下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
铝片表面未见紫红色固体,
探究铝在浓硝酸中会形成 将去除氧化膜的铝片放入浓硝酸中,片
A 说明铝片表面已形成致密的
致密氧化膜 刻后取出用水洗净,放入硫酸铜溶液
氧化膜
证明Cu与浓硫酸反应后的 取2mL反应后的混合液,加水稀释, 若稀释液 pH<7,证明
B
混合液中存在HSO 冷却至室温后测溶液pH HSO 有剩余
2 4 2 4
探究乙醇在油脂皂化反应 向2mL植物油中加入2mL40%的NaOH 最终溶液不分层,说明乙醇
C
中的作用 溶液,再加入 乙醇,振荡 能催化油脂的皂化反应
在两支试管a、b中各加2mL5%H O 溶 若a中产生气泡快于b中,
探究Fe3+、Cu2+对HO 溶 2 2
D 2 2 液,分别滴入0.1mol·L-1 FeCl 溶液和 则说明Fe3+的催化效果强于
液分解的催化效果强弱 3
0.1mol·L-1 CuSO 溶液0.5mL Cu2+
4
21.(2022·浙江省名校协作体高三下学期化学模拟联考)根据下列实验操作和现象所得到的结论正确的是(
)
选项 实验操作和现象 结论
A 向某溶液中先加入氯水,再滴加KSCN溶液,溶液变红色 原溶液中可能含有Fe3+
B 向黄色的硝酸铁溶液中滴加氢碘酸,溶液变为紫红色 氧化性Fe3+>I-
C 向苯酚溶液中滴加少量浓溴水,振荡,无白色沉淀 苯酚浓度低
D 取6%的HO 溶液于两支试管中,分别加入0.1g的CuO
2 2 Fe O 比CuO的催化效果好
和0.1g的Fe O 粉末,记录10s内收集到的O 体积后者多 2 3
2 3 2
22.(2022·浙江省宁波“十校”高三下学期联考)下列实验方案设计、现象和结论中正确的是( )
选项 实验方案设计 现象和结论
取A、B两支试管,各加入4mL0.5mol·L-1 A、B中溶液均褪色且B中褪色快,
A KMnO,然后向A中加入 说明其他条件不变时,反应物浓度
4
2mL0.1mol·L-1HC O,同时向B中加入 越大,反应速率越快
2 2 42mL0.2mol·L-1HC O
2 2 4
将pH相同的NaClO 溶液和CHCOONa溶液均 pH(NaClO)>pH(CHCOONa),说明
B 3 3
稀释10倍 HClO酸性弱于CHCOOH
3
鉴别NaCl和NaNO 时,分别取少量固体于两支
C 2 产生白色沉淀的试管内为NaCl
试管中,加水溶解,再滴加AgNO 溶液
3
将乙醇和PO 共热产生的气体依次通入足量的 高锰酸钾溶液褪色,证明发生了消
D 2 5
KOH溶液、稀酸性高锰酸钾溶液 去反应
23.(2022·浙江省十校联盟高三下学期第二次联考)下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
检验某无色溶液中 取少量该溶液于试管中,加稀硝酸 若有白色沉淀生成,则该溶液中一定
A
是否含有SO 2- 酸化,再加入硝酸钡溶液 含有SO 2-
4 4
取2支试管,向2支试管中各加入5
探究不同金属离于
mL 6%HO 溶液,分别向试管中各 相同时间内产生气泡多的,则催化效
B 对HO 分解速率的 2 2
2 2 加入1mL0.1mol·L-1 FeCl 溶液和 果好
影响 3
0.1mol·L-1 CuSO 溶液
4
判断某有机物是否 取2mL样品溶液于试管中,加入 若产生砖红色沉淀,则该有机物属于
C
为醛类 5~6滴新制氢氧化铜,加热 醛类
检验某无色气体是 若通入气体后品红溶液褪色,加热该
D 将气体通入品红溶液中,再加热
否为SO 褪色溶液能恢复红色,则一定为SO
2 2
24.(2022·浙江省浙南名校高三联考)下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
在试管中加入2mL淀粉溶液和少量稀硫
若溶液未变蓝,则淀粉已
A 探究淀粉水解程度 酸,加热3-4分钟,冷却后加入NaOH溶液
完全水解
至碱性,再滴加碘水
在试管中加入2克PO 并注入4mL95%的乙 若溴水褪色,则乙醇脱水
B 探究乙醇脱水产物 2 5
醇,加热,将产生的气体通入溴水中 产物有乙烯生成
若先生成白色沉淀,后产
探究Cu(OH) 和
2 向NaOH溶液中加入一定量的MgCl 溶液, 生蓝色沉淀,则证明
C Mg(OH) 的溶解度大 2
2 充分反应后再加少量的CuCl 溶液 Cu(OH) 比Mg(OH) 溶解
小 2 2 2
度小
检验某溶液中是否 取少量该溶液于试管中,加少量硫酸酸化的 若KMnO 溶液褪色,则该
D 4
含有NO -离子 KMnO 溶液 溶液中含有NO -离子
2 4 2
25.(原创)根据下列实验操作和现象所得到的结论不正确的是( )
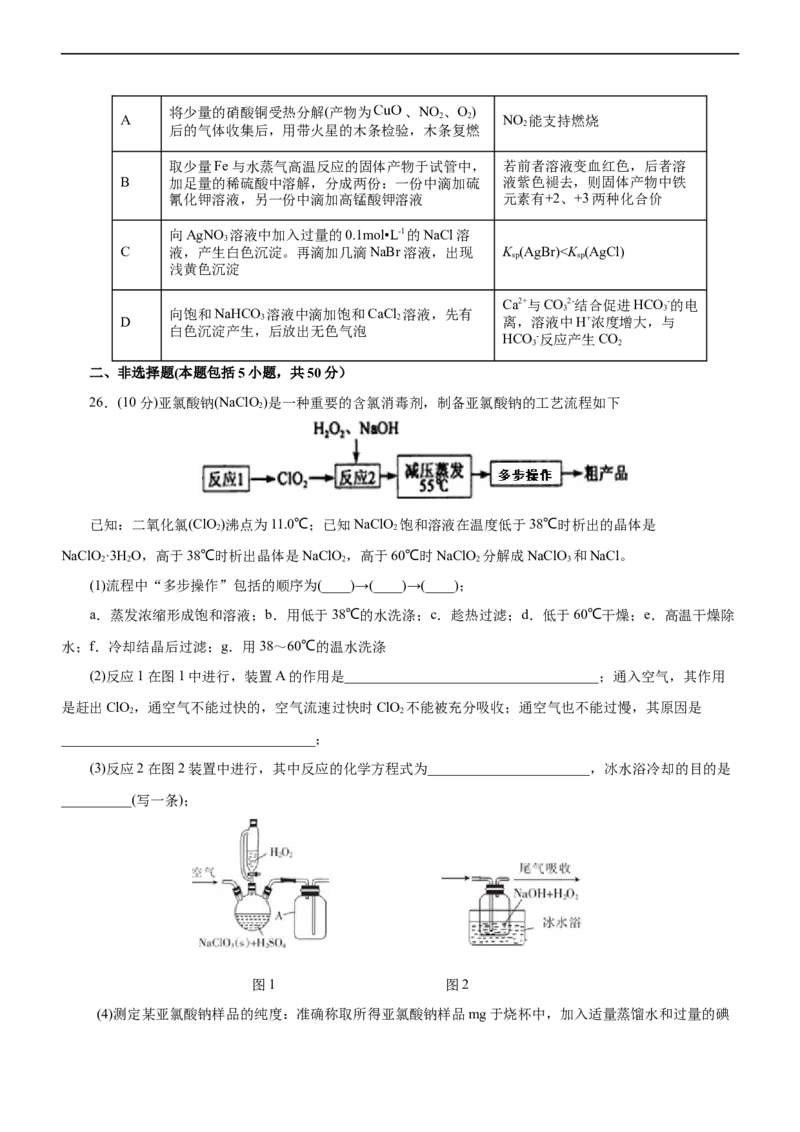
选项 实验操作和现象 实验结论将少量的硝酸铜受热分解(产物为 、NO 、O)
A 2 2 NO 能支持燃烧
2
后的气体收集后,用带火星的木条检验,木条复燃
取少量Fe与水蒸气高温反应的固体产物于试管中, 若前者溶液变血红色,后者溶
B 加足量的稀硫酸中溶解,分成两份:一份中滴加硫 液紫色褪去,则固体产物中铁
氰化钾溶液,另一份中滴加高锰酸钾溶液 元素有+2、+3两种化合价
向AgNO 溶液中加入过量的0.1mol•L-1的NaCl溶
3
C 液,产生白色沉淀。再滴加几滴NaBr溶液,出现 K (AgBr)