文档内容
专题 13 盐类的水解
2021年化学高考题
一、单选题
c2(M)
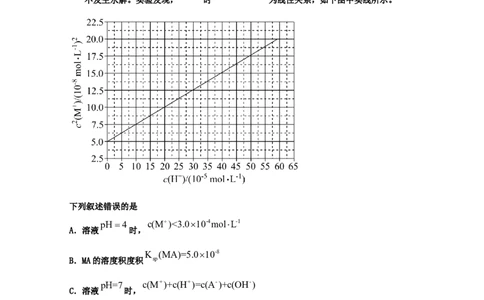
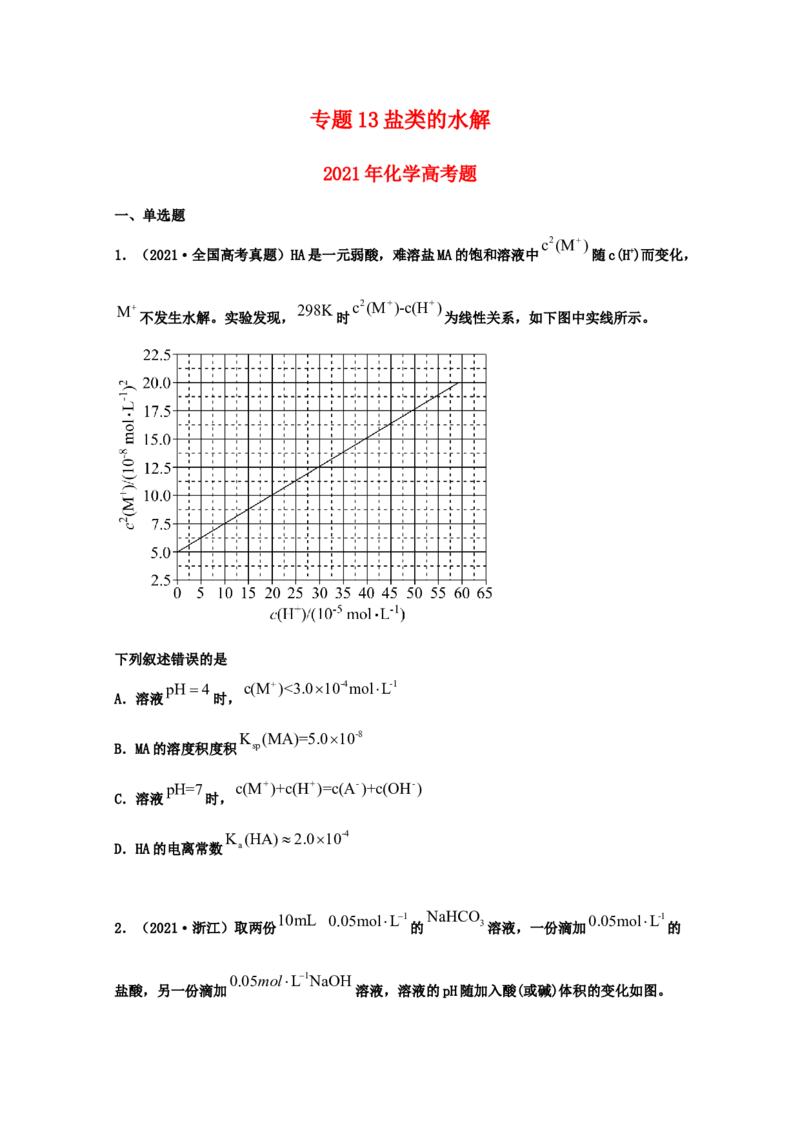
1.(2021·全国高考真题)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化,
M 298K
c2(M+)-c(H+)
不发生水解。实验发现, 时 为线性关系,如下图中实线所示。
下列叙述错误的是
pH4 c(M)<3.010-4molL-1
A.溶液 时,
K (MA)=5.010-8
B.MA的溶度积度积 sp
pH=7 c(M+)+c(H+)=c(A-)+c(OH-)
C.溶液 时,
K (HA)2.010-4
D.HA的电离常数 a
10mL 0.05molL1 NaHCO 0.05molL-1
2.(2021·浙江)取两份 的 3溶液,一份滴加 的
0.05molL1NaOH
盐酸,另一份滴加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是
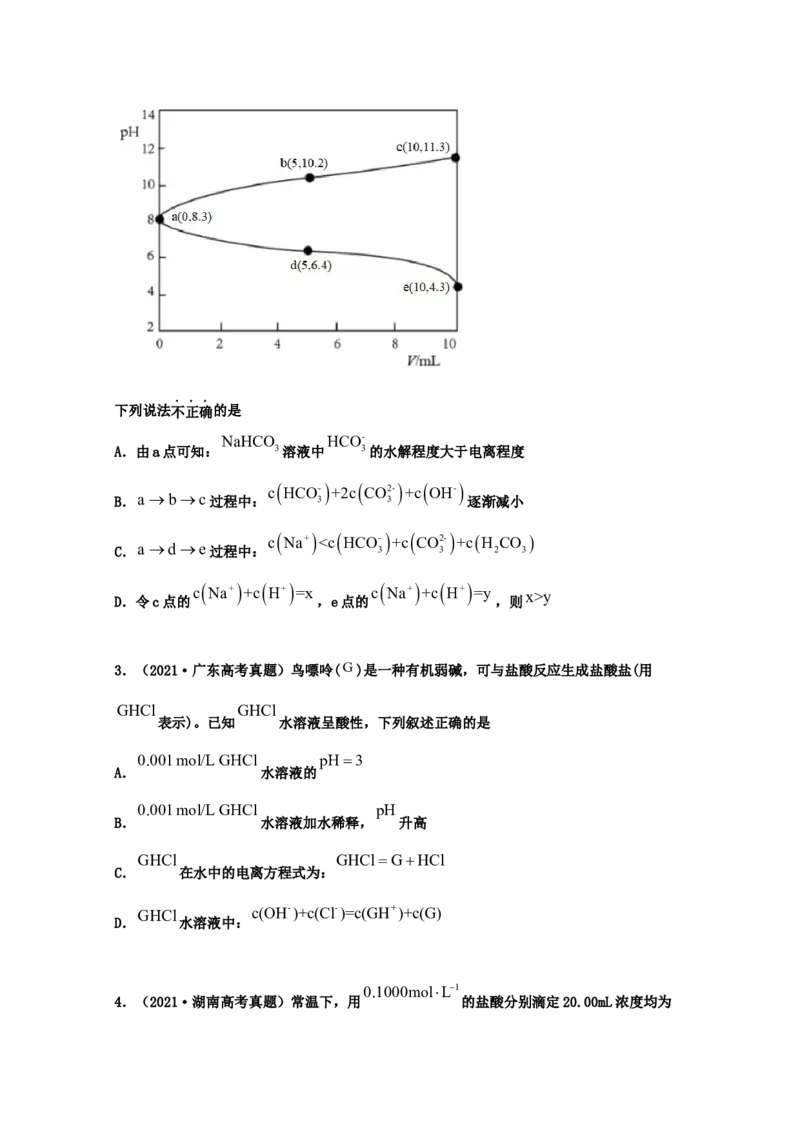
NaHCO HCO-
A.由a点可知: 3溶液中 3的水解程度大于电离程度
c
HCO-
+2c
CO2-
+c
OH-
B.a bc过程中: 3 3 逐渐减小
c Na+ y
D.令c点的 ,e点的 ,则
3.(2021·广东高考真题)鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用
GHCl GHCl
表示)。已知 水溶液呈酸性,下列叙述正确的是
0.001mol/LGHCl pH3
A. 水溶液的
0.001mol/LGHCl pH
B. 水溶液加水稀释, 升高
GHCl GHClGHCl
C. 在水中的电离方程式为:
GHCl
c(OH-)+c(Cl-)=c(GH+)+c(G)
D. 水溶液中:
0.1000molL1
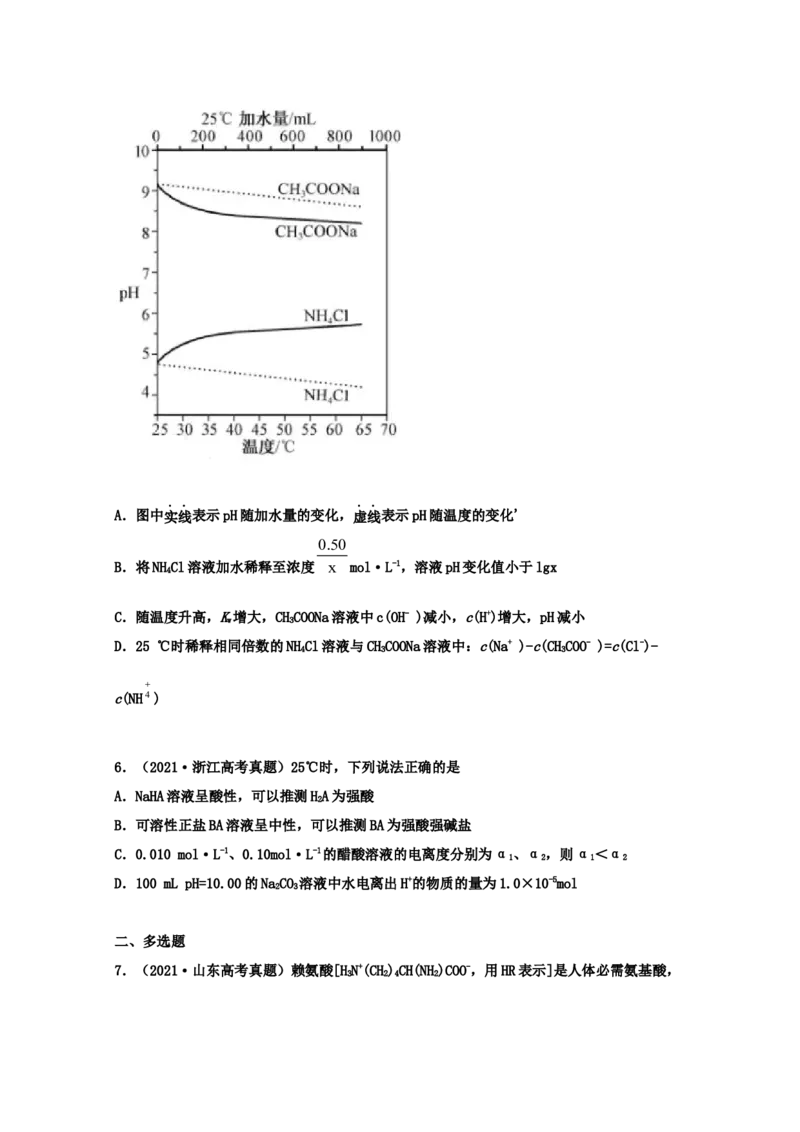
4.(2021·湖南高考真题)常温下,用 的盐酸分别滴定20.00mL浓度均为NaX、NaY、NaZ
0.1000molL1
三种一元弱酸的钠盐 溶液,滴定曲线如图所示。下列
判断错误的是
c
Na
c
X
c
OH
c
H
A.该NaX溶液中:
K (HX) K (HY) K (HZ)
B.三种一元弱酸的电离常数: a a a
c
X
c
Y
c
Z
C.当pH7时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
c
X
c
Y
c
Z
c
H
c
OH
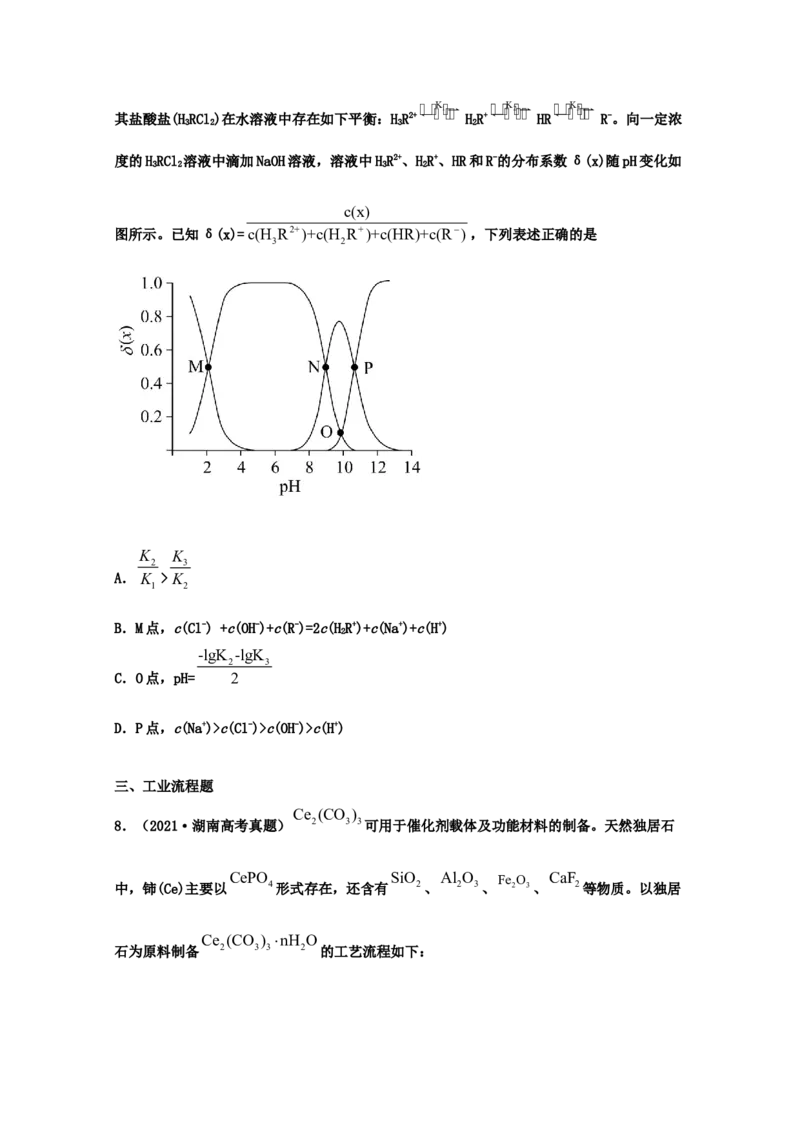
5.(2021·浙江高考真题)实验测得10 mL 0.50 mol·L-1NHCl溶液、10 mL
4
0.50mol·L-1CHCOONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时
3
CHCOOH和NH·HO的电离常数均为1.8×10-5.下列说法不正确的是
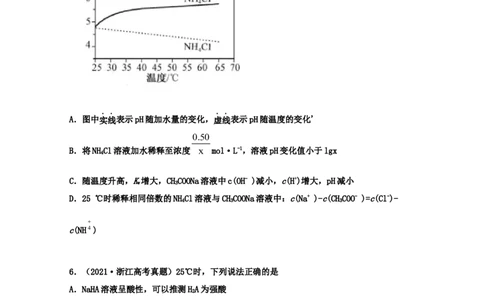
3 3 2A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
0.50
B.将NHCl溶液加水稀释至浓度 x mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NHCl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-
4 3 3
c(NH4)
6.(2021·浙江高考真题)25℃时,下列说法正确的是
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α、α,则α<α
1 2 1 2
D.100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
二、多选题
7.(2021·山东高考真题)赖氨酸[HN+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,
3 2 4 2其盐酸盐(HRCl)在水溶液中存在如下平衡:HR2+ K 1 HR+ K 2 HR K 3 R-。向一定浓
3 2 3 2
度的HRCl 溶液中滴加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如
3 2 3 2
c(x)
图所示。已知δ(x)=c(H R2+)+c(H R+)+c(HR)+c(R) ,下列表述正确的是
3 2
K K
2 3
A. K >K
1 2
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(HR+)+c(Na+)+c(H+)
2
-lgK -lgK
2 3
C.O点,pH= 2
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
三、工业流程题
Ce (CO )
8.(2021·湖南高考真题) 2 3 3可用于催化剂载体及功能材料的制备。天然独居石
CePO SiO Al O Fe O CaF
中,铈(Ce)主要以 4形式存在,还含有 2、 2 3、 2 3、 2等物质。以独居
Ce (CO ) nH O
石为原料制备 2 3 3 2 的工艺流程如下:回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
(3)滤渣Ⅲ的主要成分是_______(填化学式);
(4)加入絮凝剂的目的是_______;
Ce (CO ) nH O
(5)“沉铈”过程中,生成 2 3 3 2 的离子方程式为_______,常温下加入的
NH HCO NH H O
4 3溶液呈_______(填“酸性”“碱性”或“中性”)(已知: 3 2 的
K 1.75105 H CO K 4.4107 K 4.71011
b , 2 3的 al , a2 );
FePO Li CO C H O FePO
(6)滤渣Ⅱ的主要成分为 4,在高温条件下, 2 3、葡萄糖( 6 12 6)和 4可
H O
制备电极材料 LiFePO 4,同时生成CO和 2 ,该反应的化学方程式为_______
2021年化学高考模拟题
一、单选题
1.(2021·九龙坡区·重庆市育才中学高三三模)室温下,用mmol/L的二甲胺[(CH)NH]溶
3 2
液(二甲胺在水中的电离与一水合氨相似)滴定10.00mL0.1mol/L的盐酸溶液。溶液pH随加入
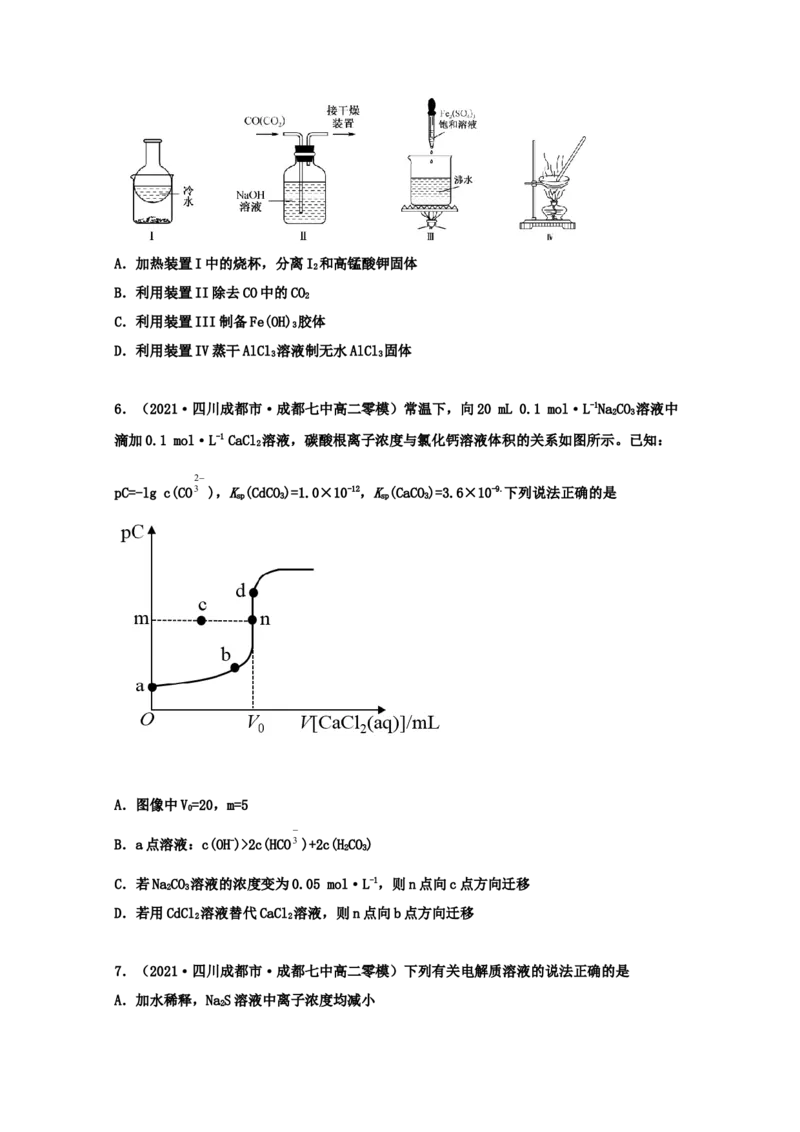
二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是A.本实验应该选择酚酞作指示剂
0.1
B.室温下,K [(CH ) NHH O] 107
b 3 2 2 m0.1
C.a点溶液中水的电离程度最大
+
D.b点溶液中存在:c[(CH)NH2]>c(OH-)>c(Cl-)>c(H+)
3 2
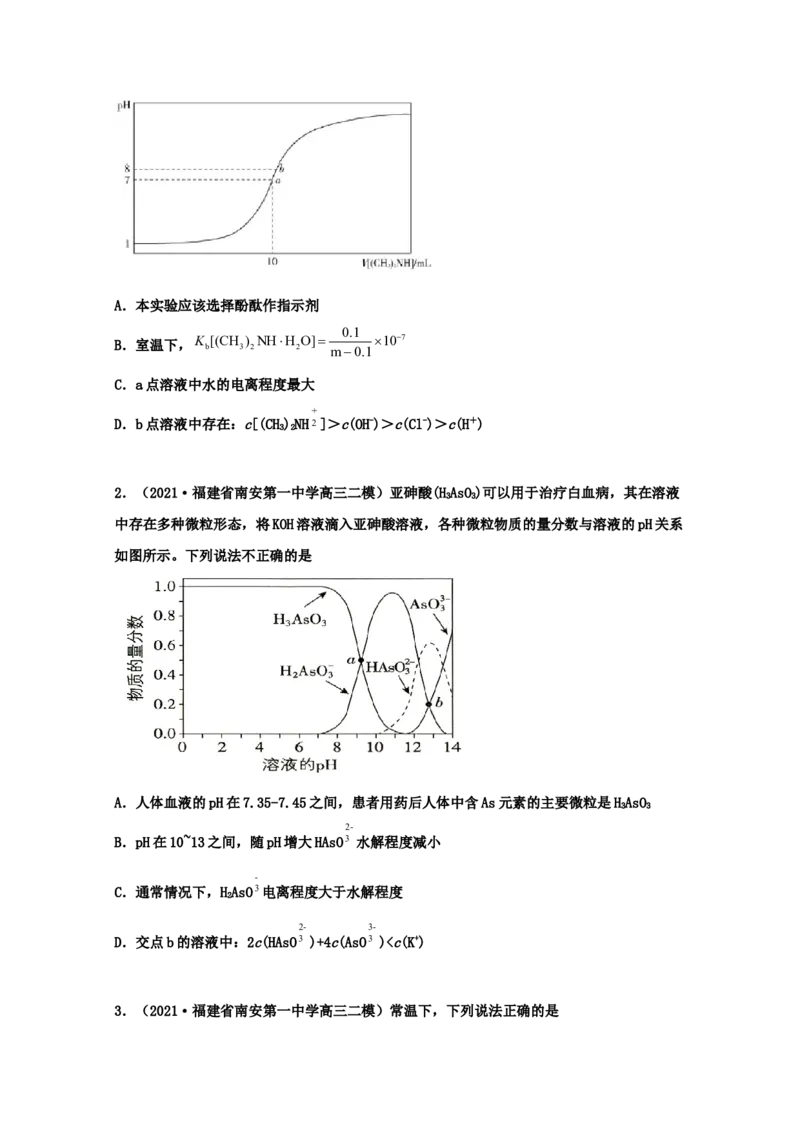
2.(2021·福建省南安第一中学高三二模)亚砷酸(HAsO)可以用于治疗白血病,其在溶液
3 3
中存在多种微粒形态,将KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液的pH关系
如图所示。下列说法不正确的是
A.人体血液的pH在7.35-7.45之间,患者用药后人体中含As元素的主要微粒是HAsO
3 3
2-
B.pH在10~13之间,随pH增大HAsO3 水解程度减小
-
C.通常情况下,HAsO3电离程度大于水解程度
2
2- 3-
D.交点b的溶液中:2c(HAsO3 )+4c(AsO3 )2c(HCO3 )+2c(HCO)
2 3
C.若NaCO 溶液的浓度变为0.05 mol·L-1,则n点向c点方向迁移
2 3
D.若用CdCl 溶液替代CaCl 溶液,则n点向b点方向迁移
2 2
7.(2021·四川成都市·成都七中高二零模)下列有关电解质溶液的说法正确的是
A.加水稀释,NaS溶液中离子浓度均减小
2B.0.1 mol/L NaOH溶液中滴加等体积等浓度醋酸溶液,溶液的导电性增强
C.pH相同的①CHCOONa②NaHCO③NaClO三种溶液的c(Na+):①>②>③
3 3
D.向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH﹣)/c(NH·HO)增大
3 2
c(HX) c(HX)
8.(2021·浙江高三其他模拟)已知:p[c(X-) ]=-lg[c(X-) ]。室温下向HX溶液中滴加
c(HX)
等物质的量浓度的NaOH溶液,溶液pH随p[c(X-) ]变化关系如图所示。下列说法正确的是
A.a点溶液中:10c(Na+)=c(HX)
B.溶液中由水电离出的c(H+):a>b>c
C.b点溶液中:c(Na+)+c(H+)=c(HX)+c(OH-)
D.当溶液呈中性时:c(Na+)=c(HX)
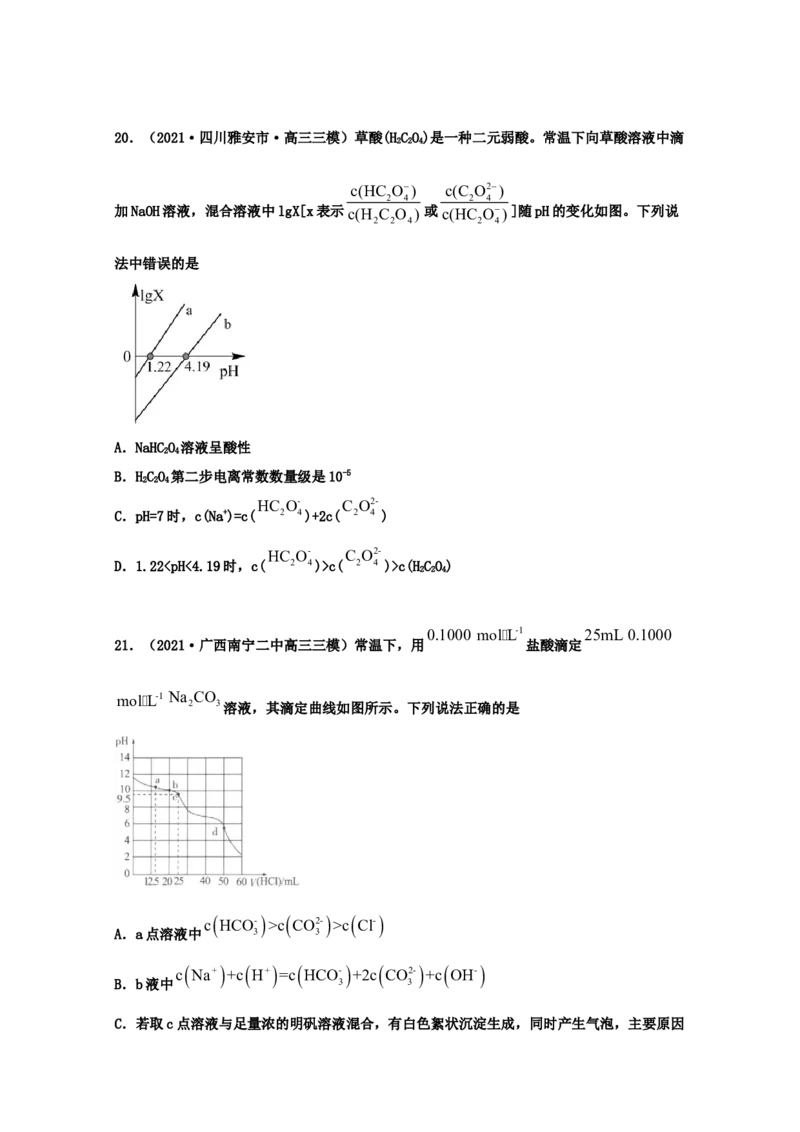
9.(2021·河南新乡市·新乡县一中高三其他模拟)为测定某二元弱酸HA与NaOH溶液反
2
应过程中溶液pH与粒子关系,在25℃时进行实验,向HA溶液中滴加NaOH溶液,混合溶液
2
c(HA-)
c(A2-)
中lgX[X表示c(H A) 或 c(HA-) ]随溶液pH的变化关系如图所示。下列说法正确的是
2c(HA-)
A.直线II中X表示的是c(H A)
2
B.当pH=3.81时,溶液中c(HA-):c(HA)=10:1
2
C.0.1 mol·L-1 NaHA溶液中:c(Na+)>c(HA-)>c(HA)>c(A2-)
2
D.当pH=6.91时,对应的溶液中,3c(A2-)=c(Na+)+c(H+)-c(OH-)
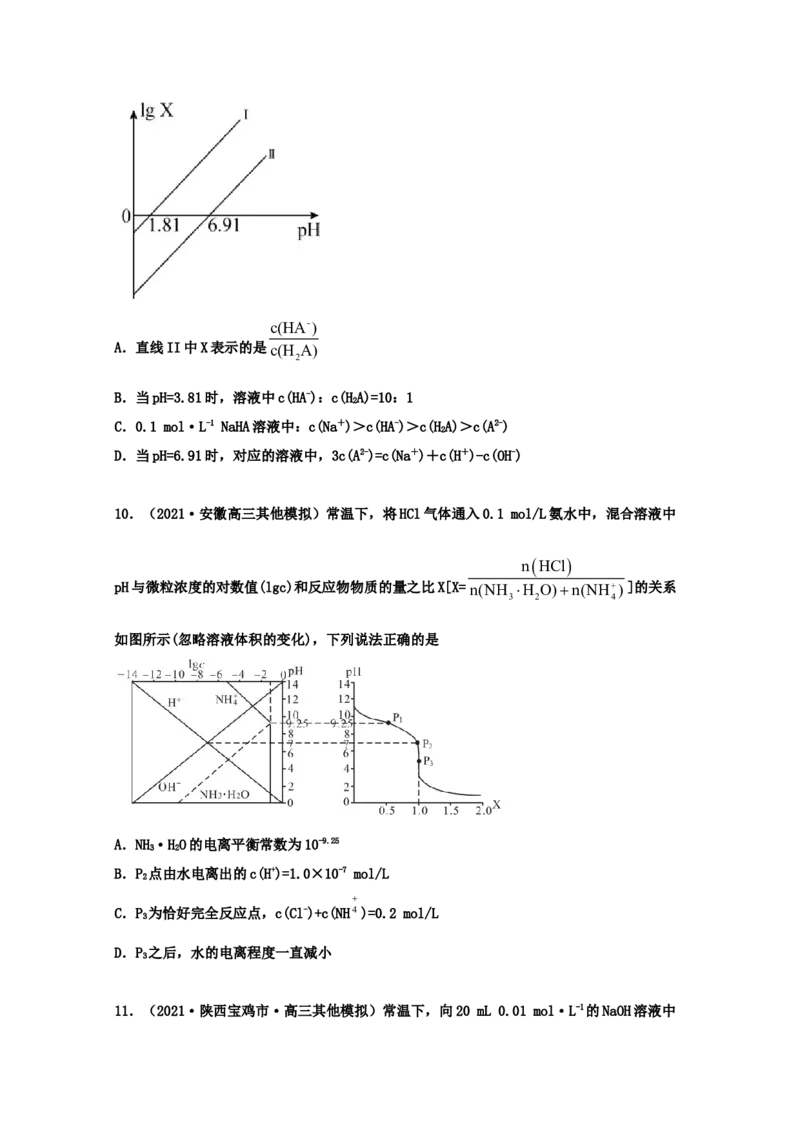
10.(2021·安徽高三其他模拟)常温下,将HCl气体通入0.1 mol/L氨水中,混合溶液中
nHCl
pH与微粒浓度的对数值(lgc)和反应物物质的量之比X[X=n(NH H O)n(NH)]的关系
3 2 4
如图所示(忽略溶液体积的变化),下列说法正确的是
A.NH·HO的电离平衡常数为10-9.25
3 2
B.P 点由水电离出的c(H+)=1.0×10-7 mol/L
2
C.P 为恰好完全反应点,c(Cl-)+c(NH4)=0.2 mol/L
3
D.P 之后,水的电离程度一直减小
3
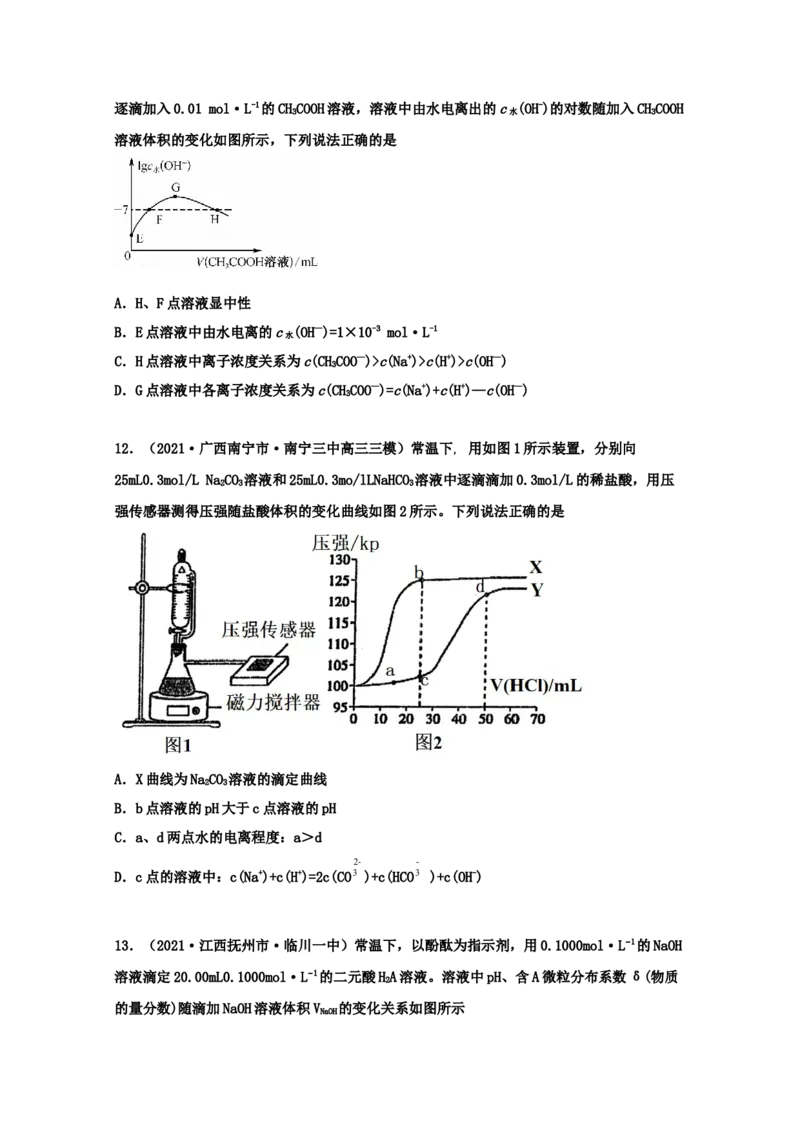
11.(2021·陕西宝鸡市·高三其他模拟)常温下,向20 mL 0.01 mol·L-1的NaOH溶液中逐滴加入0.01 mol·L-1的CHCOOH溶液,溶液中由水电离出的c (OH-)的对数随加入CHCOOH
3 水 3
溶液体积的变化如图所示,下列说法正确的是
A.H、F点溶液显中性
B.E点溶液中由水电离的c (OH—)=1×10-3 mol·L-1
水
C.H点溶液中离子浓度关系为c(CHCOO—)>c(Na+)>c(H+)>c(OH—)
3
D.G点溶液中各离子浓度关系为c(CHCOO—)=c(Na+)+c(H+)—c(OH—)
3
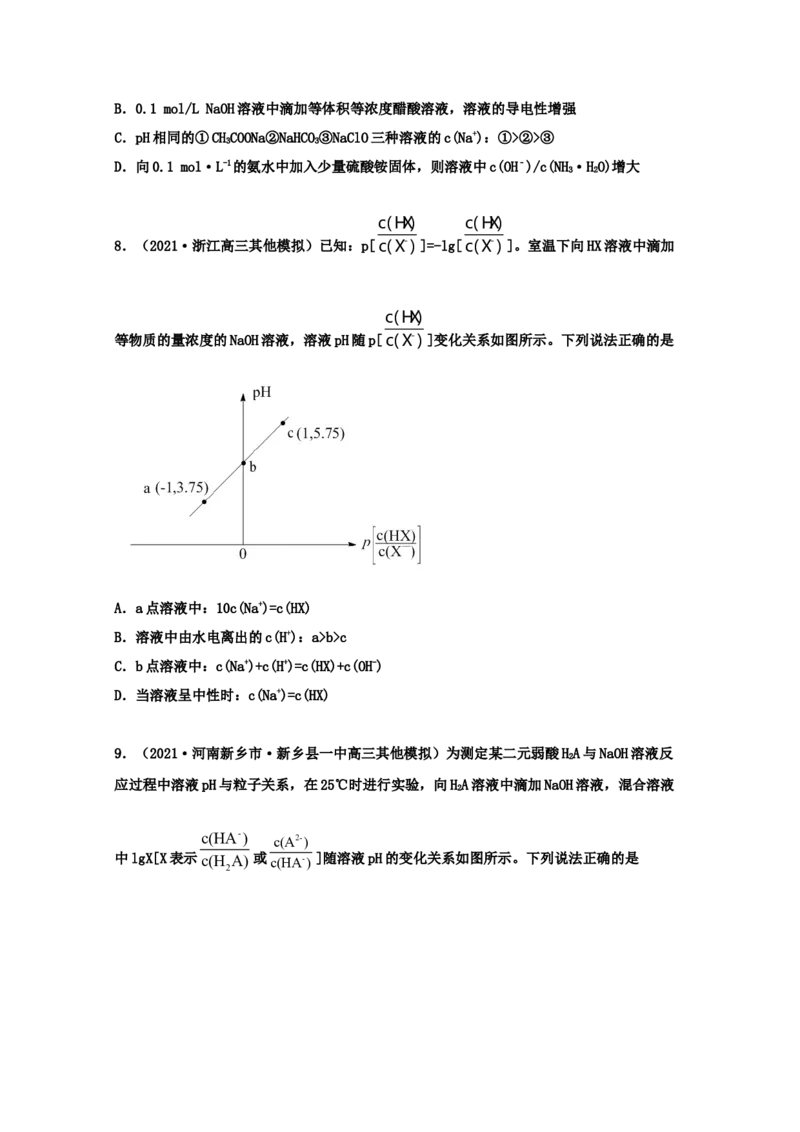
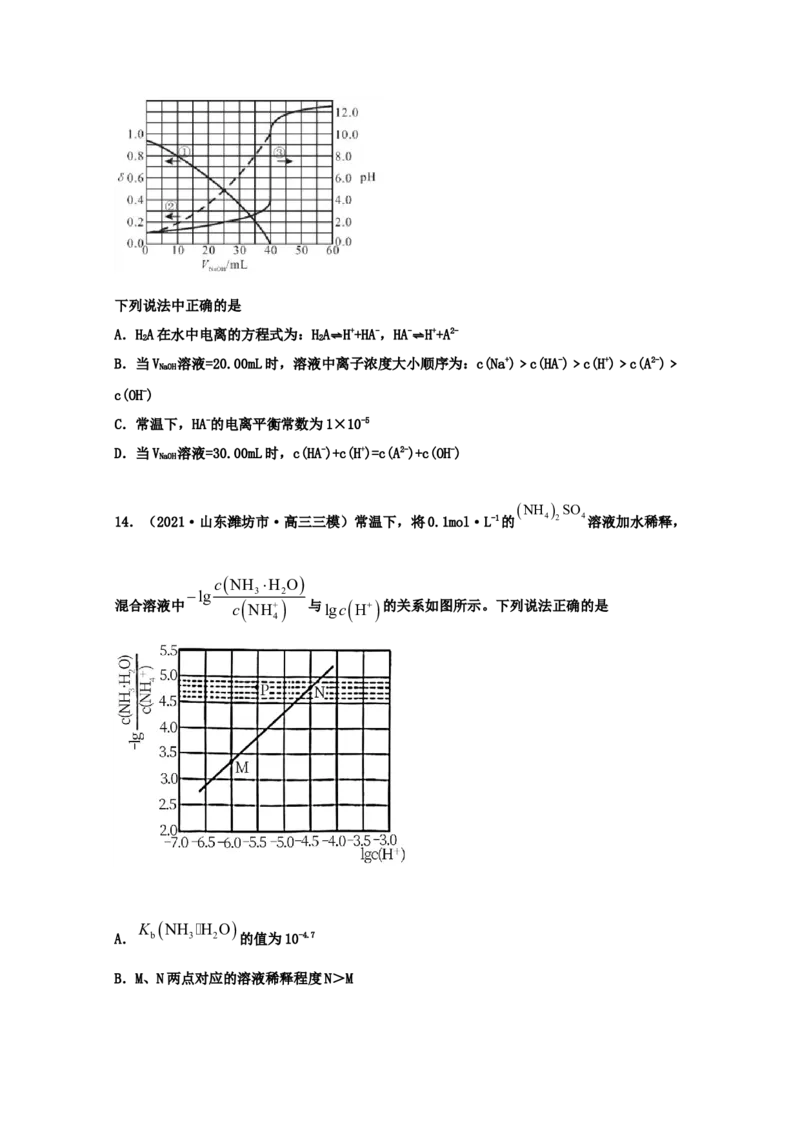
12.(2021·广西南宁市·南宁三中高三三模)常温下 用如图1所示装置,分别向
,
25mL0.3mol/L NaCO 溶液和25mL0.3mo/lLNaHCO 溶液中逐滴滴加0.3mol/L的稀盐酸,用压
2 3 3
强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
A.X曲线为NaCO 溶液的滴定曲线
2 3
B.b点溶液的pH大于c点溶液的pH
C.a、d两点水的电离程度:a>d
2- -
D.c点的溶液中:c(Na+)+c(H+)=2c(CO3 )+c(HCO3 )+c(OH-)
13.(2021·江西抚州市·临川一中)常温下,以酚酞为指示剂,用0.1000mol·L−1的NaOH
溶液滴定20.00mL0.1000mol·L−1的二元酸HA溶液。溶液中pH、含A微粒分布系数δ(物质
2
的量分数)随滴加NaOH溶液体积V 的变化关系如图所示
NaOH下列说法中正确的是
A.HA在水中电离的方程式为:HA H++HA-,HA- H++A2-
2 2 ⇌ ⇌
B.当V 溶液=20.00mL时,溶液中离子浓度大小顺序为:c(Na+)﹥c(HA-)﹥c(H+)﹥c(A2-)﹥
NaOH
c(OH-)
C.常温下,HA-的电离平衡常数为1×10-5
D.当V 溶液=30.00mL时,c(HA-)+c(H+)=c(A2-)+c(OH-)
NaOH
NH SO
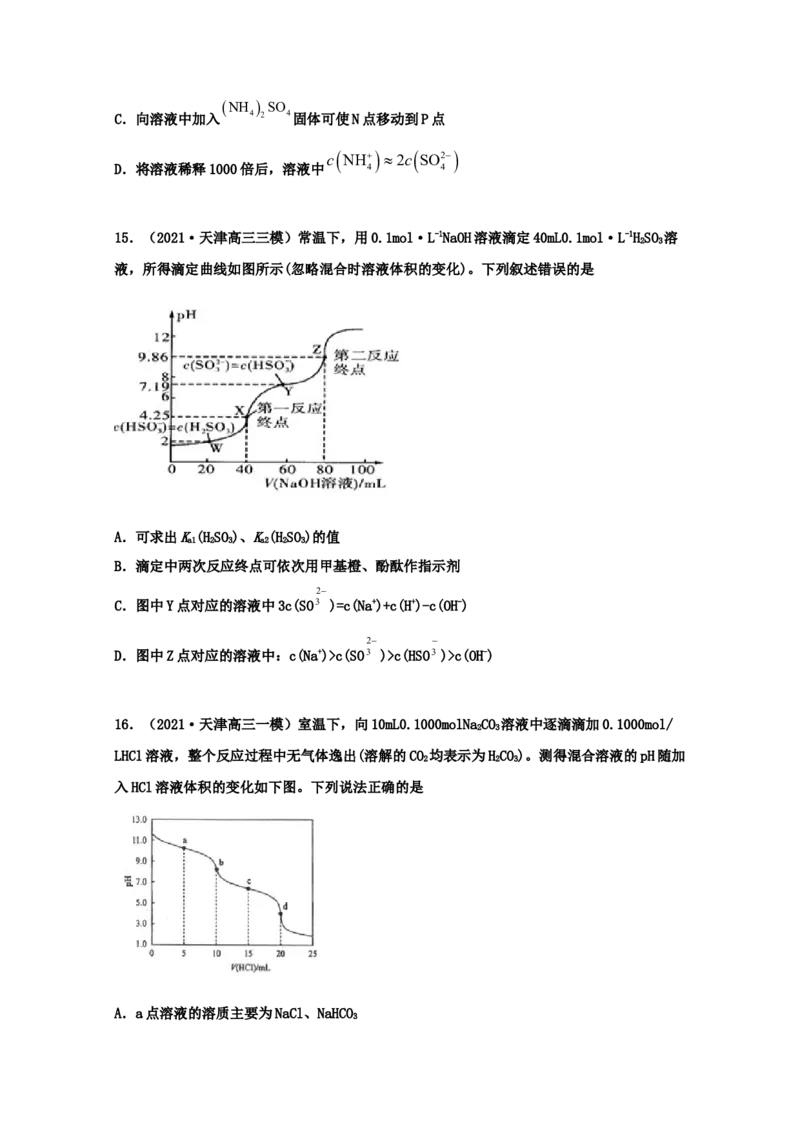
14.(2021·山东潍坊市·高三三模)常温下,将0.1mol·L-1的 4 2 4溶液加水稀释,
cNH H O
lg 3 2
混合溶液中 c NH 与lgc H的关系如图所示。下列说法正确的是
4
K NH H O
A. b 3 2 的值为10-4.7
B.M、N两点对应的溶液稀释程度N>MNH SO
C.向溶液中加入 4 2 4固体可使N点移动到P点
c
NH
2c
SO2
D.将溶液稀释1000倍后,溶液中 4 4
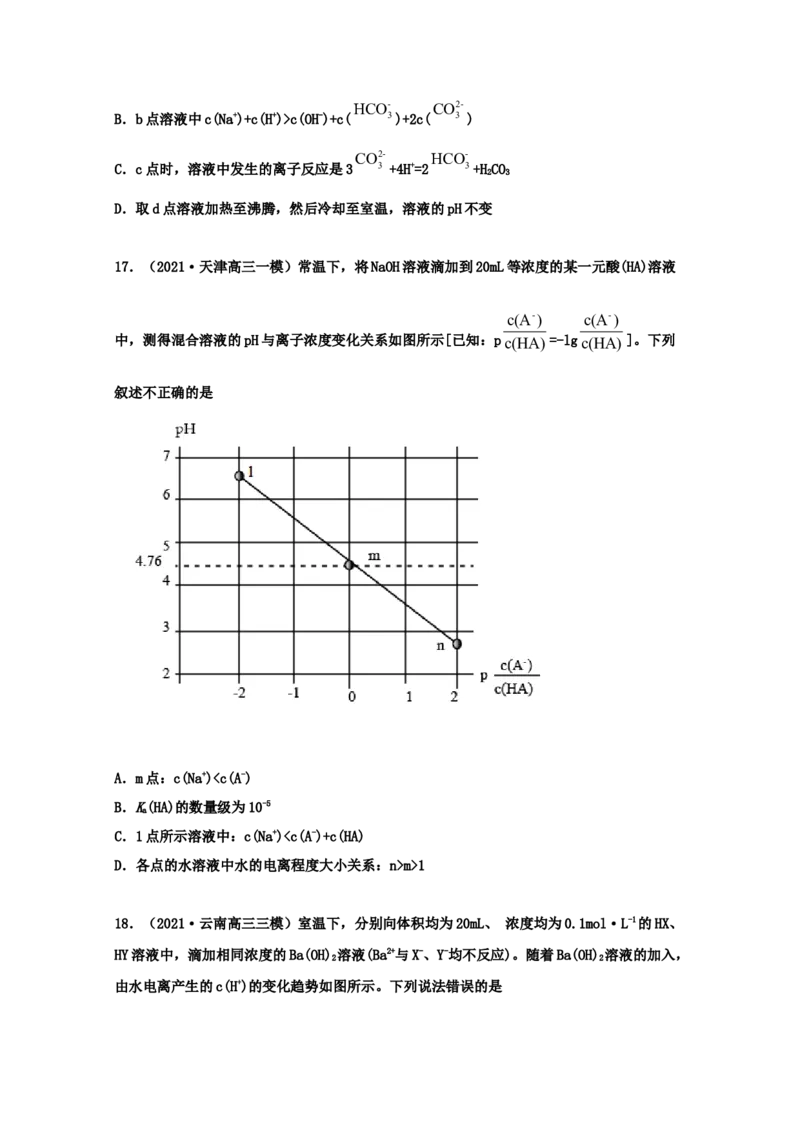
15.(2021·天津高三三模)常温下,用0.1mol·L-1NaOH溶液滴定40mL0.1mol·L-1HSO 溶
2 3
液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。下列叙述错误的是
A.可求出K(HSO)、K(HSO)的值
a1 2 3 a2 2 3
B.滴定中两次反应终点可依次用甲基橙、酚酞作指示剂
2
C.图中Y点对应的溶液中3c(SO3 )=c(Na+)+c(H+)-c(OH-)
2
D.图中Z点对应的溶液中:c(Na+)>c(SO3 )>c(HSO3 )>c(OH-)
16.(2021·天津高三一模)室温下,向10mL0.1000molNaCO 溶液中逐滴滴加0.1000mol/
2 3
LHCl溶液,整个反应过程中无气体逸出(溶解的CO 均表示为HCO)。测得混合溶液的pH随加
2 2 3
入HCl溶液体积的变化如下图。下列说法正确的是
A.a点溶液的溶质主要为NaCl、NaHCO
3HCO- CO2-
B.b点溶液中c(Na+)+c(H+)>c(OH-)+c( 3)+2c( 3 )
CO2- HCO-
C.c点时,溶液中发生的离子反应是3 3 +4H+=2 3+HCO
2 3
D.取d点溶液加热至沸腾,然后冷却至室温,溶液的pH不变
17.(2021·天津高三一模)常温下,将NaOH溶液滴加到20mL等浓度的某一元酸(HA)溶液
c(A-) c(A-)
中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:pc(HA) =-lgc(HA) ]。下列
叙述不正确的是
A.m点:c(Na+)m>1
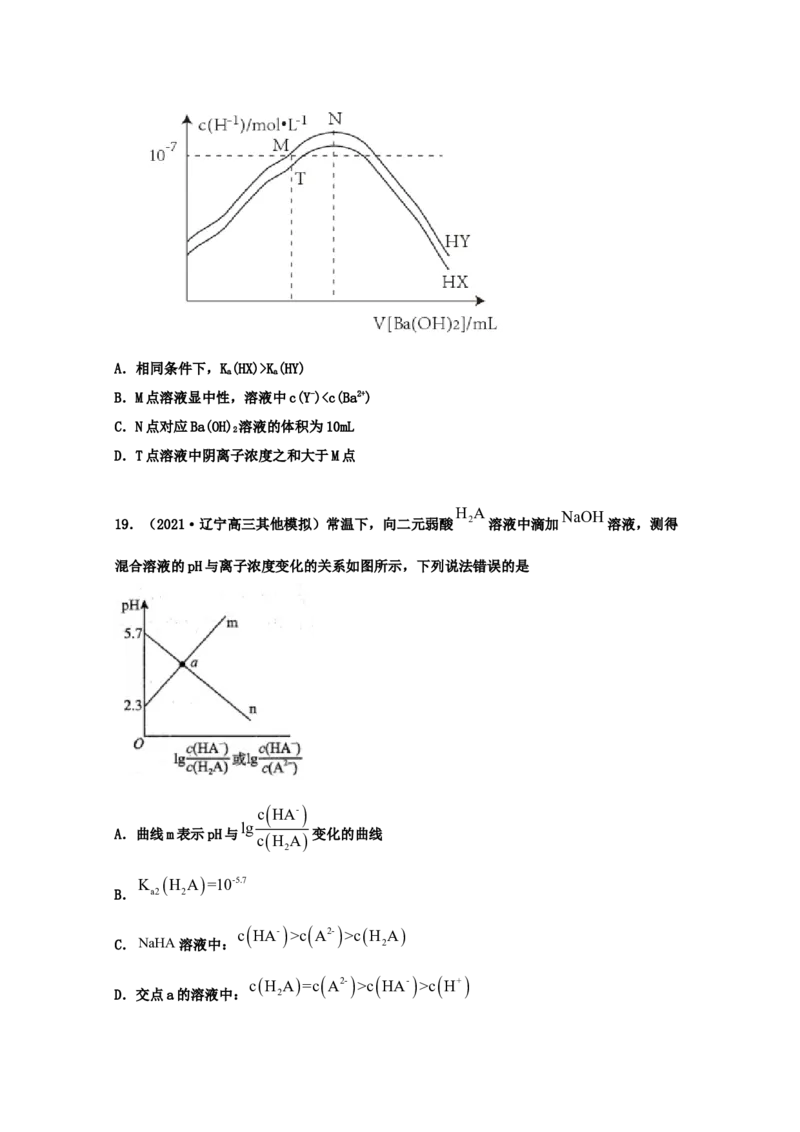
18.(2021·云南高三三模)室温下,分别向体积均为20mL、 浓度均为0.1mol·L-1的HX、
HY溶液中,滴加相同浓度的Ba(OH) 溶液(Ba2+与X-、Y-均不反应)。随着Ba(OH) 溶液的加入,
2 2
由水电离产生的c(H+)的变化趋势如图所示。下列说法错误的是A.相同条件下,K(HX)>K(HY)
a a
B.M点溶液显中性,溶液中c(Y-)c A2- >cH A
C.NaHA溶液中: 2
cH A=c A2- >c HA- >c H+
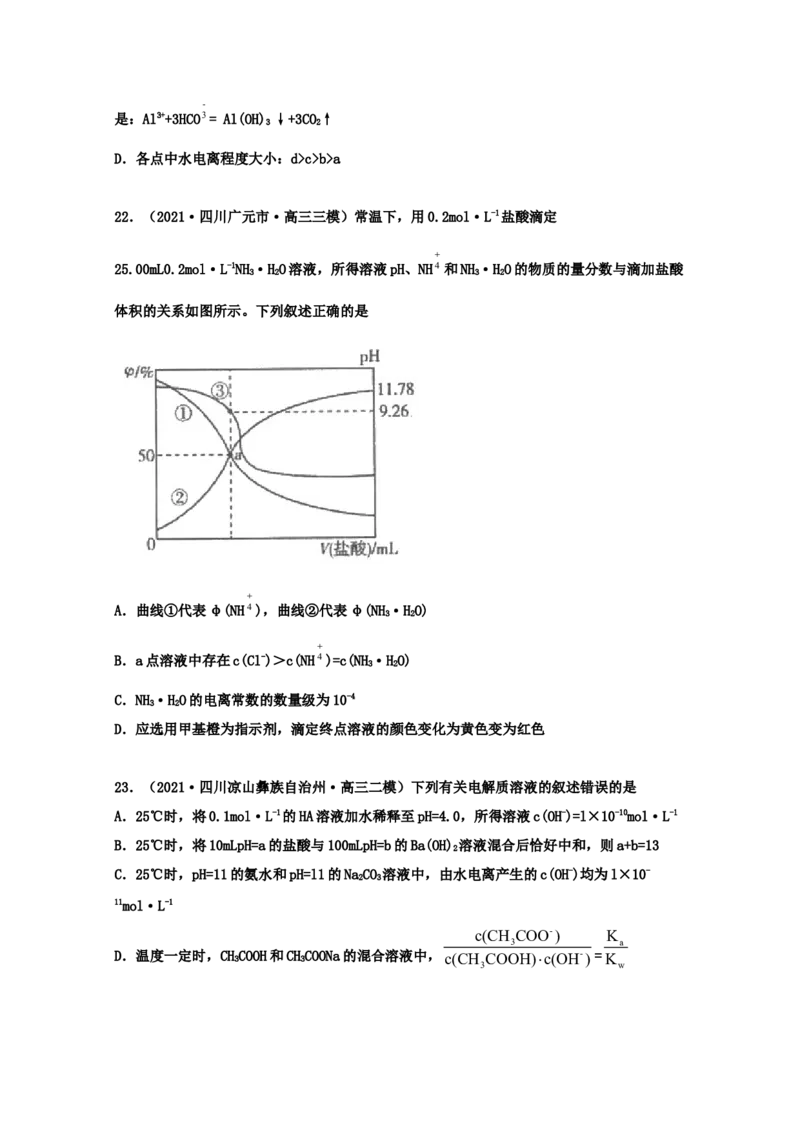
D.交点a的溶液中: 220.(2021·四川雅安市·高三三模)草酸(HCO)是一种二元弱酸。常温下向草酸溶液中滴
2 2 4
c(HC O) c(C O2)
2 4 2 4
加NaOH溶液,混合溶液中lgX[x表示c(H C O ) 或c(HC O)]随pH的变化如图。下列说
2 2 4 2 4
法中错误的是
A.NaHCO 溶液呈酸性
2 4
B.HCO 第二步电离常数数量级是10-5
2 2 4
HC O- C O2-
C.pH=7时,c(Na+)=c( 2 4)+2c( 2 4 )
HC O- C O2-
D.1.22c( 2 4 )>c(HCO)
2 2 4
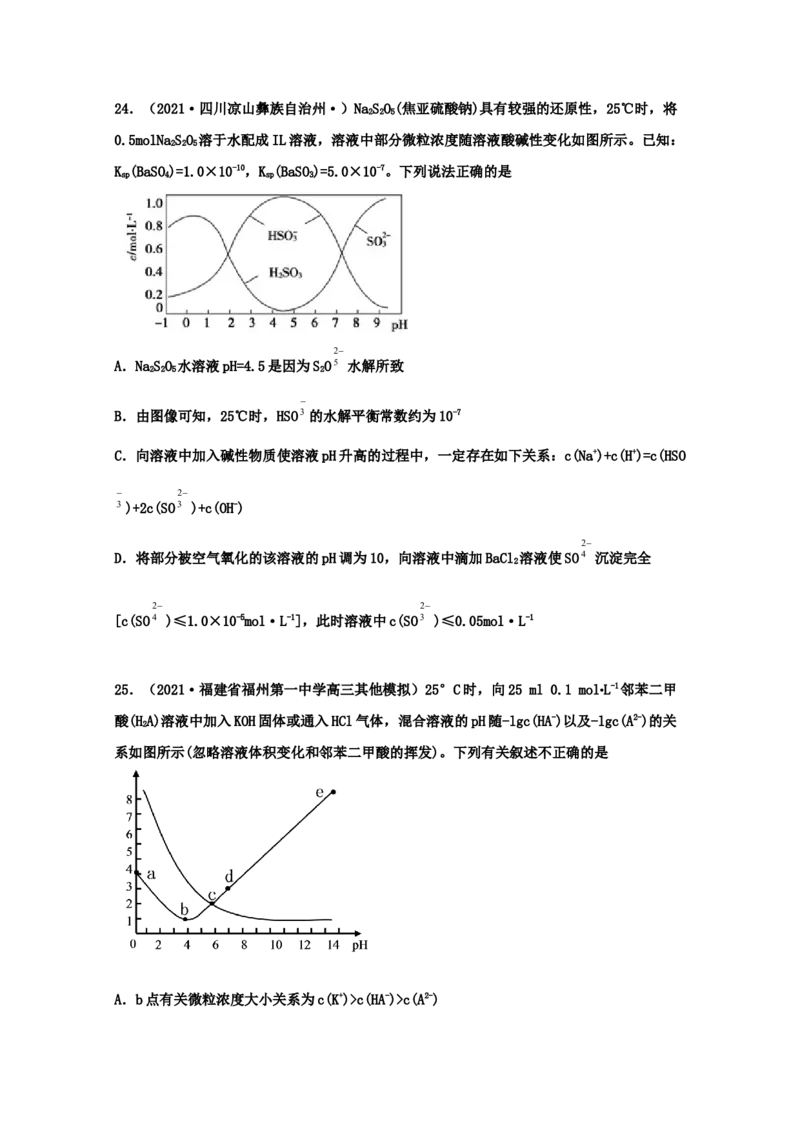
0.1000 molL-1 25mL 0.1000
21.(2021·广西南宁二中高三三模)常温下,用 盐酸滴定
molL-1 Na
2
CO
3溶液,其滴定曲线如图所示。下列说法正确的是
c
HCO-
>c
CO2-
>c
Cl-
A.a点溶液中 3 3
c
Na+
+c
H+
=c
HCO-
+2c
CO2-
+c
OH-
B.b液中 3 3
C.若取c点溶液与足量浓的明矾溶液混合,有白色絮状沉淀生成,同时产生气泡,主要原因-
是:Al3++3HCO3= Al(OH) ↓+3CO↑
3 2
D.各点中水电离程度大小:d>c>b>a
22.(2021·四川广元市·高三三模)常温下,用0.2mol·L-1盐酸滴定
25.00mL0.2mol·L-1NH·HO溶液,所得溶液pH、NH4和NH·HO的物质的量分数与滴加盐酸
3 2 3 2
体积的关系如图所示。下列叙述正确的是
A.曲线①代表φ(NH4),曲线②代表φ(NH·HO)
3 2
B.a点溶液中存在c(Cl-)>c(NH4)=c(NH·HO)
3 2
C.NH·HO的电离常数的数量级为10-4
3 2
D.应选用甲基橙为指示剂,滴定终点溶液的颜色变化为黄色变为红色
23.(2021·四川凉山彝族自治州·高三二模)下列有关电解质溶液的叙述错误的是
A.25℃时,将0.1mol·L-1的HA溶液加水稀释至pH=4.0,所得溶液c(OH-)=l×10-10mol·L-1
B.25℃时,将10mLpH=a的盐酸与100mLpH=b的Ba(OH) 溶液混合后恰好中和,则a+b=13
2
C.25℃时,pH=11的氨水和pH=l1的NaCO 溶液中,由水电离产生的c(OH-)均为l×10-
2 3
11mol·L-1
c(CH COO-) K
3 a
D.温度一定时,CH
3
COOH和CH
3
COONa的混合溶液中,c(CH COOH)c(OH-) =K
3 w24.(2021·四川凉山彝族自治州·)NaSO(焦亚硫酸钠)具有较强的还原性,25℃时,将
2 2 5
0.5molNaSO 溶于水配成IL溶液,溶液中部分微粒浓度随溶液酸碱性变化如图所示。已知:
2 2 5
K (BaSO)=1.0×10-10,K (BaSO)=5.0×10-7。下列说法正确的是
sp 4 sp 3
2
A.NaSO 水溶液pH=4.5是因为SO5 水解所致
2 2 5 2
B.由图像可知,25℃时,HSO3 的水解平衡常数约为10-7
C.向溶液中加入碱性物质使溶液pH升高的过程中,一定存在如下关系:c(Na+)+c(H+)=c(HSO
2
3 )+2c(SO3 )+c(OH-)
2
D.将部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl 溶液使SO4 沉淀完全
2
2 2
[c(SO4 )≤1.0×10-5mol·L-1],此时溶液中c(SO3 )≤0.05mol·L-1
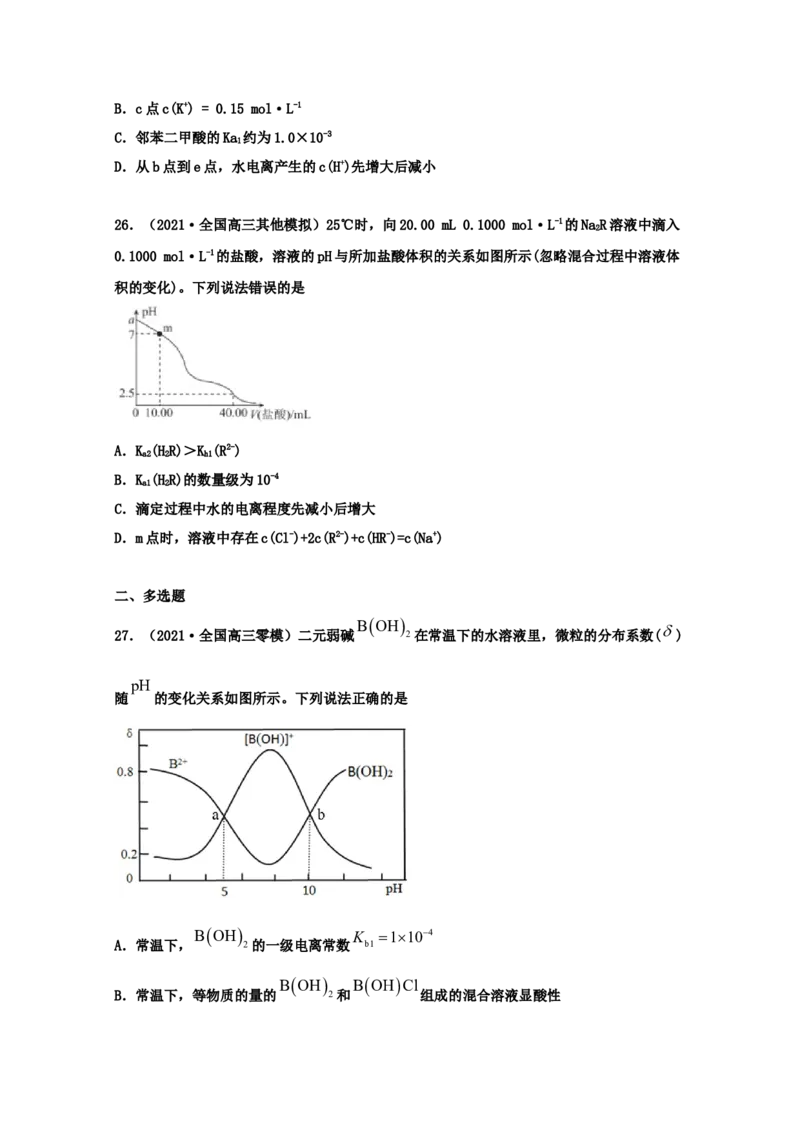
25.(2021·福建省福州第一中学高三其他模拟)25°C时,向25 ml 0.1 mol∙L-1邻苯二甲
酸(HA)溶液中加入KOH固体或通入HCl气体,混合溶液的pH随-lgc(HA-)以及-lgc(A2-)的关
2
系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发)。下列有关叙述不正确的是
A.b点有关微粒浓度大小关系为c(K+)>c(HA-)>c(A2-)B.c点c(K+) = 0.15 mol·L-1
C.邻苯二甲酸的Ka 约为1.0×10-3
1
D.从b点到e点,水电离产生的c(H+)先增大后减小
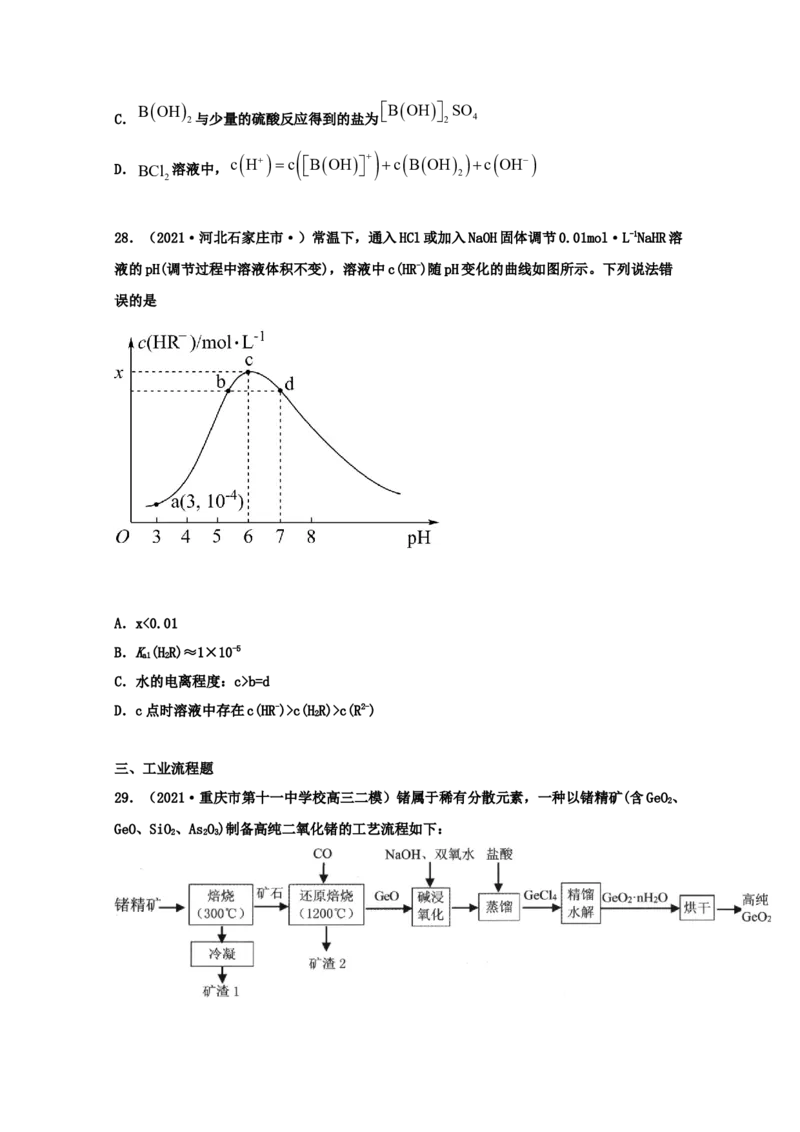
26.(2021·全国高三其他模拟)25℃时,向20.00 mL 0.1000 mol·L-1的NaR溶液中滴入
2
0.1000 mol·L-1的盐酸,溶液的pH与所加盐酸体积的关系如图所示(忽略混合过程中溶液体
积的变化)。下列说法错误的是
A.K (HR)>K (R2-)
a2 2 h1
B.K (HR)的数量级为10-4
a1 2
C.滴定过程中水的电离程度先减小后增大
D.m点时,溶液中存在c(Cl-)+2c(R2-)+c(HR-)=c(Na+)
二、多选题
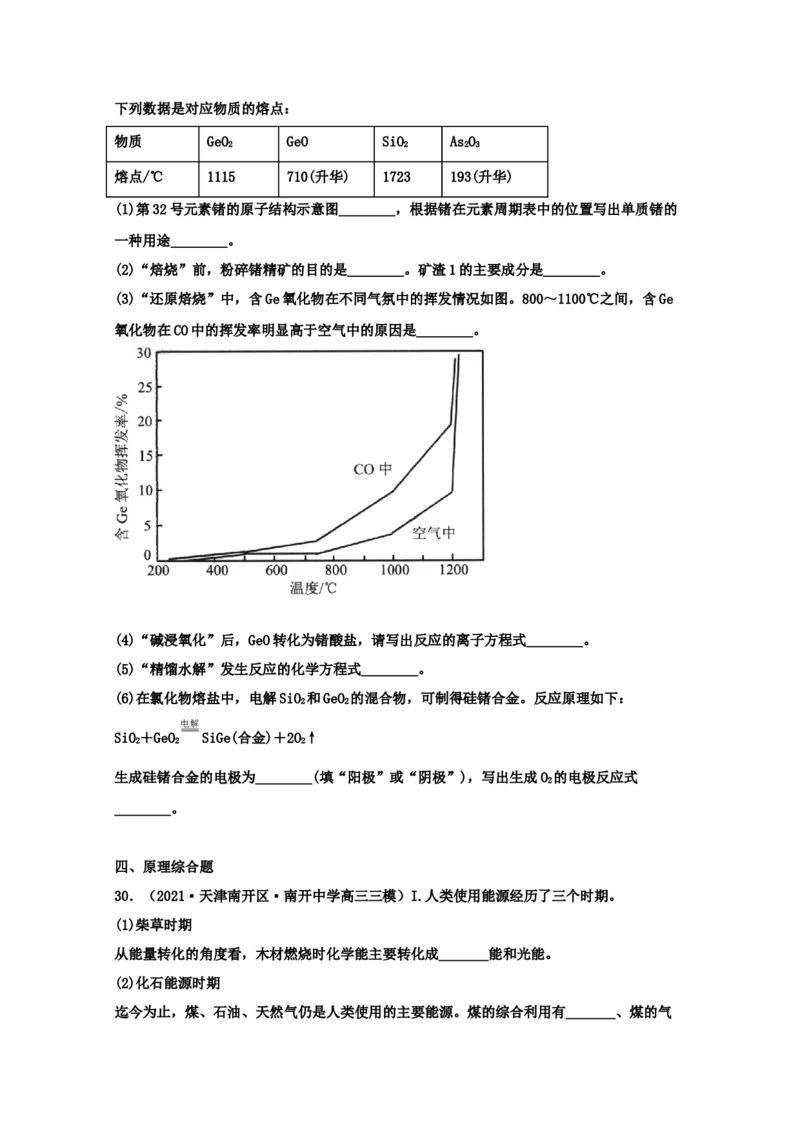
BOH
27.(2021·全国高三零模)二元弱碱 2在常温下的水溶液里,微粒的分布系数( )
pH
随 的变化关系如图所示。下列说法正确的是
BOH K 1104
A.常温下, 2的一级电离常数 b1
BOH BOHCl
B.常温下,等物质的量的 2和 组成的混合溶液显酸性BOH BOH SO
C. 2与少量的硫酸反应得到的盐为 2 4
c H c
BOH
c BOH c OH
D.BCl 溶液中,
2
2
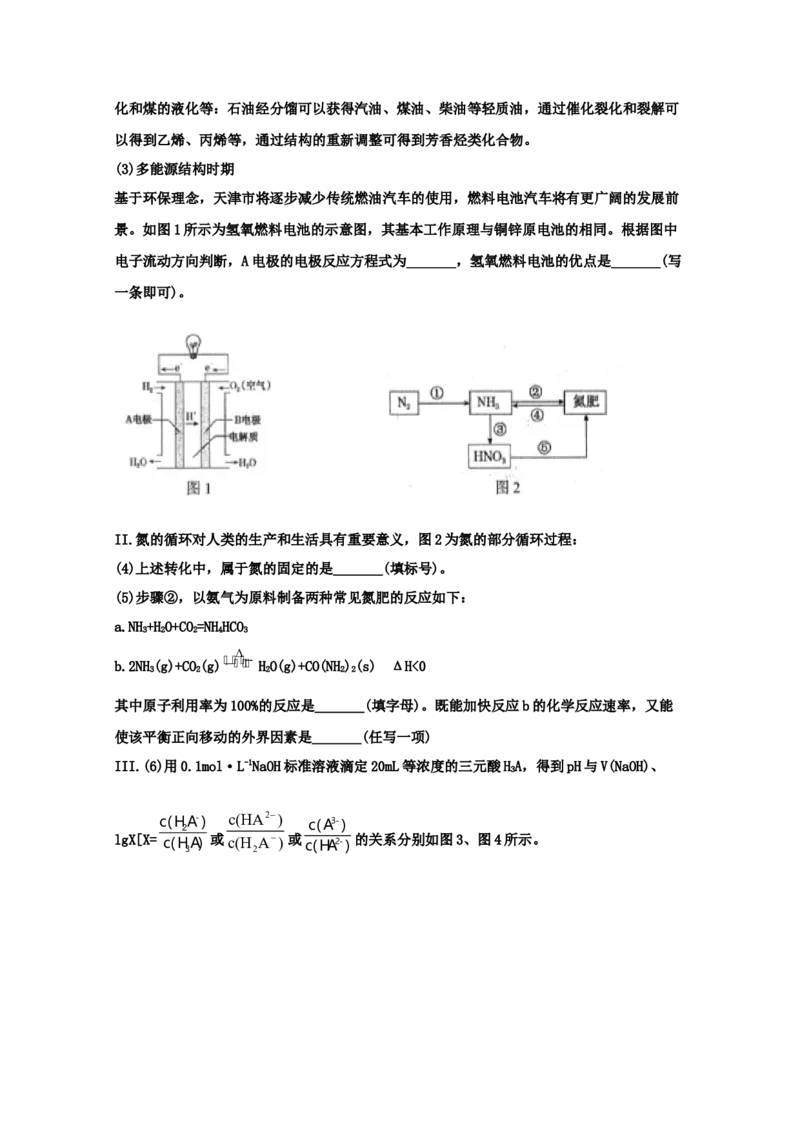
28.(2021·河北石家庄市·)常温下,通入HCl或加入NaOH固体调节0.01mol·L-1NaHR溶
液的pH(调节过程中溶液体积不变),溶液中c(HR-)随pH变化的曲线如图所示。下列说法错
误的是
A.x<0.01
B.K(HR)≈1×10-5
a1 2
C.水的电离程度:c>b=d
D.c点时溶液中存在c(HR-)>c(HR)>c(R2-)
2
三、工业流程题
29.(2021·重庆市第十一中学校高三二模)锗属于稀有分散元素,一种以锗精矿(含GeO、
2
GeO、SiO、AsO)制备高纯二氧化锗的工艺流程如下:
2 2 3下列数据是对应物质的熔点:
物质 GeO GeO SiO AsO
2 2 2 3
熔点/℃ 1115 710(升华) 1723 193(升华)
(1)第32号元素锗的原子结构示意图________,根据锗在元素周期表中的位置写出单质锗的
一种用途________。
(2)“焙烧”前,粉碎锗精矿的目的是________。矿渣1的主要成分是________。
(3)“还原焙烧”中,含Ge氧化物在不同气氛中的挥发情况如图。800~1100℃之间,含Ge
氧化物在CO中的挥发率明显高于空气中的原因是________。
(4)“碱浸氧化”后,GeO转化为锗酸盐,请写出反应的离子方程式________。
(5)“精馏水解”发生反应的化学方程式________。
(6)在氯化物熔盐中,电解SiO 和GeO 的混合物,可制得硅锗合金。反应原理如下:
2 2
电解
SiO+GeO SiGe(合金)+2O↑
2 2 2
生成硅锗合金的电极为________(填“阳极”或“阴极”),写出生成O 的电极反应式
2
________。
四、原理综合题
30.(2021·天津南开区·南开中学高三三模)I.人类使用能源经历了三个时期。
(1)柴草时期
从能量转化的角度看,木材燃烧时化学能主要转化成_______能和光能。
(2)化石能源时期
迄今为止,煤、石油、天然气仍是人类使用的主要能源。煤的综合利用有_______、煤的气化和煤的液化等:石油经分馏可以获得汽油、煤油、柴油等轻质油,通过催化裂化和裂解可
以得到乙烯、丙烯等,通过结构的重新调整可得到芳香烃类化合物。
(3)多能源结构时期
基于环保理念,天津市将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前
景。如图1所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中
电子流动方向判断,A电极的电极反应方程式为_______,氢氧燃料电池的优点是_______(写
一条即可)。
II.氮的循环对人类的生产和生活具有重要意义,图2为氮的部分循环过程:
(4)上述转化中,属于氮的固定的是_______(填标号)。
(5)步骤②,以氨气为原料制备两种常见氮肥的反应如下:
a.NH+HO+CO=NHHCO
3 2 2 4 3
Δ
b.2NH(g)+CO(g) HO(g)+CO(NH)(s) ΔH<0
3 2 2 2 2
其中原子利用率为100%的反应是_______(填字母)。既能加快反应b的化学反应速率,又能
使该平衡正向移动的外界因素是_______(任写一项)
III.(6)用0.1mol·L-1NaOH标准溶液滴定20mL等浓度的三元酸HA,得到pH与V(NaOH)、
3
c(HA-) c(HA2) c(A3-)
2
lgX[X= c(HA) 或c(H A) 或 c(HA2-) 的关系分别如图3、图4所示。
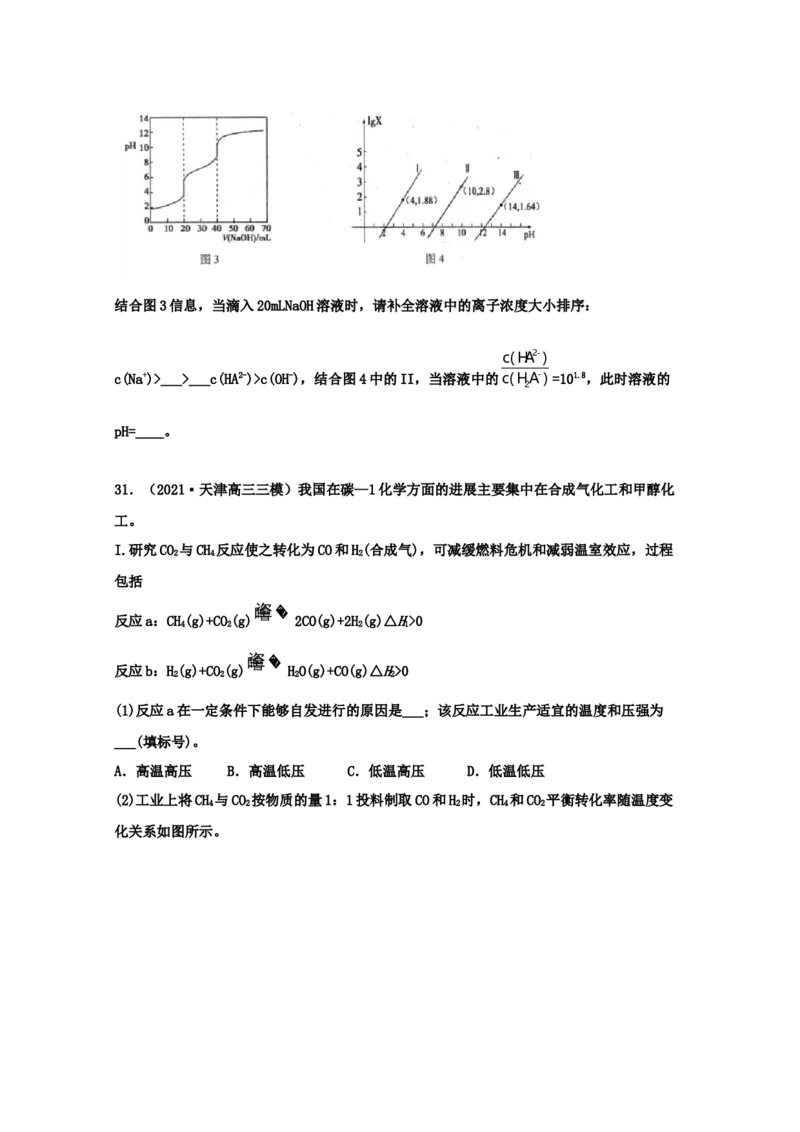
3 2结合图3信息,当滴入20mLNaOH溶液时,请补全溶液中的离子浓度大小排序:
c(HA2-)
c(Na+)>___>___c(HA2-)>c(OH-),结合图4中的II,当溶液中的c(HA-) =101.8,此时溶液的
2
pH=____。
31.(2021·天津高三三模)我国在碳—1化学方面的进展主要集中在合成气化工和甲醇化
工。
I.研究CO 与CH 反应使之转化为CO和H(合成气),可减缓燃料危机和减弱温室效应,过程
2 4 2
包括
噲垐 ��
反应a:CH(g)+CO(g) 2CO(g)+2H(g)△H>0
4 2 2 1
噲垐 ��
反应b:H(g)+CO(g) HO(g)+CO(g)△H>0
2 2 2 2
(1)反应a在一定条件下能够自发进行的原因是___;该反应工业生产适宜的温度和压强为
___(填标号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
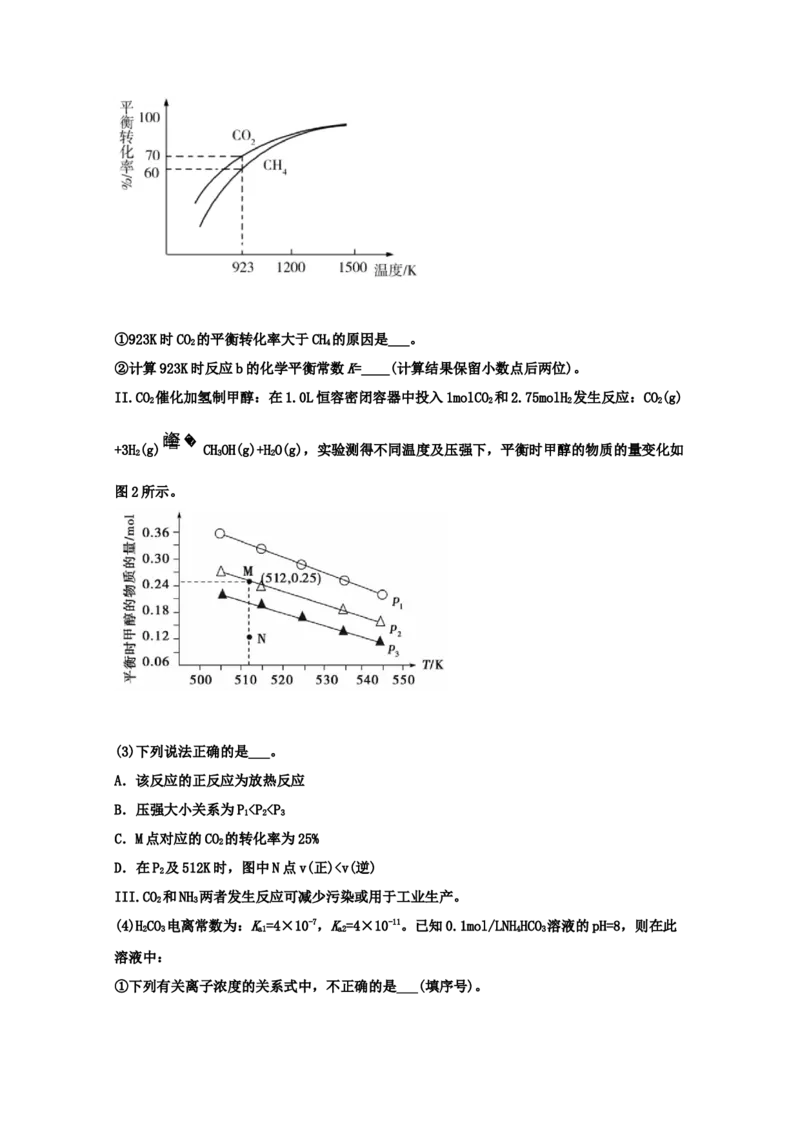
(2)工业上将CH 与CO 按物质的量1:1投料制取CO和H 时,CH 和CO 平衡转化率随温度变
4 2 2 4 2
化关系如图所示。①923K时CO 的平衡转化率大于CH 的原因是___。
2 4
②计算923K时反应b的化学平衡常数K=____(计算结果保留小数点后两位)。
II.CO 催化加氢制甲醇:在1.0L恒容密闭容器中投入1molCO 和2.75molH 发生反应:CO(g)
2 2 2 2
噲垐 ��
+3H(g) CHOH(g)+HO(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如
2 3 2
图2所示。
(3)下列说法正确的是___。
A.该反应的正反应为放热反应
B.压强大小关系为Pc(OH-)+c(HCO3 )+2c(CO3 )
2
②c(HCO):c(CO3 )=___(结果保留三位有效数字)。
2 3