文档内容
专题三 离子反应和离子方程式 专题检验
一、选择题(16×3=48分)
1.(2022·吉林长春·二模)下列对应离子方程式书写错误的是
A.向BaCl 溶液中通入CO 气体: Ba2++CO + H O= BaCO ↓+2H+
2 2 2 2 3
B.向FeCl 溶液中通入Cl : 2Fe2+ Cl = 2Fe3+ +2Cl-
2 2 2
2-
C.向NaClO溶液中通入过量SO : ClO- +SO +H O = Cl-+SO4 +2H+
2 2 2
2-
D.向NH Al(SO ) 溶液中加入同体积同浓度的Ba(OH) 溶液:2A13++3SO4 +3Ba2++6OH-
4 4 2 2
=3BaSO ↓+2Al(OH) ↓
4 3
【答案】A
【解析】A项: 碳酸的酸性弱于盐酸,向BaCl 溶液中通入CO 气体不反应,故A错误;
2 2
B项: 向FeCl 溶液中通入Cl 生成氯化铁: 2Fe2+ Cl = 2Fe3+ +2Cl-,故B正确;
2 2 2
2-
C项: 向NaClO溶液中通入过量SO 生成硫酸钠和氯化钠: ClO- +SO +H O = Cl-+SO4
2 2 2
+2H+,故C正确;
-
D项: 碱性:OH->AlO2>NH ·H O>Al(OH) ,向NH Al(SO ) 溶液中加入同浓度的Ba(OH) 溶
3 2 3 4 4 2 2
-
液,先生成氢氧化铝,再生成NH ·H O,再生成AlO2,当n(OH-):n(A13+)<3:1时生成
3 2
氢氧化铝,向NH Al(SO ) 溶液中加入同体积同浓度的Ba(OH) 溶液,n(OH-):
4 4 2 2
2-
n(A13+)=2:1<3:1:2A13++3SO4 +3Ba2++6OH-=3BaSO ↓+2Al(OH) ↓,故D正确;
4 3
故选A。
2.(2022·安徽马鞍山·三模)下列指定反应的离子方程式正确的是
NH+ SO2-
A.用氨水吸收足量的SO 气体: 2NH ·H O + SO = 2 4+ 3 + H O
2 3 2 2 2
B.将Cl 通入石灰乳中制漂白粉: Cl + 2OH- = ClO- + Cl-+ H O
2 2 2
CO2-
C.ZnCO 溶于稀盐酸: 3 + 2H+= H O + CO ↑
3 2 2
D.向AgBr悬浊液中滴加足量Na S溶液,出现黑色沉淀: 2AgBr(s)+S2- (aq)=Ag S(s) +2Br-
2 2
(aq)【答案】D
NH+
【解析】A项:用氨水吸收足量的SO 气体,反应生成亚硫酸氢铵:NH ·H O + SO = 4+
2 3 2 2
HSO-
3,选项A错误;
B项:将Cl 通入石灰乳中制漂白粉,反应生成氯化钙、次氯酸钙和水,反应的离子方程式
2
为:2Cl + 2Ca(OH) = 2Ca2++2ClO- +2Cl-+ 2H O,选项B错误;
2 2 2
ZnCO
C项:ZnCO 溶于稀盐酸生成氯化锌、二氧化碳和水,反应的离子方程式为: 3 +
3
2H+= Zn2++H O + CO ↑,选项C错误;
2 2
D项:向AgBr悬浊液中滴加足量Na S溶液,出现黑色沉淀,转化为更难溶的硫化银,反应
2
的离子方程式为: 2AgBr(s)+S2- (aq)=Ag S(s) +2Br-(aq),选项D正确;
2
答案选D。
3.(2022·新高考广东卷)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
【答案】B
【解析】A项:向氢氧化钠溶液中通入足量的二氧化碳,碱可以转化成酸式盐,离子方程
式为:CO +OH-= ,故A错误;
2
B项:氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:
Cl +2OH-=Cl-+ClO-+H O,故B正确;
2 2
C项:钠的过氧化物为Na O ,可以和水反应生成氢氧化钠,但在离子方程式里Na O 不能
2 2 2 2
拆成离子,故C错误;
D项:硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
故选B。
4.(2022·安徽芜湖·三模)下列离子能大量共存,且加入相应试剂后发生反应的离子方程式书写正确的是
选项 离子 加入试剂 加入试剂后发生反应的离子方程式
A Fe3+、Cl-、SO 2 4 、K+ 铜粉 2Fe3++Cu=2Fe2++Cu2+
B K+、HCO3 、AlO2 、Cl- 盐酸 H++ AlO2 +H O=Al(OH) ↓
2 3
C Na+、Fe2+、Br-、Mg2+ 氯气 2 Br-+Cl =Br +2Cl-
2 2
2
D NH4、Na+、SO4 、HCO3 NaOH NH4+OH-=NH ·H O
3 2
【答案】A
2
【解析】A项:Fe3+、Cl-、SO4 、K+之间不反应能够大量共存,加入铜粉后与Fe3+发生氧化
还原反应,离子方程式为2Fe3++Cu=2Fe2++Cu2+,A符合题意;
CO2-
B项:由于HCO3的酸性强于HAlO ,故HCO3+AlO2+H O=Al(OH) ↓+ 3 ,即HCO3、AlO2
2 2 3
在水溶液中不能大量共存,B不合题意;
C项:Na+、Fe2+、Br-、Mg2+各离子互不反应可以大量共存,但由于Fe2+的还原性强于Br-,通
入Cl 时,先发生的离子方程式为:2Fe2++Cl =2Fe3++2Cl-,C不合题意;
2 2
2
D项:NH4、Na+、SO4 、HCO3各离子互不反应可以大量共存,但由于HCO3先与OH-反
CO2-
应,故加入NaOH后,先发生的离子方程式为:HCO3+OH-= 3 +H O,D不合题意;
2
故答案为:A。
5.(2022·安徽马鞍山·一模)下列指定反应的离子方程式正确的是
A.向Ca(ClO) 溶液中通入过量CO :Ca2++2ClO-+CO +H O=2HClO+CaCO
2 2 2 2 3
SO2
B.向Na SO 溶液中滴加稀HNO 溶液: 3 +2H+=SO ↑+H O
2 3 3 2 2
C.向FeI 溶液中通入等物质的量的Cl :2Fe2++2I-+2Cl =2Fe3++I +4Cl-
2 2 2 2
SO2
D.向NH HSO 溶液中滴加少量的Ba(OH) 溶液:Ba2++2OH-+2H++ 4 =BaSO ↓+2H O
4 4 2 4 2
【答案】D
【解析】A项:Ca(ClO) 溶液中通入过量CO 制取次氯酸,反应生成次氯酸和碳酸氢根离
2 2HCO
子,正确的离子方程式为:ClO-+H O+CO =HClO+ 3,故A错误;
2 2
B项:向Na SO 溶液中滴加稀HNO 溶液,二者发生氧化还原反应,正确的离子反应为:2
2 3 3
NO SO2 SO2
3+3 3 +2H+═3 4 +2NO↑+H O,故B错误;
2
C项:由于I-的还原性大于Fe2+的还原性,则氯气先与I-反应,将I-氧化完后,再氧化Fe2+,
根据得失电子守恒可知,等量的Cl 刚好氧化I-,Fe2+不被氧化,正确的离子反应方程式
2
应为:2I-+Cl =I +2Cl-,故C错误;
2 2
D项:在NH HSO 溶液中滴加少量Ba(OH) 溶液,氢氧根离子只与氢离子反应,不与铵根离
4 4 2
SO2
子反应,正确的离子方程式为:Ba2++2OH-+2H++ 4 =BaSO ↓+2H O,故D正
4 2
确;
故选:D。
6.(2022·宁夏吴忠·二模)下列各组离子在指定溶液中能大量共存的是
SO2- NO-
A.中性溶液中:Fe3+、Na+、 4 、 3
c
H+
B.lg
c
OH-=10的溶液中:Na+、K+、CH
3
COO-、Cl-
NH+
C.明矾溶液中: 4、K+、I-、Br-
NO-
D.加入铝粉会产生H 的溶液中:Cu2+、Mg2+、 3、ClO-
2
【答案】C
【解析】A项:中性溶液中Fe3+会发生水解,生成氢氧化铁沉淀,不能共存,A项错误;
c
H+
B项:lg
c
OH-=10的溶液中显酸性,酸性条件下,CH
3
COO-与氢离子会结合,不能共存,
B项错误;
NH+
C项:明矾溶液中存在Al3+,Al3+、 4、K+、I-、Br-互不反应,能大量共存,C项正确;
D项:加入铝粉会产生H 的溶液中可能显酸性也可能显碱性,酸性条件下,ClO-不能大量
2
共存,碱性条件下,Cu2+、Mg2+不能大量共存,D项错误;答案选C。
7.(2022·河南开封·二模)下列过程中的化学反应,相应的离子方程式错误的是
A.将稀H SO 加入NaIO 和NaI的混合溶液中:5I-+IO3+6H+=3I +3H O
2 4 3 2 2
2 2
B.向稀HNO 中滴加Na SO 溶液:3SO3 +2H++2NO3=3SO4 +2NO↑+H O
3 2 3 2
C.将Na O 加入CuSO 溶液中:2Na O +2Cu2++2H O=4Na++2Cu(OH) ↓+O ↑
2 2 4 2 2 2 2 2
2
D.向NaHCO 溶液中加入足量Ba(OH) 溶液:2HCO3+Ba2++2OH-=BaCO ↓+2H O+CO3
3 2 3 2
【答案】D
【解析】A项:H SO 、NaIO 和NaI反应生成碘单质,I的化合价由+5价降低为0价,I的化
2 4 3
合价由-1价升高为0价,根据化合价升降守恒、原子守恒和电荷守恒,可得:5I-+IO3
+6H+=3I +3H O,A正确;
2 2
B项: HNO 和Na SO 反应生成一氧化氮和硫酸钠,N的化合价由+5价降低为+2价,S的
3 2 3
化合价由+4价升高为+6价,根据化合价升降守恒、原子守恒和电荷守恒,可得:3SO
2 2
3 +2H++2NO3=3SO4 +2NO↑+H O,B正确;
2
C项:Na O 和CuSO 溶液反应生成氧气和氢氧化铜,O的化合价既由-1价降低为-2价,S的
2 2 4
化合价又由+1价升高为+0价,根据化合价升降守恒、原子守恒和电荷守恒,可得:
2Na O +2Cu2++2H O=4Na++2Cu(OH) ↓+O ↑,C正确;
2 2 2 2 2
D项:假设量少的物质为1mol,过量的物质用多少写多少,NaHCO 为1mol,所以需要
3
1molBa(OH) ,NaHCO +Ba(OH) =BaCO ↓+NaOH+H O,所以反应的离子方程式为:HCO3
2 3 2 3 2
+Ba2++OH-=BaCO ↓+H O,故D错误;
3 2
答案选D。
8.(2022·河南许昌·二模)下列反应对应的离子方程式书写正确的是
A.将H S通入Hg(NO ) 溶液中:Hg2++S2-=HgS↓
2 3 2
B.向FeBr 溶液中通入过量Cl :3Cl +2Fe2++4Br-=2Fe3++2Br +6Cl-
2 2 2 2
NH+
C.向NH Al(SO ) 溶液中滴入少量NaOH溶液: 4+OH-=NH ·H O
4 4 2 3 2MnO-
D.向KMnO 酸性溶液中滴入H O 溶液:2 4+3H O +6H+=2Mn2++4O ↑+6H O
4 2 2 2 2 2 2
【答案】B
【解析】A项:将H S通入Hg(NO ) 溶液中生成HgS沉淀和稀硝酸:Hg2++H S=HgS↓+2H+,A
2 3 2 2
错误;
B项: 向FeBr 溶液中通入过量Cl 生成氯化铁和溴单质:3Cl +2Fe2++4Br-=2Fe3++2Br +6Cl-,B
2 2 2 2
正确;
C项: 向NH Al(SO ) 溶液中滴入少量NaOH溶液,铝离子先产生沉淀:
4 4 2
Al3++3OH-=Al(OH)
3 ,C错误;
D项: 向KMnO 酸性溶液中滴入H O 溶液生成硫酸锰、硫酸钾、氧气和水,得失电子、
4 2 2
MnO-
电荷和元素应守恒:2 4+5H O +6H+=2Mn2++5O ↑+8H O,D错误;
2 2 2 2
答案选B。
9.(2022·河南郑州·一模)下列相关原理或化学用语错误的是
通电
A.电解MgCl 水溶液制取Mg:MgCl Mg+Cl ↑
2 2 2
B.海水提溴的过程中用Cl 氧化Br-:Cl +2Br-=Br +2Cl-
2 2 2
2
C.食盐水精制的过程中用Na CO 除去Ba2+:Ba2++CO3 =BaCO ↓
2 3 3
2 2
D.锅炉除垢的过程中把CaSO 转化为CaCO :CaSO (s)+CO3 (aq)=CaCO (s)+SO4 (aq)
4 3 4 3
【答案】A
【解析】A项:电解MgCl 水溶液无法得到Mg单质,会得到Mg(OH) ,A错误;
2 2
B项:海水提溴的过程中用Cl 氧化Br-得到溴单质,离子方程式为Cl +2Br-=Br +2Cl-,B正
2 2 2
确;
2
C项:Na CO 可以除去Ba2+且不引入新的杂质,离子方程式为Ba2++CO3 =BaCO ↓,C正
2 3 3
确;
D项:CaSO 与浓度较大的可溶性碳酸盐反应可以得到碳酸钙,再用酸可以将其除去,离子
4
2 2
方程式为CaSO (s)+CO3 (aq)=CaCO (s)+SO4 (aq),D正确;
4 3综上所述答案为A。
10.(2022·甘肃·二模)下列过程中的化学反应,相应的离子方程式书写不正确的是
A.向稀盐酸中加入少量钠粒:2Na+2H O=Na++2OH-+H ↑
2 2
B.硫酸酸化的淀粉碘化钾溶液久置后变蓝:4I-+O +4H+=2I +2H O
2 2 2
S O2-
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠: 2 3 +2H+=SO ↑+S↓+H O
2 2
D.向含氯化铁的氯化镁溶液中加入氧化镁:2Fe3++3MgO+3H O=2Fe(OH) ↓+3Mg2+
2 3
【答案】A
【解析】A项:向稀盐酸中加入少量钠粒,钠和HCl电离的氢离子反应,2Na+2H+=2Na+
+H ↑,A错误;
2
B项:硫酸酸化的碘化钾淀粉溶液久置后变蓝是因为碘离子被空气中的氧气氧化为碘单
质,B正确;
C项:硫代硫酸钠在酸性条件下发生反应生成二氧化硫、硫单质和水,该离子方程式正
确,C正确;
D项:向含氯化铁的氯化镁溶液中加入氧化镁,氧化镁消耗Fe3+水解产生的氢离子,使
Fe3+的水解平衡正向移动生成Fe(OH) 沉淀,该离子方程式正确,D正确;
3
答案选A。
11.(2022·山西临汾·三模)下列关于离子反应或离子共存表达正确的是
CO2- AlO-
A.以下离子在0.1mol·L-1NaOH溶液中能大量共存:Na+、K+、 3 、 2
B.以下离子在0.1mol·L-1K CO 溶液中能大量共存:Na+、Ba2+、Cl-、OH-
2 3
AlO- NH+
C.向氯化铝溶液中滴加过量氨水:4NH ·H O+Al3+= 2+4 4+2H O
3 2 2
D.漂白粉漂白原理:Ca(ClO) +2CO +2H O=Ca(HCO ) +2HClO
2 2 2 3 2
【答案】A
CO2- AlO-
【解析】A项:OH-与Na+、K+、 3 、 2都不反应,可以共存,故A正确;
CO2-
B项: 3 与Ba2+反应生成BaCO 沉淀,不能共存,故B错误;
3
C项:氢氧化铝为两性氢氧化物,但氢氧化铝不溶于氨水,正确的离子方程式为Al3+
NH+
+3NH ·H O=Al(OH) ↓+3 4,故C错误;
3 2 3D项:漂白粉漂白原理为:Ca(ClO) +CO +H O=CaCO ↓+2HClO,故D错误;
2 2 2 3
故选A。
12.(2022·山西太原·二模)宏观辨识和微观探析是化学学科的核心素养之一。下列描述物
质制备和应用的离子方程式正确的是
2
A.泡沫灭火器的反应原理:2Al3++3CO3 +3H O=2Al(OH) ↓+3CO ↑
2 3 2
B.海水提溴工艺中,用纯碱溶液富集Br :Br +2OH-=Br-+BrO-+H O
2 2 2
2
2
C.锅炉除垢过程中将CaSO 转化为CaCO :CaSO (s)+CO3 (aq) CaCO (s)+SO4 (aq)
4 3 4 3
通电
D.用惰性电极电解饱和MgCl 溶液:2Cl-+2H O Cl ↑+H ↑+2OH-
2 2 2 2
【答案】C
【解析】A项:泡沫灭火器的反应原理:Al3++3HCO3=Al(OH) ↓+3CO ↑,故A错误;
3 2
2
B项:海水提溴工艺中,用纯碱溶液富集Br :3Br +3CO3 =5Br-+BrO3+3CO ↑,故B错误;
2 2 2
2
2
C项:CaCO 比CaSO 更难溶,故为CaSO (s)+CO3 (aq) CaCO (s)+SO4 (aq),故C正确;
3 4 4 3
通电
D项:用惰性电极电解饱和MgCl 溶液:Mg2++2Cl-+2H O Cl ↑+H ↑+Mg(OH) ↓,故D错
2 2 2 2 2
误;
故选C。
13.(2022·山西吕梁·一模)下列离子方程式正确的是
0.1molL1MgCl Mg2++Ca(OH) =Mg(OH) +Ca2+
A. 2溶液中加入足量石灰乳: 2 2
AlO-+CO +2H O=Al(OH) +HCO-
B.在偏铝酸钠溶液中通入少量二氧化碳: 2 2 2 3 3
4H++2Fe2++SO2-=2Fe3++SO 2H O
C.酸化的硫酸亚铁溶液长时间存放溶液变黄: 4 2 2
2MnO-+5C O2-+16H+=2Mn2++10CO +8H O
D.用高锰酸钾标准溶液滴定草酸: 4 2 4 2 2
【答案】A
【解析】A项:MgCl 溶液中加入足量石灰乳反应生成氢氧化镁和氯化钙,Ca(OH) 主要以
2 2
固体存在,应该写化学式,反应的离子方程式为:Mg2++Ca(OH) =Mg(OH) +Ca2+,A正
2 2确;
B项:在偏铝酸钠溶液中通入少量二氧化碳生成Al(OH) 沉淀和Na CO ,反应的离子反应方
3 2 3
AlO CO2
程式:2 2+CO +3H O=2Al(OH) ↓+ 3 ,B错误;
2 2 3
C项:酸化的FeSO 溶液长时间存放溶液变黄是由于Fe2+被溶解在溶液中的O 氧化为Fe3+,
4 2
反应的离子方程式为:4H++4Fe2++O =4Fe3++2H O,C错误;
2 2
D项:草酸是二元弱酸,主要以电解质分子存在,不能拆写为离子形式,离子方程式应该
2MnO-+5H C O +6H+=2Mn2++10CO +8H O
为: 4 2 2 4 2 2 ,D错误;
故合理选项是A。
14.(2022·山西吕梁·一模)常温下,下列各组离子在指定溶液中可能大量共存的是
c
OH-
=11012
A.在 c H+ 的溶液中: HCO、K、Na、SO2
3 4
Na、OH、Br、K
B.含有大量Fe3+的溶液中:
pH0 Na+、K+、SO2-、S O2-
C. 的溶液中: 4 2 3
K
w 11012molL1
D.在c
OH-
的溶液中:Na、Ba2、Cl、Br
【答案】D
c
OH-
=1×1012
【解析】A项:
c
H+ 的溶液显碱性,含有大量OH-,OH-与HCO
反应产生H
2
O、
3
CO2
3 ,不能大量共存,A错误;
B项:含有大量Fe3+的溶液中,Fe3+与OH-会反应产生Fe(OH) 沉淀而不能大量共存,B错
3
误;
2
C项: pH=0的溶液呈酸性含有大量H+,H+与S O3 在强酸性溶液中会反应产生H O、S、
2 2
SO 而不能大量共存,C错误;
2K
W =1×10-12
D项:c
OH-
溶液呈碱性,含有大量OH-,OH-与选项离子Na+、Ba2+、Cl-、Br-不能
发生任何反应,可以大量共存,D正确;
故合理选项是D。
15.(2022·吉林延边·一模)下列过程中的化学反应对应的离子方程式正确的是
A.用KSCN试剂检验Fe3+:Fe3++3SCN-=Fe(SCN) ↓
3
2 2
B.向Na S O 溶液中加入足量稀硫酸:2S O3 +4H+=SO4 +3S↓+2H O
2 2 3 2 2
2
C.向Na CO 溶液中通入过量SO :CO3 +2SO +H O=CO +2HSO3
2 3 2 2 2 2
D.将洗净的鸡蛋壳浸泡在米醋中获得溶解液:2H++CaCO =Ca2++H O+CO ↑
3 2 2
【答案】C
【解析】A项:Fe3+遇KSCN溶液变为血红色,不是生成沉淀,反应的离子方程式:Fe3+
+3SCN-=Fe(SCN) ,故A错误;
3
B项:硫代硫酸钠与稀硫酸反应生成硫单质和二氧化硫气体,溶液出现浑浊,生成无色刺
2
激性气味气体,反应的离子方程式为:S O3 +2H+═SO ↑+S↓+H O,故B错误;
2 2 2
2
C项:亚硫酸的酸性比碳酸强,向Na CO 溶液中通入过量SO ,离子方程式为:CO3
2 3 2
+2SO +H O=CO +2HSO3,故C正确;
2 2 2
D项:醋酸是弱酸,应保留化学式,鸡蛋壳中含碳酸钙难溶于水,也保留化学式,反应的
离子方程式为:2CH COOH+CaCO =Ca2++H O+CO ↑+2CH COO-,故D错误;
3 3 2 2 3
故选:C。
16.(2022·新高考湖南三模)下列离子方程式正确的是
A. 通入冷水中:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:【答案】C
【解析】A项:Cl 通入冷水中发生反应生成盐酸和次氯酸,该反应的离子方程式为
2
Cl +H O=Cl-+HClO+H+,A错误;
2 2
B项:用醋酸和淀粉-KI溶液检验加碘盐中的 的原理是 在酸性条件下与I-发生归中
反应生成I 而遇淀粉变蓝,由于醋酸是弱酸,在离子方程式中不能用H+表示,因此B
2
不正确;
C项:H O 具有较强的氧化性,FeSO 溶液中加入H O 产生的沉淀是氢氧化铁,该反应的离
2 2 4 2 2
子方程式为2Fe2++ H O +4H O=2Fe(OH) ↓+4H+,C正确;
2 2 2 3
D项:NaHCO 溶液与少量的Ba(OH) 溶液混合后发生反应生成碳酸钡沉淀、碳酸钠和水,
3 2
NaHCO 过量,Ba(OH) 全部参加反应,因此该反应的离子方程式为2 +Ba2++2OH-
3 2
=BaCO ↓+ +2H O,D不正确;
3 2
综上所述,本题选C。
二、主观题(4×13=42分)
17.(13分)(2022·山西太原·二模)某工业生产上用铜镍矿石(主要成分为CuS、NiS、
FeS、SiO 及不溶于酸的杂质)制备胆矾CuSO •5H O的流程如图。
2 4 2
已知:有机萃取剂HR可以萃取Cu2+,其萃取原理(org为有机相)Cu2+(aq)+2HR(org)
反
萃
萃
取
取
CuR (org)+2H+(aq)。
2
回答下列问题:
(1)为了提高焙烧的速度,可采取的措施是____。(2)“调节pH时,生成氢氧化铁沉淀的离子方程式为____,
(3)25℃时,“调节pH”后,测得滤液中各离子浓度及相关数据如表所示。(lg2=0.3)
离子 Fe3+ Cu2+ Ni2+ Fe2+
浓度/(mol·L-1) 1.0×10-6 5.0 1.2 0
对应氢氧化物的K 6.4×10-38 2.2×10-20 2.0×10-15 8.0×10-16
sp
该滤液的pH为___;加入的Cu(OH) ____(填“已经”或“没有”)完全溶解。
2
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,该反
应的离子方程式为___。
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为___。
(6)将得到的胆矾产品做热重分析,测得的数据如图所示。
已知:杂质不分解,250℃时,胆矾失去所有结晶水。则A点胆矾分解得到的物质为___(填
化学式)。
【答案】(1)粉碎
(2) 2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+,
2 3
(3) 3.6 已经
(4)2Ni2++ClO-+4OH-=2NiOOH↓+Cl-+H O
2
(5)向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,重复操作2~3次。
(6) CuSO •3H O
4 2
【解析】由题中流程可知,铜镍矿石(主要成分为CuS、NiS、FeS、SiO 及不溶于酸的杂质)
2
粉碎焙烧,充分氧化,烟气的主要成分为二氧化硫,加稀硫酸酸浸,过滤,滤渣1为SiO
2
和不溶于酸的杂质,滤液中加入H O ,氧化Fe2+生成Fe3+,再加入Cu(OH) 调节溶液pH,使
2 2 2
Fe3+完全转化为Fe(OH) 沉淀,继续过滤,滤渣2为Fe(OH) ,滤液中加入HR进行萃取,除
3 3
去镍离子,有机相中加入硫酸进行反萃取,水相的主要成分为硫酸铜溶液,加热蒸发,冷
却结晶,过滤,洗涤,干燥即可获得产品;据此解答。(1)由上述分析可知,焙烧前粉碎的目的是增大接触面积,提高反应速率,使矿石充分氧化;
答案为粉碎。
(2)由上述分析可知,加入Cu(OH) 调节溶液pH,使Fe3+完全转化为Fe(OH) 沉淀,生成氢氧
2 3
化铁沉淀的离子方程式为2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+;由题中信息Cu2+(aq)+2HR(org)
2 3
反 萃 萃 取 取 CuR (org)+2H+(aq)可知,要使平衡逆向移动,则增加H+浓度,即有机相中加入硫
2
酸进行反萃取,可以分离铜离子,还不会产生杂质,所以选项c正确;答案为2Fe3+
+3Cu(OH) =2Fe(OH) ↓+3Cu2+;c。
2 3
(3)由题中表格数据可知,25℃时,“调节pH”后,测得滤液中c(Fe3+)=1.0×10-6mol/L,
c(Cu2+)=5.0mol/L,因为K [Fe(OH) ]= 6.4×10-38,所以c(Fe3+)×c3(OH-)= K [Fe(OH) ],则c(OH-)=
sp 3 sp 3
K FeOH
sp 3 6.41038 K 11014 1
3 c Fe3 = 3 =4×10-11mol/L,c(H+)= w = ×10-3mol/L,
1106 c(OH) 41011 4
pH=3+lg4=3+2lg2=3.6;又c(Cu2+)×c2(OH-)=5×(4×10-11)2=8×10-21<K [Cu(OH) ]=2.2×10-20,所以
sp 2
Cu(OH) 已经完全溶解;答案为3.6;已经。
2
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,即
NiSO 与NaClO发生氧化还原反应,该反应的化学方程式为
4
2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O;答案为2Ni2++ClO-+4OH-=2NiOOH↓+Cl-
4 2 4 2
+H O。
2
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流
下后,重复操作2~3次;答案为向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,重复
操作2~3次。
(6)由题中信息和图示可知,杂质不分解,250℃时,胆矾失去所有结晶水,此时失重率为
34.75%,设产品总质量为m克,该胆矾产品的纯度为x,则
CuSO ·5H O CuSO 5H O
4 2 4 2
250g 90g
25034.75%
,解之x= =96.53%;A点时,失重率
mgx mg34.75% 90
为13.90%,设A点胆矾分解得到的物质为CuSO •yH O,则
4 2CuSO ·5H O CuSO ·yH O (5y)H O
4 2 4 2 2
250g 185yg
,所以 ,解
mg96.53% mg13.90% 25013.90%18(5y)96.53%
之y=3,所以A点胆矾分解得到的物质为CuSO •3H O;答案为CuSO •3H O;96.53%。
4 2 4 2
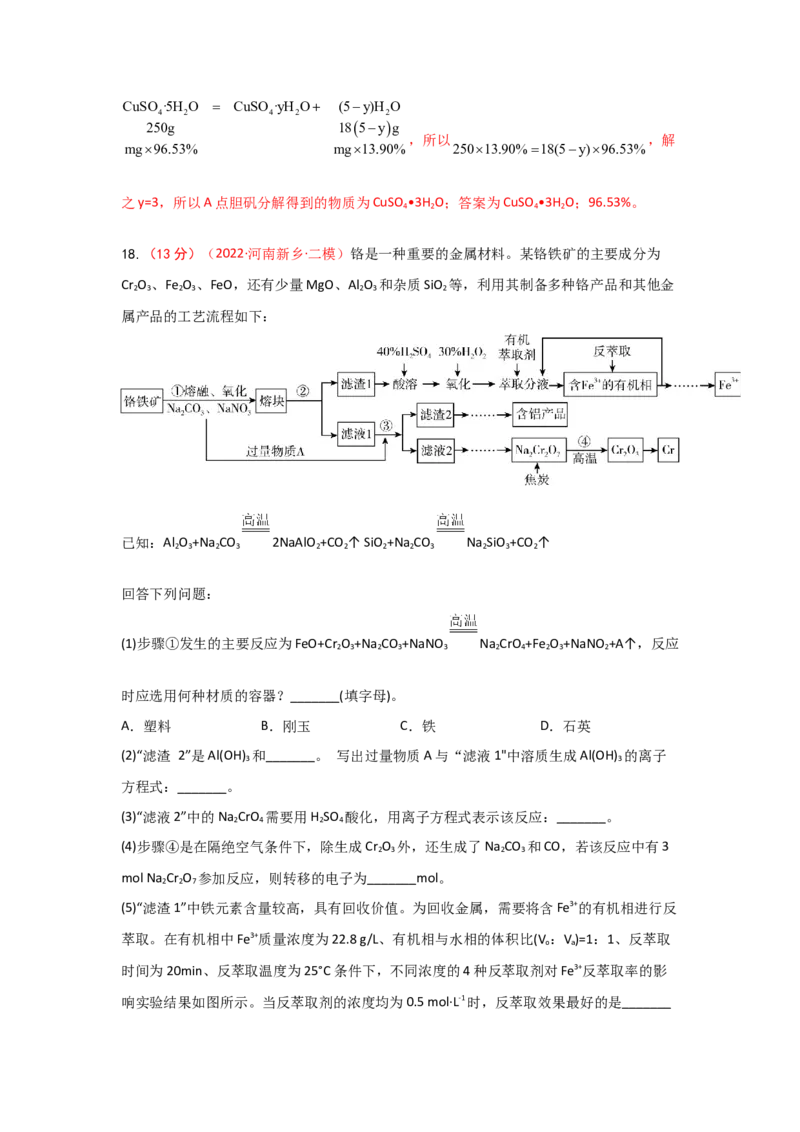
18.(13分)(2022·河南新乡·二模)铬是一种重要的金属材料。某铬铁矿的主要成分为
Cr O 、Fe O 、FeO,还有少量MgO、Al O 和杂质SiO 等,利用其制备多种铬产品和其他金
2 3 2 3 2 3 2
属产品的工艺流程如下:
已知:Al O +Na CO 2NaAlO +CO ↑ SiO +Na CO Na SiO +CO ↑
2 3 2 3 2 2 2 2 3 2 3 2
回答下列问题:
(1)步骤①发生的主要反应为FeO+Cr O +Na CO +NaNO Na CrO +Fe O +NaNO +A↑,反应
2 3 2 3 3 2 4 2 3 2
时应选用何种材质的容器?_______(填字母)。
A.塑料 B.刚玉 C.铁 D.石英
(2)“滤渣 2”是Al(OH) 和_______。 写出过量物质A与“滤液1"中溶质生成Al(OH) 的离子
3 3
方程式:_______。
(3)“滤液2”中的Na CrO 需要用H SO 酸化,用离子方程式表示该反应:_______。
2 4 2 4
(4)步骤④是在隔绝空气条件下,除生成Cr O 外,还生成了Na CO 和CO,若该反应中有3
2 3 2 3
mol Na Cr O 参加反应,则转移的电子为_______mol。
2 2 7
(5)“滤渣1”中铁元素含量较高,具有回收价值。为回收金属,需要将含Fe3+的有机相进行反
萃取。在有机相中Fe3+质量浓度为22.8 g/L、有机相与水相的体积比(V:V)=1:1、反萃取
o a
时间为20min、反萃取温度为25°C条件下,不同浓度的4种反萃取剂对Fe3+反萃取率的影
响实验结果如图所示。当反萃取剂的浓度均为0.5 mol·L-1时,反萃取效果最好的是_______(填化学式),在实际操作中需在该反萃取剂中加入一定量H PO 溶液,其目的是_______ ;
3 4
但H PO 浓度不宜过大,其原因是_______。[已知:(NH ) HPO 溶液pH=7.8 ~8.2]
3 4 4 2 4
【答案】(1)C
(2) H SiO AlO +CO +2H O=Al(OH) ↓+HCO
2 3 2 2 3
(3)2CrO +2H+ Cr O +H O
2 2
(4) 18
(5) (NH ) HPO 调节溶液的pH,防止Fe3+在反萃取时可能生成沉淀 pH小会生
4 2 4
成NH H PO ,反萃取率低(或其他合理解释)
4 2 4
【解析】根据题干信息,铬铁矿的主要成分为Cr O 、Fe O 、FeO,还有少量MgO、Al O 和
2 3 2 3 2 3
杂质SiO 等,现向熔融的铬铁矿中加入Na CO 、NaNO 氧化,步骤①发生的反应有
2 2 3 3
Al O +Na CO 2NaAlO +CO ↑、SiO +Na CO Na SiO +CO ↑、
2 3 2 3 2 2 2 2 3 2 3 2
2FeO+Cr O +2Na CO +4NaNO 2Na CrO +Fe O +4NaNO +2A↑,则A为CO ,熔块经水浸、
2 3 2 3 3 2 4 2 3 2 2
过滤后分离出滤渣1含Fe O ,滤渣1经酸溶、氧化、萃取分液、反萃取得到Fe3+。滤液1
2 3
中含NaAlO 、Na CrO 、Na SiO 、NaNO 、NaNO 等,向滤液1中通入过量的CO ,得到滤渣
2 2 4 2 3 2 3 2
2含H SiO 、Al(OH) ,滤液2中含Na CrO ,酸化后得到Na Cr O ,再加入焦炭高温还原得到
2 3 3 2 4 2 2 7
Cr O ,进而得到Cr,据此分析解答。
2 3
(1)步骤①中发生反应2FeO+Cr O +2Na CO +4NaNO 2Na CrO +Fe O +4NaNO +2CO ↑,因
2 3 2 3 3 2 4 2 3 2 2
此该步骤不能使用石英容器,原因是二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳,刚玉(氧化铝)与碱性物质高温下反应,塑料不耐热,可选铁坩埚,故答案选C;
(2)由分析,步骤②得到滤渣1和滤液2,故操作为水浸、过滤,滤液1中通入过量的CO ,
2
得到滤渣2含H SiO 、Al(OH) ,生成Al(OH) 的离子方程式为AlO +CO +2H O=Al(OH) ↓+HCO
2 3 3 3 2 2 3
;
(3)滤液2中含Na CrO ,酸化后得到Na Cr O ,转化的离子方程式为2CrO +2H+ Cr O
2 4 2 2 7 2
+H O;
2
(4)步骤④是在隔绝空气条件下,除生成Cr O 外,还生成了Na CO 和CO,Cr元素由+6价降
2 3 2 3
低为+3价,若该反应中有3 mol Na Cr O 参加反应,则转移的电子为3mol×2×3=18mol;
2 2 7
(5)结合图像可知,浓度为0.5mol/L时,(NH ) HPO 的反萃取率较高,因此反萃取效果最好
4 2 4
的是(NH ) HPO ,由于Fe3+易生成Fe(OH) ,因此在该反萃取剂中加入一定量H PO 溶液调节
4 2 4 3 3 4
溶液的pH,防止Fe3+在反萃取时可能生成Fe(OH) 沉淀,但pH过小会生成NH H PO ,导致
3 4 2 4
反萃取率低,因此H PO 溶液浓度不宜过大。
3 4
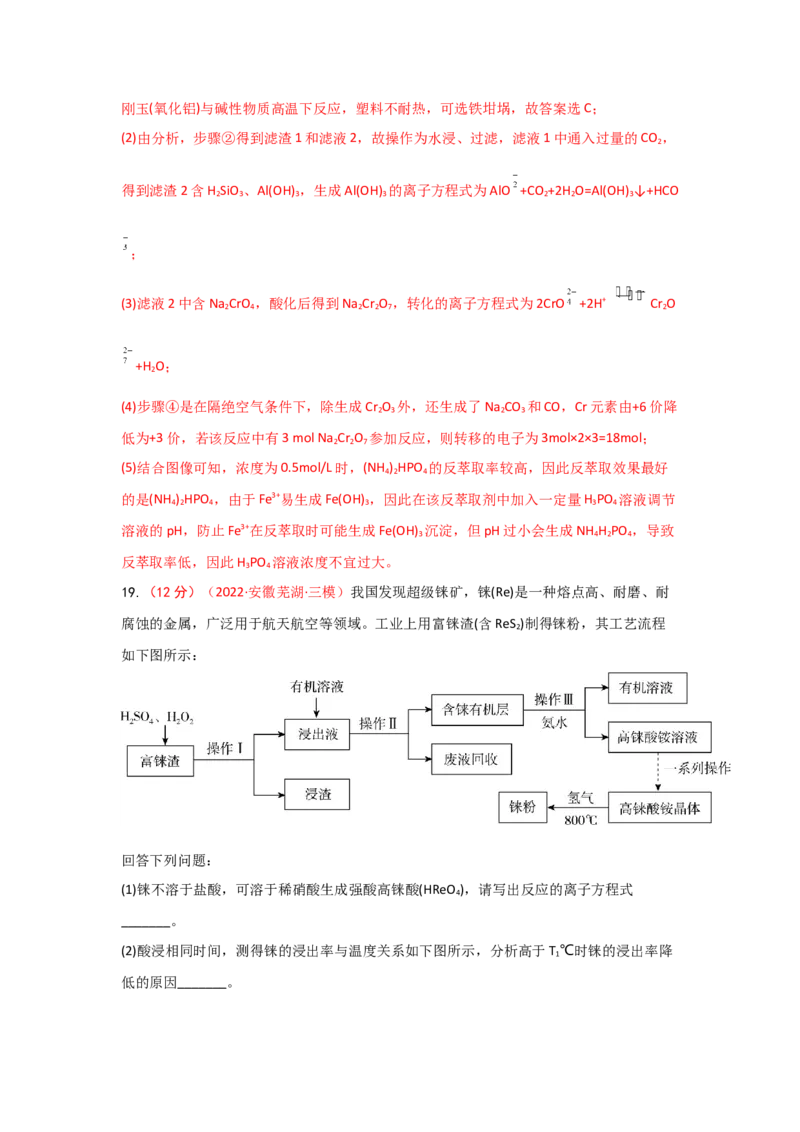
19.(12分)(2022·安徽芜湖·三模)我国发现超级铼矿,铼(Re)是一种熔点高、耐磨、耐
腐蚀的金属,广泛用于航天航空等领域。工业上用富铼渣(含ReS )制得铼粉,其工艺流程
2
如下图所示:
回答下列问题:
(1)铼不溶于盐酸,可溶于稀硝酸生成强酸高铼酸(HReO ),请写出反应的离子方程式
4
_______。
(2)酸浸相同时间,测得铼的浸出率与温度关系如下图所示,分析高于T ℃时铼的浸出率降
1
低的原因_______。(3)操作II所用的主要玻璃仪器是_______。
(4)高铼酸铵和氢气制取单质铼的化学方程式为_______;
(5)由高铼酸铵溶液获得高铼酸铵晶体的一系列操作为_______、洗涤、干燥。
(6)整个工艺流程中除有机溶液可循环利用外,还有_______。
【答案】(1)3Re +4H+ +7NO = 3ReO +7 NO↑+ 2H O
2
(2) 超过T °C时,过氧化氢分解
1
(3)分液漏斗
(4) 2NH ReO + 7H 2NH +2Re+8H O
4 4 2 3 2
(5)蒸发浓缩、冷却结晶
(6)NH 或H SO
3 2 4
【解析】由题给流程可知,向富铼渣中加入稀硫酸和过氧化氢溶液浸取,二硫化铼与过氧
化氢溶液反应得到高铼酸和硫酸,过滤得到滤渣和含有高铼酸、硫酸的浸出液;向浸出液
中加入有机溶液萃取高铼酸,分液得到含有高铼酸的有机层和含有硫酸的废液;向有机层
中加入氨水反萃取,分液得到有机溶液和高铼酸铵溶液;高铼酸铵溶液经蒸发浓缩、冷却
结晶等一系列操作得到高铼酸铵晶体,高铼酸铵晶体与氢气在800℃条件下共热反应制得
铼粉,整个工艺流程中有机溶液、氨气、硫酸可循环利用可循环利用。
(1)由题意可知,铼与稀硝酸反应生成高铼酸、一氧化氮和水,反应的离子方程式为3Re
+4H+ +7NO = 3ReO +7 NO↑+ 2H O,故答案为:3Re +4H+ +7NO = 3ReO +7 NO↑+ 2H O;
2 2
(2)温度高于T ℃时,过氧化氢受热易分解,过氧化氢的浓度降低,所以酸浸相同时间铼的
1
浸出率降低,故答案为:将富铼渣粉碎、适当增大H SO 和H O 的浓度、适当升温、搅拌
2 4 2 2
等;超过T °C时,过氧化氢分解;
1
(3)由分析可知,操作II为分液,所用的主要玻璃仪器为分液漏斗,故答案为:分液漏斗;(4)由分析可知,高铼酸铵晶体与氢气在800℃条件下共热反应生成铼、氨气和水,反应的
化学方程式为2NH ReO + 7H 2NH +2Re+8H O;得到铼粉时,为防止铼被空气中氧气氧
4 4 2 3 2
化,反应开始时,需要用氢气排尽装置内空气,反应结束时,需要用保护气,所以反应过
程中,实际消耗氢气的量大于理论值,故答案为:2NH ReO + 7H 2NH +2Re+8H O;
4 4 2 3 2
(5)由分析可知,高铼酸铵溶液经蒸发浓缩、冷却结晶等一系列操作得到高铼酸铵晶体,故
答案为:蒸发浓缩、冷却结晶;
(6)由分析可知,整个工艺流程中有机溶液、氨气、硫酸可循环利用可循环利用,故答案为:
NH 或H SO 。
3 2 4
20.(14分)(2022·陕西汉中·二模)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主
要成分为含锰化合物及FeS)与氧化锰矿(主要成分为MnO 等锰的氧化物)为原料制备硫酸锰
2
的工艺流程如下:
已知:①“混合焙烧”后烧渣含MnSO 、Fe O 及少量FeO、Al O 、MgO。
4 2 3 2 3
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
物质 Fe(OH) Fe(OH) Mn(OH) Al(OH)
3 2 2 3
开始沉淀的pH 1.9 7.6 7.3 3.0
完全沉淀的pH 3.2 9.6 9.3 5.2
③离子浓度≤10-5mol·L-1时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______(2)若试剂a为MnO ,则氧化步骤发生反应的离子方程式为_______,若省略“氧化”步骤,
2
造成的影响是_______。
(3)“中和除杂”时,应控制溶液的pH范围是_______。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1。则溶液中c(Mg2+)和c(Ca2+)的比值
=_______(已知:K (MgF )=6.4×10-10;K (CaF )=3.6×10-12)
sp 2 sp 2
(5)“碳化结晶”时发生反应的离子方程式为_______,选择NH HCO 而不选择Na CO 溶液的
4 3 2 3
原因是_______。
【答案】(1)除去矿物中的硫元素(或将硫化物转变为金属氧化物)
(2) MnO +4H++2Fe2+=Mn2++2Fe3++2H O Fe2+完全沉淀时Mn2+已经完全沉淀,造成Mn2+损
2 2
失
(3)5.2≤pH<7.3(或5.2~7.3)
(4)1600/9(177.8或177.78)
-
(5) Mn2++2HCO3=MnCO ↓+CO ↑+H O 碳酸钠溶液碱性强,会使Mn2+水解为Mn(OH)
3 2 2 2
【解析】高硫锰矿(主要成分为含锰化合物及FeS)与氧化锰矿混合焙烧,得到MnSO 、Fe O
4 2 3
及少量FeO、Al O 、MgO,加入硫酸,得到Mn2+、Fe2+、Fe3+、Mg2+、Al3+的酸性溶液,加入
2 3
二氧化锰将亚铁离子氧化为铁离子,再加入碳酸钙中和,将铁离子与铝离子以氢氧化物的
形式除去,加入MnF 氟化除杂,使溶液中的Mg2+、Ca2+沉淀完全,此时溶液中的金属离子
2
-
为锰离子,加入碳酸氢铵发生Mn2++2HCO3=MnCO ↓+CO ↑+H O,加入硫酸溶解得硫酸锰
3 2 2
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等系列操作得到硫酸锰晶体。
(1)高锰矿含有FeS, “混合焙烧”可以将金属硫化物转化为金属氧化物,同时除去硫元素,
故“混合焙烧”主要目的是除去矿物中的硫元素(或将硫化物转变为金属氧化物);
(2)若试剂a为MnO ,氧化时用二氧化锰氧化亚铁离子生成三价铁离子,本身被还原成二价
2
锰离子,则氧化步骤发生反应的离子方程式为MnO +4H++2Fe2+=Mn2++2Fe3++2H O;若省略
2 2
“氧化”步骤,则铁元素只能以Fe2+形式除去,但是由表格可知除去亚铁离子的同时锰离
子也除去了,即造成的影响是Fe2+完全沉淀时Mn2+已经完全沉淀,造成Mn2+损失;
(3)“中和除杂”的目的是使铝离子、铁离子完全沉淀且锰离子不沉淀,则由表格可知要控制
溶液的pH范围是5.2≤pH<7.3(或5.2~7.3);
(4)“氟化除杂”后,溶液中c(F- )浓度为0.05mol/L。则溶液中c(Mg2+):c(Ca2+)=K (MgF ):
sp 2
K (CaF )=(6.4×10-10):(3.6×10-12)=1600/9(177.8或177.78);
sp 2(5)“碳化结晶”时选择NH HCO ,生成碳酸锰,结合原子守恒、电荷守恒可知发生反应的离
4 3
-
子方程式为Mn2++2HCO3=MnCO ↓+CO ↑+H O;碳酸根离子水解程度大,碱性强,会促进
3 2 2
锰离子水解为氢氧化锰,故“碳化结晶”时不选择Na CO 溶液的原因是:碳酸钠溶液碱性
2 3
强,会使Mn2+水解为Mn(OH) 。
2