文档内容
催化机理循环图
催化剂:在连续反应中从一开始就参与了反应,在最后又生成,所以仅从结果上来看似乎并没有发生
变化,实则是消耗多少后续又生成了多少。
中间产物:在连续反应中为某一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看
似乎并没有生成,实则是生成多少后续又消耗多少。
在含少量I-的溶液中,H O 分解的机理为
2 2
H O +I-―→H O+IO- 慢
2 2 2
H O +IO-―→O +I-+H O 快
2 2 2 2
在该反应中I-为催化剂,IO-为中间产物。
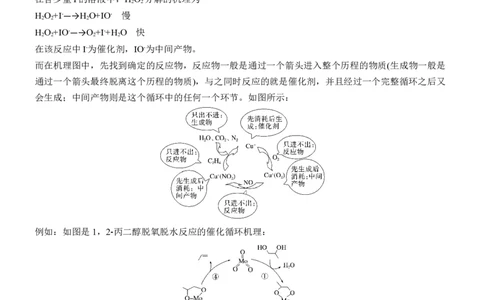
而在机理图中,先找到确定的反应物,反应物一般是通过一个箭头进入整个历程的物质(生成物一般是
通过一个箭头最终脱离这个历程的物质),与之同时反应的就是催化剂,并且经过一个完整循环之后又
会生成;中间产物则是这个循环中的任何一个环节。如图所示:
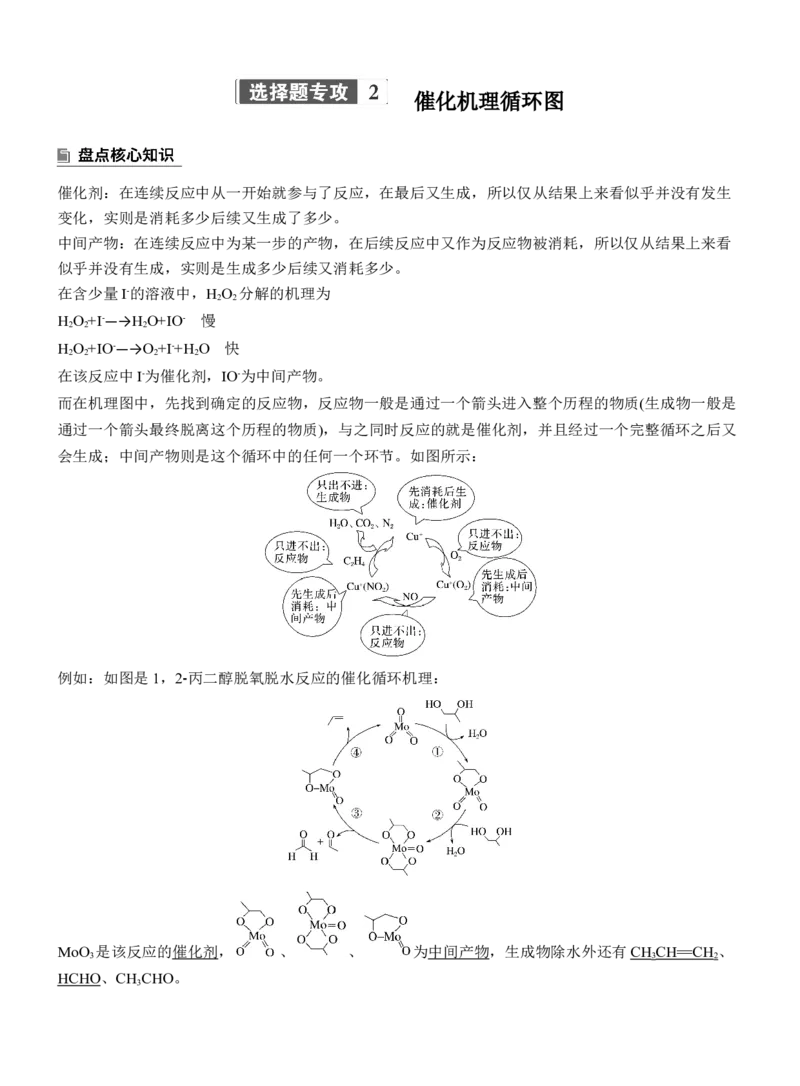
例如:如图是1,2⁃ 丙二醇脱氧脱水反应的催化循环机理:
MoO 是该反应的催化剂, 、 、 为中间产物,生成物除水外还有CH CH == CH 、
3 3 2
HCHO、CH CHO。
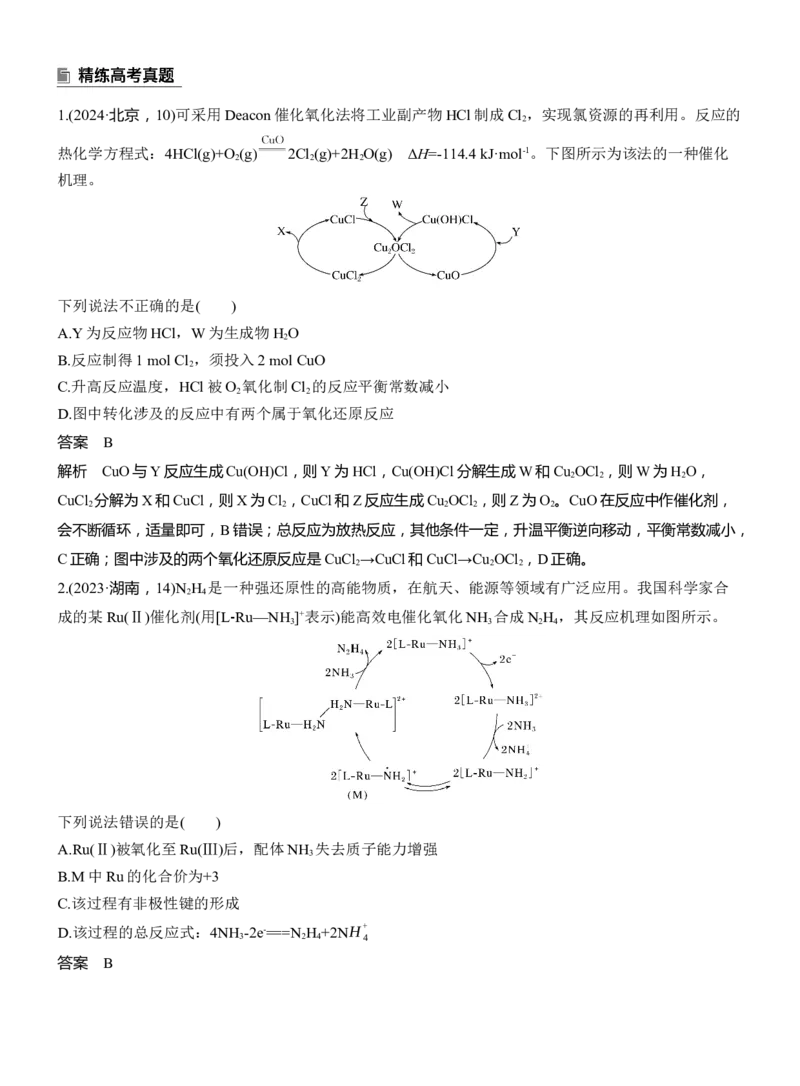
31.(2024·北京,10)可采用Deacon催化氧化法将工业副产物HCl制成Cl ,实现氯资源的再利用。反应的
2
热化学方程式:4HCl(g)+O (g) 2Cl (g)+2H O(g) ΔH=-114.4 kJ·mol-1。下图所示为该法的一种催化
2 2 2
机理。
下列说法不正确的是( )
A.Y为反应物HCl,W为生成物H O
2
B.反应制得1 mol Cl ,须投入2 mol CuO
2
C.升高反应温度,HCl被O 氧化制Cl 的反应平衡常数减小
2 2
D.图中转化涉及的反应中有两个属于氧化还原反应
答案 B
解析 CuO与Y反应生成Cu(OH)Cl,则Y为HCl,Cu(OH)Cl分解生成W和Cu OCl ,则W为H O,
2 2 2
CuCl 分解为X和CuCl,则X为Cl ,CuCl和Z反应生成Cu OCl ,则Z为O 。CuO在反应中作催化剂,
2 2 2 2 2
会不断循环,适量即可,B错误;总反应为放热反应,其他条件一定,升温平衡逆向移动,平衡常数减小,
C正确;图中涉及的两个氧化还原反应是CuCl →CuCl和CuCl→Cu OCl ,D正确。
2 2 2
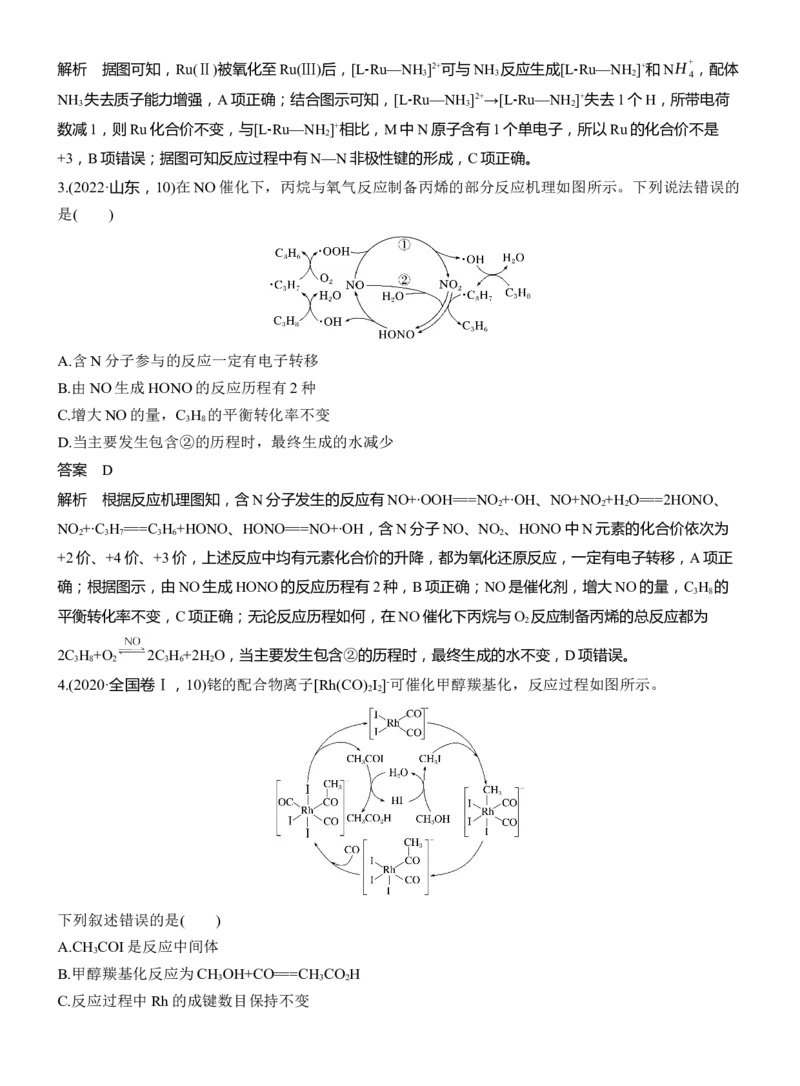
2.(2023·湖南,14)N H 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合
2 4
成的某Ru(Ⅱ)催化剂(用[L⁃Ru—NH
3
]+表示)能高效电催化氧化NH
3
合成N
2
H
4
,其反应机理如图所示。
下列说法错误的是( )
A.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,配体NH 失去质子能力增强
3
B.M中Ru的化合价为+3
C.该过程有非极性键的形成
D.该过程的总反应式:4NH -2e-===N H
+2NH+
3 2 4 4
答案 B解析 据图可知,Ru(Ⅱ)被氧化至Ru(Ⅲ)后,[L⁃Ru—NH
3
]2+可与NH
3
反应生成[L⁃Ru—NH
2
]+和NH+
4
,配体
NH
3
失去质子能力增强,A项正确;结合图示可知,[L⁃Ru—NH
3
]2+→[L⁃Ru—NH
2
]+失去1个H,所带电荷
数减1,则Ru化合价不变,与[L⁃Ru—NH
2
]+相比,M中N原子含有1个单电子,所以Ru的化合价不是
+3,B项错误;据图可知反应过程中有N—N非极性键的形成,C项正确。
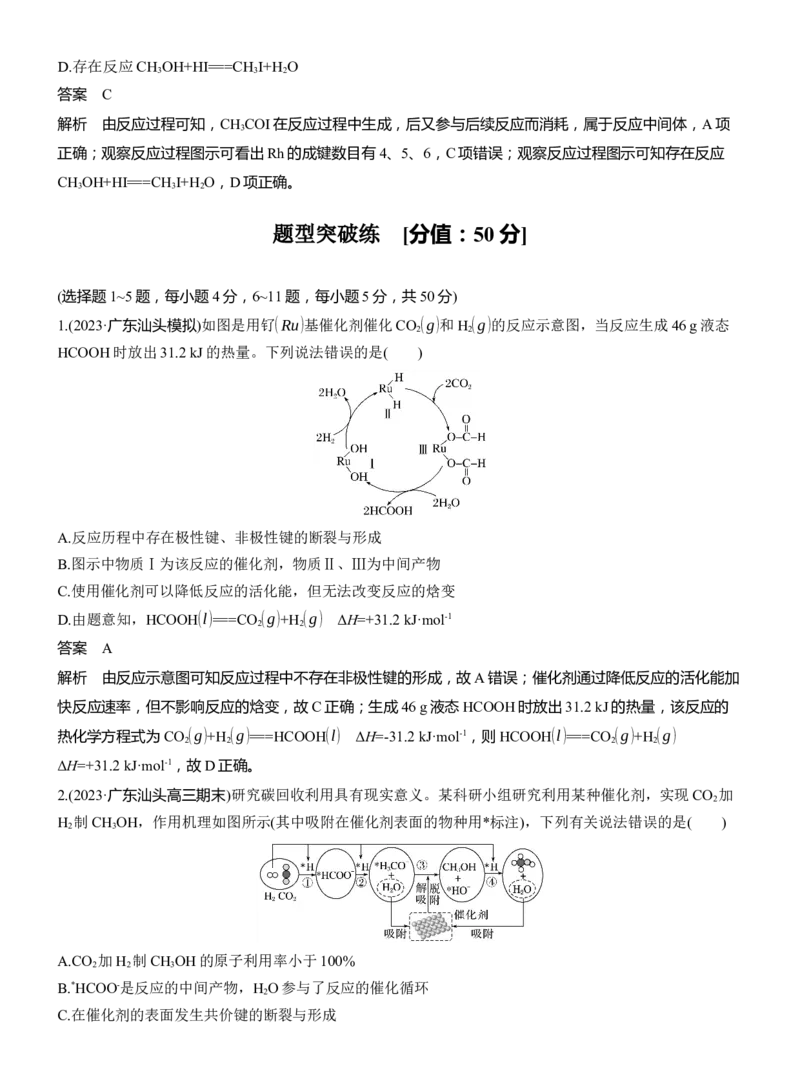
3.(2022·山东,10)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的
是( )
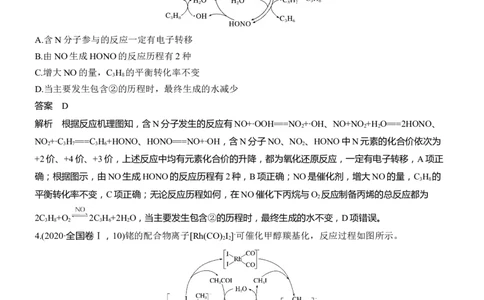
A.含N分子参与的反应一定有电子转移
B.由NO生成HONO的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8
D.当主要发生包含②的历程时,最终生成的水减少
答案 D
解析 根据反应机理图知,含N分子发生的反应有NO+∙OOH===NO +∙OH、NO+NO +H O===2HONO、
2 2 2
NO +∙C H ===C H +HONO、HONO===NO+∙OH,含N分子NO、NO 、HONO中N元素的化合价依次为
2 3 7 3 6 2
+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有电子转移,A项正
确;根据图示,由NO生成HONO的反应历程有2种,B项正确;NO是催化剂,增大NO的量,C H 的
3 8
平衡转化率不变,C项正确;无论反应历程如何,在NO催化下丙烷与O 反应制备丙烯的总反应都为
2
2C H +O 2C H +2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误。
3 8 2 3 6 2
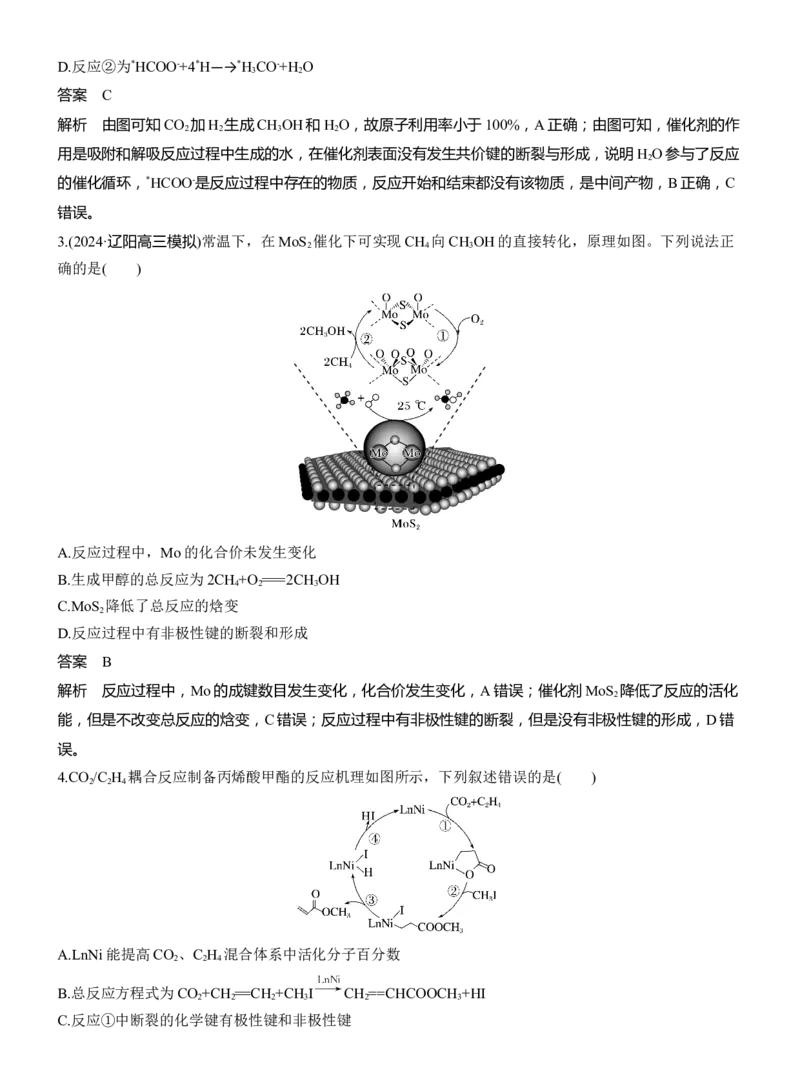
4.(2020·全国卷Ⅰ,10)铑的配合物离子[Rh(CO) I ]-可催化甲醇羰基化,反应过程如图所示。
2 2
下列叙述错误的是( )
A.CH COI是反应中间体
3
B.甲醇羰基化反应为CH OH+CO===CH CO H
3 3 2
C.反应过程中Rh的成键数目保持不变D.存在反应CH OH+HI===CH I+H O
3 3 2
答案 C
解析 由反应过程可知,CH COI在反应过程中生成,后又参与后续反应而消耗,属于反应中间体,A项
3
正确;观察反应过程图示可看出Rh的成键数目有4、5、6,C项错误;观察反应过程图示可知存在反应
CH OH+HI===CH I+H O,D项正确。
3 3 2
题型突破练 [分值:50 分]
(选择题1~5题,每小题4分,6~11题,每小题5分,共50分)
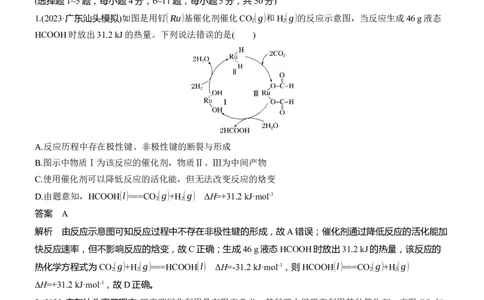
1.(2023·广东汕头模拟)如图是用钌(Ru)基催化剂催化CO (g)和H (g)的反应示意图,当反应生成46 g液态
2 2
HCOOH时放出31.2 kJ的热量。下列说法错误的是( )
A.反应历程中存在极性键、非极性键的断裂与形成
B.图示中物质Ⅰ为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物
C.使用催化剂可以降低反应的活化能,但无法改变反应的焓变
D.由题意知,HCOOH(l)===CO (g)+H (g) ΔH=+31.2 kJ·mol-1
2 2
答案 A
解析 由反应示意图可知反应过程中不存在非极性键的形成,故A错误;催化剂通过降低反应的活化能加
快反应速率,但不影响反应的焓变,故C正确;生成46 g液态HCOOH时放出31.2 kJ的热量,该反应的
热化学方程式为CO (g)+H (g)===HCOOH(l) ΔH=-31.2 kJ·mol-1,则HCOOH(l)===CO (g)+H (g)
2 2 2 2
ΔH=+31.2 kJ·mol-1,故D正确。
2.(2023·广东汕头高三期末)研究碳回收利用具有现实意义。某科研小组研究利用某种催化剂,实现CO 加
2
H 制CH OH,作用机理如图所示(其中吸附在催化剂表面的物种用*标注),下列有关说法错误的是( )
2 3
A.CO 加H 制CH OH的原子利用率小于100%
2 2 3
B.*HCOO-是反应的中间产物,H O参与了反应的催化循环
2
C.在催化剂的表面发生共价键的断裂与形成D.反应②为*HCOO-+4*H―→*H CO-+H O
3 2
答案 C
解析 由图可知CO 加H 生成CH OH和H O,故原子利用率小于100%,A正确;由图可知,催化剂的作
2 2 3 2
用是吸附和解吸反应过程中生成的水,在催化剂表面没有发生共价键的断裂与形成,说明H O参与了反应
2
的催化循环,*HCOO-是反应过程中存在的物质,反应开始和结束都没有该物质,是中间产物,B正确,C
错误。
3.(2024·辽阳高三模拟)常温下,在MoS 催化下可实现CH 向CH OH的直接转化,原理如图。下列说法正
2 4 3
确的是( )
A.反应过程中,Mo的化合价未发生变化
B.生成甲醇的总反应为2CH +O ===2CH OH
4 2 3
C.MoS 降低了总反应的焓变
2
D.反应过程中有非极性键的断裂和形成
答案 B
解析 反应过程中,Mo的成键数目发生变化,化合价发生变化,A错误;催化剂MoS 降低了反应的活化
2
能,但是不改变总反应的焓变,C错误;反应过程中有非极性键的断裂,但是没有非极性键的形成,D错
误。
4.CO /C H 耦合反应制备丙烯酸甲酯的反应机理如图所示,下列叙述错误的是( )
2 2 4
A.LnNi能提高CO 、C H 混合体系中活化分子百分数
2 2 4
B.总反应方程式为CO +CH ==CH +CH I CH ==CHCOOCH +HI
2 2 2 3 2 3
C.反应①中断裂的化学键有极性键和非极性键D.该反应的原子利用率为100%
答案 D
解析 LnNi是催化剂,能降低反应的活化能,提高反应物中活化分子的百分数,A正确;CO 、
2
CH ==CH 、CH I为反应物,CH ==CHCOOCH 、HI为生成物,则总反应方程式为CO +CH ==CH +CH I
2 2 3 2 3 2 2 2 3
CH ==CHCOOCH +HI,B正确;反应①中断裂了极性键(C==O)和非极性键(C==C),C正确;由总反
2 3
应方程式可知,除目标产物丙烯酸甲酯外还有HI生成,原子利用率不是100%,D错误。
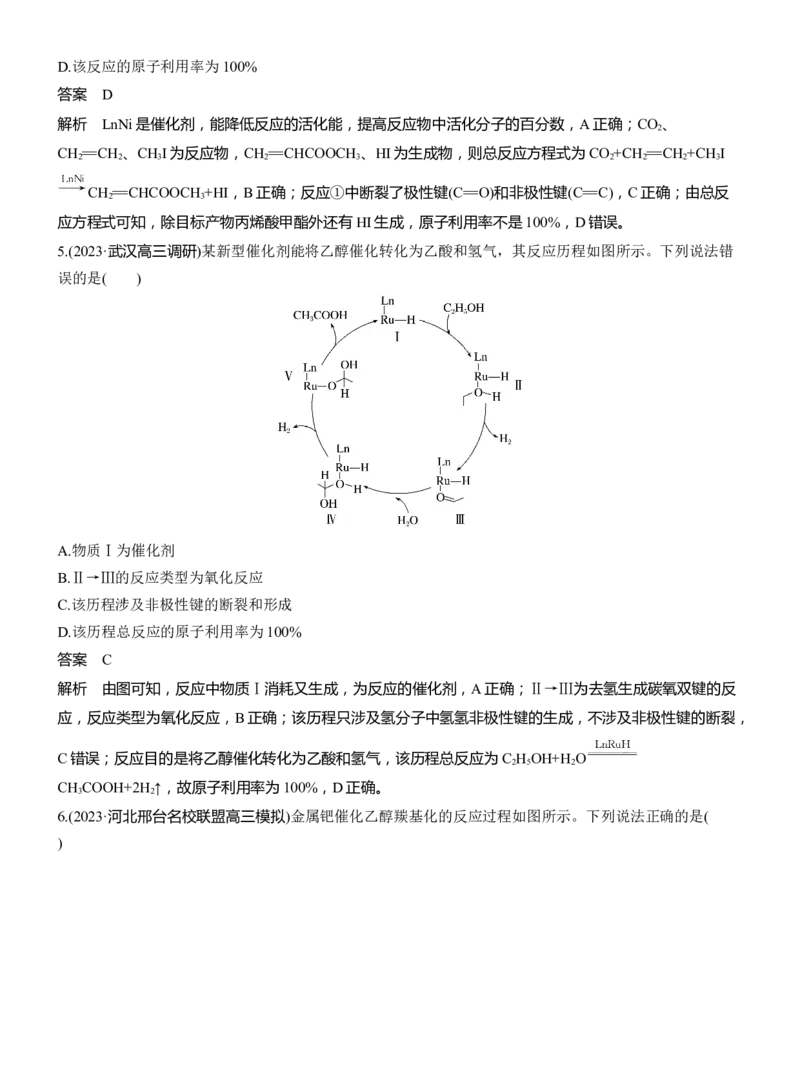
5.(2023·武汉高三调研)某新型催化剂能将乙醇催化转化为乙酸和氢气,其反应历程如图所示。下列说法错
误的是( )
A.物质Ⅰ为催化剂
B.Ⅱ→Ⅲ的反应类型为氧化反应
C.该历程涉及非极性键的断裂和形成
D.该历程总反应的原子利用率为100%
答案 C
解析 由图可知,反应中物质Ⅰ消耗又生成,为反应的催化剂,A正确;Ⅱ→Ⅲ为去氢生成碳氧双键的反
应,反应类型为氧化反应,B正确;该历程只涉及氢分子中氢氢非极性键的生成,不涉及非极性键的断裂,
C错误;反应目的是将乙醇催化转化为乙酸和氢气,该历程总反应为C H OH+H O
2 5 2
CH COOH+2H ↑,故原子利用率为100%,D正确。
3 2
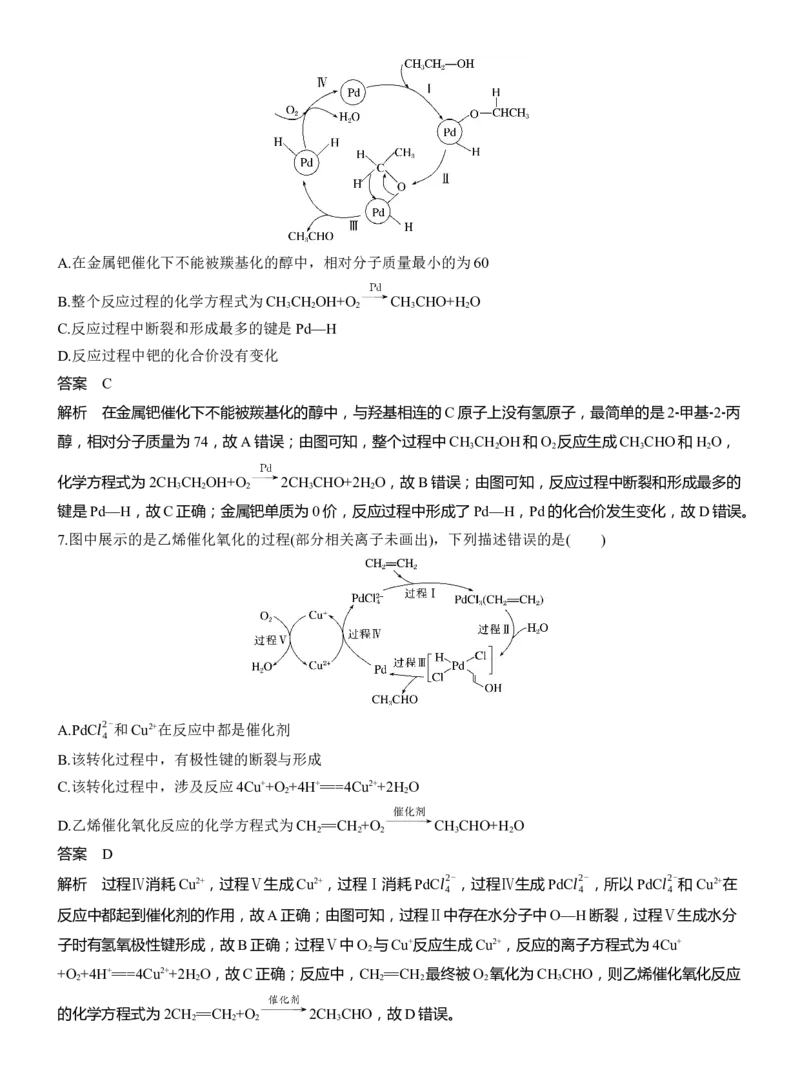
6.(2023·河北邢台名校联盟高三模拟)金属钯催化乙醇羰基化的反应过程如图所示。下列说法正确的是(
)A.在金属钯催化下不能被羰基化的醇中,相对分子质量最小的为60
B.整个反应过程的化学方程式为CH CH OH+O CH CHO+H O
3 2 2 3 2
C.反应过程中断裂和形成最多的键是Pd—H
D.反应过程中钯的化合价没有变化
答案 C
解析 在金属钯催化下不能被羰基化的醇中,与羟基相连的C原子上没有氢原子,最简单的是2⁃甲基⁃2⁃丙
醇,相对分子质量为74,故A错误;由图可知,整个过程中CH CH OH和O 反应生成CH CHO和H O,
3 2 2 3 2
化学方程式为2CH CH OH+O 2CH CHO+2H O,故B错误;由图可知,反应过程中断裂和形成最多的
3 2 2 3 2
键是Pd—H,故C正确;金属钯单质为0价,反应过程中形成了Pd—H,Pd的化合价发生变化,故D错误。
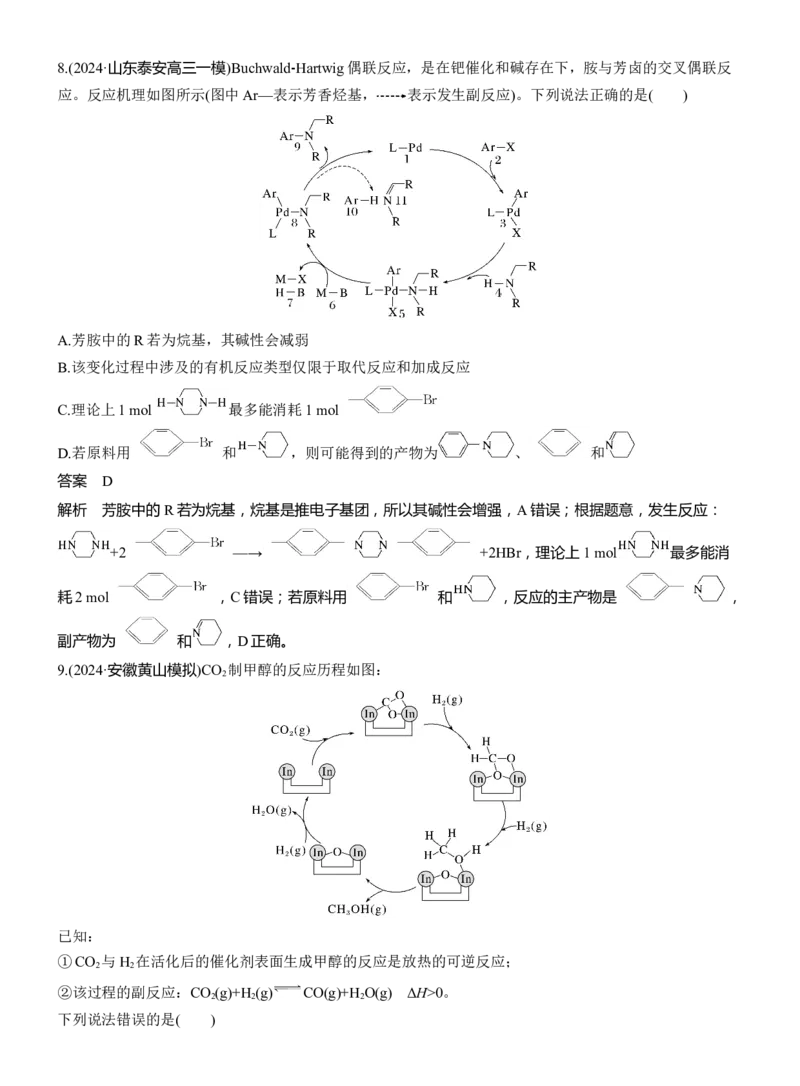
7.图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下列描述错误的是( )
A.PdCl2-和Cu2+在反应中都是催化剂
4
B.该转化过程中,有极性键的断裂与形成
C.该转化过程中,涉及反应4Cu++O +4H+===4Cu2++2H O
2 2
D.乙烯催化氧化反应的化学方程式为CH ==CH +O CH CHO+H O
2 2 2 3 2
答案 D
解析
过程Ⅳ消耗Cu2+,过程Ⅴ生成Cu2+,过程Ⅰ消耗PdCl2- ,过程Ⅳ生成PdCl2- ,所以PdCl2-
和Cu2+在
4 4 4
反应中都起到催化剂的作用,故A正确;由图可知,过程Ⅱ中存在水分子中O—H断裂,过程Ⅴ生成水分
子时有氢氧极性键形成,故B正确;过程Ⅴ中O 与Cu+反应生成Cu2+,反应的离子方程式为4Cu+
2
+O +4H+===4Cu2++2H O,故C正确;反应中,CH ==CH 最终被O 氧化为CH CHO,则乙烯催化氧化反应
2 2 2 2 2 3
的化学方程式为2CH ==CH +O 2CH CHO,故D错误。
2 2 2 38.(2024·山东泰安高三一模)Buchwald⁃Hartwig偶联反应,是在钯催化和碱存在下,胺与芳卤的交叉偶联反
应。反应机理如图所示(图中Ar—表示芳香烃基, 表示发生副反应)。下列说法正确的是( )
A.芳胺中的R若为烷基,其碱性会减弱
B.该变化过程中涉及的有机反应类型仅限于取代反应和加成反应
C.理论上1 mol 最多能消耗1 mol
D.若原料用 和 ,则可能得到的产物为 、 和
答案 D
解析 芳胺中的R若为烷基,烷基是推电子基团,所以其碱性会增强,A错误;根据题意,发生反应:
+2 —→ +2HBr,理论上1 mol 最多能消
耗2 mol ,C错误;若原料用 和 ,反应的主产物是 ,
副产物为 和 ,D正确。
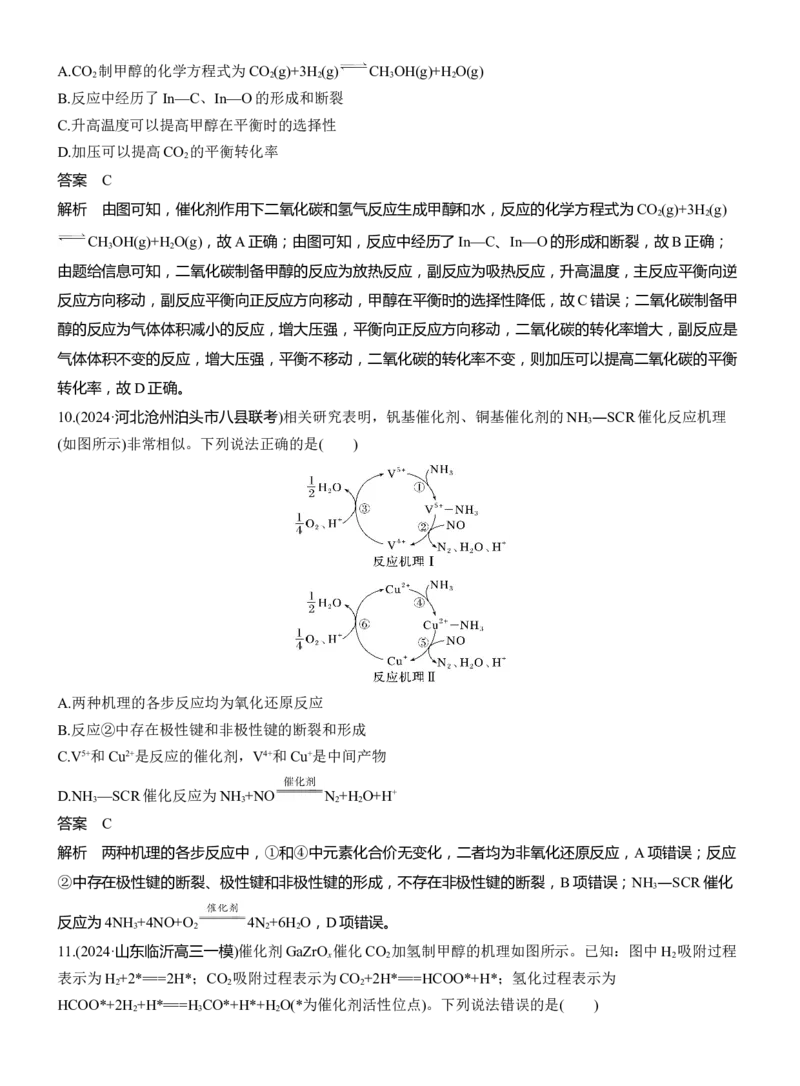
9.(2024·安徽黄山模拟)CO 制甲醇的反应历程如图:
2
已知:
①CO 与H 在活化后的催化剂表面生成甲醇的反应是放热的可逆反应;
2 2
②该过程的副反应:CO (g)+H (g) CO(g)+H O(g) ΔH>0。
2 2 2
下列说法错误的是( )A.CO 制甲醇的化学方程式为CO (g)+3H (g) CH OH(g)+H O(g)
2 2 2 3 2
B.反应中经历了In—C、In—O的形成和断裂
C.升高温度可以提高甲醇在平衡时的选择性
D.加压可以提高CO 的平衡转化率
2
答案 C
解析 由图可知,催化剂作用下二氧化碳和氢气反应生成甲醇和水,反应的化学方程式为CO (g)+3H (g)
2 2
CH OH(g)+H O(g),故A正确;由图可知,反应中经历了In—C、In—O的形成和断裂,故B正确;
3 2
由题给信息可知,二氧化碳制备甲醇的反应为放热反应,副反应为吸热反应,升高温度,主反应平衡向逆
反应方向移动,副反应平衡向正反应方向移动,甲醇在平衡时的选择性降低,故C错误;二氧化碳制备甲
醇的反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,二氧化碳的转化率增大,副反应是
气体体积不变的反应,增大压强,平衡不移动,二氧化碳的转化率不变,则加压可以提高二氧化碳的平衡
转化率,故D正确。
10.(2024·河北沧州泊头市八县联考)相关研究表明,钒基催化剂、铜基催化剂的NH ―SCR催化反应机理
3
(如图所示)非常相似。下列说法正确的是( )
A.两种机理的各步反应均为氧化还原反应
B.反应②中存在极性键和非极性键的断裂和形成
C.V5+和Cu2+是反应的催化剂,V4+和Cu+是中间产物
D.NH —SCR催化反应为NH +NO N +H O+H+
3 3 2 2
答案 C
解析 两种机理的各步反应中,①和④中元素化合价无变化,二者均为非氧化还原反应,A项错误;反应
②中存在极性键的断裂、极性键和非极性键的形成,不存在非极性键的断裂,B项错误;NH ―SCR催化
3
反应为4NH +4NO+O 4N +6H O,D项错误。
3 2 2 2
11.(2024·山东临沂高三一模)催化剂GaZrO 催化CO 加氢制甲醇的机理如图所示。已知:图中H 吸附过程
x 2 2
表示为H +2*===2H*;CO 吸附过程表示为CO +2H*===HCOO*+H*;氢化过程表示为
2 2 2
HCOO*+2H +H*===H CO*+H*+H O(*为催化剂活性位点)。下列说法错误的是( )
2 3 2A.氧空位浓度高,有利于增强CO 的吸附能力
2
B.CO 活化位点和H 活化位点是相同的
2 2
C.脱附过程表示为H CO*+H*===CH OH+2*
3 3
D.降低氢化过程的活化能,不一定能有效加快甲醇的生成速率
答案 B
解析 根据图示,氧空位与二氧化碳作用,氧空位浓度高,有利于增强CO 的吸附能力,故A正确;根据
2
图示,CO 活化位点是氧空位,与H 活化位点不相同,故B错误;根据图示,脱附过程表示为
2 2
H CO*+H*===CH OH+2*,故C正确;降低氢化过程的活化能,氢化过程的速率加快,总反应速率由慢反
3 3
应决定,所以不一定能有效加快甲醇的生成速率,故D正确。