文档内容
专题八 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39 Ca 40
Mn 55 Fe 56 Cu 64
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
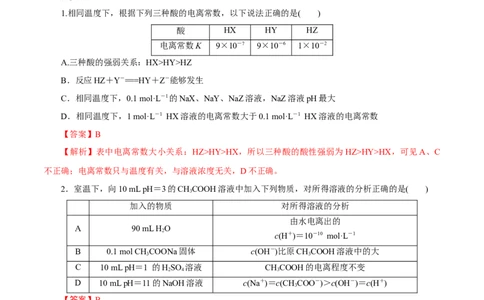
1.相同温度下,根据下列三种酸的电离常数,以下说法正确的是( )
酸 HX HY HZ
电离常数K 9×10-7 9×10-6 1×10-2
A.三种酸的强弱关系:HX>HY>HZ
B.反应HZ+Y-===HY+Z-能够发生
C.相同温度下,0.1 mol·L-1的NaX、NaY、NaZ溶液,NaZ溶液pH最大
D.相同温度下,1 mol·L-1 HX溶液的电离常数大于0.1 mol·L-1 HX溶液的电离常数
【答案】B
【解析】表中电离常数大小关系:HZ>HY>HX,所以三种酸的酸性强弱为HZ>HY>HX,可见A、C
不正确;电离常数只与温度有关,与溶液浓度无关,D不正确。
2.室温下,向10 mL pH=3的CHCOOH溶液中加入下列物质,对所得溶液的分析正确的是( )
3
加入的物质 对所得溶液的分析
由水电离出的
A 90 mL H O
2
c(H+)=10-10 mol·L-1
B 0.1 mol CH COONa固体 c(OH-)比原CHCOOH溶液中的大
3 3
C 10 mL pH=1 的HSO 溶液 CHCOOH的电离程度不变
2 4 3
D 10 mL pH=11的NaOH溶液 c(Na+)=c(CHCOO-)>c(OH-)=c(H+)
3
【答案】B
【解析】向10 mL pH=3的CHCOOH溶液中加入90 mL H O,醋酸的电离平衡正向移动,则 c(H
3 2
+)>10-4 mol·L-1,故由水电离出的c(H+)<10-10 mol·L-1,选项A错误;向10 mL pH=3的CHCOOH溶液
3
中加入0.1 mol CH COONa固体,醋酸根离子浓度增大,酸的电离平衡逆向移动,c(H+)减小,故c(OH-)比
3
原CHCOOH溶液中的大,选项B正确;向10 mL pH=3的CHCOOH溶液中加入10 mL pH=1 的HSO
3 3 2 4
溶液,氢离子浓度增大,抑制醋酸的电离,CHCOOH的电离程度减小,选项C错误;向10 mL pH=3的
3
CHCOOH溶液中加入10 mL pH=11的NaOH溶液,醋酸过量,所得溶液呈酸性,故c(CHCOO-)>c(Na
3 3+)>c(H+)>c(OH-),选项D错误。
3.25 ℃时,0.1 mol·L-1的CHCOOH溶液pH=3,0.1 mol·L-1的HCN溶液pH=4。下列说法正确的
3
是( )
A.CHCOOH与HCN均为弱酸,酸性:HCN>CH COOH
3 3
B.25 ℃时,水电离出来的c(H+)均为10-11 mol·L-1的两种酸,酸的浓度:HCN>CH COOH
3
C.25 ℃时,浓度均为0.1 mol·L-1的CHCOONa和NaCN溶液中,pH大小:CHCOONa>NaCN
3 3
D.25 ℃时,pH均为3的CHCOOH与HCN溶液各100 mL与等浓度的NaOH溶液完全反应,消耗
3
NaOH溶液的体积:CHCOOH>HCN
3
【答案】B
【解析】同浓度时CHCOOH溶液pH小,酸性较强,A错误;水电离出来的c(H+)均为10-11 mol·L-
3
1,因此两种酸的溶液中 c(H+)=10-3 mol·L-1,由于酸性:CHCOOH>HCN,故酸的浓度:
3
HCN>CH COOH,B 正确; CHCOONa 和 NaCN 浓度相同且 NaCN 更易水解,故 pH 大小:
3 3
NaCN>CHCOONa,C错误;pH均为3的CHCOOH与HCN相比,HCN浓度大,故消耗NaOH溶液的体
3 3
积:HCN>CH COOH,D错误。
3
4.HPO 的电离是分步进行的,常温下K =7.6×10-3,K =6.3×10-8,K =4.4×10-13。下列说法
3 4 a1 a2 a3
正确的是( )
A.浓度均为0.1 mol·L-1的NaOH溶液和HPO 溶液按照体积比2∶1混合,混合液的pH<7
3 4
B.NaHPO 溶液中,c(H+)+c(H PO)+c(H PO )=c(PO)+c(OH-)
2 4 2 3 4
C.向0.1 mol·L-1的HPO 溶液中通入HCl气体(忽略溶液体积的变化),溶液pH=1时,溶液中大约
3 4
有7.1%的HPO 电离
3 4
D.在HPO 溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=11时,
3 4
c(PO)>c(HPO)
【答案】C
【解析】浓度均为0.1 mol·L-1的NaOH溶液和HPO 溶液按照体积比2∶1混合,二者恰好反应生成
3 4
NaHPO ,在溶液中HPO存在电离平衡:HPO PO+H+,也存在着水解平衡:HPO+HO HPO+
2 4 2 2
OH-,电离平衡常数K =4.4×10-13,水解平衡常数K ====≈1.59×10-7>K =4.4×10-13,水解程度
a3 h2 a3
大于电离程度,因此溶液显碱性,pH>7,A错误;在NaHPO 溶液中,根据质子守恒可得:c(H+)+
2 4
c(H PO)+2c(H PO )=c(PO)+c(OH-),B错误;向0.1 mol·L-1的HPO 溶液中通入HCl气体(忽略溶液体积
2 3 4 3 4
的变化),溶液pH=1时,c(H+)=0.1 mol·L-1,假设电离的HPO 浓度为x,根据电离平衡常数K ===
3 4 a1
=7.6×10-3,解得x≈0.007 1 mol·L-1,因此溶液中HPO 电离度=×100%=7.1%,C正确;在HPO 溶液
3 4 3 4
中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=11时,c(H+)=10-11 mol·L-1,K ===4.4×10-13,则=4.4×10-2 ,则c(PO)<c(HPO),D错误。
a3
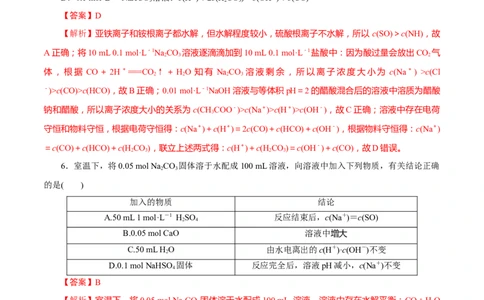
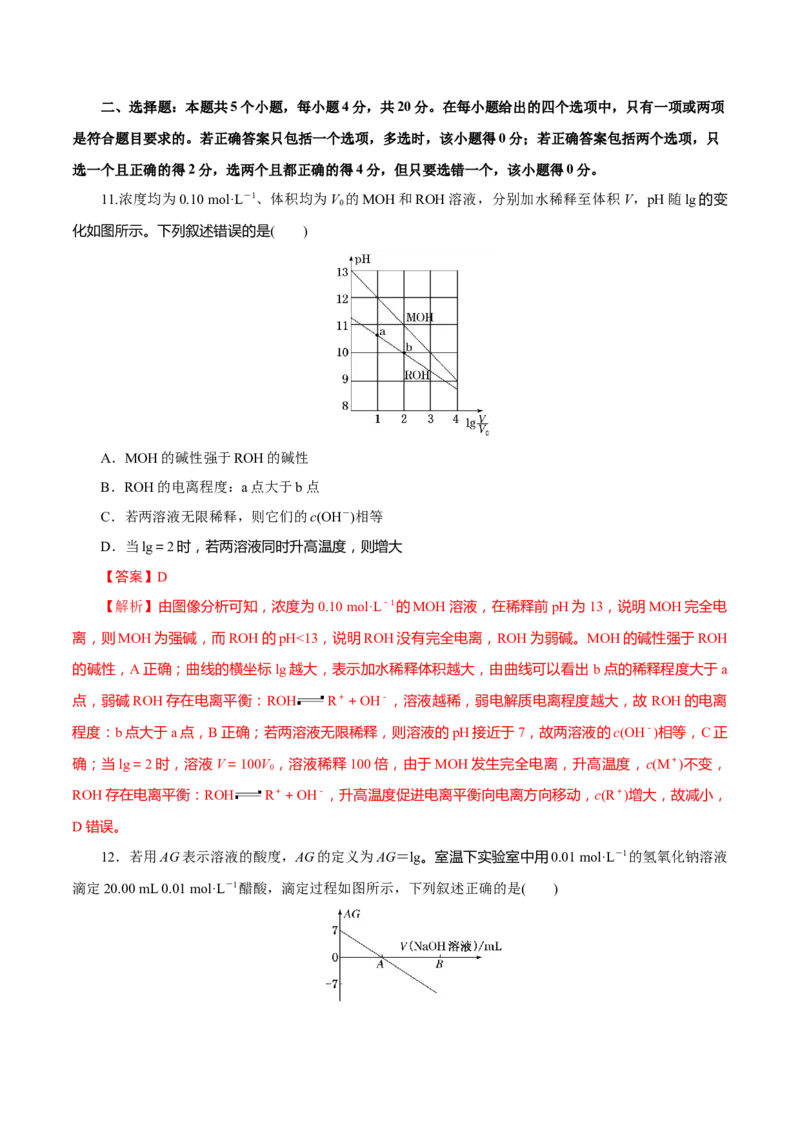
5.常温下,下列溶液中,有关微粒的物质的量浓度关系不正确的是( )
A.0.1 mol·L-1 (NH )Fe(SO ) 溶液:c(SO)>c(NH)>c(Fe2+)>c(H+)
4 2 4 2
B.将10 mL 0.1 mol·L-1 Na CO 溶液逐滴滴加到10 mL 0.1 mol·L-1盐酸中:
2 3
c(Na+)>c(Cl-)>c(CO)>c(HCO)
C.0.01 mol·L-1 NaOH溶液与等体积pH=2的醋酸混合后的溶液中:
c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
D.0.1 mol·L-1 NaHCO 溶液:c(H+)+2c(H CO)=c(OH-)+c(CO)
3 2 3
【答案】D
【解析】亚铁离子和铵根离子都水解,但水解程度较小,硫酸根离子不水解,所以 c(SO)>c(NH),故
A正确;将10 mL 0.1 mol·L-1NaCO 溶液逐滴滴加到10 mL 0.1 mol·L-1盐酸中:因为酸过量会放出CO 气
2 3 2
体,根据 CO+2H+===CO ↑+HO 知有 NaCO 溶液剩余,所以离子浓度大小为 c(Na+) >c(Cl
2 2 2 3
-)>c(CO)>c(HCO),故B正确;0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中溶质为醋酸
钠和醋酸,所以离子浓度大小的关系为c(CHCOO-)>c(Na+)>c(H+)>c(OH-),故C正确;溶液中存在电荷
3
守恒和物料守恒,根据电荷守恒得:c(Na+)+c(H+)=2c(CO)+c(HCO)+c(OH-),根据物料守恒得:c(Na+)
=c(CO)+c(HCO)+c(H CO),联立上述两式得:c(H+)+c(H CO)=c(OH-)+c(CO),故D错误。
2 3 2 3
6.室温下,将0.05 mol Na CO 固体溶于水配成100 mL溶液,向溶液中加入下列物质,有关结论正确
2 3
的是( )
加入的物质 结论
A.50 mL 1 mol·L-1 HSO 反应结束后,c(Na+)=c(SO)
2 4
B.0.05 mol CaO 溶液中增大
C.50 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D.0.1 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
【答案】B
【解析】室温下,将0.05 mol Na CO 固体溶于水配成100 mL 溶液,溶液中存在水解平衡:CO+HO
2 3 2
HCO+OH-,使溶液呈碱性。加入50 mL 1 mol·L-1 HSO ,HSO 与NaCO 恰好反应,则反应后溶
2 4 2 4 2 3
液中溶质为NaSO ,根据物料守恒,反应结束后 c(Na+)=2c(SO),故A项错误;加入0.05 mol CaO,则
2 4
CaO+HO===Ca(OH) ,则c(OH-)增大,且Ca(OH) 与NaCO 反应生成CaCO 和NaOH,使CO+HO
2 2 2 2 3 3 2
HCO+OH-平衡左移,c(HCO)减小,溶液中增大,故B项正确;加入50 mL H O,溶液体积变大,
2
CO+HO HCO+OH-平衡右移,但c(OH-)减小,NaCO 溶液中的OH-来源于水的电离,因由水电离
2 2 3
产生的c(H+)=c(OH-),故由水电离出的c(H+)·c(OH-)减小,故C项错误;加入0.1 mol NaHSO 固体,
4NaHSO 为强酸的酸式盐,电离出的H+与CO反应,则反应后溶液为NaSO 溶液,溶液呈中性,溶液pH
4 2 4
减小,引入了Na+,c(Na+)增大,故D项错误。
7.测定0.1 mol·L-1NaSO 溶液先升温再降温过程中的pH,数据如下:
2 3
时刻 ① ② ③ ④
温度/℃ 25 30 40 25
pH 9.66 9.52 9.37 9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色沉淀多。
2
下列说法不正确的是( )
A.NaSO 溶液中存在水解平衡:SO+HO HSO+OH-
2 3 2
B.④的pH与①不同,是由SO浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的K 值相等
w
【答案】C
【解析】NaSO 是强碱弱酸盐,在水溶液中发生水解,存在水解平衡:SO+HOHSO+OH-,A
2 3 2
项正确;实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色沉淀多,
2
说明④中的SO数目多,SO数目少,所以④中的OH-数目小于①中的OH-数目,且pH不同,B项正确;
①→③的过程中,温度升高,SO的水解平衡正向移动,而c(SO)减小,水解平衡逆向移动,故温度和浓度
对水解平衡移动方向的影响不一致,C项错误;K 只与温度有关,温度相同则K 相同,D项正确。
w w
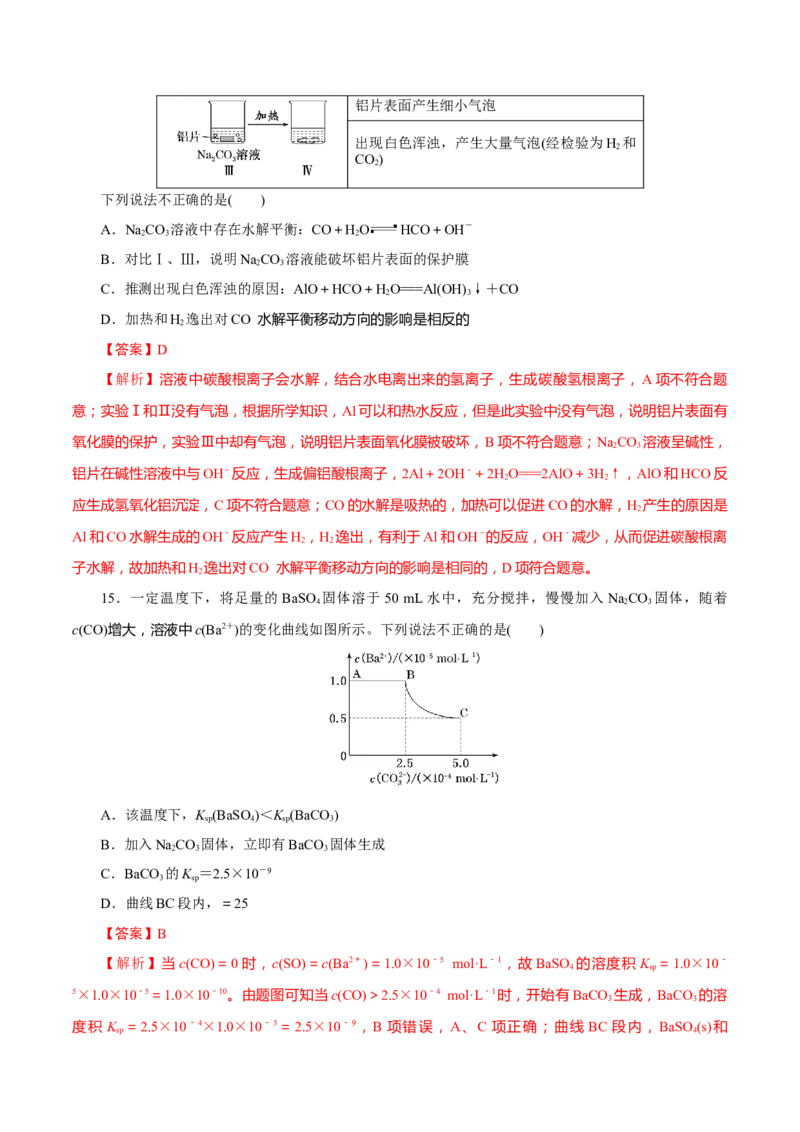
8.已知 25 ℃时,RSO (s)+CO(aq ) RCO(s)+SO(aq)的平衡常数 K=1.75×104,K (RCO)=
4 3 sp 3
2.80×10-9,下列叙述中正确的是( )
A.向c(CO)=c(SO)的混合液中滴加RCl 溶液,首先析出RSO 沉淀
2 4
B.将浓度均为6×10-6mol·L-1的RCl 、NaCO 溶液等体积混合后可得到RCO 沉淀
2 2 3 3
C.25 ℃时,RSO 的K 约为4.9×10-5
4 sp
D.相同温度下,RCO 在水中的K 大于在NaCO 溶液中的K
3 sp 2 3 sp
【答案】C
【解析】RSO (s)+CO(aq ) RCO(s)+SO(aq)的平衡常数 K====1.75×104,K (RSO )=
4 3 sp 4
1.75×104×K (RCO) = 1.75×104×2.80×10 - 9 = 4.9×10 - 5 。 RSO 、 RCO 属 于 同 种 类 型 且
sp 3 4 3
K (RSO )>K (RCO),故向c(CO)=c(SO)的混合液中滴加RCl 溶液,首先析出RCO 沉淀,A项错误;将
sp 4 sp 3 2 3
浓度均为6×10-6mol·L-1的RCl 、NaCO 溶液等体积混合后,c(R2+)=3×10-6mol·L-1、c(CO)=3×10-
2 2 3
6mol·L-1,此时的离子积Q=c(R2+)·c(CO)=3×10-6×3×10-6=9×10-12K(HClO)
a2 2 3
D.在新制氯水中加入少量 NaHCO 固体可以提高溶液中 HClO 的浓度
3
【答案】D
【解析】根据“越弱越水解”并结合表格数据知,酸性的强弱顺序为HCO>HClO >HCO。pH试纸不
2 3
能用于测量具有氧化性和漂白性的溶液的 pH,NaClO具有强氧化性,故A错误;正确的反应方程式为
NaClO+CO +HO===NaHCO +HClO,故B错误;由于酸性HClO >HCO,则电离常数: K ( H CO)c>a,氢离子浓度越大,水的电离程度越
小,三种溶液中水的电离程度由大到小的顺序为a>c>b;②醋酸在稀释过程中会促进电离,所以氢离子的
物质的量增加,氢离子的浓度变化程度小,硫酸和盐酸溶液中氢离子物质的量不变且相等,所以 c(H+)由
大到小的顺序为a>b=c。
【答案】(1)①> 温度升高,水的电离程度增大,水的离子积增大 ②1 000∶1 ③碱 (2)①a>c>
b ②a>b=c
18.(15分)某化学学习小组探究测定草酸晶体(H C O·xHO)中的x值。查阅资料得知,草酸易溶于
2 2 4 2
水,水溶液可以用酸性KMnO 溶液进行滴定:2MnO+5HC O+6H+===2Mn2++10CO↑+8HO。
4 2 2 4 2 2
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀硫酸。
③用浓度为0.100 0 mol·L-1的酸性KMnO 标准溶液进行滴定,达到终点时消耗10.00 mL。
4
(1)上述步骤②中使用的锥形瓶是否需要事先用待测液润洗________(填“是”或“否”)。滴定时,将酸性KMnO 标准液装在如图中的________(填“甲”或“乙”)滴定管中。
4
(2)本实验到达滴定终点的标志可以是___________________________。
(3)通过上述数据,求得x=________。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的 x值会________(填“偏大”“偏小”或“不
变”,下同)。
②根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进方法
________________________。
【解析】(1)如果用待测液润洗锥形瓶就会有少量液体残留在瓶壁上,造成滴定的待测物增多,使得计
算值大于实际浓度,故上述步骤②中使用的锥形瓶不需要事先用待测液润洗;酸性高锰酸钾溶液具有强氧
化性,腐蚀橡皮管,所以用酸性滴定管,选甲。(2)可用酸性高锰酸钾自身的颜色作为指示剂判断滴定终
点,当滴入最后一滴酸性高锰酸钾溶液时,溶液由无色变为紫色,且半分钟内不褪色,表明到达滴定终
点。
(3)2MnO+5HC O+6H+===2Mn2++10CO↑+8HO
2 2 4 2 2
2 5
0.100 0×0.01 0.002 5
则25.00 mL待测液中含有0.002 5 mol草酸,故100 mL待测液中含有0.01 mol草酸,其质量为0.9 g。
所以1.260 g草酸晶体中水的质量为1.260 g-0.9 g=0.36 g,其物质的量为0.02 mol,则x=2;①若滴定终
点时俯视滴定管读数,则消耗酸性高锰酸钾溶液的体积偏小,所得草酸的物质的量偏小,则水的物质的量
偏大;②根据上述实验计算的数据可信性不强,为了提高实验的准确性,应重复步骤②③增加平行实验。
【答案】(1)否 甲 (2)当滴入最后一滴酸性KMnO 溶液时,溶液由无色变为紫色,且半分钟内不褪
4
色,即到达滴定终点 (3)2 ①偏大 ②重复步骤②③增加平行实验
19.(15分)钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛
白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc O)的一种流程如下:
2 3回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合
而成。混合的实验操作是______________________________。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是________;再向滤液加入氨水调节pH=6,滤液中
Sc3+的浓度为________________{已知:K [Mn(OH) ]=1.9×10-13、K [Fe(OH) ]=2.6×10-39,K [Sc(OH) ]=
sp 2 sp 3 sp 3
9.0×10-31}。
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中=________(保留两位有效数字)。写出“沉钪”得到
草酸钪的离子方程式______________________________________[已知K (H C O)=5.9×10-2,K (H C O)
a1 2 2 4 a2 2 2 4
=6.4×10-5]。
(4)草酸钪“灼烧”氧化的化学方程式为_______________________________________。
(5)废酸中含钪量为15 mg·L-1,V L废酸最多可提取Sc O 的质量为____________。
2 3
【解析】(1)不同的液体在混合时,一般先加密度较小,易挥发的,后加密度大的、难挥发的,若混合
时放热,则最后加受热易分解的,因此,混合的实验操作是将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃
棒不断搅拌,冷却后再慢慢注入 HO 中,并不断搅拌。(2)废酸中含钪、钛、铁、锰等离子,洗涤“油
2 2
相”已除去大量的钛离子,根据K [Mn(OH) ]=1.9×10-13、K [Fe(OH) ]=2.6×10-39,K [Sc(OH) ]=9.0×10
sp 2 sp 3 sp 3
-31,可以求出余下三种离子沉淀完全(离子浓度小于10-5 mol·L-1)时的pH,则锰离子沉淀完全时pH约为
10,钪离子沉淀完全时pH约为5,而铁离子沉淀完全时pH约为4,所以先加入氨水调节pH=3,过滤,
滤渣主要成分是Fe(OH) ;再向滤液加入氨水调节pH=6,此时溶液中,c(OH-)=10-8 mol·L-1,滤液中
3
Sc3+的浓度 c(Sc3+)===9.0×10-7 mol·L-1。(3)25 ℃时 pH=2 的草酸溶液中 =××=
K (H C O)×K (H C O)×=6.4×10-5×5.9×10-2×≈3.8×10-2, “沉钪”得到草酸钪的离子方程式为2Sc3
a2 2 2 4 a1 2 2 4
++ 3HC O===Sc (C O)↓+ 6H+。(4)草酸钪“灼烧”氧化的化学方程式为2Sc (C O)+3O 高温,2Sc O
2 2 4 2 2 4 3 2 2 4 3 2 2 3
+12CO 。(5)废酸中含钪量为15 mg·L-1,则V L废酸中含钪的质量为15×10-3 g·L-1×V L=0.015V g,
2
所以最多可提取Sc O 的质量为×=0.023V g。
2 3
【答案】(1)将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入 HO 中,
2 2
并不断搅拌 (2)Fe(OH) 9.0×10-7mol·L-l (3)3.8×10-2 2Sc3++ 3HC O===Sc (C O)↓+ 6H+
3 2 2 4 2 2 4 3
(4)2Sc (C O)+3O 高温,2Sc O+12CO
2 2 4 3 2 2 3 2(5)0.023V g