文档内容
电离常数、水解常数、溶度积常数的综合应用
1.电离常数(K )与电离度(α)的关系(以一元弱酸HA为例)
电离
HA H+ + A-
起始浓度: c 0 0
酸
平衡浓度: c ·(1-α) c ·α c ·α
酸 酸 酸
(c ·α) 2 c ·α2
K = 酸 = 酸 。
电离 c ·(1-α) 1-α
酸
√K
若α很小,可认为1-α≈1,则K =c ·α2或α= 电离。
电离 酸 c
酸
2.电离常数与水解常数的关系
(1)对于一元弱酸HA,K 与K 的关系
a h
c(H+ )·c(A- ) c(OH- )·c(HA)
HA H++A-,K= ;A-+H O HA+OH-,K = 。则
a c(HA) 2 h c(A- )
K
w
K·K =c(H+)·c(OH-)=K ,故K = 。
a h w h K
a
1.0×10-14
常温时K·K =K =1.0×10-14,K = 。
a h w h K
a
(2)对于二元弱酸H B,K (H B)、K (H B)与K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
c(OH- )·c(H B) c(H+ )·c(OH- )·c(H B) K
2 2 w
HB-+H O H B+OH-,K (HB-)= = = 。
2 2 h c(HB-
)
c(H+ )·c(HB-
)
K
a1
c(OH- )·c(HB- ) c(H+ )·c(OH- )·c(HB- ) K
w
B2-+H O HB-+OH-,K (B2-)= = = 。
2 h c(B2- ) c(H+ )·c(B2- ) K
a2
3.H CO 溶液、NaHCO 溶液、Na CO 溶液中的电离或水解
2 3 3 2 3
碳酸的电离:
H CO
H++HCO-
K =4.3×10-7
2 3 3 a1
HCO- H++CO2-
K =5.6×10-11
3 3 a2
Na CO 的水解(K >K ):
2 3 h1 h2
CO2-
+H O
HCO-
+OH- K
3 2 3 h1
HCO-
+H O H CO +OH- K
3 2 2 3 h2K K
w w
K = ,K = 。
h1 K h2 K
a2 a1
比较NaHCO 酸式盐溶液中电离与水解程度大小:
3
K =5.6×10-11
a2
K 1×10-14
w
K = =
h2 K 4.5×10-7
a1
K >K
,故HCO-
的水解程度大于其电离程度。
h2 a2 3
常温时,对于一元弱酸HA,当K>1.0×10-7时,K <1.0×10-7,此时将等物质的量浓度的HA溶液与
a h
NaA溶液等体积混合,HA的电离程度大于A-的水解程度,溶液呈酸性;同理,当K<1.0×10-7时,
a
K
w
K >1.0×10-7,A-的水解程度大于HA的电离程度,溶液呈碱性。对于多元弱酸,K = ,K 是其阴离子结
h h K a
a
合一个H+所形成的粒子的电离常数。
1.[2023·海南,16(4)]298 K时,H PO (aq)+KCl(aq) KH PO (aq)+HCl(aq)的平衡常数K=
3 4 2 4
。(已知H PO 的K =6.9×10-3)
3 4 a1
答案 6.9×10-3
解析 298 K时,H PO (aq)+KCl(aq) KH PO (aq)+HCl(aq)的离子方程式为H PO (aq) H
PO-
(aq)+H+
3 4 2 4 3 4 2 4
c(H+ )·c(H PO- )
(aq),其平衡常数K= 2 4 =K =6.9×10-3。
c(H PO ) a1
3 4
2.[2023·福建,10(3)]25 ℃时,K (CuS)=6.3×10-36,H S的K =1.1×10-7,K =1.3×10-13。反应CuS(s)+2H+
sp 2 a1 a2
(aq)===Cu2+(aq)+H S(aq)的平衡常数K= (列出计算式即可)。经计算可判断CuS难溶于稀硫酸。
2
K (CuS) 6.3×10-36
sp
答案 (或 )
K ·K 1.1×10-7×1.3×10-13
a1 a2
c(Cu2+ )·c(H S) K (CuS)
解析 CuS(s)+2H+(aq)===Cu2+(aq)+H S(aq)的平衡常数K= 2 = sp =
2 c2 (H+
)
K ·K
a1 a2
6.3×10-36
。
1.1×10-7×1.3×10-13
3.[2023·广东,18(2)]已知:氨性溶液由NH ·H O、(NH ) SO 和(NH ) CO 配制。常温下,Ni2+、Co2+、
3 2 4 2 3 4 2 3
Co3+与NH 形成可溶于水的配离子;lg K (NH ·H O)=-4.7。
3 b 3 2
常温下,pH=9.9的氨性溶液中,c(NH ·H O)
c(NH+
)(填“>”“<”或“=”)。
3 2 4
答案 >c(N H+ )·c(OH- )
解析 常温下,pH=9.9的氨性溶液中,lg K (NH ·H O)=-4.7,K (NH ·H O)=10-4.7= 4 ,
b 3 2 b 3 2 c(N H ·H O)
3 2
c(N H+ ) 10-4.7 10-4.7
4 = = =10-0.6<1,则c(NH ·H O)>c(N H+ )。
c(N H ·H O) c(OH- ) 10-4.1 3 2 4
3 2
4.[2020·天津,16(5)节选]已知25 ℃碳酸电离常数为K 、K ,当溶液pH=12时,c(H CO
)∶c(HCO-
)∶c(C
a1 a2 2 3 3
O2-
)=1∶ ∶ 。
3
答案 1012·K 1024·K ·K
a1 a1 a2
解析 H CO 是二元弱酸,分步发生电离:H CO
HCO- +H+、HCO- CO2-
+H+,则有K =
2 3 2 3 3 3 3 a1
c(HCO- )·c(H+ ) c(CO2- )·c(H+ ) c(CO2- )·c2 (H+ )
3 3 3
、K = ,从而可得:K ·K = 。当溶液pH=12时,
c(H CO ) a2 c(HCO- ) a1 a2 c(H CO )
2 3 3 2 3
c(H+)=10-12 mol·L-1,代入K 、K ·K 可得:c(H CO
)∶c(HCO-
)=1∶(1012·K ),c(H CO
)∶c(CO2-
a1 a1 a2 2 3 3 a1 2 3 3
)=1∶(1024·K ·K ),综合可得:c(H CO
)∶c(HCO- )∶c(CO2-
)=1∶(1012·K )∶(1024·K ·K )。
a1 a2 2 3 3 3 a1 a1 a2
题型突破练 [分值:100 分]
1.(4分)已知常温下,Na CO 溶液的水解常数K
=2×10-4,则当溶液中c(HCO- )∶c(CO2-
)=2∶1时,试求该溶液
2 3 h 3 3
的pH= 。
答案 10
c(HCO- )·c(OH-
)
解析 K =
3 =2×10-4,又c(HCO- )∶c(CO2-
)=2∶1,则c(OH-)=10-4 mol·L-1,结合K =1.0×10-
h c(CO2-
)
3 3 w
3
14,可得c(H+)=10-10 mol·L-1。
2.(8分)已知:常温下,K (H CrO )=0.18,K (H CrO )=3.2×10-7。试推测常温下,KHCrO 溶液呈 (填
a1 2 4 a2 2 4 4
“酸性”“碱性”或“中性”),其原因是
(用必要的文字说明)。
K 10-14
答案 酸性 KHCrO 在溶液中可发生水解,其水解常数K =
w
= ≈5.56×10-14
a2 2 c(HS-
)
sp 4
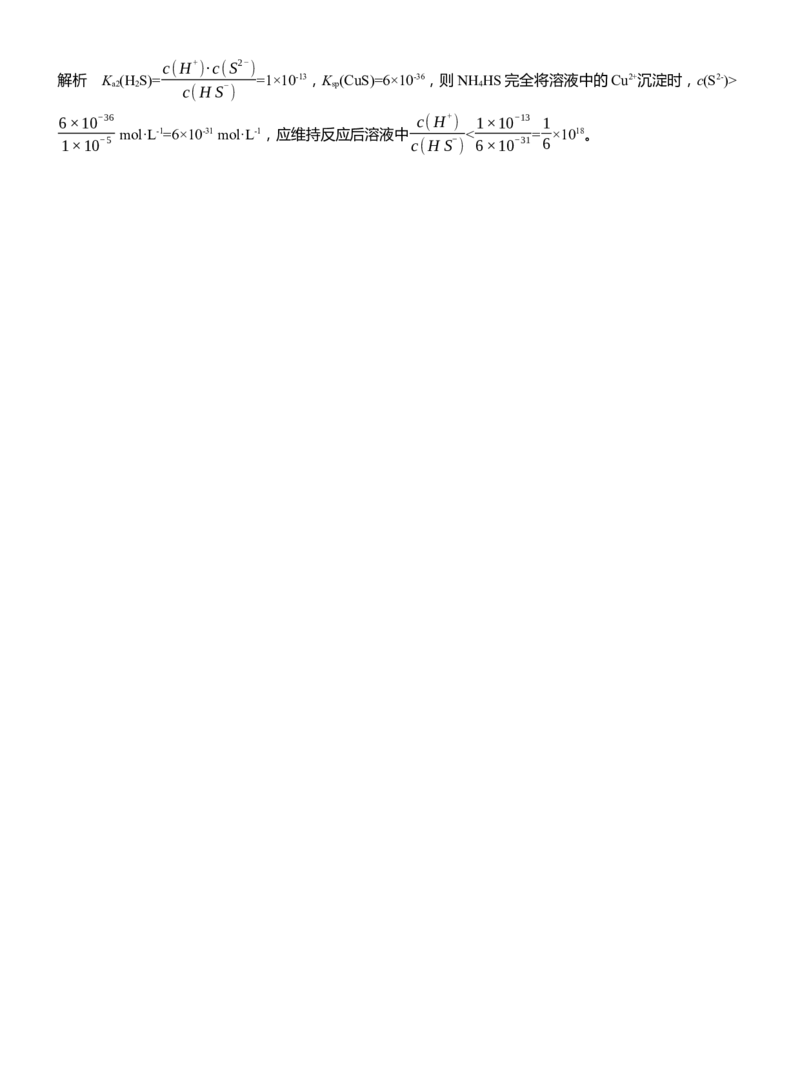
6×10-36 c(H+ ) 1×10-13 1
mol·L-1=6×10-31 mol·L-1,应维持反应后溶液中 < = ×1018。
1×10-5 c(HS- ) 6×10-31 6