文档内容
化工流程中的有关计算
1.(6分)(2023·湖南校联考模拟)钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是
V O 、V O ,含有SiO 、FeS 及Mg、Al、Mn等化合物杂质)制备单质钒的工艺流程如图所示:
2 3 2 4 2 2
已知:①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 Fe3+ Mg2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
②K (CaCO )=2.8×10-9、K (CaSiO )=2.5×10-8、K [Ca(V O ) ]远大于K (CaCO )。
sp 3 sp 3 sp 3 2 sp 3
③一般认为平衡常数K>105反应较完全。
“水浸”加入Na CO 调节溶液的pH为8.5,可完全除去的金属离子有 ,及部分的
2 3
。“水浸”加入Na CO 不能使CaSiO 完全转化,原因是 。
2 3 3
2.(3分)钨是熔点最高的金属,是重要的战略物资。自然界中黑钨矿的主要成分是FeWO 、MnWO ,还含
4 4
有少量Si、P、As的化合物。由黑钨矿制备WO 的工艺流程如下:
3
浸出液中的溶质有Na WO 、Na SiO 、Na PO 、Na AsO ,加入MgSO 、H SO 将溶液的pH调至9时,溶
2 4 2 3 3 4 3 4 4 2 4
c(PO3-
)
4
液中 = 。
c(AsO3-
)
4
(已知K [Mg (PO ) ]=2.0×10-24、K [Mg (AsO ) ]=2.0×10-20)
sp 3 4 2 sp 3 4 23.(3分)铍作为一种稀有元素,在航空航天、电子加工等领域具有重要意义。用铍矿石(含BeO及少量Ca、
Mg、Mn元素)与配料生产工业氧化铍的工艺流程如下:
已知:碱性条件下KMnO 的还原产物为MnO 。
4 2
碱化时,室温下加入NaOH,控制pH=11,析出颗粒状的Be(OH) ,所得浸出液中c(F-)=1 mol·L-1,此时溶
2
液中c(BeF2-
)= mol·L-1。
4
c(Be2+ )·c4 (F-
)
(已知K [Be(OH)
]=7×10-22,BeF2-
的解离常数K = =4×10-12)
sp 2 4 d c(BeF2-
)
4
4.(8分)粗Co(OH) 是以铜钴矿为原料湿法提取而得到的粗制钴盐中间品,含有MnOOH以及Al O 、
3 2 3
Fe O 、Mg等杂质,粗氢氧化钴湿法制取精制硫酸钴流程如下:
3 4
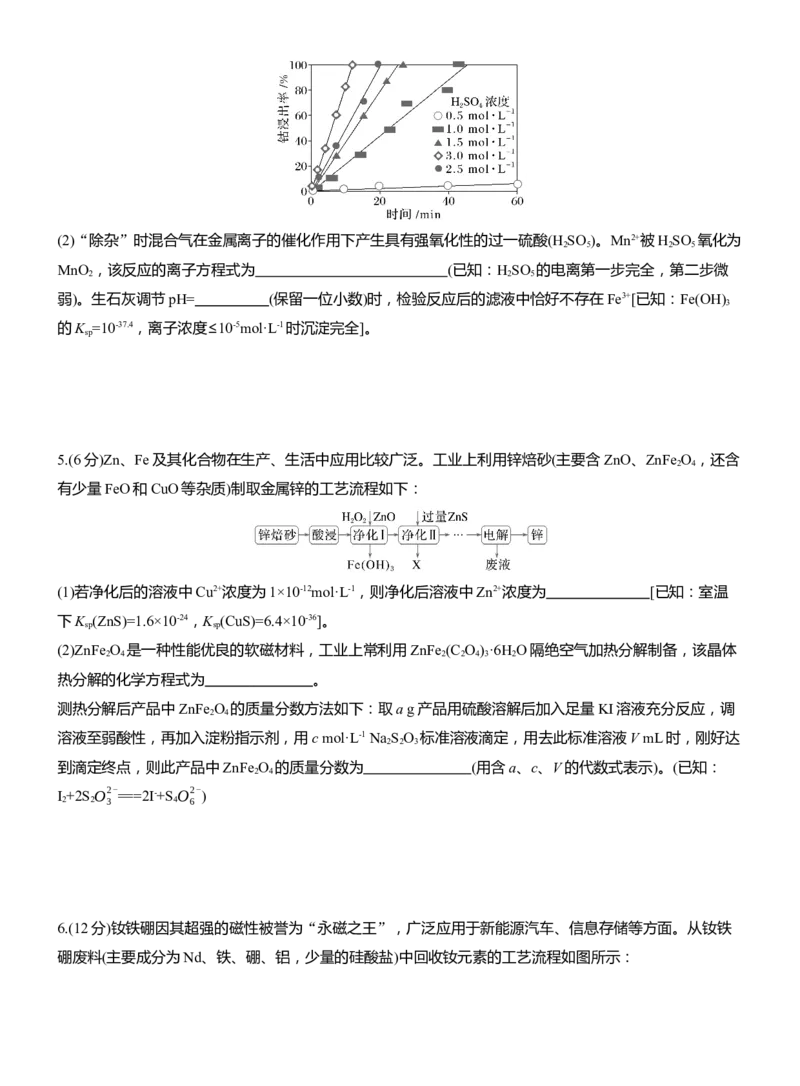
(1)浸出时添加还原剂SO 对原料中的锰和 (填元素名称)进行有效浸出。保持温度、SO 流速等条
2 2
件不变,钴浸出率与时间关系如图所示,则H SO 浓度最适宜为 mol·L-1。
2 4(2)“除杂”时混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H SO )。Mn2+被H SO 氧化为
2 5 2 5
MnO ,该反应的离子方程式为 (已知:H SO 的电离第一步完全,第二步微
2 2 5
弱)。生石灰调节pH= (保留一位小数)时,检验反应后的滤液中恰好不存在Fe3+[已知:Fe(OH)
3
的K =10-37.4,离子浓度≤10-5mol·L-1时沉淀完全]。
sp
5.(6分)Zn、Fe及其化合物在生产、生活中应用比较广泛。工业上利用锌焙砂(主要含ZnO、ZnFe O ,还含
2 4
有少量FeO和CuO等杂质)制取金属锌的工艺流程如下:
(1)若净化后的溶液中Cu2+浓度为1×10-12mol·L-1,则净化后溶液中Zn2+浓度为 [已知:室温
下K (ZnS)=1.6×10-24,K (CuS)=6.4×10-36]。
sp sp
(2)ZnFe O 是一种性能优良的软磁材料,工业上常利用ZnFe (C O ) ·6H O隔绝空气加热分解制备,该晶体
2 4 2 2 4 3 2
热分解的化学方程式为 。
测热分解后产品中ZnFe O 的质量分数方法如下:取a g产品用硫酸溶解后加入足量KI溶液充分反应,调
2 4
溶液至弱酸性,再加入淀粉指示剂,用c mol·L-1 Na S O 标准溶液滴定,用去此标准溶液V mL时,刚好达
2 2 3
到滴定终点,则此产品中ZnFe O 的质量分数为 (用含a、c、V的代数式表示)。(已知:
2 4
I +2S O2- ===2I-+S O2- )
2 2 3 4 6
6.(12分)钕铁硼因其超强的磁性被誉为“永磁之王”,广泛应用于新能源汽车、信息存储等方面。从钕铁
硼废料(主要成分为Nd、铁、硼、铝,少量的硅酸盐)中回收钕元素的工艺流程如图所示:已知:①硼难溶于非氧化性酸,Nd(H PO ) 难溶于水和稀酸,滤液1中主要金属离子为Na+、Fe2+,沉淀
2 4 3
时得到Nd (C O ) ·10H O。
2 2 4 3 2
②部分金属离子(0.1 mol·L-1)形成氢氧化物沉淀的pH范围如表:
金属离子 Fe2+ Fe3+ Al3+
开始沉淀 6.3 1.5 3.4
完全沉淀(离子浓度:
8.3 2.8 4.7
10-5 mol·L-1)
回答下列问题:
(1)若“酸溶”后溶液中Fe2+的浓度为1.0 mol·L-1,则“沉钕”时调节pH范围为 ,“碱转化”过程
Nd元素发生反应的离子方程式为 。
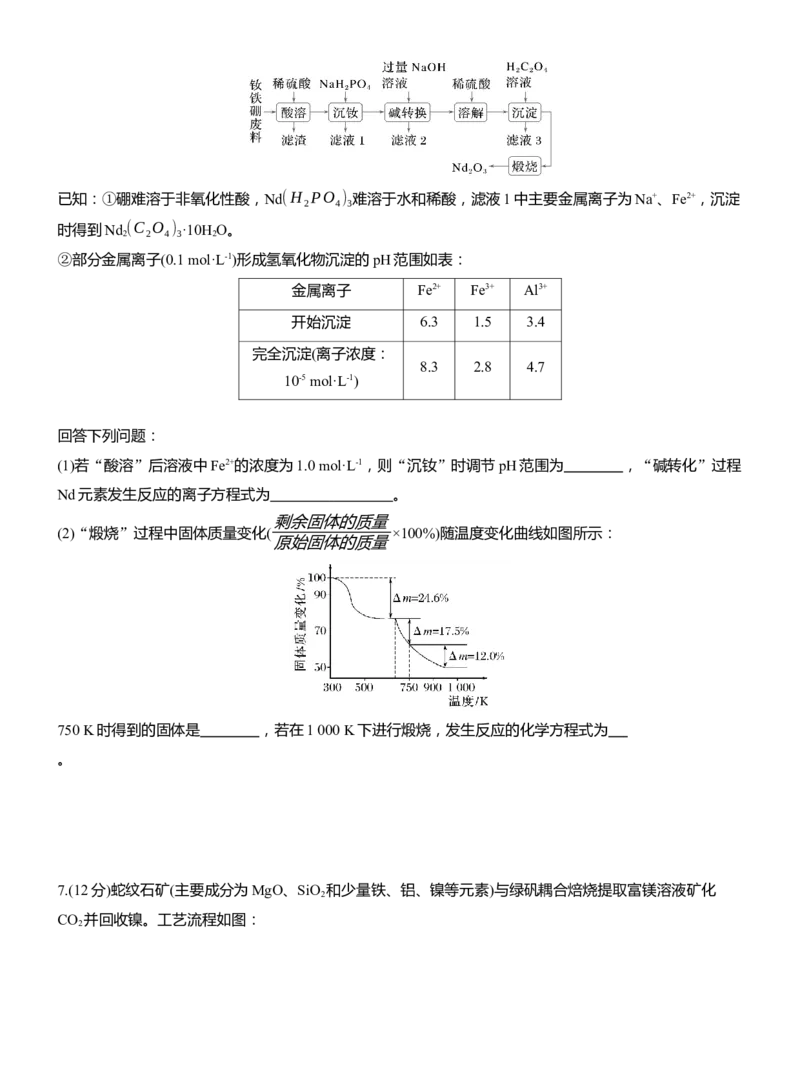
剩余固体的质量
(2)“煅烧”过程中固体质量变化( ×100%)随温度变化曲线如图所示:
原始固体的质量
750 K时得到的固体是 ,若在1 000 K下进行煅烧,发生反应的化学方程式为
。
7.(12分)蛇纹石矿(主要成分为MgO、SiO 和少量铁、铝、镍等元素)与绿矾耦合焙烧提取富镁溶液矿化
2
CO 并回收镍。工艺流程如图:
2已知:①DDTC[ ]是一种常见的络合剂,对低浓度镍离子的络合效果好;
②25 ℃时,K [Fe(OH) ]=4.0×10-38,K [Al(OH) ]=1.3×10-33。
sp 3 sp 3
回答下列问题:
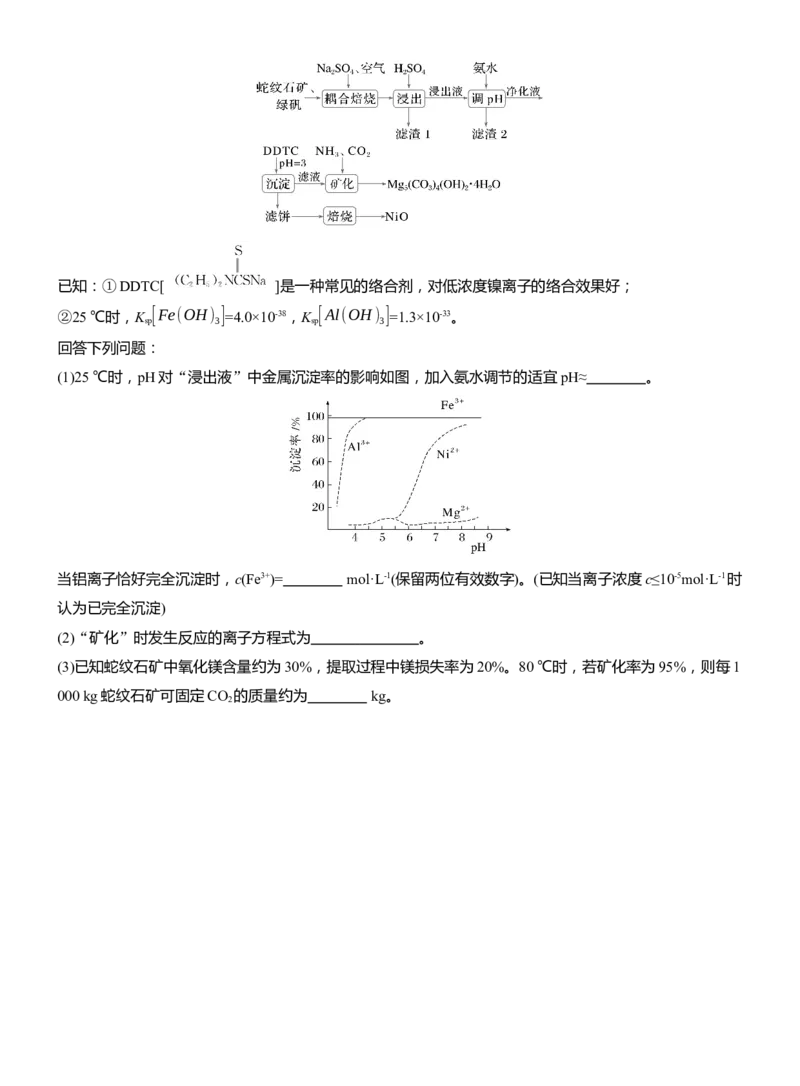
(1)25 ℃时,pH对“浸出液”中金属沉淀率的影响如图,加入氨水调节的适宜pH≈ 。
当铝离子恰好完全沉淀时,c(Fe3+)= mol·L-1(保留两位有效数字)。(已知当离子浓度c≤10-5mol·L-1时
认为已完全沉淀)
(2)“矿化”时发生反应的离子方程式为 。
(3)已知蛇纹石矿中氧化镁含量约为30%,提取过程中镁损失率为20%。80 ℃时,若矿化率为95%,则每1
000 kg蛇纹石矿可固定CO 的质量约为 kg。
2答案精析
c(SiO2-
)
1.Fe3+、Al3+ Mg2+、Mn2+ 反应CaSiO (s)+CO2- (aq) SiO2- (aq)+CaCO (s)的平衡常数K= 3 =
3 3 3 3 c(CO2-
)
3
K (CaSiO ) 2.5×10-8
sp 3 = <105
K (CaCO ) 2.8×10-9
sp 3
2.10-2
解析 已知K [Mg (PO )
]=c3(Mg2+)·c2(PO3-
)=2.0×10-24、K [Mg (AsO )
]=c3(Mg2+)·c2(AsO3-
)=2.0×10-20,将溶
sp 3 4 2 4 sp 3 4 2 4
√K [M g (PO ) ]
sp 3 4 2
c(PO3- ) c3 (M g2+ ) √2.0×10-24
4
液的pH调至9时,溶液中 = = =10-2。
c(AsO3- ) √K [M g (AsO ) ] 2.0×10-20
4 sp 3 4 2
c3 (M g2+ )
3.1.75×10-4
解析 K [Be(OH) ]=c(Be2+)·c2(OH-)=7×10-22,室温下pH=11时,c(OH-)=1×10-3 mol·L-1,则c(Be2+)=7×10-16
sp 2
c(Be2+ )·c4 (F-
)
7×10-16×14
mol·L-1,又c(F-)=1
mol·L-1,BeF2-
的解离常数K = =
=4×10-12,则c(BeF2-
4 d c(BeF2-
)
c(BeF2-
)
4
4 4
)=1.75×10-4 mol·L-1。
4.(1)钴、铁 3.0 (2)H O+Mn2++HSO- ===MnO ↓+SO2- +3H+ 3.2
2 5 2 4
解析 由题干工艺流程图可知,将粗Co(OH) 加水打磨成浆后加入H SO 和SO 进行浸出,得到含Co2+、
3 2 4 2
Fe2+、Al3+、Mg2+、Mn2+的浸出液,过滤除去其他不溶性杂质,向滤液中加入生石灰、热空气和SO ,过滤
2
出Fe(OH) 和MnO ,向滤液中加入萃取剂P204以萃取Co2+,分液后水相含有Al3+、Ca2+和Mg2+,有机相
3 2
含有Co2+,对有机相进行反萃取得到水相中含有CoSO ,据此分析解题。(2)“除杂”时混合气在金属离子
4
的催化作用下产生具有强氧化性的过一硫酸(H SO ),H SO 中含有一个过氧键,故Mn2+被H SO 氧化为
2 5 2 5 2 5
MnO ,H SO 转化为H SO ,该反应的离子方程式为H
O+Mn2++HSO-
===MnO
↓+SO2-
+3H+,检验反应
2 2 5 2 4 2 5 2 4
√K [Fe(OH) ] √10-37.4
后的滤液中恰好不存在Fe3+,即c(Fe3+)=10-5 mol·L-1,此时c(OH-)= 3 sp 3 =3 mol·L-1≈10-10.8
c(Fe3+
)
10-5
K 10-14
w
mol·L-1,则c(H+)= = mol·L-1=10-3.2 mol·L-1,即生石灰调节pH=3.2。
c(OH-
)
10-10.8
241cV
5.(1)0.25 mol·L-1 (2)ZnFe (C O ) ·6H O ZnFe O +4CO↑+2CO ↑+6H O 20a %
2 2 4 3 2 2 4 2 2K (CuS) 6.4×10-36
sp
解析 (1)若净化后的溶液中Cu2+浓度为1×10-12mol·L-1,c(S2-)= = mol·L-1=6.4×10-
c(Cu2+
)
1×10-12
K (ZnS) 1.6×10-24
sp
24mol·L-1,则净化后溶液中c(Zn2+)= = mol·L-1=0.25 mol·L-1。(2)由题可知关系式:
c(S2-
)
6.4×10-24
0.5cV ×10-3×241 241cV
ZnFe O ~I ~2S
O2-
,w(ZnFe O )= ×100%= %。
2 4 2 2 3 2 4 a 20a
6.(1)4.7≤pH<5.8 Nd(H PO ) +9OH-===Nd(OH) +3PO3- +6H O (2)Nd O(CO ) (或Nd C O )
2 4 3 3 4 2 2 3 2 2 2 7
Nd 2 (C 2 O 4 ) 3·10H 2 O Nd 2 O 3 +3CO↑+3CO 2 ↑+10H 2 O
解析 (1)由信息可知,0.1 mol·L-1的Fe2+开始沉淀的pH=6.3,此时c(H+)=1×10-6.3 mol·L-1,c(OH-)=1×10-7.7
mol·L-1,K [Fe(OH) ]=c(Fe2+)·c2(OH-)=0.1×(1×10-7.7)2=1×10-16.4,则当c(Fe2+)=1.0 mol·L-1时,c(OH-)=
sp 2
√K [Fe(OH) ] √1×10-16.4
sp 2 = mol·L-1=1×10-8.2 mol·L-1时开始沉淀,此时pH=5.8,“沉钕”时需保证Al3+
c(Fe2+ ) 1.0
完全沉淀,而Fe2+ 不沉淀,所以调节pH范围为4.7≤pH<5.8;“碱转化”过程Nd元素由Nd(H PO ) 转
2 4 3
化为Nd(OH) ,发生反应的离子方程式为Nd(H PO ) +9OH-===Nd(OH) +3PO3- +6H O。(2)设
3 2 4 3 3 4 2
Nd (C O ) ·10H O物质的量为1 mol,即732 g。750 K时质量减少(24.6%+17.5%)×732 g≈308 g,此时减少的
2 2 4 3 2
除10个结晶水外,还减少C和O元素的质量,12x+16y+180=308,解得x=4,y=5,即一个
Nd (C O ) ·10H O减少了10个结晶水、4个C和5个O,剩余的为Nd C O ,所以此时得到的固体为
2 2 4 3 2 2 2 7
Nd C O 或写作Nd O(CO ) ;若在1 000 K下进行煅烧,由质量不再减少可知此时所得固体为Nd O ,由
2 2 7 2 3 2 2 3
(C O )
原子守恒以及得失电子守恒可知发生反应的化学方程式为Nd 2 2 4 3·10H 2 O
Nd O +3CO↑+3CO ↑+10H O。
2 3 2 2
7.(1)4.5 3.1×10-10 (2)5Mg2++10NH +4CO +10H O===Mg (CO ) (OH) ·4H O↓+10N H+ (3)200.64
3 2 2 5 3 4 2 2 4
解析 (1)根据图示,为使Fe3+、Al3+尽可能沉淀,Ni2+、Mg2+尽可能不损失,加入氨水调节的适宜
c(Fe3+ ) K [Fe(OH) ]
sp 3
pH≈4.5。当铝离子恰好完全沉淀时,c(Al3+)=1.0×10-5 mol·L-1,根据 = 得
c(Al3+ ) K [Al(OH) ]
sp 3
24
c(Fe3+)≈3.1×10-10 mol·L-1。(3)根据有关数据,“矿化”时实际反应的Mg2+质量为1 000 kg×30%× ×(1-
40
20%)×95%=136.8 kg,根据“矿化”反应的离子方程式得关系式:
5Mg2+~4CO
2
5×24 4×44
136.8 kg m
4×44×136.8
m= kg=200.64 kg。
5×24