文档内容
化工流程题的综合分析(A)
1.(10分)(2024·山东,18)以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag的工艺流程如下:
2
(1)“热浸”时,难溶的PbS和Ag S转化为[PbCl ]2-和[AgCl ]-及单质硫。溶解等物质的量的PbS和Ag S时,
2 4 2 2
消耗Fe3+物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时HCl挥发外,另一目
的是防止产生 (填化学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属Pb。“电解Ⅰ”阳极
2
产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填标号)。
A.Al B.Zn
C.Pb D.Ag
“置换”反应的离子方程式为 。
(5)“电解Ⅱ”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。
2.(10分)电子级氢氟酸是微电子行业的关键性基础材料之一,由萤石粉(主要成分为CaF ,含有少量SiO 和
2 2
微量As O 等)制备的工艺如下:
2 3(1)“酸浸”时生成HF的化学方程式为 ,工业生产时往往会适当加热,
目的是 。
(2)“精馏1”设备使用的材料可选用 (填字母)。
A.玻璃 B.陶瓷
C.石英 D.金
(3)已知H SiF 是一种配位酸,酸性与硝酸相近,可与KMnO 溶液反应制备极易溶于水的强酸HMnO ,反
2 6 4 4
应的离子方程式为 。
(4)“氧化”时将AsF 氧化为AsF 。AsF 的沸点高于AsF ,原因是 。
3 5 5 3
(5)液态HF是酸性溶剂,能发生自偶电离:HF H++F-,由于H+和F-都溶剂化,常表示为3HF H F+
2
+HF-
。在HF溶剂中AsF 、BF 呈酸性,HClO 、HNO 、H O呈碱性,比如AsF 、HClO 的电离方程式分
2 5 3 3 3 2 5 3
别为AsF +2HF
AsF-
+H F+、HOClO +2HF (HO)
ClO++HF-
。在HF作用下:
5 6 2 2 2 2
①写出BF 与HNO 反应的离子方程式: 。
3 3
②已知:H O与AsF 反应生成HAsF 。结合H+的能力:H O
(填“>”“<”或“=”)AsF-
。
2 5 6 2 6
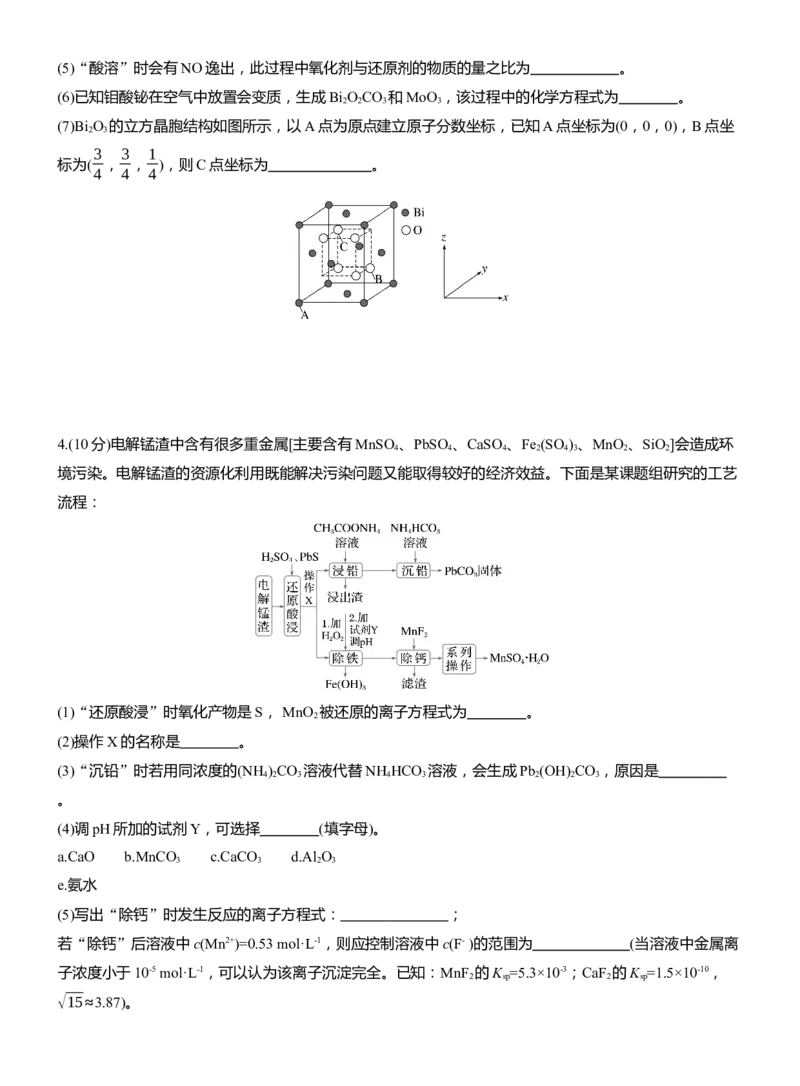
3.(10分)(2023·石家庄质量检测)钼酸铋作为新型半导体光催化材料,因其具有优异的离子导电性、介电性、
气体传感性和催化性而广泛应用于生产生活中。以氧化铋渣(主要成分是Bi O 、Sb O ,还含有Fe O 、
2 3 2 3 2 3
ZnO、Ag O和SiO 等杂质)为原料制备钼酸铋(Bi MoO ,其中Mo为+6价)的工艺流程如图:
2 2 2 6
(1)基态 Bi的价层电子排布为 。
83
(2)“浸渣”的主要成分为 (填化学式)。
(3)“除锑”过程中发生反应的化学方程式为 ;
该过程需要加热的原因为 。
(4)已知:硫代乙酰胺( )在酸性溶液中会水解为乙酰胺( )和硫化氢;H S的
2
K =1.0×10-7,K =1.0×10-13;K (Bi S )=2.0×10-99。
a1 a2 sp 2 3
①硫化氢会进一步发生反应:2Bi3+(aq)+3H S(aq)===Bi S (s)+6H+(aq),计算该反应的平衡常数K=
2 2 3
。
②硫代乙酰胺比乙酰胺的沸点低,其原因为 。(5)“酸溶”时会有NO逸出,此过程中氧化剂与还原剂的物质的量之比为 。
(6)已知钼酸铋在空气中放置会变质,生成Bi O CO 和MoO ,该过程中的化学方程式为 。
2 2 3 3
(7)Bi O 的立方晶胞结构如图所示,以A点为原点建立原子分数坐标,已知A点坐标为(0,0,0),B点坐
2 3
3 3 1
标为( , , ),则C点坐标为 。
4 4 4
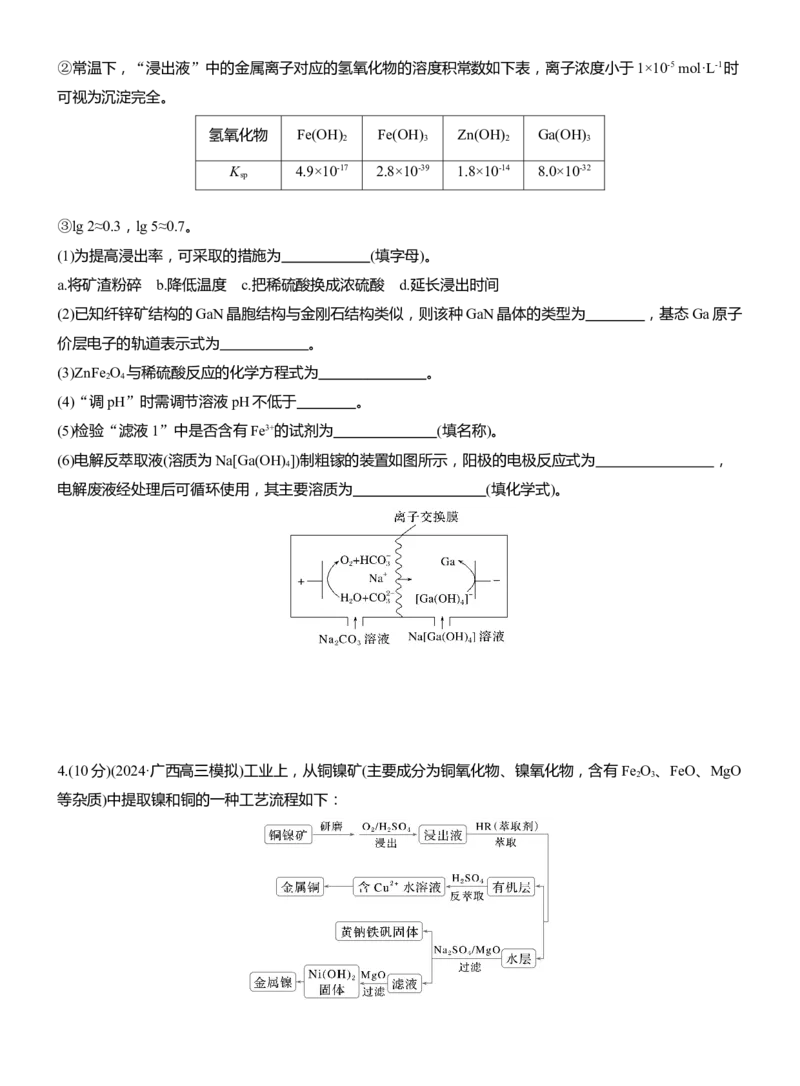
4.(10分)电解锰渣中含有很多重金属[主要含有MnSO 、PbSO 、CaSO 、Fe (SO ) 、MnO 、SiO ]会造成环
4 4 4 2 4 3 2 2
境污染。电解锰渣的资源化利用既能解决污染问题又能取得较好的经济效益。下面是某课题组研究的工艺
流程:
(1)“还原酸浸”时氧化产物是S, MnO 被还原的离子方程式为 。
2
(2)操作X的名称是 。
(3)“沉铅”时若用同浓度的(NH ) CO 溶液代替NH HCO 溶液,会生成Pb (OH) CO ,原因是
4 2 3 4 3 2 2 3
。
(4)调pH所加的试剂Y,可选择 (填字母)。
a.CaO b.MnCO c.CaCO d.Al O
3 3 2 3
e.氨水
(5)写出“除钙”时发生反应的离子方程式: ;
若“除钙”后溶液中c(Mn2+)=0.53 mol·L-1,则应控制溶液中c(F- )的范围为 (当溶液中金属离
子浓度小于10-5 mol·L-1,可以认为该离子沉淀完全。已知:MnF 的K =5.3×10-3;CaF 的K =1.5×10-10,
2 sp 2 sp
√15≈3.87)。5.(10分)硼化钛(结构式为B==Ti==B)常用于制备导电陶瓷材料和PTC材料。工业上以高钛渣(主要成分为
TiO 、SiO 、Al O 和CaO,另有少量MgO、Fe O )为原料制取TiB 的流程如下:
2 2 2 3 2 3 2
已知:①电弧炉是由石墨电极和石墨坩埚组成的高温加热装置;
②B O 高温下蒸气压大、易挥发;
2 3
③TiO 可溶于热的浓硫酸形成TiO2+。
2
(1)“水解”需在沸水中进行,离子方程式为 , 该工艺中,经处理可循环利用的物质为
(填化学式)。
(2)“热还原”中发生反应的化学方程式为 ,B O 的实际用量超过
2 3
了理论化学计量所要求的用量,原因是 。仅增大配料中B O 的用量,
2 3
产品中的杂质含量变化如图所示。杂质TiC含量随w%增大而降低的原因是 (用化学方程
式解释)。
(3)原料中的B O 可由硼酸脱水制得。以NaB(OH) 为原料,用电渗析法制备硼酸(H BO )的工作原理如图所
2 3 4 3 3
示,产品室中发生反应的离子方程式为 。
若反应前后NaOH溶液的质量变化为m kg,则制得H BO 的质量为 kg。
3 3化工流程题的综合分析(B)
1.(10分)(2024·河南高三适应性测试)硝酸镉晶体[Cd(NO ) ·4H O]常用作玻璃和陶瓷的着色剂。以镉黄
3 2 2
废料(主要含CdS,含少量的FeO、Al O 、SiO )为原料制备硝酸镉晶体的流程如下:
2 3 2
已知:常温下,有关金属离子形成氢氧化物沉淀的相关pH见下表。
Fe(OH) Al(OH) Cd(OH)
3 3 2
开始沉淀的pH 2.3 4.0 8.2
沉淀完全的pH 4.2 5.2 9.7
(1)Cd位于第五周期,与Zn同族,基态镉原子的价层电子排布式为 。
(2)“酸溶”时,反应温度不宜过高,原因是 。
(3)“滤渣1”的主要成分是 。
(4)“除杂”步骤中,加入CdCO 的目的是调pH,范围为 ;该过程中Fe3+发生反应
3
的离子方程式为 。
(5)“系列操作”步骤中,将滤液送入蒸发器浓缩至 ,然后送至结晶器进行冷却结晶,可得到硝酸
镉晶体。
(6)硝酸镉晶体需在低温的条件下烘干。其在111.2 ℃时失去结晶水,217.3 ℃时分解产生CdO和红棕色的
混合气体,该混合气体可以使带火星的木条复燃。硝酸镉在217.3 ℃时分解的化学方程式为
。
2.(10分)(2024·甘肃酒泉模拟)甘肃矿产资源丰富,金属冶炼在国民经济发展中有着重要的作用。锰酸锂离
子蓄电池是第二代锂离子动力电池,工业上用某软锰矿(主要成分为MnO ,还含有少量铁、铝及硅的氧化
2
物)为原料制备锰酸锂(LiMn O ),流程如图所示:
2 4(1)“酸浸”时,为了提高各物质的浸出速率,除了适当升高温度外,还可以采取的措施是
(写一条即可)。
(2)“还原”步骤得到的溶液中阳离子主要是Mn2+,生成Mn2+的离子方程式为 ;
滤渣1的主要成分为 。
(3)已知某离子浓度[用c(M)表示]形成沉淀与溶液pH的关系如图所示:
则“精制”过程中,加MnO调节pH的范围是 。
(4)“沉锰”得到的是Mn(OH) 和Mn (OH) SO 滤饼,所得滤液回收可用于 。
2 2 2 4
(5)“锂化”是将MnO 和Li CO 按4∶1的物质的量比配料,球磨3~5 h,然后升温至600~750 ℃,保温24
2 2 3
h,自然冷却至室温得产品,写出反应的化学方程式: 。
3.(10分)(2024·南宁模拟)GaN是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主
要含铁酸镓[Ga (Fe O ) ]、铁酸锌(ZnFe O ),还含少量Fe及一些难溶于酸的物质}获得金属盐,并进一
2 2 4 3 2 4
步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
已知:①Fe
O2-
在酸性条件下不稳定,易转化为Fe3+。
2 4②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于1×10-5 mol·L-1时
可视为沉淀完全。
氢氧化物 Fe(OH) Fe(OH) Zn(OH) Ga(OH)
2 3 2 3
K 4.9×10-17 2.8×10-39 1.8×10-14 8.0×10-32
sp
③lg 2≈0.3,lg 5≈0.7。
(1)为提高浸出率,可采取的措施为 (填字母)。
a.将矿渣粉碎 b.降低温度 c.把稀硫酸换成浓硫酸 d.延长浸出时间
(2)已知纤锌矿结构的GaN晶胞结构与金刚石结构类似,则该种GaN晶体的类型为 ,基态Ga原子
价层电子的轨道表示式为 。
(3)ZnFe O 与稀硫酸反应的化学方程式为 。
2 4
(4)“调pH”时需调节溶液pH不低于 。
(5)检验“滤液1”中是否含有Fe3+的试剂为 (填名称)。
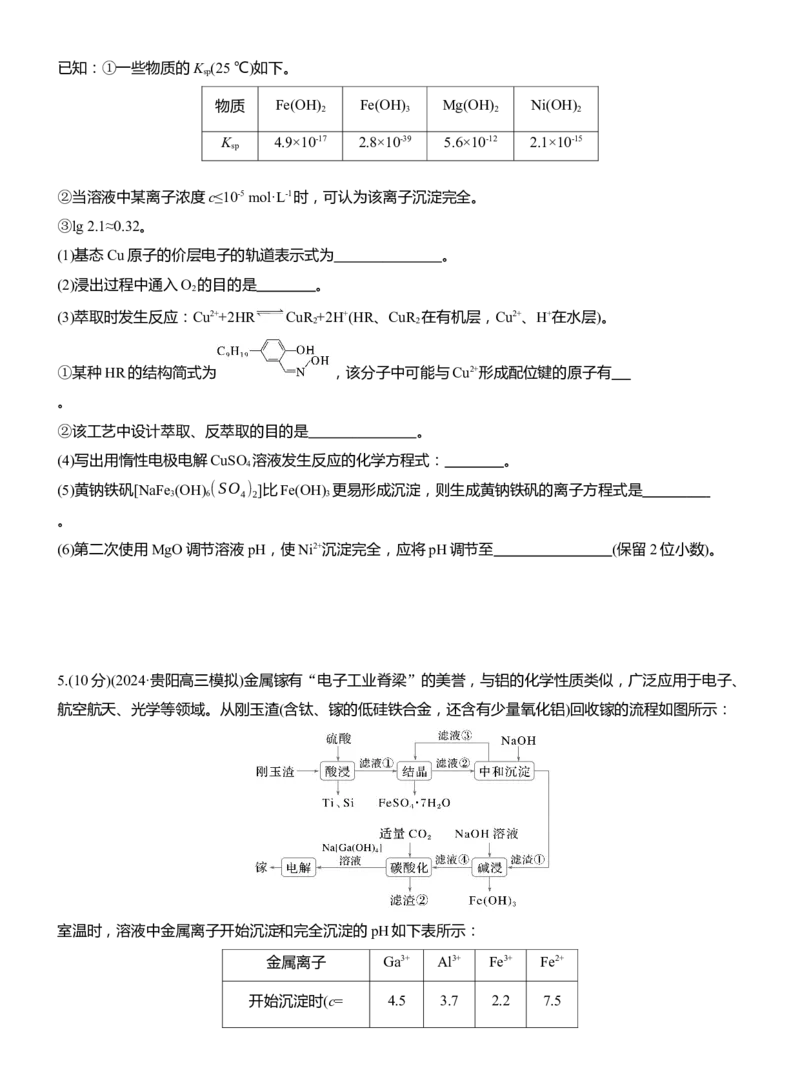
(6)电解反萃取液(溶质为Na[Ga(OH) ])制粗镓的装置如图所示,阳极的电极反应式为 ,
4
电解废液经处理后可循环使用,其主要溶质为 (填化学式)。
4.(10分)(2024·广西高三模拟)工业上,从铜镍矿(主要成分为铜氧化物、镍氧化物,含有Fe O 、FeO、MgO
2 3
等杂质)中提取镍和铜的一种工艺流程如下:已知:①一些物质的K (25 ℃)如下。
sp
物质 Fe(OH) Fe(OH) Mg(OH) Ni(OH)
2 3 2 2
K 4.9×10-17 2.8×10-39 5.6×10-12 2.1×10-15
sp
②当溶液中某离子浓度c≤10-5 mol·L-1时,可认为该离子沉淀完全。
③lg 2.1≈0.32。
(1)基态Cu原子的价层电子的轨道表示式为 。
(2)浸出过程中通入O 的目的是 。
2
(3)萃取时发生反应:Cu2++2HR CuR +2H+(HR、CuR 在有机层,Cu2+、H+在水层)。
2 2
①某种HR的结构简式为 ,该分子中可能与Cu2+形成配位键的原子有
。
②该工艺中设计萃取、反萃取的目的是 。
(4)写出用惰性电极电解CuSO 溶液发生反应的化学方程式: 。
4
(5)黄钠铁矾[NaFe (OH) (SO ) ]比Fe(OH) 更易形成沉淀,则生成黄钠铁矾的离子方程式是
3 6 4 2 3
。
(6)第二次使用MgO调节溶液pH,使Ni2+沉淀完全,应将pH调节至 (保留2位小数)。
5.(10分)(2024·贵阳高三模拟)金属镓有“电子工业脊梁”的美誉,与铝的化学性质类似,广泛应用于电子、
航空航天、光学等领域。从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的流程如图所示:
室温时,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ga3+ Al3+ Fe3+ Fe2+
开始沉淀时(c= 4.5 3.7 2.2 7.50.01 mol·L-1)的pH
完全沉淀时(c=1.0×
5.5 4.7 3.2 9.0
10-5 mol·L-1)的pH
(1)基态镓原子的价层电子排布式为 。
(2)从溶液中得到FeSO ·7H O的具体操作为 、 、过滤、洗涤、干燥。
4 2
(3)“中和沉淀”过程中分离出的滤渣①有Fe(OH) 和 (填化学式),若滤液②中阳离子浓
3
度均为0.1 mol·L-1,“中和沉淀”过程中pH应调节的范围为 。
(4)“碱浸”时镓元素发生反应的离子方程式为 。
(5)“碳酸化”过程中为防止镓损耗,不能通入过量CO 的原因为
2
(用离子方程式表示)。
(6)以纯镓为原料可制得GaN,GaN晶体的一种立方晶胞如图所示,Ga的配位数为 ,
已知晶胞中Ga和N的最近距离为a nm,阿伏加德罗常数的值为N ,则GaN的晶体密度为
A
g·cm-3(列出计算式)。答案精析
A
1.(1)1∶1 H S (2)热浸 (3)将过量的Fe3+还原为Fe2+
2
(4)C Pb+2[AgCl ]-===2Ag+[PbCl ]2- (5)阳极
2 4
解析 本题以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag,“热浸”时,难溶的PbS和Ag S转
2 2
化为[PbCl ]2-和[AgCl ]-及单质硫,Fe3+被还原为Fe2+,“过滤Ⅰ”除掉含硫滤渣,滤液中[PbCl ]2-在稀释冷
4 2 4
却的过程中转化为PbCl 沉淀,然后用饱和食盐水热溶,增大氯离子浓度,使PbCl 又转化为[PbCl ]2-,电
2 2 4
解得到Pb;“过滤Ⅱ”后的滤液成分主要为[AgCl ]-、FeCl 、FeCl ,故加入铅精矿主要将FeCl 还原为
2 2 3 3
FeCl ,试剂X将[AgCl ]-置换为Ag,得到富银铅泥,试剂X的金属性应比Ag强,为不引入新的杂质,可
2 2
知X为铅,尾液为FeCl 。(1)“热浸”时,Fe3+将PbS和Ag S中-2价的硫氧化为单质硫,Fe3+被还原为
2 2
Fe2+,在这个过程中Pb和Ag的化合价保持不变,所以溶解等物质的量的PbS和Ag S时,S2-的物质的量相
2
等,消耗Fe3+的物质的量相等;溶液中盐酸浓度过大,会与S2-结合生成H S气体。(2)“过滤Ⅱ”得到的
2
PbCl 沉淀反复用饱和食盐水热溶,会溶解为[PbCl ]2-,电解[PbCl ]2-溶液制备金属Pb,Pb在阴极产生,阳
2 4 4
极Cl-放电产生Cl ,可将尾液中的FeCl 氧化为FeCl ,在“热浸”中循环使用。(3)“过滤Ⅱ”所得的滤液
2 2 3
中有过量的未反应的Fe3+,根据还原之后可以得到含硫滤渣,“还原”中加入铅精矿的目的是将过量的
Fe3+还原为Fe2+。(5)“电解Ⅱ”中将富银铅泥做阳极板,银变成阳极泥而沉降下来,铅失电子转化为
Pb2+,阴极Pb2+得电子析出Pb。
2.(1)CaF +H SO (浓)===CaSO +2HF↑ 加快反应速率,提高CaF 的转化率 (2)D (3)2K++SiF2-
2 2 4 4 2 6
===K SiF ↓ (4)AsF 、AsF 均为分子晶体(分子间均不存在氢键),AsF 相对分子质量大,范德华力大,沸
2 6 5 3 5
点高
(5)①BF +HNO +HF===(HO)
NO++BF-
②<
3 3 2 4
解析 “酸浸”发生反应:CaF +H SO (浓)===CaSO +2HF↑,二氧化硅与HF发生反应:
2 2 4 4
SiO +4HF===SiF ↑+2H O,As O 与HF发生反应:As O +6HF===2AsF +3H O;“硫酸吸附”:加入硫酸,
2 4 2 2 3 2 3 3 2
部分HF、SiF 以气体形式释放出去,然后加入水吸收为H SiF ,部分HF、AsF 、多余硫酸进入精馏
4 2 6 3
1;“精馏1”:因为硫酸熔、沸点较高,因此精馏1中得到HF、AsF ;“氧化”:根据问题(4),过氧化
3
氢将AsF 氧化成熔、沸点较高的AsF ;“精馏2”:蒸馏得到HF。
3 5
(2)HF能与二氧化硅发生反应,玻璃、陶瓷、石英均含有二氧化硅,HF不与金反应,因此“精馏1”设备
以金为材料。
(3)KMnO →HMnO 中Mn的价态没有发生变化,H SiF 酸性与硝酸相似,即H SiF 为强酸,HMnO 为溶于
4 4 2 6 2 6 4
水的强酸,该反应为复分解反应,生成K SiF
沉淀,即离子方程式为2K++SiF2-
===K SiF ↓。
2 6 6 2 6(5)①HNO 在HF中呈碱性,其电离方程式为HNO +2HF (HO)
NO++HF-
,BF 在HF中呈酸性,其电离
3 3 2 2 3
方程式为BF +2HF
BF-
+H F+,因此两者混合,发生类似的中和反应,其离子方程式为
3 4 2
BF +HNO +HF===(HO) NO++BF- 。②H O与AsF 反应生成HAsF ,从而推出H O结合H+能力小于AsF-
3 3 2 4 2 5 6 2 6
。
3.(1)6s26p3 (2)AgCl、SiO (3)2SbCl +3H O Sb O ↓+6HCl 盐酸易挥发,加热有利于HCl挥发,水解
2 3 2 2 3
平衡正向移动 (4)①5.0×1038 ②乙酰胺分子间氢键的键能及数目均大于硫代乙酰胺 (5)2∶1
1 3 3
(6)Bi MoO +CO ===Bi O CO +MoO (7)( , , )
2 6 2 2 2 3 3 4 4 4
解析 氧化铋渣(主要成分是Bi O 、Sb O ,还含有Fe O 、ZnO、Ag O和SiO 等杂质)加入盐酸和氯化钠溶
2 3 2 3 2 3 2 2
液,二氧化硅不与盐酸反应,氧化银和盐酸反应生成氯化银,其他物质和盐酸生成相应氯化物,过滤,向
滤液中加水加热得到Sb O ,过滤,向滤液中加入 沉铋,过滤,向Bi S 中加入硝酸得到单质硫、
2 3 2 3
NO和硝酸铋,向硝酸铋溶液中加入(NH ) Mo O ·4H O得到Bi MoO 。
4 6 7 24 2 2 6
(4)①硫化氢会进一步发生反应:2Bi3+(aq)+3H S(aq)===Bi S (s)+6H+(aq),则该反应的平衡常数K=
2 2 3
c6 (H+ ) c6 (H+ )·c3 (S2- ) K3 (H S)·K3 (H S)
= ,K= a1 2 a2 2 =
c2 (Bi3+ )·c3 (H S) c2 (Bi3+ )·c3 (S2- )·c3 (H S) K (Bi S )
2 2 sp 2 3
(1.0×10-7
)
3×(1.0×10-13
)
3
=5.0×1038。(5)“酸溶”时会有NO逸出,即Bi S 和硝酸反应得到单质硫、NO
2.0×10-99 2 3
和硝酸铋,Bi S 中硫元素化合价从-2价升高到0价,硝酸中氮元素化合价从+5价降低到+2价,因此此过
2 3
程中氧化剂与还原剂的物质的量之比为2∶1。(7)Bi O 的立方晶胞结构如图所示,以A点为原点建立原子
2 3
3 3 1
分数坐标,已知A点坐标为(0,0,0),B点坐标为( , , ),则C点位于体对角线的四分之一处,其
4 4 4
1 3 3
坐标为( , , )。
4 4 4
4.(1)MnO +PbS+4H++SO2- ===Mn2++PbSO +S+2H O (2)过滤 (3)CO2-更易水解生成OH-,从而易生成
2 4 4 2 3
Pb (OH) CO (4)abc (5)MnF (s)+Ca2+(aq) Mn2+(aq)+CaF (s) 3.87×10-3 mol·L-1