文档内容
专题四 元素及其化合物
考 点 高考年 考频解密 考点分布
2022年河北卷〔4,5〕;2022年北京卷
〔4〕;2022年山东卷〔6,12〕;2022年
常见金属 钠及其化合物〔10次〕,镁
江苏卷〔11〕;2022年湖北卷〔4〕;
及其化合物〔1次〕,铁及
及其化合 2022 年 2022年广东卷〔4,5,12,14〕;2022年
其化合物〔12次〕,铝及其
海南卷〔1,5,6〕;2022年湖南卷
物的性质 化合物〔6次〕,
〔7〕;2022年全国甲卷〔3〕;2022年全
国乙卷〔1〕等
2022年河北卷〔1,3〕;2022年北京卷
氯及其化合物〔7次〕,氮
无机非金属 〔4,10〕;2022年山东卷〔2,10,
族元素及其化合物〔12
11〕;2022年江苏卷〔1,4,8,11〕;
物质及其化 2022 年 次〕,氧族元素及其化合物
2022年广东卷〔8,12〕;2022年海南卷
合物性质 〔13次〕,碳族元素及其化
〔3〕;2022年湖南卷〔2,7〕;2022年
合物〔16次〕
全国甲卷〔1〕;
一、金属单质的性质
<一>常见金属的主要性质
1.钠及其化合物
①等物质的量的金属钠被氧化成NaO和NaO 时转移的电子数相同。
2 2 2
②钠与酸反应时,先与酸反应,酸不足再与水反应。
③钠与盐的溶液反应:钠不能置换出溶液中的金属,钠直接与水反应,反应后的碱再与溶液中的其他物质
反应。
④Na O 与CO 或HO反应时,生成1 mol O ,转移电子的物质的量为2 mol。
2 2 2 2 2
⑤Na O 跟CO 和水蒸气组成的混合气体反应时,应先考虑 NaO 跟CO 的反应。因为若先发生反应:
2 2 2 2 2 2
2NaO+2HO===4NaOH+O↑,必定还发生反应:2NaOH+CO===Na CO+HO。
2 2 2 2 2 2 3 2
⑥Na O 与SO 反应的化学方程式为:NaO+SO ===Na SO 。
2 2 2 2 2 2 2 4
⑦向NaCO 溶液中逐滴滴入盐酸,反应是分步进行的。反应的离子方程式依次为:CO+H+===HCO、
2 3
HCO+H+===HO+CO↑。
2 22.镁、铝及其化合物
①镁在空气中燃烧主要发生反应:2Mg+O=====2MgO,此外还发生反应:3Mg+N=====MgN 、2Mg
2 2 3 2
+CO 2MgO+C。
2
②Mg N 与水反应:MgN+6HO===3Mg(OH) +2NH ↑。
3 2 3 2 2 2 3
③加热Mg(HCO ) 溶液生成的是Mg(OH) 沉淀,而不是MgCO 沉淀,因为Mg(OH) 比MgCO 更难溶于
3 2 2 3 2 3
水。反应方程式为Mg(HCO ) Mg(OH) ↓+2CO↑。
3 2 2 2
④铝与NaOH溶液、非氧化性强酸反应生成H。常温下,浓硝酸、浓硫酸使铝发生钝化。
2
⑤Al O、Al(OH) 仅能溶于强酸和强碱溶液中(如在氨水和碳酸中不溶)。
2 3 3
⑥Al3+、AlO只能分别存在于酸性、碱性溶液中。Al3+与下列离子不能大量共存:OH-、CO、HCO、SO、
S2-、ClO-、AlO,其中OH-是因为直接反应,其余均是因为发生了剧烈的双水解反应。AlO与下列离子
不能大量共存:H+、HCO、Al3+、Fe2+、Fe3+,其中H+和HCO是因为与AlO直接反应(AlO+HCO+
HO===Al(OH) ↓+CO),其余也是因为发生了剧烈的双水解反应。
2 3
⑦明矾的净水原理:明矾的化学式为KAl(SO )·12H O,它在水中能电离:KAl(SO )===K++Al3++2SO。
4 2 2 4 2
铝离子发生水解反应,生成的氢氧化铝胶体具有很强的吸附能力,吸附水中的悬浮物,使之沉降以达到净
水目的:Al3++3HO Al(OH) (胶体)+3H+。
2 3
3.铁、铜及其化合物
①Fe与Cl 反应只能生成FeCl ,与I 反应生成FeI,与反应物的用量无关。
2 3 2 2
②Fe与水蒸气在高温下反应生成H 和Fe O,而不是Fe O。
2 3 4 2 3
③过量的Fe与硝酸作用,或在Fe和Fe O 的混合物中加入盐酸,均生成Fe2+。要注意产生的Fe3+还可以
2 3
氧化单质Fe这一隐含反应:Fe+2Fe3+===3Fe2+。
④NO与Fe2+在酸性条件下不能共存。
⑤Fe O、Fe(OH) 与氢碘酸反应时,涉及Fe3+与I-的氧化还原反应,产物为Fe2+、I 和HO。
2 3 3 2 2
⑥FeCl 溶液加热浓缩时,因Fe3+水解和HCl的挥发,得到的固体为Fe(OH) ,灼烧后得到红棕色Fe O 固
3 3 2 3
体;而Fe (SO ) 溶液蒸干时,因硫酸是难挥发性的酸,将得不到 Fe(OH) 固体,最后得到的固体仍为
2 4 3 3
Fe (SO )。
2 4 3
⑦注意亚铁盐及Fe(OH) 易被空气中氧气氧化成三价铁的化合物。如某溶液中加入碱溶液后,最终得到红
2
褐色沉淀,并不能断定该溶液中一定含有Fe3+,也可能含有Fe2+。
<二>常见金属的性质比较
金属活动
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
性顺序表
性质变化规 元素的金属性逐渐减弱,单质的还原性依次减弱,离子的氧化性逐渐增强律
与冷水剧 与沸水缓 高温与水
烈反应 慢反应 蒸气反应
和水的反应 — 不跟水反应
生成氧化
生成碱和氢气
物和氢气
剧烈反应 反应逐渐减缓 不能置换稀酸中的氢
和酸的 与非氧化性酸反应放出H ;与浓硫酸、浓硝 与氧化性
2
— 只溶于
反应 酸及稀硝酸反应,不放出H ,一般产物为: 酸反应(但
2
王水
盐+水+成酸元素的低价化合物 不放出H)
2
金属先与水反
和盐溶液
应生成碱,碱 排在前面的金属可将后面的金属从其盐溶液中置换出来
的反应
再与盐反应
和氧气 常温生成 加热能 加热能 不能被
易被氧化 —
的反应 氧化膜 被氧化 被氧化 氧化
金属氧化物 氧化物跟水剧
对应的水化 烈反应,生成 氧化物不溶于水,也不跟水反应,对应碱的热稳定性逐渐
物及碱的热 碱,碱受热不 减弱
稳定性 易分解
电解法 热还原法 煅烧法 —
金属的 高 温 下 用 CO( 或
冶炼 电解熔融盐或氧化物 Al)从其氧化物中还 — —
原出来
只以游
自然界中存 多以化合态存在,但有极少的游
只以化合态(盐、氧化物)存在 离态存
在的形式 离态
在
<三>金属元素及其化合物的重要性质和应用
常见物质 日常应用 利用的性质
钠 核反应堆的传热介质 熔点较低,导热性好
氢氧化钠 制肥皂 与油脂发生皂化反应生成高级脂肪酸钠
调味剂 具有咸味
氯化钠
配制生理盐水(0.9%) 体液替代物
发酵粉、
2NaHCO NaCO+HO+CO↑
3 2 3 2 2
膨松剂
碳酸氢钠 胃酸中和剂 HCO+H+===H O+CO↑
2 2
Al (SO )+6NaHCO ===
2 4 3 3
用于泡沫灭火器
2Al(OH) ↓+6CO↑+3NaSO
3 2 2 4
碳酸钠 清洗油污 水解,溶液显碱性制玻璃 NaCO+SiO NaSiO+CO↑
2 3 2 2 3 2
氧化铝 耐火材料 熔点高
铝制品 表面易生成致密的氧化膜
铝
铝热剂(焊接钢轨) 2Al+Fe O Al O+2Fe(放出大量热量)
2 3 2 3
氢氧化铝 胃酸中和剂 碱性较弱Al(OH) +3H+===Al3++3HO
3 2
在水中生成Al(OH) [或Fe(OH) ]胶体,其可
3 3
明矾、铁盐 净水剂
以和悬浮的泥沙形成絮状不溶物沉降下来
氧化铁 红色油漆和涂料 氧化铁是一种红棕色粉末
硫酸铜 配制农药,杀菌消毒 铜离子(重金属离子)能使蛋白质变性
二、非金属及其化合物的性质应用
<一>常见非金属单质的性质
非金属单质 Cl、Br 、I、O、O、N、H、S、C、Si
2 2 2 2 3 2 2
①气态的有Cl 、O 、O 、N 、H ;固态的有S、C、Si、I ;Br 为液态。
2 2 3 2 2 2 2
物 颜色、状态
②Cl 黄绿色、Br 深红棕色、I 紫黑色、S淡黄色
2 2 2
理
Cl、Br 溶于水;S不溶于水、微溶于酒精、易溶于CS,其他均不易溶于
2 2 2
性 溶解性
水
质
毒性 Cl、Br 、I 有一定的毒性
2 2 2
①N 放电或高温时反应;②H 、S、C、Si加热或点燃时反应,其他一般
2 2
与O
2
不反应
化
与H ①Cl 光照爆炸;②O 点燃爆炸;③N 在高温高压催化剂条件下反应
2 2 2 2
学
与HO ①Cl、Br 与水反应,既作氧化剂,又作还原剂;②C与水高温下反应
2 2 2
性
与碱 Br 、I 与碱反应,既作氧化剂,又作还原剂
2 2
质
与氧化剂 S、C与强氧化性酸如浓硫酸、浓硝酸反应
与还原剂 Cl、Br 、O、O 与HSO 、NaSO 、HS、NaS、Fe2+、I-等还原剂反应
2 2 2 3 2 3 2 3 2 2
特性及用途 I 使淀粉变蓝、Si作半导体材料
2
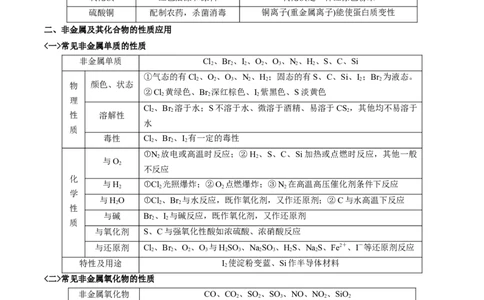
<二>常见非金属氧化物的性质
非金属氧化物 CO、CO、SO 、SO 、NO、NO 、SiO
2 2 3 2 2
色、 ①除 SiO 外,其余均为气体;②除 NO 红棕色外,其他均无色;
2 2
物理
状、味 ③SO 、NO 有刺激性气味;④SO 易液化
2 2 2
性质
毒性 除CO、SiO 外均有毒
2 2
类型 CO、SO 、SO 、SiO 是酸性氧化物;CO、NO、NO 是不成盐氧化物
2 2 3 2 2
①SO 、SO 、CO 生成相应酸;②NO 生成酸和NO;③SiO 、NO、
2 3 2 2 2
与HO
2
化学 CO不溶于水
性质 与碱 CO、SO 、SO 、SiO 等酸性氧化物与碱溶液反应生成正盐或酸式盐
2 2 3 2
氧化性 ①SO 能氧化HS;②CO、SiO 能在高温下被C还原
2 2 2 2①SO 具有较强还原性,能被Cl 、Br 、I 、O 、MnO、Fe3+、HNO 等
2 2 2 2 3 3
还原性
氧化剂氧化为SO;②NO遇空气被氧化为红棕色的NO
2
特性 ①SO 具有漂白性;②SiO 能与氢氟酸反应;③2NO NO
2 2 2 2 4
SO 、NO、NO 、CO均是大气污染物:SO →酸雨、NO、NO →光化学
2 2 2 2
环保
烟雾、CO→有毒气体
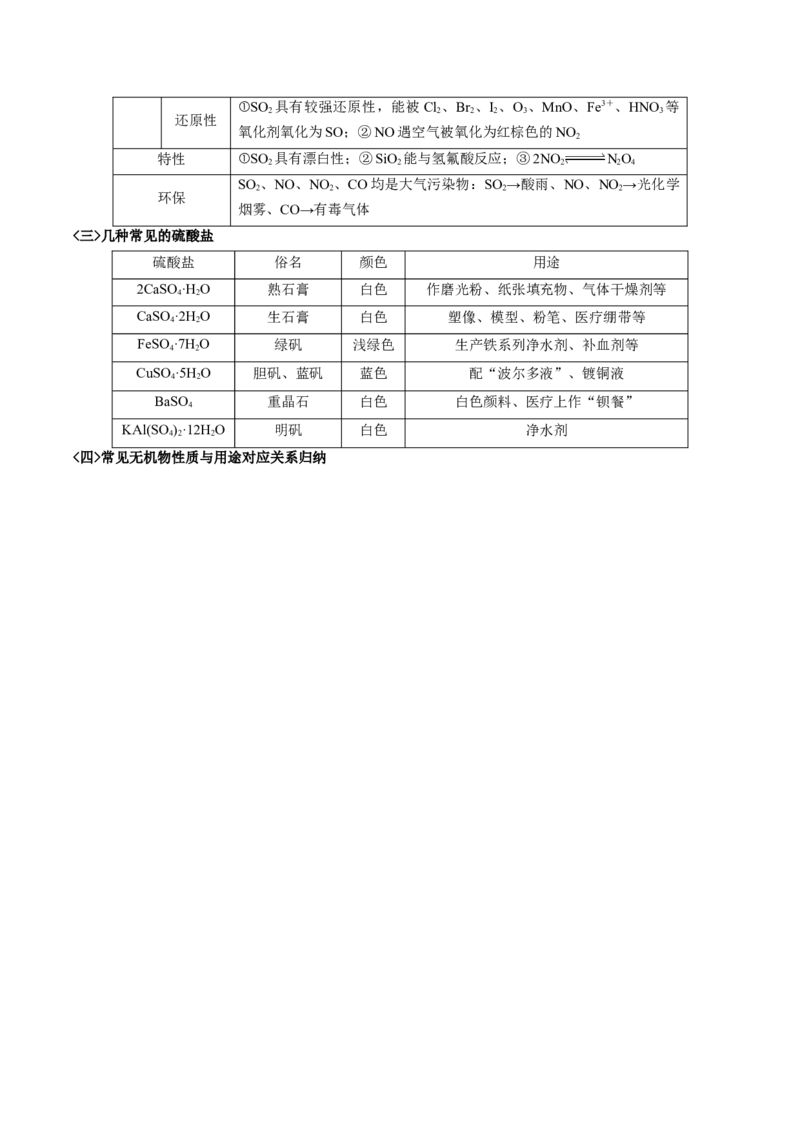
<三>几种常见的硫酸盐
硫酸盐 俗名 颜色 用途
2CaSO·H O 熟石膏 白色 作磨光粉、纸张填充物、气体干燥剂等
4 2
CaSO·2H O 生石膏 白色 塑像、模型、粉笔、医疗绷带等
4 2
FeSO ·7H O 绿矾 浅绿色 生产铁系列净水剂、补血剂等
4 2
CuSO ·5H O 胆矾、蓝矾 蓝色 配“波尔多液”、镀铜液
4 2
BaSO 重晶石 白色 白色颜料、医疗上作“钡餐”
4
KAl(SO )·12H O 明矾 白色 净水剂
4 2 2
<四>常见无机物性质与用途对应关系归纳性质 用途
硅是常用的半导体材料 可作太阳能电池板
二氧化硅导光能力强,并且有硬度和柔韧度 可作光导纤维
4HF+SiO===2H O+SiF↑ 用HF雕刻玻璃
2 2 4
2C+SiO=====Si+2CO↑ 碳还原二氧化硅制备粗硅
2
碘酸钾在常温下稳定 食盐中的加碘物质
氮气的化学性质稳定 作保护气
浓氨水具有挥发性和还原性 用浓氨水检验输送氯气的管道是否漏气
草木灰和硫铵反应生成氨气,使肥效降低 草木灰和硫铵不能混合施用
二氧化硫具有还原性 二氧化硫可用于制作葡萄酒的食品添加剂
氦气化学性质稳定、密度小 可用于填充飞艇、气球
钠具有较强的还原性 可用于冶炼钛、锆、铌等金属
NaHCO 受热分解生成CO,能与酸反应 可用作焙制糕点的膨松剂、胃酸中和剂
3 2
NaCO 水解使溶液显碱性 用热的纯碱溶液洗去油污
2 3
NaO 与HO、CO 反应均生成O 作供氧剂
2 2 2 2 2
肥皂水显碱性 肥皂水作蚊虫叮咬处的清洗剂
水玻璃不燃不爆 可用作耐火材料
硅酸钠的水溶液是一种无机黏合剂 盛放碱性溶液的试剂瓶不能用玻璃塞
锂质量轻、比能量大 可用作电池负极材料
Al具有良好的延展性和抗腐蚀性 常用铝箔包装物品
铝有还原性,能发生铝热反应 可用于焊接铁轨、冶炼难熔金属
MgO、Al O 的熔点很高 作耐高温材料
2 3
小苏打与硫酸铝溶液发生双水解反应 可以作泡沫灭火器
Al(OH) 有弱碱性 可用于中和胃酸
3
镁铝合金质量轻、强度大 可用作高铁车厢材料
Fe粉具有还原性 可用于防止食品氧化变质
Fe O 是红棕色粉末 可用作红色颜料
2 3
Cu+2FeCl ===2FeCl +CuCl FeCl 腐蚀Cu刻制印刷电路板
3 2 2 3
CuSO 使蛋白质变性 误服CuSO 溶液,喝蛋清或豆浆解毒
4 4
BaSO 不溶于水,不与胃酸反应 在医疗上用作“钡餐”透视
4
探究一 铝及其化合物的性质对于下列实验,能正确描述其反应的离子方程式是( )
A.等物质的量浓度、等体积的Ca(HCO ) 溶液与NaOH溶液混合:Ca2++ +OH—=CaCO ↓+H O
3 2 3 2
B.向饱和NaCO 溶液中通入CO: +CO +H O=2
2 3 2 2 2
C.AlCl 溶液中加入过量的浓氨水:Al3++4NH·H O= +4 +2H O
3 3 2 2
D.向明矾溶液中滴加Ba(OH) 溶液,恰好使 沉淀完全:2Al3++3 +3Ba2++6OH—=Al(OH) ↓+
2 3
3BaSO↓
4
规律总结:
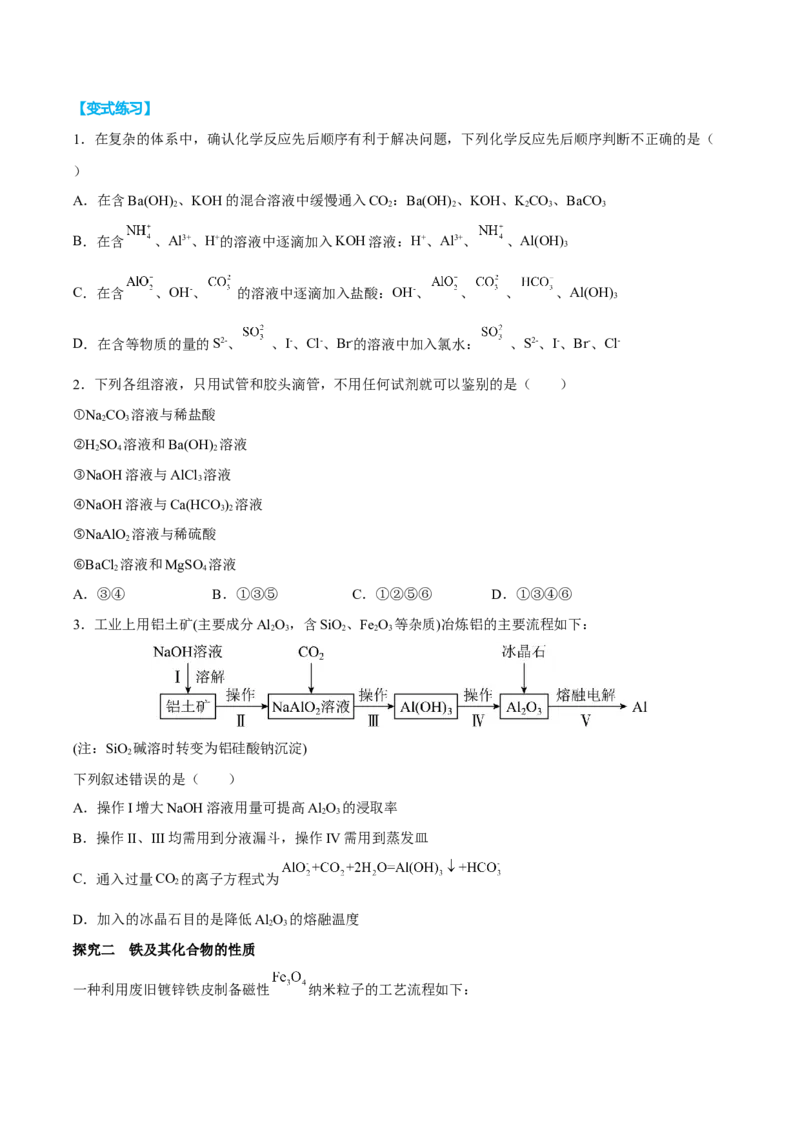
1.解答“铝三角”的转化及应用题,关键是抓住Al(OH)₃的两性,熟练掌握Al³⁺、 、Al(OH)₃之间的转
化反应。
①分析酸(或碱)的强弱及其物质的量,结合反应物的用量确定物质之间的反应情况及定量关系。
②结合盐类的水解原理,牢记A1³⁺与 、 、 、S²⁻、HS⁻等在水溶液中因发生相互促进的
水解反应而不能大量共存。
③抓住n(OH-)、n(Al³⁺)的关系,分段讨论,确定可溶性铝盐与强碱溶液反应时, Al元素的存在形式及生成
Al(OH) 的量,用数轴表示为:
3
2.解答与Al(OH)₃有关的图像题,要抓住六个“关键”:
①分析图中各点横、纵坐标物理量的意义,尤其是起始点、折点、极值点、拐点、最终点的横、纵坐标的意
义。
②判断加入酸或碱的强弱, Al(OH) 不溶于弱酸(如H CO 等)和弱碱。
3 2 3
③明确所加入试剂的量或滴加顺序,因为滴加顺序不同产生的现象可能不同。
④若产生沉淀有多种,则应仔细分析相关量间的关系。
⑤特别关注沉淀是否完全,沉淀物是否溶于所加入的过量试剂。
⑥掌握 Al(OH) 溶解所需酸、碱的物质的量与 Al(OH) 的定量关系。
3 3【变式练习】
1.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断不正确的是(
)
A.在含Ba(OH) 、KOH的混合溶液中缓慢通入CO:Ba(OH) 、KOH、KCO、BaCO
2 2 2 2 3 3
B.在含 、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、 、Al(OH)
3
C.在含 、OH-、 的溶液中逐滴加入盐酸:OH-、 、 、 、Al(OH)
3
D.在含等物质的量的S2-、 、I-、Cl-、Br-的溶液中加入氯水: 、S2-、I-、Br-、Cl-
2.下列各组溶液,只用试管和胶头滴管,不用任何试剂就可以鉴别的是( )
①Na CO 溶液与稀盐酸
2 3
②H SO 溶液和Ba(OH) 溶液
2 4 2
③NaOH溶液与AlCl 溶液
3
④NaOH溶液与Ca(HCO ) 溶液
3 2
⑤NaAlO 溶液与稀硫酸
2
⑥BaCl 溶液和MgSO 溶液
2 4
A.③④ B.①③⑤ C.①②⑤⑥ D.①③④⑥
3.工业上用铝土矿(主要成分Al O,含SiO、Fe O 等杂质)冶炼铝的主要流程如下:
2 3 2 2 3
(注:SiO 碱溶时转变为铝硅酸钠沉淀)
2
下列叙述错误的是( )
A.操作I增大NaOH溶液用量可提高Al O 的浸取率
2 3
B.操作II、III均需用到分液漏斗,操作IV需用到蒸发皿
C.通入过量CO 的离子方程式为
2
D.加入的冰晶石目的是降低Al O 的熔融温度
2 3
探究二 铁及其化合物的性质
一种利用废旧镀锌铁皮制备磁性 纳米粒子的工艺流程如下:已知:
下列有关说法正确的是( )
A.“酸溶”时将稀硫酸改为浓硫酸会显著提高溶解效率
B.“氧化”时发生反应的离子方程式为
C.“氧化”时后的溶液中主要有 、 、 三种阳离子
D.两次加入NaOH溶液时均发生氧化还原反应
规律总结:解答“铁三角”的转化及应用题,要以氧化还原反应知识为理论指导,抓住物质的氧化性和还
原性,考虑反应物的量对产物的影响。
1.结合物质的氧化性、还原性与所含元素化合价的关系,认识Fe的还原性、Fe3+的氧化性及Fe2+的氧化性
和还原性。
2.抓住Fe2+的还原性、氧化性和Fe3+的氧化性,从铁元素的三种价态的相互转化角度,认识Fe2+、Fe3+参与
陌生反应的实质,结合守恒规律书写相应离子方程式。
3.结合Fe3+的沉淀性[易生成Fe(OH) 沉淀]理解工艺流程中除去Fe2+的原理及方法。大多加入氧化剂(如
3
H O 等)将Fe2+氧化成Fe3+,调节溶液pH,使Fe3+转化为Fe(OH) 沉淀,再过滤除去杂质。
2 2 3
4.迁移应用教材中Fe2+、Fe3+的检验方法及原理,解决溶液中有关Fe2+、Fe3+的检验(或推断)问题。
【变式练习】
1.向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,
线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是( )
A.线段Ⅰ表示Fe2+的变化情况B.根据图象可计算a=5
C.线段Ⅳ发生反应的离子方程式为I+5Cl+12OH-=2 +10Cl-+6H O
2 2 2
D.原溶液中c(Fe2+):c(I-):c(Br-)=2:1:3
2.满足下列前提条件的离子方程式书写正确的是( )
A.向Fe(NO ) 溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I
3 3 2
B.Mg(HCO ) 溶液与过量NaOH溶液反应:Mg2++2HCO +4OH-=Mg(OH) ↓+2H O+2CO
3 2 2 2
C.向Ba(OH) 溶液中滴加NaHSO 溶液至混合溶液恰好为中性:Ba2++OH-+H++SO =BaSO ↓+H O
2 4 4 2
D.向FeBr 溶液中通入适量的氯气至溶液中有一半的Br-被氧化成Br :2Fe2++4Br-+3Cl=2Fe3++2Br +6Cl-
2 2 2 2
3.工业生产硫酸的黄铁矿烧渣(主要成分为Fe O,还含有少量的FeS、SiO、Cu、Au、Ag等)是工业三废
2 3 2
之一,其综合利用是一条变废为宝的重要途径。以黄铁矿烧渣为原料制备颜料铁红(Fe O)和回收(NH )SO
2 3 4 2 4
的生产工艺流程如图所示。
下列说法不正确的是( )
A.将矿渣粉碎和提高溶解温度能提高“废渣溶解”速率
B.“氧化”的目的是将+2价铁氧化为+3价铁
C.(NH )Fe (SO )(OH) 中Fe的化合价为+3价
4 2 6 4 4 12
D.该工艺流程中,两次加入氨水都是为了把Fe3+转化为Fe(OH)
3
探究三 氯及其化合物的性质
某兴趣小组用 和浓HCl制取 ,并探究氯、溴、碘的相关性质,装置图如下所示(夹持装置已略去)。
下列说法错误的是( )A.装置A发生反应的化学方程式为:
B.若装置C发生堵塞,则装置B中长颈漏斗内液面会上升
C.为了验证氯气是否具有漂白性,Ⅰ、Ⅱ、Ⅲ分别放置湿润的有色布条、无水氯化钙、干燥的有色布条
D.充分反应后,打开装置E的活塞,将少量溶液滳入D中,振荡,若观察到锥形瓶下层液体呈紫红色,
则可证明氧化性
规律总结:
1.氯气的实验室制备及性质探究题,要按照“制备──除杂─→性质探究(或收集)──尾气处理”的顺序
进行分析。
①依据反应原理选择制备 Cl 的发生装置:MnO 与浓盐酸反应需要加热,选择“固+液 气”发生装
2 2
置;KMnO 、KClO 等与浓盐酸在常温下反应,选择“固+液→气”发生装置。
4 4
②根据Cl 中所含杂质[HCl、H O(g)]的性质,确定除杂试剂及顺序:先将氯气通过盛有饱和食盐水的洗气瓶
2 2
除去HCl,再通过盛有浓硫酸的洗气瓶除去H O(g)。
2
③结合Cl 易与NaOH溶液反应的性质,选择NaOH溶液吸收尾气,注意防止倒吸。
2
④结合Cl 具有强氧化性及氧化还原反应知识,分析Cl 与金属、水、强碱溶液等发生的反应,并结合电子
2 2
得失守恒规律进行相关计算。
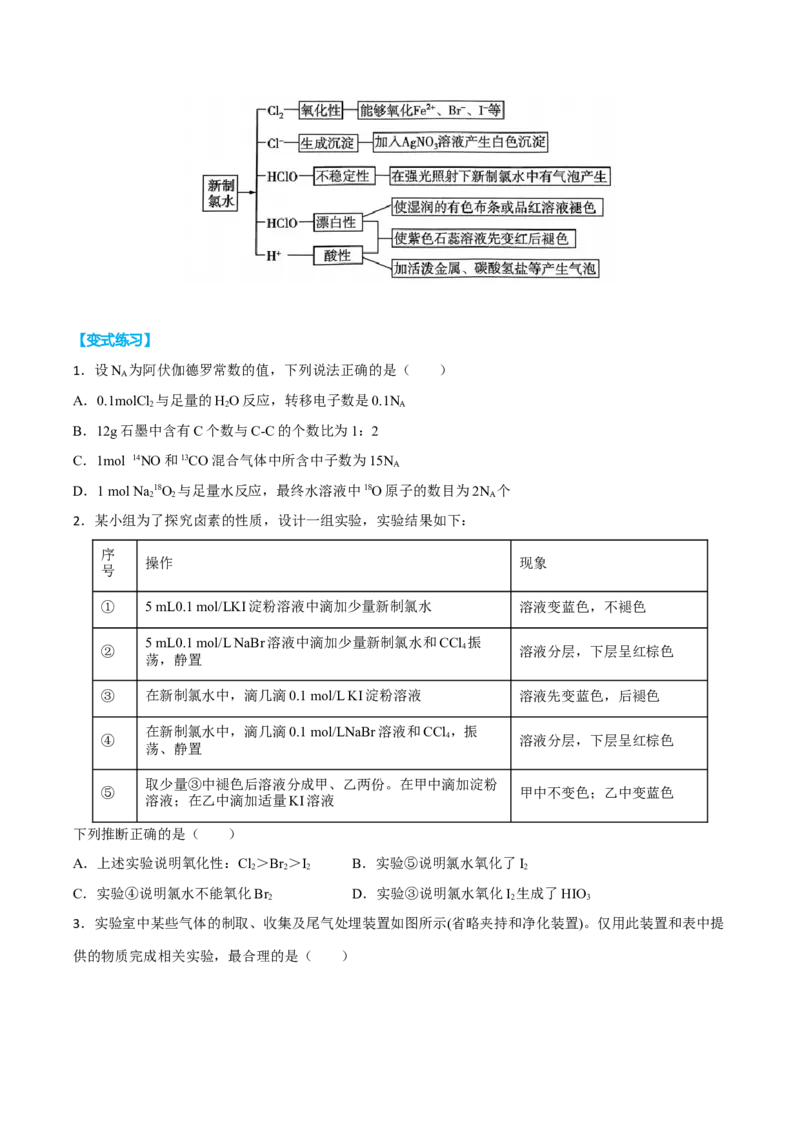
2.氯水的成分及性质题,要抓住氯水成分的“多样性”和性质的“多重性”。
①结合Cl 与H O反应的可逆性,认识氯水成分的“多样性”。氯水中存在 3个平衡:Cl +H O⇌H++Cl-
2 2 2 2
+HClO、HClO⇌H++ClO-、H O⇌OH+H+。故新制氯水是一个“三分子(Cl 、HClO和H O)、四离子
2 2 2
(H+、Cl-、ClO-和OH-)”的混合体系。
②由氯水成分的“多样性”,认识氯水性质的“多重性”。【变式练习】
1.设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A.0.1molCl 与足量的HO反应,转移电子数是0.1N
2 2 A
B.12g石墨中含有C个数与C-C的个数比为1:2
C.1mol 14NO和13CO混合气体中所含中子数为15N
A
D.1 mol Na 18O 与足量水反应,最终水溶液中18O原子的数目为2N 个
2 2 A
2.某小组为了探究卤素的性质,设计一组实验,实验结果如下:
序
操作 现象
号
① 5 mL0.1 mol/LKI淀粉溶液中滴加少量新制氯水 溶液变蓝色,不褪色
5 mL0.1 mol/L NaBr溶液中滴加少量新制氯水和CCl 振
② 4 溶液分层,下层呈红棕色
荡,静置
③ 在新制氯水中,滴几滴0.1 mol/L KI淀粉溶液 溶液先变蓝色,后褪色
在新制氯水中,滴几滴0.1 mol/LNaBr溶液和CCl ,振
④ 4 溶液分层,下层呈红棕色
荡、静置
取少量③中褪色后溶液分成甲、乙两份。在甲中滴加淀粉
⑤ 甲中不变色;乙中变蓝色
溶液;在乙中滴加适量KI溶液
下列推断正确的是( )
A.上述实验说明氧化性:Cl>Br >I B.实验⑤说明氯水氧化了I
2 2 2 2
C.实验④说明氯水不能氧化Br D.实验③说明氯水氧化I 生成了HIO
2 2 3
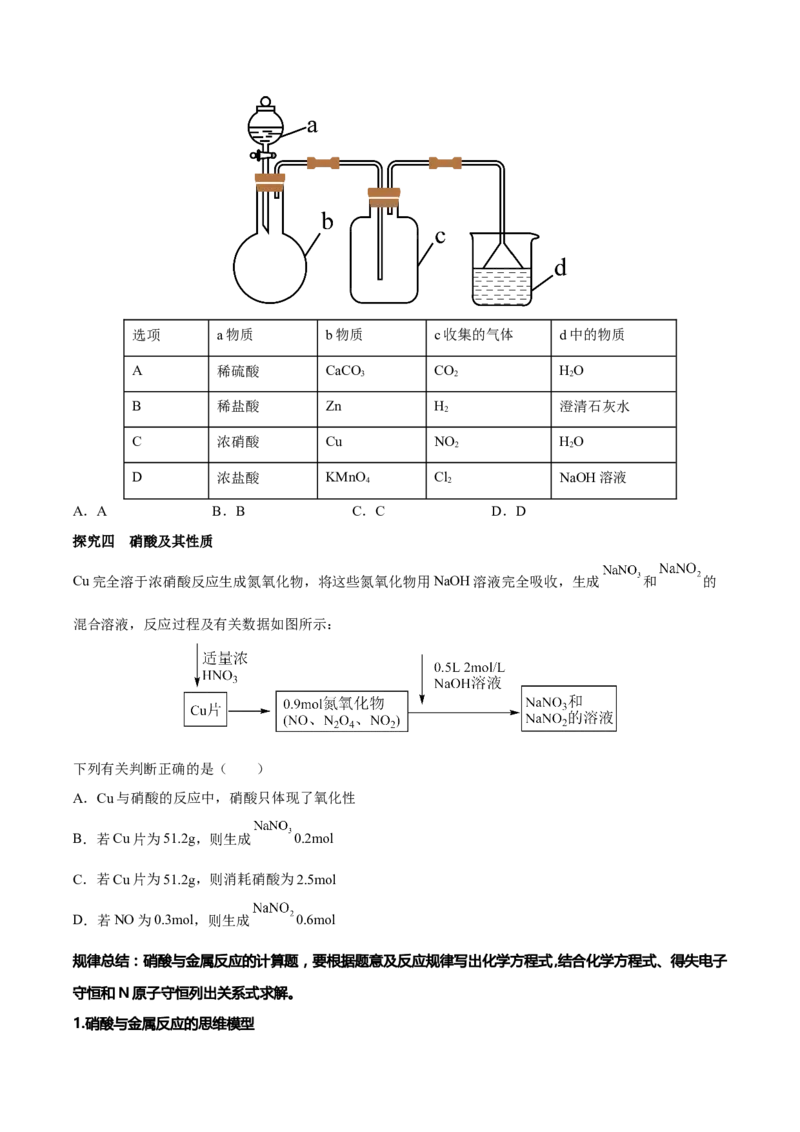
3.实验室中某些气体的制取、收集及尾气处埋装置如图所示(省略夹持和净化装置)。仅用此装置和表中提
供的物质完成相关实验,最合理的是( )选项 a物质 b物质 c收集的气体 d中的物质
A 稀硫酸 CaCO CO HO
3 2 2
B 稀盐酸 Zn H 澄清石灰水
2
C 浓硝酸 Cu NO HO
2 2
D 浓盐酸 KMnO Cl NaOH溶液
4 2
A.A B.B C.C D.D
探究四 硝酸及其性质
Cu完全溶于浓硝酸反应生成氮氧化物,将这些氮氧化物用NaOH溶液完全吸收,生成 和 的
混合溶液,反应过程及有关数据如图所示:
下列有关判断正确的是( )
A.Cu与硝酸的反应中,硝酸只体现了氧化性
B.若Cu片为51.2g,则生成 0.2mol
C.若Cu片为51.2g,则消耗硝酸为2.5mol
D.若NO为0.3mol,则生成 0.6mol
规律总结:硝酸与金属反应的计算题,要根据题意及反应规律写出化学方程式,结合化学方程式、得失电子
守恒和N原子守恒列出关系式求解。
1.硝酸与金属反应的思维模型2.“守恒法”在解答硝酸与金属反应的计算题中的应用
(1)原子守恒法
HNO 与金属反应时,一部分HNO 起酸的作用,以NO 的形式存在于溶液中;一部分作为氧化剂转化为还
3 3 3
原产物。这两部分中氮原子的总物质的量等于反应消耗的HNO₃中氮原子的物质的量。
(2)得失电子守恒法
HNO₃与金属的反应属于氧化还原反应,HNO 中氮原子得电子的物质的量等于金属失电子的物质的量。
3
(3)电荷守恒法
HNO 过量时,反应后溶液中(不考虑OH-)有:c(NO )=c(H+)+nc(Mn+)(Mn+代表金属离子)。
3 3
【变式练习】
1.下列指定反应的离子方程式书写正确的是( )
A.海水提溴工艺中,用纯碱溶液富集 :
B.水玻璃中加入过量稀 :
C.用 溶液吸收 :
D.过量铁粉与稀硝酸反应:
2.下列实验操作能达到实验目的的是( )
A.将NO和 的混合气体通过氢氧化钠溶液进行分离
B.为检验某品牌食盐中是否含有碘元素,将样品溶解后滴加淀粉溶液
C.向 溶液中滴加氢硫酸,产生淡黄色沉淀,证明 具有氧化性
D.向浓 中插入红热的炭,产生红棕色气体,证明炭可与浓 反应生成
3.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO 、NO的混合气体2.24L(标准状况),这些气体与
2一定体积O(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入
2
4mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确.的是( )
A.参加反应的硝酸是0.4mol B.消耗氧气的体积为1.12L
C.此反应过程中转移的电子为0.3mol D.参加反应的铜的质量是3.2g
1.氯化硫酰( )常用作氧化剂,它是一种无色液体,熔点: ,沸点:69.1℃,可用干燥的
和 在活性炭作催化剂的条件下制取: 。工业
上电解饱和食盐水制备氯气,实验室常用 与浓盐酸制备氯气。制备氯气时,下列装置能达到相应实
验目的的是( )
A.电解法制氯气 B.实验室制氯气
C.除去氯气中的HCl D.氯气收集和尾气处理
2.化学与生产、生活密切相关。下列说法错误的是( )
A.使用氯气对自来水消毒,生成的有机氯化物可能对人体有害
B.稀土元素包括镧系元素以及钪和钇,在科技、生产中有广泛的用途
C.按标准添加适量SO 能防止葡萄酒中的一些成分被氧化
2
D.植物油较动物脂肪含更多饱和脂肪酸的甘油酯,因而熔点较低
3.下列离子方程式书写正确的是( )
A.明矾溶液与过量氨水混合:B.用醋酸和淀粉 溶液检验加碘盐中的 :
C.过量铁粉与稀硝酸反应,产生无色气体:
D.少量 溶液与 溶液混合:
4.下列说法正确的是( )
A.实验室中,浓硝酸保存在棕色细口玻璃试剂瓶中,并置于阴凉处
B.金属汞洒落在实验室桌面上,必须收集,并深埋处理
C.浓硫酸溅到皮肤上,先用大量水冲洗,再涂抹硼酸溶液
D.用玻璃棒蘸取NaOH溶液点在湿润的pH试纸中央,与标准比色卡对比,读出pH值
5.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
选
实验 现象 结论
项
向浓 中加入炭粉并加热,产生的气体 有红棕色气体产生,石
A 有 和 产生
通入少量澄清石灰水 灰水变浑浊
溶液变为浅绿色且有白 被还原为 ,白色
B 向 和 混合溶液中通入足量
色沉淀生成
沉淀为
C 用熔融氯化铝做导电性实验 电流指针不偏转 氯化铝是非电解质
将乙醇与浓硫酸混合加热,产生的气体通入 产生的气体中一定含有乙
D 溶液紫红色褪去
酸性 溶液 烯
A.A B.B C.C D.D
6.有关硫元素的几种化合物的转化关系中说法正确的是( )
A.反应①中浓硫酸只表现出强氧化性
B.反应②中 通入滴有酚酞的NaOH溶液,溶液褪色,说明 具有漂白作用
C.反应④中 是既是氧化剂又是还原剂
D.上述反应均为氧化还原反应
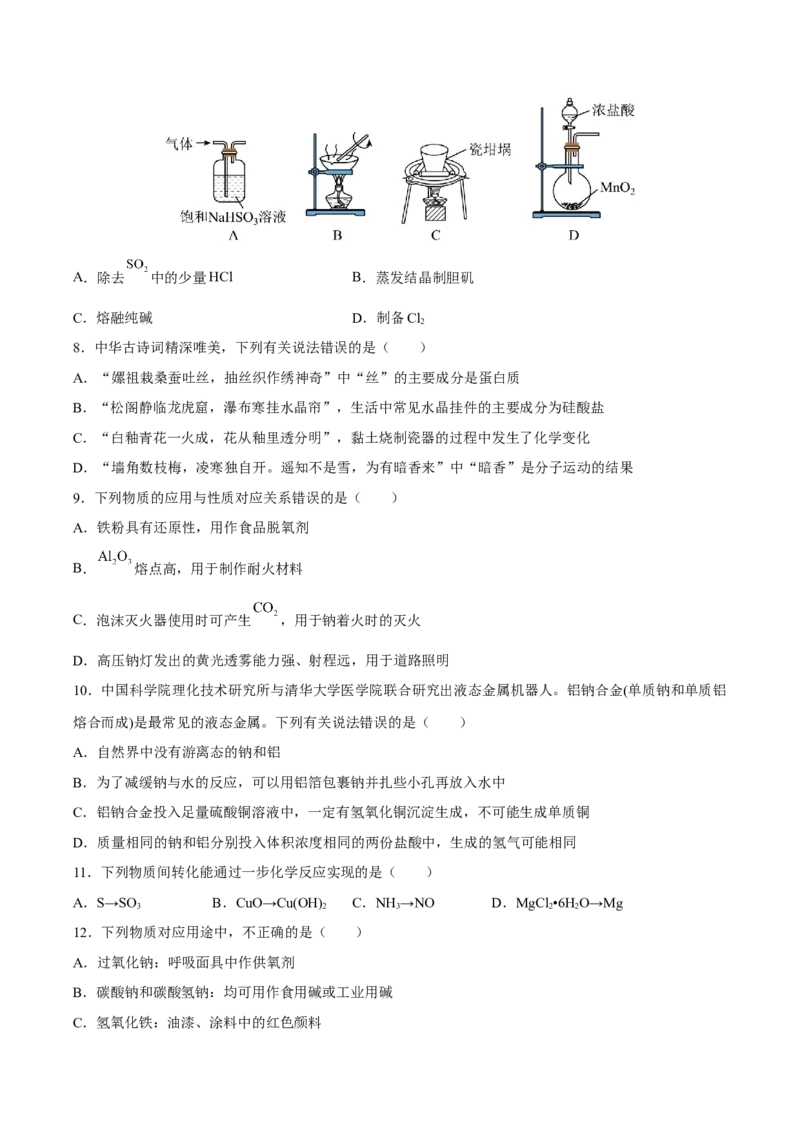
7.化学实验操作是进行科学实验的基础。下列操作能达到实验目的的是( )A.除去 中的少量HCl B.蒸发结晶制胆矶
C.熔融纯碱 D.制备Cl
2
8.中华古诗词精深唯美,下列有关说法错误的是( )
A.“嫘祖栽桑蚕吐丝,抽丝织作绣神奇”中“丝”的主要成分是蛋白质
B.“松阁静临龙虎窟,瀑布寒挂水晶帘”,生活中常见水晶挂件的主要成分为硅酸盐
C.“白釉青花一火成,花从釉里透分明”,黏土烧制瓷器的过程中发生了化学变化
D.“墙角数枝梅,凌寒独自开。遥知不是雪,为有暗香来”中“暗香”是分子运动的结果
9.下列物质的应用与性质对应关系错误的是( )
A.铁粉具有还原性,用作食品脱氧剂
B. 熔点高,用于制作耐火材料
C.泡沫灭火器使用时可产生 ,用于钠着火时的灭火
D.高压钠灯发出的黄光透雾能力强、射程远,用于道路照明
10.中国科学院理化技术研究所与清华大学医学院联合研究出液态金属机器人。铝钠合金(单质钠和单质铝
熔合而成)是最常见的液态金属。下列有关说法错误的是( )
A.自然界中没有游离态的钠和铝
B.为了减缓钠与水的反应,可以用铝箔包裹钠并扎些小孔再放入水中
C.铝钠合金投入足量硫酸铜溶液中,一定有氢氧化铜沉淀生成,不可能生成单质铜
D.质量相同的钠和铝分别投入体积浓度相同的两份盐酸中,生成的氢气可能相同
11.下列物质间转化能通过一步化学反应实现的是( )
A.S→SO B.CuO→Cu(OH) C.NH →NO D.MgCl •6H O→Mg
3 2 3 2 2
12.下列物质对应用途中,不正确的是( )
A.过氧化钠:呼吸面具中作供氧剂
B.碳酸钠和碳酸氢钠:均可用作食用碱或工业用碱
C.氢氧化铁:油漆、涂料中的红色颜料D.硬铝:制造飞机和宇宙飞船的理想材料
13.下列说法不正确的是( )
A.次氯酸有强氧化性,不仅可以消毒,还可以漂白棉、麻和纸张等
B.火灾现场有大量金属钠时,不能用水灭火,需用干燥的沙土灭火
C. 有漂白性,葡萄酒中加 是为了将红葡萄酒漂白成白葡萄酒
D.铝粉与NaOH遇水产生气体,且碱性液体能腐蚀食物残渣,故可做厨卫管道疏通剂
14.下列有关铁及其化合物的说法中正确的是( )
A. 和 都可以通过化合反应制取
B.细铁丝在空气里剧烈燃烧,火星四射,生成黑色固体
C.向饱和 溶液中滴加过量氨水,可制取 胶体
D.若某铁的氧化物可表示为 ,则该氧化物中
15.下列生活中的物质与其有效成分的化学式、用途的对应关系中,错误的是( )
选项 A B C D
物质 食盐 磁铁 小苏打 苛性钠
有效成分化学
NaCl Fe O NaCO NaOH
式 3 4 2 3
制备钠和氯气 药品制作、造
用途 炼铁原料 食用碱
原料 纸
A.A B.B C.C D.D
16.下列有关物质用途的说法正确的是( )
A.氢氟酸具有强酸性,可用于刻蚀玻璃
B.生石灰、铁粉、硅胶是食品包装中常用的干燥剂
C.硫铁矿(主要成分为FeS)主要用于工业制硫酸,其矿渣可用于炼铁
2
D.工业上用焦炭在高温下还原SiO 制取粗硅:SiO+C Si+CO ↑
2 2 2
17.下列关于物质用途的说法不合理的是( )
A. 用于制玻璃 B.铝制餐具用于蒸煮酸性食物C. 用作油漆红色颜料 D. 用作棉、麻、纸张的漂白剂
18.用浸有硝酸汞溶液的脱脂棉擦拭已打磨过的铝片,其中一片置于空气中,铜片表面生出“白毛”,另
一片投入蒸馏水中,持续产生气泡,下列说法不正确的是( )
A.白毛是铝被氧化得到的Al O B.气泡是铝与水反应生成的氢气
2 3
C.汞能抑制铝表面形成致密的膜 D.在上述反应中硝酸汞作催化剂
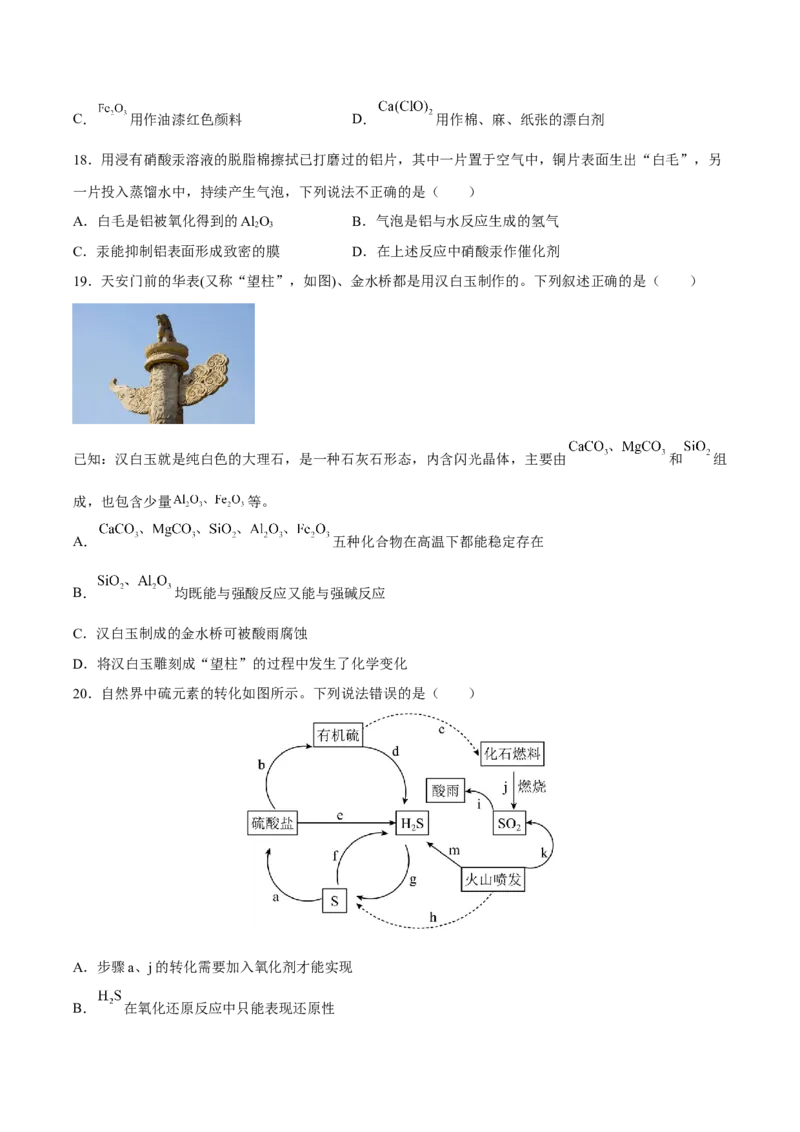
19.天安门前的华表(又称“望柱”,如图)、金水桥都是用汉白玉制作的。下列叙述正确的是( )
已知:汉白玉就是纯白色的大理石,是一种石灰石形态,内含闪光晶体,主要由 和 组
成,也包含少量 等。
A. 五种化合物在高温下都能稳定存在
B. 均既能与强酸反应又能与强碱反应
C.汉白玉制成的金水桥可被酸雨腐蚀
D.将汉白玉雕刻成“望柱”的过程中发生了化学变化
20.自然界中硫元素的转化如图所示。下列说法错误的是( )
A.步骤a、j的转化需要加入氧化剂才能实现
B. 在氧化还原反应中只能表现还原性C.在燃煤中添加生石灰可减少 的排放
D.用盐酸和 溶液可以检验可溶性硫酸盐中的阴离子
1某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实验:① 混合物溶于水,得
4 3
到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液中加碱,产生白色沉淀。根据实
验现象可判断其组成为( )
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
2.能正确表示下列反应的离子方程式为( )
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO ↓+2H O
2 4 4 4 2
3.下列实验设计不能达到实验目的的是( )
实验目的 实验设计
检验溶液中 是否被氧
A 取少量待测液,滴加 溶液,观察溶液颜色变化
化
B 净化实验室制备的 气体依次通过盛有饱和 溶液、浓 的洗气瓶
C 测定 溶液的pH 将待测液滴在湿润的pH试纸上,与标准比色卡对照
D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
A.A B.B C.C D.D
4.下列说法不正确的是( )
A.某些胶态金属氧化物分散于玻璃中可制造有色玻璃B.通常以海水提取粗食盐后的母液为原料制取溴
C.生物炼铜中通常利用某些细菌把不溶性的硫化铜转化为可溶性铜盐
D.工业制备硝酸的主要设备为沸腾炉、接触室和吸收塔
5.铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单元是硅氧四面体和铝氧四面体,
化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2
下列推测不正确的是( )
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
B.若a=x/2,则M为二价阳离子
C.调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D.分子筛中的笼状空穴和通道,可用于筛分分子
6.劳动开创未来。下列劳动项目与所述的化学知识没有关联的是( )
选
劳动项目 化学知识
项
A 面包师用小苏打作发泡剂烘焙面包 可与酸反应
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性
C 工人将模具干燥后再注入熔融钢水 铁与 高温下会反应
D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
A.A B.B C.C D.D
7.陈述Ⅰ和Ⅱ均正确但不具有因果关系的是( )
选
陈述Ⅰ 陈述Ⅱ
项
A 用焦炭和石英砂制取粗硅 可制作光导纤维
B 利用海水制取溴和镁单质 可被氧化, 可被还原
C 石油裂解气能使溴的 溶液褪色 石油裂解可得到乙烯等不饱和烃D 水解可生成 胶体 可用作净水剂
A.A B.B C.C D.D
8.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )
A.化合、置换、分解、复分解
B.置换、复分解、化合、分解
C.置换、化合、分解、复分解
D.置换、化合、复分解、分解
9.下列说法正确的是( )
A.铁与碘反应易生成碘化铁
B.电解ZnSO 溶液可以得到Zn
4
C.用石灰沉淀富镁海水中的Mg2+,生成碳酸镁
D.SO 通入BaCl 溶液中生成BaSO 沉淀
2 2 3
10.下列由实验现象所得结论错误的是( )
A.向NaHSO 溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 具有氧化性
3
B.向酸性KMnO 溶液中加入Fe O 粉末,紫色褪去,证明Fe O 中含Fe(Ⅱ)
4 3 4 3 4
C.向浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
11.化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是( )
选
操作或做法 目的
项
A 将铜丝插入浓硝酸中 制备
B 将密闭烧瓶中的 降温 探究温度对平衡移动的影响
C 将溴水滴入 溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余 固体放回原试剂瓶 节约试剂
A.A B.B C.C D.D
12.室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下实验。对实验现象的分析正
2 2
确的是( )A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C.取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +H O⇌H SO 、HSO ⇌H++
2 2 2 3 2 3
、 ⇌H++
D.取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO 挥发
2
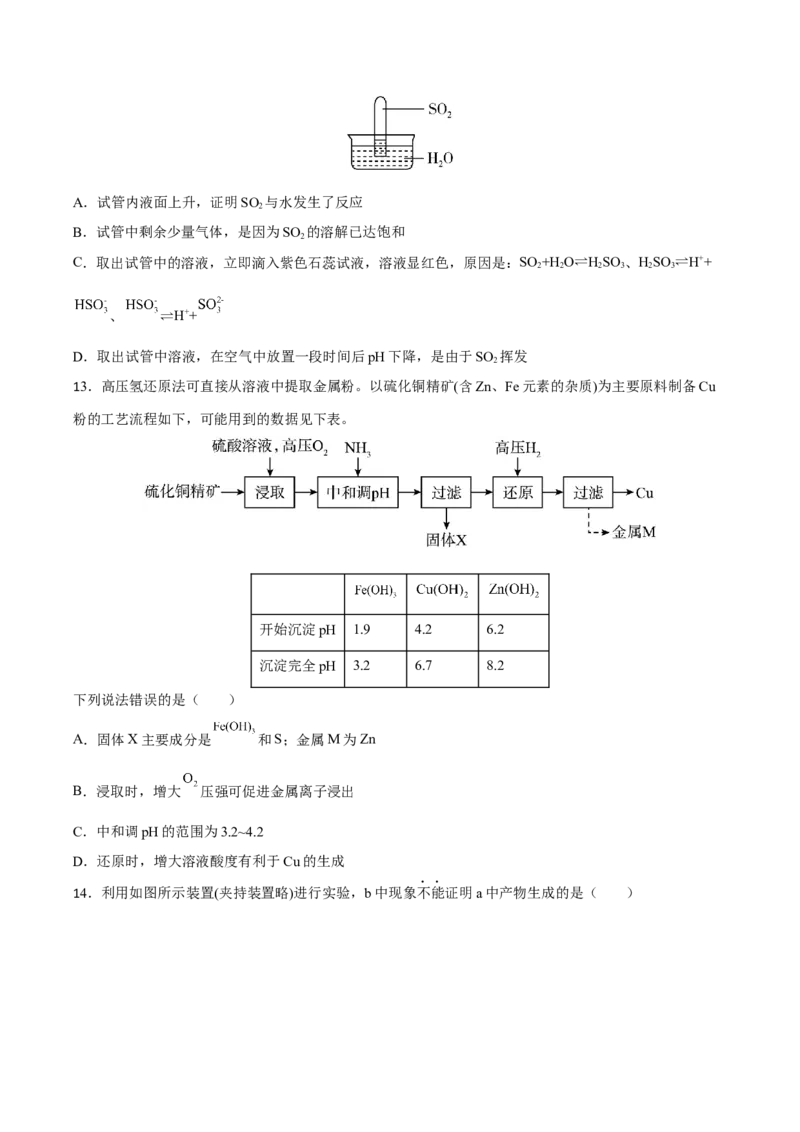
13.高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu
粉的工艺流程如下,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是( )
A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
14.利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是( )a中反应 b中检测试剂及现象
A 浓 分解生成 淀粉 溶液变蓝
B 与浓 生成 品红溶液褪色
C 浓 与 溶液生成 酚酞溶液变红
D 与 乙醇溶液生成丙烯 溴水褪色
A.A B.B C.C D.D
15.关于反应 ,达到平衡后,下列说法不正确的是(
)
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明
上述反应存在限度
16.下列说法不正确的是( )
A.镁合金密度较小、强度较大,可用于制造飞机部件
B.还原铁粉可用作食品干燥剂
C.氯气、臭氧、二氧化氯都可用于饮用水的消毒
D.油脂是热值最高的营养物质
17.化学与生活、科技、社会发展息息相关。下列有关说法错误的是( )
A.德尔塔(Delta),是新冠病毒变异毒株,传播性更强,其成分含有蛋白质
B.中芯国际是我国生产芯片的龙头企业,所生产芯片的主要成分是二氧化硅C.市面上的防晒衣通常采用聚酯纤维材料制作。忌长期用肥皂或碱性较强的液体洗涤
D.“天和”核心舱电推进系统中的霍尔推力器腔体,使用的氮化硼陶瓷基复合材料属于无机非金属材料
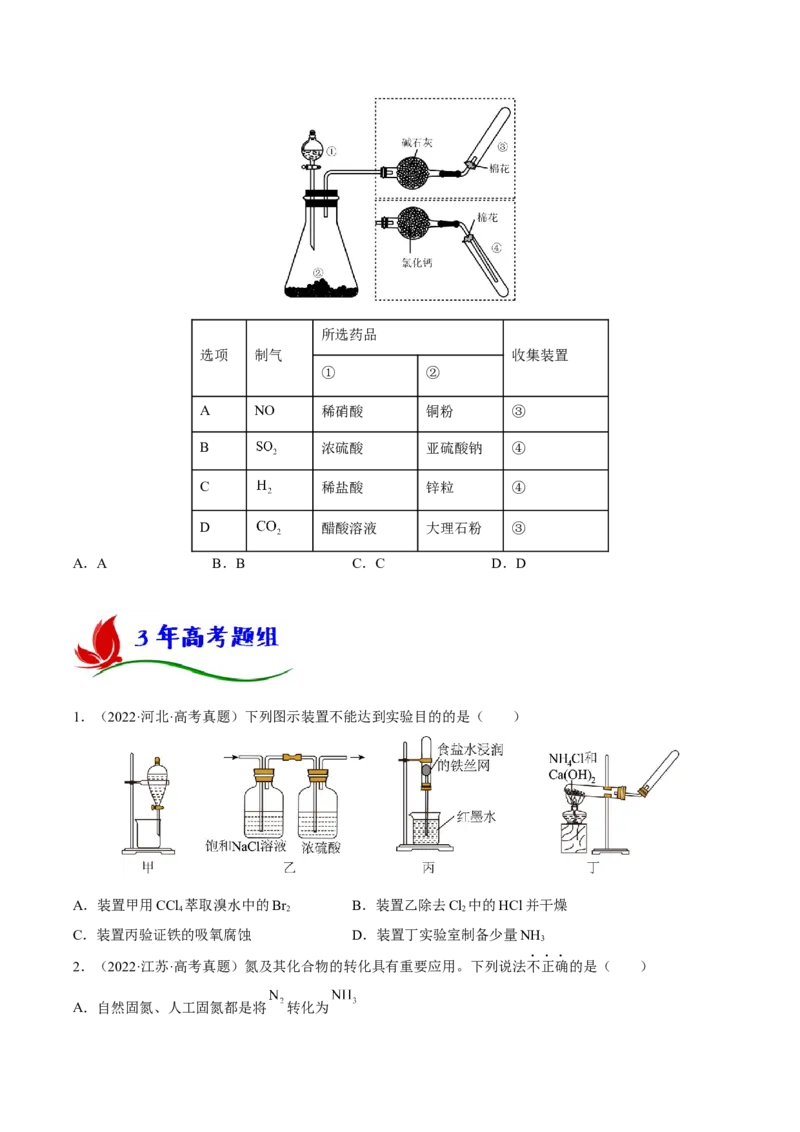
18.M是一种可溶性结晶水合物,为了确定M的组成,取少量M溶于水配成容液进行如下实验:
下列有关M的推断正确的是( )
A.由实验(1)(2)的现象知,M含
B.由实验(3)(4)的现象知,该气体显碱性
C.由实验(6)的现象知,白色沉淀可能是
D.由上述实验推知,M可能是
19.珍贵文物蕴含着璀璨文化和深远历史,记录着人类文明和社会进步。下列珍稀文物中主要由天然有机
高分子材料制造的是( )
选
A B C D
项
文
物
名
唐代纸绢画《五牛图》 西汉玉器皇后之玺 隋代瓷枕定窑孩儿枕 商州太阳鸟金饰
称
A.A B.B C.C D.D
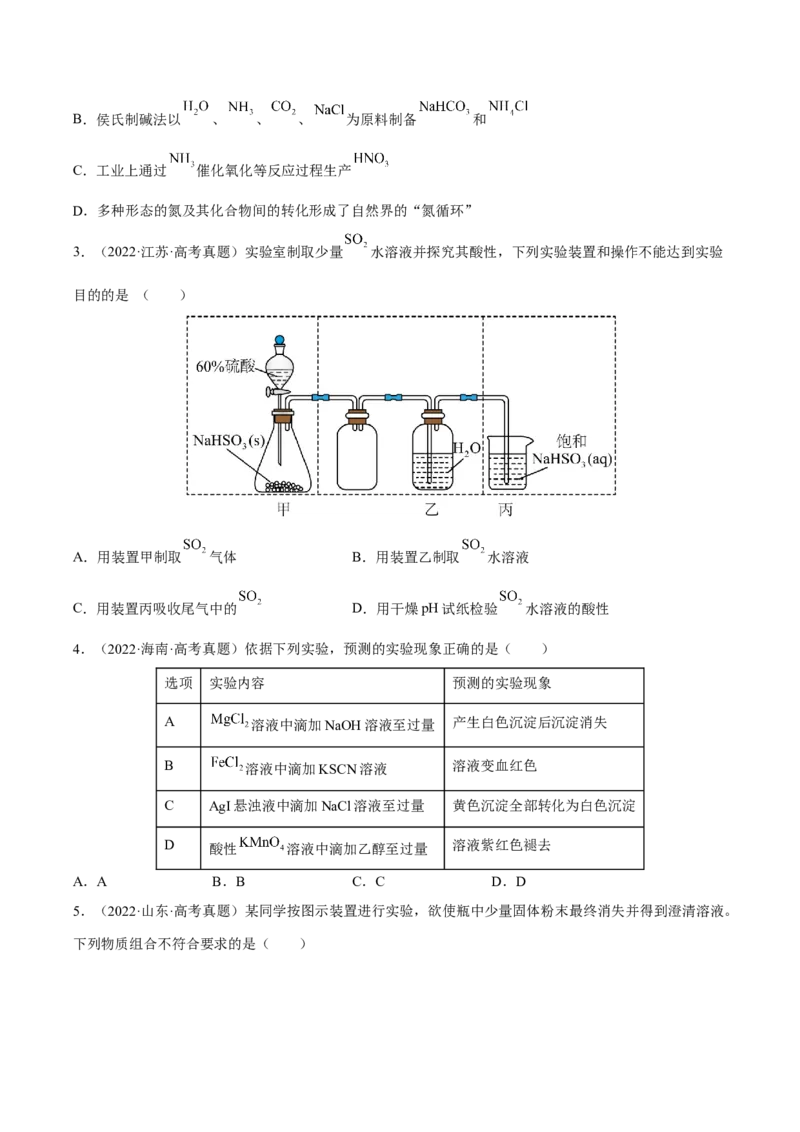
20.下列有关制取气体的设计方案正确的是(图中的棉花已被能够吸收尾气的液体浸湿)所选药品
选项 制气 收集装置
① ②
A NO 稀硝酸 铜粉 ③
B 浓硫酸 亚硫酸钠 ④
C 稀盐酸 锌粒 ④
D 醋酸溶液 大理石粉 ③
A.A B.B C.C D.D
1.(2022·河北·高考真题)下列图示装置不能达到实验目的的是( )
A.装置甲用CCl 萃取溴水中的Br B.装置乙除去Cl 中的HCl并干燥
4 2 2
C.装置丙验证铁的吸氧腐蚀 D.装置丁实验室制备少量NH
3
2.(2022·江苏·高考真题)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将 转化为B.侯氏制碱法以 、 、 、 为原料制备 和
C.工业上通过 催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
3.(2022·江苏·高考真题)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验
目的的是 ( )
A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
4.(2022·海南·高考真题)依据下列实验,预测的实验现象正确的是( )
选项 实验内容 预测的实验现象
A 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
B 溶液中滴加KSCN溶液 溶液变血红色
C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性 溶液中滴加乙醇至过量 溶液紫红色褪去
A.A B.B C.C D.D
5.(2022·山东·高考真题)某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。
下列物质组合不符合要求的是( )气体 液体 固体粉末
A 饱和 溶液
B 溶液
C
溶液
D
A.A B.B C.C D.D
6.(2021·重庆·高考真题)25°时, 下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0 mol·L-1氯化钡溶液中: Mg2+、K+、Br-、
B.1.0 mol·L-1硫酸中: A13+、 Na+、Cl-、
C.pH=1l 的氨水中: Fe2+、 Na+、 、ClO-
D.pH=1的硝酸中: Fe3+、K+、I-、
7.(2021·江苏·高考真题)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产
2 3
HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反
3 3 2 2
应生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO 和
2 2 2 x
水体中过量的NH 、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为
N,也可将水体中的NO 转化为N。在指定条件下,下列选项所示的物质间转化能实现的是( )
2 2
A.NO(g) HNO(aq)
3B.稀HNO(aq) NO (g)
3 2
C.NO(g) N(g)
2
D.NO (aq) N(g)
2
8.(2021·江苏·高考真题)下列有关物质的性质与用途不具有对应关系的是( )
A.铁粉能与O 反应,可用作食品保存的吸氧剂
2
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C.FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D.聚合硫酸铁能水解并形成胶体,可用于净水
9.(2021·辽宁·高考真题)下列说法正确的是( )
A. (标准状况)与水充分反应转移 电子
B. 和 均可通过化合反应得到
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D. 与 溶液反应:
10.(2021·辽宁·高考真题)含S元素的某钠盐a能发生如图转化。下列说法错误的是( )
A.a可能为正盐,也可能为酸式盐 B.c为不溶于盐酸的白色沉淀
C.d为含极性键的非极性分子 D.反应②中还可能生成淡黄色沉淀