文档内容
专题四 氧化还原反应
必备知识 解读
1
必备知识点
氧化还原反应的基本概念
一.记住基础
失去电子、化合价升高、被氧化、是还原剂
得到电子、化合价降低、被还原、是氧化剂
掌握一个规律:化合价升降必相等,得失守恒律
转移电子数=(高价-低价)×化合价变化的原子数
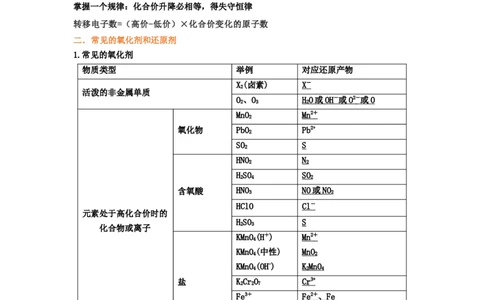
二.常见的氧化剂和还原剂
1.常见的氧化剂
物质类型 举例 对应还原产物
X(卤素) X -
2
活泼的非金属单质
O、O H O 或 O H - 或 O 2 - 或 O
2 3 2
MnO M n 2 +
2
氧化物 PbO Pb2+
2
SO S
2
HNO N
2 2
HSO SO
2 4 2
含氧酸 HNO N O 或 N O
3 2
HClO C l -
元素处于高化合价时的
HSO S
2 3
化合物或离子
KMnO(H+) M n 2 +
4
KMnO(中性) M n O
4 2
KMnO(OH-) K M n O
4 2 4
盐 KCrO C r 3 +
2 2 7
Fe3+ F e 2 + 、 F e
NaClO C l - 或 C l
2
ClO- C l - 或 C l
3 2
过氧化物 NaO、HO H O 或 O H -
2 2 2 2 2
2.常见的还原剂
物质类型 举例 对应氧化产物
活泼的金属单质 Na、Fe、Al Na+、Fe2+或Fe3+、Al3+
某些非金属单质 H、C、S H+或HO、
2 2CO或CO、SO
2 2
CO CO
2
氧化物
SO
2
NH N 或 N O
3 2
氢化物
HS S 或 S O 或
2 2
变价元素中低价态 SO SO
化合物或离子 NO- NO-
2 3
离子
Fe2+ F e 3 +
I-
FeS
硫化物 F e 3 + 和 S 或 S O
2
FeS
2
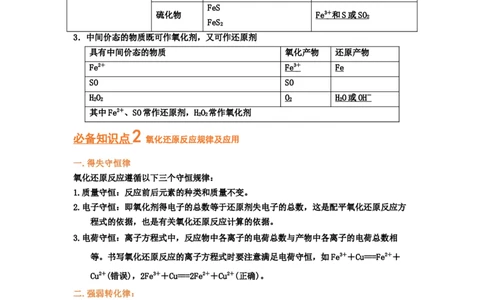
3.中间价态的物质既可作氧化剂,又可作还原剂
具有中间价态的物质 氧化产物 还原产物
Fe2+ F e 3 + Fe
SO SO
HO O H O 或 O H -
2 2 2 2
其中Fe2+、SO常作还原剂,HO 常作氧化剂
2 2
2
必备知识点
氧化还原反应规律及应用
一.得失守恒律
氧化还原反应遵循以下三个守恒规律:
1.质量守恒:反应前后元素的种类和质量不变。
2.电子守恒:即氧化剂得电子的总数等于还原剂失电子的总数,这是配平氧化还原反应方
程式的依据,也是有关氧化还原反应计算的依据。
3.电荷守恒:离子方程式中,反应物中各离子的电荷总数与产物中各离子的电荷总数相
等。书写氧化还原反应的离子方程式时要注意满足电荷守恒,如Fe3++Cu===Fe2++
Cu2+(错误),2Fe3++Cu===2Fe2++Cu2+(正确)。
二.强弱转化律:
运用这条规律,要弄清谁能氧化谁:强氧化剂和强还原剂发生氧化还原反应;
也要弄清产物是什么:强氧化剂转化为弱还原剂,强还原剂转化为弱氧化剂;
也就是说氧化产物和还原产物是弱还原剂和弱氧化剂。
三. 先强后弱律:
多种还原剂(氧化剂)与同一氧化剂(还原剂)反应,强还原剂(氧化剂)先反应,弱
还原剂(氧化剂)后反应,
四.价态归中(歧化)律:归中反应规律思维模型:同元素高价氧化低价,价态向中靠不相交
歧化反应规律思维模型:“中间价―→高价+低价”。
应考能力 解 密
一、能正确写出氧化还原反应方程式,并写出离子反应方程式:
1. 判断产物:
(1)要知道:哪些物质之间能发生氧化还原反应,哪些物质之间不能反应,谁能氧化谁,
谁能还原谁。要能比较氧化性、还原性的强弱。
(2)要知道常见氧化剂被还原,还原产物是什么,常见还原剂被氧化,氧化产物是什么。
预测氧化还原反应的主要产物
掌握一个规律:强强反应律:强氧化剂和强还原剂发生氧化还原反应。
常见氧化剂强弱顺序: KMnO >HCIO>CI >H O > HNO >浓H SO >Fe3+>I >S
4 2 2 2 3 2 4 2
还原产物的还原性顺序:Mn2+ < Cl- < Cl- < HO < NO NO < SO < Fe2+ < I < S2-
2 2 2
常见还原剂强弱顺序:S2->SO (SO 2-)>I->Fe2+>Br->CI-
2 3
氧化产物氧化性顺序S < SO 2- < I < Fe3+
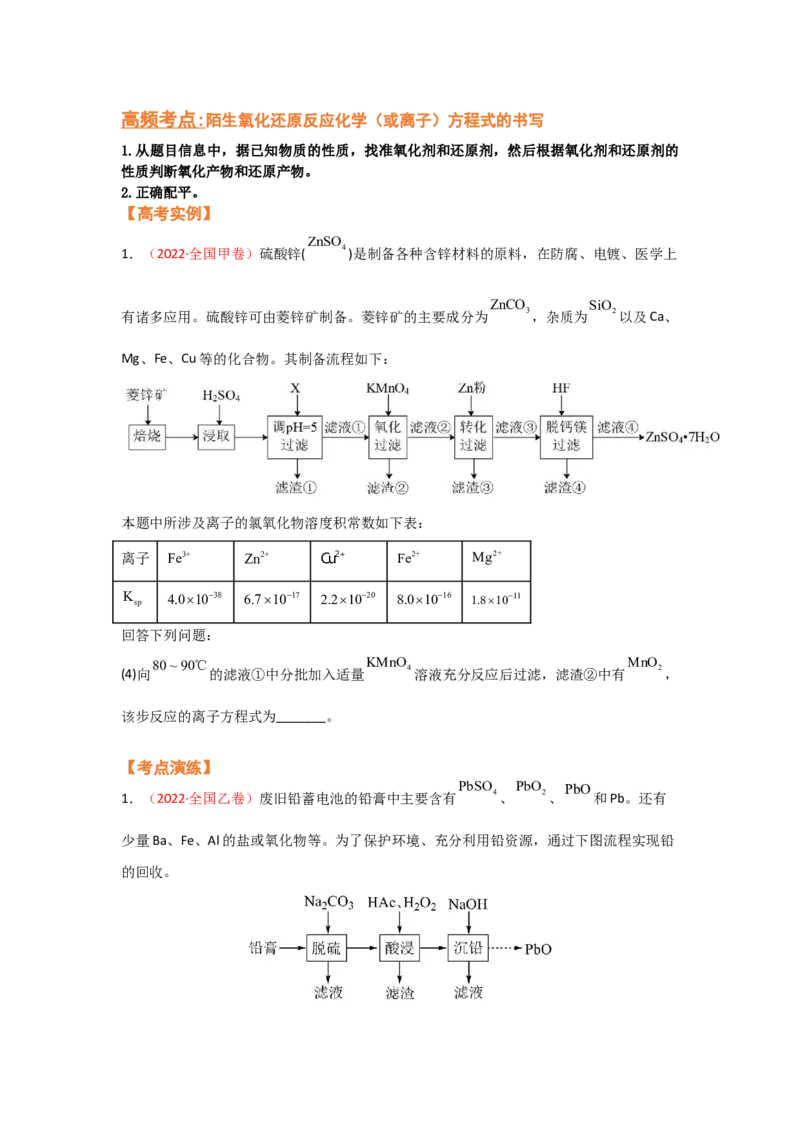
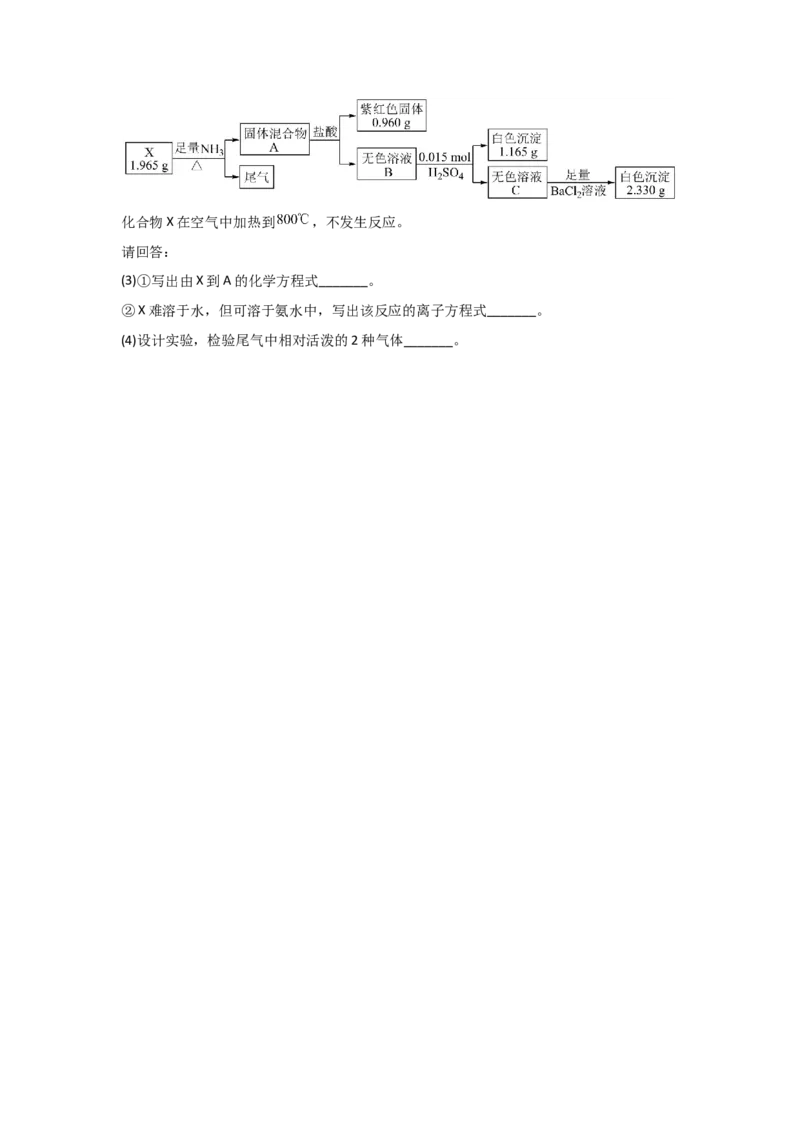
SO (SO 2-)>I->Fe2+>Br->CI- 4 2 3 HCIO能氧化的顺序::S2->SO (SO 2-)>I->Fe2+>Br->CI- 2 3 CI 能氧化的顺序::S2->SO (SO 2-)>I->Fe2+>Br- 2 2 3 H O 能氧化的顺序::S2->SO (SO 2-)>I->Fe2+ 2 2 2 3 HNO 和浓H SO 能氧化的顺序::S2->SO (SO 2-)>I->Fe2+>Br- 3 2 4 2 3 Fe3+能氧化的顺序::S2->SO (SO 2-)>I- 2 3 2.配平氧化还原反应 (1)利用氧化剂,还原剂电子得失必相等,来确定氧化剂,还原剂,氧化产物,还原 产物四种物质中其中两种物质的系数。 (2)利用观察法两边对应法配平其它物质的系数,先看氧化剂,还原剂,氧化产物,还 原产物四种物质中的各种元素或酸根 是否对应平恒 ,然后平衡氢元素,最终是氧 平衡。 (3)如果是离子方程式,第一步之后,先电荷守恒,以确定H+或OH-的系数,再定水的 系数。 (4)根据平恒的需要,在两边可加水,酸,碱。 3.配平的几种常用方法: (1). 正向配平法归中反应,一般采用正向配平法。先计算1mol氧化剂得amol电子,再计算1mol还原剂失 bmol电子,以硧定氧化剂和还原剂的系数。 = ,最简整数氧化剂系数的为b,还原剂 的系数为b。 如:_____KMnO +___SO ___+__H O==__H SO +K SO ___MnSO 4 2 2 2 4 2 4 4 (2) 逆向配平法 歧化反应和分解反应,一般采用逆向配平法:先计算得到1mol氧化产物失去Cmol电子, 再计算得到1mol还原产物得到Dmol电子,以硧定氧化产物的系数为D,还原产物的系 数为C。 例如:配平下列反应:1_______(NH)SO ===== SO+____N+____NH+____HO 4 2 4 ________ 2 2 3 2 2._____Cl+____KOH=====___KCl+_____KClO+____HO 2 3 2 (3)左右配平法: 部分被氧化或部分被还原的反应,要先定氧化剂和氧化产物 的系数,或先定还原剂和还 原产物 的系数。同样要计算:1mol 氧化剂 ( 还原剂 ) 得(失)多少mol电子,和得 到1mol氧化产物(还原产物 )失去(得到)多少电子,以确定 氧化剂 ( 还原剂 ) 和氧化产物 ( 还原产物 ) 的系数。 例如:___KMnO +___HCl----___MnCl +__KCl+____Cl ↑+___H O 4 2 2 2 ___FeS+___HNO ———____Fe (SO ) +____Fe(NO ) +____NO+____H O 3 2 4 3 3 3 2 (4). 平均标价法 在有机物参与的氧化还原反应化学方程式的配平中,一般有机物中的H显+1价,O显-2 价,根据物质中元素化合价代数和为零的原则,确定碳元素的平均价态,然后进行配 平。 例:配平下列反应: ___CH O__KCrO+___HSO KSO+___Cr(SO)+___CO↑+___HO 6 12 6 2 2 7 2 4 _____ 2 4 2 4 3 2 2 首先对碳元素平均标价并确定有元素化合价升降的物质的化学计量数: ____CH O+______KCrO+__HSO KSO+___Cr(SO)+___CO↑+___HO 6 12 6 2 2 7 2 4 _____ 2 4 2 4 3 2 2 ↑4×6 =24 ↓3×2=6 再观察配平得: CH O+4KCrO+16HSO 4KSO+4Cr(SO)+6CO↑+22HO 6 12 6 2 2 7 2 4 2 4 2 4 3 2 2(5)令价法: 将氧化剂或者是还原剂中的所有元素化合价都令为零价,升高了几价就加几,降低了几价 就减几,然后计算总的代数和。 例:___FeC+___HNO===== ___Fe(NO)+____CO+___NO+___HO 3 3 3 3 2 2 将反应前的Fe元素和C元素的化合价都为令为0价,反应后仍是+3、+4.一个FeC共升了 3 13价,生成一个NO共降低了3价,这样再用两边对应的方法,就可以配平了。 二、能用氧化还原反应的方程式进行计算 1.据化学反应式中的各物质的量与电子转移数关系进行计算 例如: 通入到100ml0.5mol/LFeI 溶液中,通入 的过程中,若氧化产物只有一种, 2 反应的化学方程式为_______;若反应物用量比 时,氧化产物为 _______;通入 标准状况下至少是_______L,转移电子数是_______个;当 ,单质碘的收率会降低,原因是_______。 2.氧化剂、还原剂、氧化产物、还原产物的物质的量之比 例如: 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少 为_______ ,氧化产物、还原产物的物质的量之比________; 在 溶液中可发 生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水 蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是_______。 高考实例剖析 高考怎么考《氧化还原反应》,根据高考指挥棒来学习《氧化还原反应》高频考点 :陌生氧化还原反应化学(或离子)方程式的书写 1.从题目信息中,据已知物质的性质,找准氧化剂和还原剂,然后根据氧化剂和还原剂的 性质判断氧化产物和还原产物。 2.正确配平。 【高考实例】 ZnSO 1.(2022·全国甲卷)硫酸锌( 4 )是制备各种含锌材料的原料,在防腐、电镀、医学上 ZnCO SiO 有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 3,杂质为 2以及Ca、 Mg、Fe、Cu等的化合物。其制备流程如下: 本题中所涉及离子的氯氧化物溶度积常数如下表: 离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+ K sp 4.01038 6.71017 2.21020 8.01016 1.81011 回答下列问题: 80~90℃ KMnO MnO (4)向 的滤液①中分批加入适量 4溶液充分反应后过滤,滤渣②中有 2, 该步反应的离子方程式为_______。 【考点演练】 PbSO PbO PbO 1.(2022·全国乙卷)废旧铅蓄电池的铅膏中主要含有 4、 2、 和Pb。还有 少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅 的回收。一些难溶电解质的溶度积常数如下表: 难溶电解质 PbSO PbCO BaSO BaCO 4 3 4 3 K 2.5108 7.41014 1.11010 2.6109 sp 一定条件下,一些金属氢氧化物沉淀时的pH如下表: 金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH) 3 2 3 2 开始沉淀的pH 2.3 6.8 3.5 7.2 完全沉淀的pH 3.2 8.3 4.6 9.1 回答下列问题: HAc H O (3)在“酸浸”中,除加入醋酸( ),还要加入 2 2。 H O (ⅰ)能被 2 2氧化的离子是________; H O Pb(Ac) (ⅱ) 2 2促进了金属Pb在醋酸中转化为 2,其化学方程式为________; 2.(2021·全国高考试题)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等 方面。回答下列问题: (1) 的一种制备方法如下图所示: ①加入 粉进行转化反应的离子方程式为_______,生成的沉淀与硝酸反应,生成_______ 后可循环使用。 ②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;若反应物用量 比 时,氧化产物为_______;当 ,单质碘 的收率会降低,原因是_______。(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化 物;再向混合溶液中加入 溶液,反应得到 ,上述制备 的总反应的离子方程 式为_______。 (3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为 _______ 。 在 溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量 的 原因是_______。 3.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下: 2 回答下列问题: (1)NaClO 中Cl的化合价为_______。 2 (2)写出“反应”步骤中生成ClO 的化学方程式_______。 2 (3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 Mg2+和Ca2+,要加入的 试剂分别为________、________。“电解”中阴极反应的主要产物是______。 (4)“尾气吸收”是吸收“电解”过程排出的少量ClO。此吸收反应中,氧化剂与还 2 原剂的物质的量之比为________,该反应的离子方程式_________。 (5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂 的氧化能力相当于多少克Cl 的氧化能力。NaClO 的有效氯含量为____。(计算结 2 2 果保留两位小数) 4.(2022·浙江卷)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:化合物X在空气中加热到 ,不发生反应。 请回答: (3)①写出由X到A的化学方程式_______。 ②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。 (4)设计实验,检验尾气中相对活泼的2种气体_______。
SO (SO 2-)>I->Fe2+>Br->CI- 4 2 3 HCIO能氧化的顺序::S2->SO (SO 2-)>I->Fe2+>Br->CI- 2 3 CI 能氧化的顺序::S2->SO (SO 2-)>I->Fe2+>Br- 2 2 3 H O 能氧化的顺序::S2->SO (SO 2-)>I->Fe2+ 2 2 2 3 HNO 和浓H SO 能氧化的顺序::S2->SO (SO 2-)>I->Fe2+>Br- 3 2 4 2 3 Fe3+能氧化的顺序::S2->SO (SO 2-)>I- 2 3 2.配平氧化还原反应 (1)利用氧化剂,还原剂电子得失必相等,来确定氧化剂,还原剂,氧化产物,还原 产物四种物质中其中两种物质的系数。 (2)利用观察法两边对应法配平其它物质的系数,先看氧化剂,还原剂,氧化产物,还 原产物四种物质中的各种元素或酸根 是否对应平恒 ,然后平衡氢元素,最终是氧 平衡。 (3)如果是离子方程式,第一步之后,先电荷守恒,以确定H+或OH-的系数,再定水的 系数。 (4)根据平恒的需要,在两边可加水,酸,碱。 3.配平的几种常用方法: (1). 正向配平法归中反应,一般采用正向配平法。先计算1mol氧化剂得amol电子,再计算1mol还原剂失 bmol电子,以硧定氧化剂和还原剂的系数。 = ,最简整数氧化剂系数的为b,还原剂 的系数为b。 如:_____KMnO +___SO ___+__H O==__H SO +K SO ___MnSO 4 2 2 2 4 2 4 4 (2) 逆向配平法 歧化反应和分解反应,一般采用逆向配平法:先计算得到1mol氧化产物失去Cmol电子, 再计算得到1mol还原产物得到Dmol电子,以硧定氧化产物的系数为D,还原产物的系 数为C。 例如:配平下列反应:1_______(NH)SO ===== SO+____N+____NH+____HO 4 2 4 ________ 2 2 3 2 2._____Cl+____KOH=====___KCl+_____KClO+____HO 2 3 2 (3)左右配平法: 部分被氧化或部分被还原的反应,要先定氧化剂和氧化产物 的系数,或先定还原剂和还 原产物 的系数。同样要计算:1mol 氧化剂 ( 还原剂 ) 得(失)多少mol电子,和得 到1mol氧化产物(还原产物 )失去(得到)多少电子,以确定 氧化剂 ( 还原剂 ) 和氧化产物 ( 还原产物 ) 的系数。 例如:___KMnO +___HCl----___MnCl +__KCl+____Cl ↑+___H O 4 2 2 2 ___FeS+___HNO ———____Fe (SO ) +____Fe(NO ) +____NO+____H O 3 2 4 3 3 3 2 (4). 平均标价法 在有机物参与的氧化还原反应化学方程式的配平中,一般有机物中的H显+1价,O显-2 价,根据物质中元素化合价代数和为零的原则,确定碳元素的平均价态,然后进行配 平。 例:配平下列反应: ___CH O__KCrO+___HSO KSO+___Cr(SO)+___CO↑+___HO 6 12 6 2 2 7 2 4 _____ 2 4 2 4 3 2 2 首先对碳元素平均标价并确定有元素化合价升降的物质的化学计量数: ____CH O+______KCrO+__HSO KSO+___Cr(SO)+___CO↑+___HO 6 12 6 2 2 7 2 4 _____ 2 4 2 4 3 2 2 ↑4×6 =24 ↓3×2=6 再观察配平得: CH O+4KCrO+16HSO 4KSO+4Cr(SO)+6CO↑+22HO 6 12 6 2 2 7 2 4 2 4 2 4 3 2 2(5)令价法: 将氧化剂或者是还原剂中的所有元素化合价都令为零价,升高了几价就加几,降低了几价 就减几,然后计算总的代数和。 例:___FeC+___HNO===== ___Fe(NO)+____CO+___NO+___HO 3 3 3 3 2 2 将反应前的Fe元素和C元素的化合价都为令为0价,反应后仍是+3、+4.一个FeC共升了 3 13价,生成一个NO共降低了3价,这样再用两边对应的方法,就可以配平了。 二、能用氧化还原反应的方程式进行计算 1.据化学反应式中的各物质的量与电子转移数关系进行计算 例如: 通入到100ml0.5mol/LFeI 溶液中,通入 的过程中,若氧化产物只有一种, 2 反应的化学方程式为_______;若反应物用量比 时,氧化产物为 _______;通入 标准状况下至少是_______L,转移电子数是_______个;当 ,单质碘的收率会降低,原因是_______。 2.氧化剂、还原剂、氧化产物、还原产物的物质的量之比 例如: 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少 为_______ ,氧化产物、还原产物的物质的量之比________; 在 溶液中可发 生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水 蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是_______。 高考实例剖析 高考怎么考《氧化还原反应》,根据高考指挥棒来学习《氧化还原反应》高频考点 :陌生氧化还原反应化学(或离子)方程式的书写 1.从题目信息中,据已知物质的性质,找准氧化剂和还原剂,然后根据氧化剂和还原剂的 性质判断氧化产物和还原产物。 2.正确配平。 【高考实例】 ZnSO 1.(2022·全国甲卷)硫酸锌( 4 )是制备各种含锌材料的原料,在防腐、电镀、医学上 ZnCO SiO 有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 3,杂质为 2以及Ca、 Mg、Fe、Cu等的化合物。其制备流程如下: 本题中所涉及离子的氯氧化物溶度积常数如下表: 离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+ K sp 4.01038 6.71017 2.21020 8.01016 1.81011 回答下列问题: 80~90℃ KMnO MnO (4)向 的滤液①中分批加入适量 4溶液充分反应后过滤,滤渣②中有 2, 该步反应的离子方程式为_______。 【考点演练】 PbSO PbO PbO 1.(2022·全国乙卷)废旧铅蓄电池的铅膏中主要含有 4、 2、 和Pb。还有 少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅 的回收。一些难溶电解质的溶度积常数如下表: 难溶电解质 PbSO PbCO BaSO BaCO 4 3 4 3 K 2.5108 7.41014 1.11010 2.6109 sp 一定条件下,一些金属氢氧化物沉淀时的pH如下表: 金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH) 3 2 3 2 开始沉淀的pH 2.3 6.8 3.5 7.2 完全沉淀的pH 3.2 8.3 4.6 9.1 回答下列问题: HAc H O (3)在“酸浸”中,除加入醋酸( ),还要加入 2 2。 H O (ⅰ)能被 2 2氧化的离子是________; H O Pb(Ac) (ⅱ) 2 2促进了金属Pb在醋酸中转化为 2,其化学方程式为________; 2.(2021·全国高考试题)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等 方面。回答下列问题: (1) 的一种制备方法如下图所示: ①加入 粉进行转化反应的离子方程式为_______,生成的沉淀与硝酸反应,生成_______ 后可循环使用。 ②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;若反应物用量 比 时,氧化产物为_______;当 ,单质碘 的收率会降低,原因是_______。(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化 物;再向混合溶液中加入 溶液,反应得到 ,上述制备 的总反应的离子方程 式为_______。 (3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为 _______ 。 在 溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量 的 原因是_______。 3.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下: 2 回答下列问题: (1)NaClO 中Cl的化合价为_______。 2 (2)写出“反应”步骤中生成ClO 的化学方程式_______。 2 (3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 Mg2+和Ca2+,要加入的 试剂分别为________、________。“电解”中阴极反应的主要产物是______。 (4)“尾气吸收”是吸收“电解”过程排出的少量ClO。此吸收反应中,氧化剂与还 2 原剂的物质的量之比为________,该反应的离子方程式_________。 (5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂 的氧化能力相当于多少克Cl 的氧化能力。NaClO 的有效氯含量为____。(计算结 2 2 果保留两位小数) 4.(2022·浙江卷)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:化合物X在空气中加热到 ,不发生反应。 请回答: (3)①写出由X到A的化学方程式_______。 ②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。 (4)设计实验,检验尾气中相对活泼的2种气体_______。