文档内容
专题突破卷 02 化学物质及其变化
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.中华文化源远流长,博大精深。下列古诗词中的物质变化只涉及物理变化的是
A.野火烧不尽,春风吹又生 B.千锤万凿出深山,烈火焚烧若等闲
C.爆竹声中一岁除,春风送暖入屠苏 D.夜来风雨声,花落知多少
【答案】D
【详解】A.野火烧不尽,春风吹又生,包含物质燃烧的反应,为化学变化,A错误;
B.千锤万凿出深山,烈火焚烧若等闲中烈火焚烧碳酸钙分解,发生了化学反应,B错误;
C.爆竹声中一岁除,春风送暖入屠苏中爆竹爆炸发生了化学反应,B错误;
D.夜来风雨声,花落知多少是风雨把花瓣打落,过程中无新物质生成,为物理变化,D正确;
故答案为:D。
2.下列关于胶体的说法中正确的是
A.胶体与溶液有明显不同的外观特征
B.胶体不稳定,静置后易产生沉淀
C.将Fe(OH) 胶体进行过滤,所得到的滤液与原来胶体的组成不同
3
D.豆浆是胶体,因为豆浆中的分散质粒子直径在1~100 nm之间
【答案】D
【详解】A.胶体与溶液的主要特征都是均一、透明、稳定的,A选项错误;
B.胶体稳定,不易产生沉淀,B选项错误;
C.胶体的分散质粒子可以透过滤纸,所以将Fe(OH) 胶体进行过滤时,胶体的所有组成都会透过滤纸,滤
3
液与胶体的组成一致,C选项错误;
D.胶体区别于其他分散系的本质在于其分散质粒子直径在1nm~100 nm之间,D选项正确;
答案选D。
3.下列物质的分类采用树状分类法的是
A.铁是单质又是导体
B.纯净物可分为有机物和无机物
C.氯化钠是钠盐又是氯化物
D.氢氧化钙是纯净物又是化合物,属于碱
【答案】B【详解】A.同时用两个标准对铁进行分类,属于交叉分类法,选项A错误;
B.用一个标准进行分类,为树状分类法,选项B正确;
C.从阴阳离子两个角度进行分类,为交叉分类法,选项C错误;
D.氢氧化钙从多个角度进行分类,为交叉分类法,选项D错误;
答案选B。
4.催雨剂的主要成分可以是干冰、液氮、碘化银(AgI)等,它们分别属于氧化物、单质、盐,下列物质与
上述三种物质的类别完全不同的是
A. B. C. D.
【答案】D
【详解】A. 属于单质,A不符合题意;
B. 属于盐,B不符合题意;
C. 属于氧化物,C不符合题意;
D. 属于酸,与题给三种物质的类别完全不同,D符合题意;
故选D。
5.下列属于物理变化的是
①石油的分馏 ②煤的干馏 ③石油的裂化 ④铝热反应 ⑤由乙烯制备聚乙烯 ⑥将氧气转化为臭氧
⑦乙烯催熟果实 ⑧将苯加入溴水中 ⑨海水蒸馏制取淡水
A.①②③④ B.①②⑤⑦ C.①⑧⑨ D.①②⑥⑨
【答案】C
【分析】有新物质生成的变化为化学变化,没有新物质生成的变化为物理变化,化学变化与物理变化的本
质区别在于有无新物质生成,据此抓住化学变化和物理变化的区别结合事实进行分析判断即可。
【详解】①石油的分馏是利用物质沸点不同将各馏分分离开来,没有新物质生成,为物理变化;
②煤的干馏是指将煤隔绝空气加强热使之分解的过程,有新物质生成,属于化学变化;
③石油的裂化是在一定的条件下,将相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较
低的烃的过程,有新物质生成,属于化学变化;
④铝热反应为铝与某些金属氧化物高温下发生的置换反应,有新物质生成,属于化学变化;
⑤由乙烯制备聚乙烯,有新物质聚乙烯生成,属于化学变化;
⑥氧气转变为臭氧,有新物质臭氧生成,属于化学变化;⑦乙烯催熟果实,有新物质生成,属于化学变化;
⑧将苯加入溴水中,苯将溴从溴水中萃取出来,没有新物质生成,为物理变化;
⑨海水蒸馏制取淡水,只是分离混合物,没有新物质生成,为物理变化;
综上分析,属于物理变化的有①⑧⑨,答案选C。
6.分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
A.根据SiO 是酸性氧化物,判断其可与NaOH溶液反应
2
B.金属氧化物一定是碱性氧化物
C.根据丁达尔现象将分散系分为胶体、溶液和浊液
D.根据酸分子中H原子个数分为一元酸、二元酸等
【答案】A
【详解】A.酸性氧化物是指能与碱反应只生成盐和水的氧化物,所以可根据SiO 是酸性氧化物,判断其
2
可与NaOH溶液反应,故A正确;
B.碱性氧化物指能与酸反应只生成盐和水的氧化物,金属氧化物不一定都是碱性氧化物,如过氧化钠,
故B错误;
C.分散系根据粒子直径大小可分为胶体、溶液和浊液,而不是丁达尔现象,故C错误;
D.一元酸、二元酸是根据酸分子中能电离出的H离子个数区分的,而不是含有的H原子个数,故D错
误;
故答案选A。
7.如图是制备Fe(OH) 胶体的示意图,下列关于制备过程的叙述正确的是
3
A.将FeCl 稀溶液滴入温水中即可
3
B.将饱和FeCl 溶液滴入NaOH溶液中
3
C.将饱和FeCl 溶液滴入加热沸腾的水中
3
D.将浓氨水滴入沸腾的饱和FeCl 溶液中
3
【答案】C
【详解】A.将FeCl 稀溶液滴入温水中,由于水解程度小,不能制备Fe(OH) 胶体,故A错误;
3 3B.将饱和FeCl 溶液滴入NaOH溶液中,发生化学反应,生成Fe(OH) 沉淀,即Fe3++3OH-=Fe(OH) ↓,故
3 3 3
B错误;
C.将饱和FeCl 溶液滴入沸水中,并继续加热煮沸得到红褐色液体即可,是实验室制备胶体的方法,即
3
Fe3++3H O Fe(OH) (胶体)+3H+,故C正确;
2 3
D.将浓氨水滴入沸腾的饱和FeCl 溶液中,发生化学反应,生成Fe(OH) 沉淀,即Fe3+
3 3
+3NH·H O=Fe(OH) ↓+3 ,故D错误;
3 2 3
答案为C。
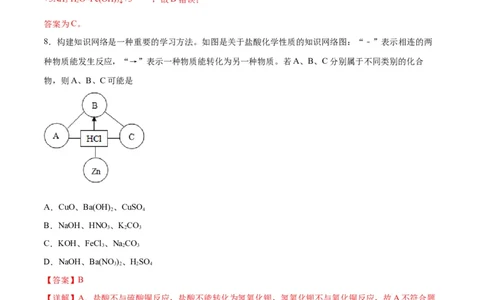
8.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“﹣”表示相连的两
种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合
物,则A、B、C可能是
A.CuO、Ba(OH) 、CuSO
2 4
B.NaOH、HNO、KCO
3 2 3
C.KOH、FeCl 、NaCO
3 2 3
D.NaOH、Ba(NO )、HSO
3 2 2 4
【答案】B
【详解】A.盐酸不与硫酸铜反应,盐酸不能转化为氢氧化钡,氢氧化钡不与氧化铜反应,故A不符合题
意;
B.盐酸和氢氧化钠、碳酸钾都能反应,和硝酸银反应生成硝酸,硝酸和氢氧化钠、碳酸钾都能反应,故
B符合题意;
C.氯化铁和碳酸钠均为盐,属于相同类别的化合物,故C不符合题意;
D.盐酸不能转化为硝酸钡,盐酸不与硫酸反应,氢氧化钠与硝酸钡不反应,故D不符合题意;
故答案:B。9.下列有关 溶液和 胶体的叙述正确的是
A.将饱和 溶液滴加到1.0 NaOH溶液中可制得 胶体
B. 胶体带正电, 溶液呈电中性
C.两种分散系的分散质具有相同的粒子直径
D.利用丁达尔效应可将两种液体区分开
【答案】D
【详解】A.将饱和FeCl 溶液滴加到1.0 mol•L-1NaOH溶液中生成氢氧化铁沉淀,而不是胶体,故A错
3
误;
B.胶体不带电,带电的是胶粒,故B错误;
C.分散系根据分散质粒子直径的不同分为溶液、胶体和浊液,即溶液、胶体和浊液的粒子直径不同,故
C错误;
D.溶液无丁达尔效应,胶体有,故当两种液体一种是胶体一种是溶液时,可以用丁达尔效应来区分,故
D正确。
答案选D。
10.下列分散系能产生“丁达尔效应”的是
A.葡萄糖溶液 B.油水 C.盐酸 D.淀粉溶液
【答案】D
【详解】A.葡萄糖溶液不是胶体,不能产生丁达尔效应,故A错误;
B.油水为浊液,不能产生丁达尔效应,故B错误;
C.盐酸为HCl的水溶液,不是胶体,不能产生丁达尔效应,故C错误;
D.淀粉溶液属于胶体,能产生丁达尔效应,故D正确;
故选:D。
11.下列表格中各项分类都正确的一组是:
纯净物 混合物 电解质 非电解质
A 生理盐水 明矾 液态KNO 蔗糖
3
B 生石灰 海水 铜 乙醇
C 胆矾 生铁 CaCO CO
3 2
D 氢氧化钠 空气 NaSO 溶液 食醋
2 4A.A B.B C.C D.D
【答案】C
【分析】电解质是指在水溶液或者熔融状态下导电的化合物。电解质常见物质是酸、碱、盐、金属氧化
物、水。非电解质常见物质是大部分有机物、非金属氧化物。
【详解】A.生理食盐水是混合物,明矾是纯净物,故A错误;
B.铜是单质既不是电解质也不是非电解质,故B错误;
C.胆矾是结晶水合物、属于纯净物,生铁是铁碳合金、属于混合物,CaCO 是盐、属于电解质,CO 水溶
3 2
液能导电但离子不是由CO 自身电离,CO 属于非电解质,各物质都符合分类,故C正确;
2 2
D.NaSO 溶液、食醋都是混合物,所以既不是电解质也不是非电解质,故D错误;
2 4
故选答案C。
12.下列关于氧化物分类的说法不正确的组合是
①金属氧化物也可以形成酸性氧化物
②非金属氧化物一定是酸性氧化物
③SiO 是酸性氧化物,硅酸是它与水反应形成的水化物
2
④碱性氧化物一定是金属氧化物
⑤Na O和NaO 均能与HO反应生成NaOH,故二者都是碱性氧化物
2 2 2 2
⑥能与酸反应生成盐和水的氧化物一定是碱性氧化物
⑦能与碱反应生成盐和水的氧化物一定是酸性氧化物
A.②③⑤⑥⑦ B.①④ C.②④⑤ D.①②④⑥⑦
【答案】A
【详解】①金属氧化物也可以形成酸性氧化物,如MnO,①正确;
2 7
②非金属氧化物不一定是酸性氧化物,如CO,②错误;
③SiO 是酸性氧化物,但不能与水反应,③错误;
2
④碱性氧化物一定是金属氧化物,④正确;
⑤Na O和NaO 均能与HO反应生成NaOH,NaO 与HO反应除生成NaOH外,还生成O,不符合碱性
2 2 2 2 2 2 2 2
氧化物的定义;⑤错误;
⑥能与酸反应生成盐和水的氧化物不一定是碱性氧化物,如Al O 是两性氧化物,⑥错误;
2 3
⑦能与碱反应生成盐和水的氧化物一定是酸性氧化物,如Al O 是两性氧化物,⑦错误;
2 3
故符合题意的是②③⑤⑥⑦,答案选A。13.下列物质之间的转化都一步能实现的是
A.
B.
C.
D.
【答案】C
【详解】A.SiO 不和水反应,不能一步反应生成HSiO,A不符合题意;
2 2 3
B.Al O 不和水反应,不能一步反应生成Al(OH) ,B不符合题意;
2 3 3
C.N 和H 反应生成NH ,NH 和O 发生催化氧化反应生成NO,NO和O 反应生成NO ,NO 和HO反
2 2 3 3 2 2 2 2 2
应生成HNO,浓HNO 和Cu反应生成NO ,均能一步实现,C符合题意;
3 3 2
D.S和O 反应只能生成SO ,S不能一步反应生成SO ,D不符合题意;
2 2 3
故选C。
14.下列说法正确的是
A.卤水点豆腐本质属于蛋白质聚沉
B.悬浊液和乳浊液的分散质均为液态
C.葡萄糖溶液和淀粉溶液都具有丁达尔效应
D.明矾可用作净水剂和消毒剂
【答案】A
【详解】A.向豆浆中加入卤水,使豆浆中的蛋白质发生聚沉,A正确;
B.悬浊液的分散质是固体小颗粒,B错误;
C.葡萄糖分子是小分子,其分子直径小于1 nm,不具备胶体颗粒大小,所以葡萄糖溶液不能产生丁达尔
效应,C错误;
D.明矾能水解生成氢氧化铝胶体,氢氧化铝胶体表面积大,具有强的吸附性,可以吸附水中悬浮的固体
小颗粒,使之形成沉淀而析出,所以可作净水剂,但该物质具有具有氧化性,因此不能作消毒剂,D错
误;
故合理选项是A。
15.图中“—”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙。下
面四组选项中,符合图示要求的是甲 乙 丙 丁
A HSO NaSO NaOH NaCl
2 4 2 4
B KCl KCO KOH HCl
2 3
C O CO CuO C
2
D Fe FeCl Zn HCl
2
A.A B.B C.C D.D
【答案】C
【详解】A.甲和乙、乙和丙、丙和丁、丁和甲均不能反应,A不选;
B.甲和乙、乙和丙、丁和甲均不能反应,B不选;
C.各反应分别是甲和乙:O+2CO 2CO,乙和丙:CO+CuO Cu+CO ,丙和丁:2CuO+C
2 2 2
2Cu+CO ↑,丁和甲:C+O CO,丁→乙:2C+O 2CO,C选;
2 2 2 2
D .Fe与FeCl 不反应,D不选。
2
选C。
二、非选择题(本题包括4小题,共55分)
16.(14分)把以下物质按要求分类: , , , , ,浑浊的河水, ,
, , , , , , , ,空气, , , ,
, 。
(1)属于单质的是 ;
(2)属于有机化合物的是 ;
(3)属于氧化物的是 ;
(4)属于酸的是 ;(5)属于碱的是 ;
(6)属于盐的是 ;
(7)属于混合物的是 。
【答案】(1)
(2)
(3)
(4)
(5)
(6)
(7)浑浊的河水、空气
【详解】(1)由同种元素组成的纯净物为单质,H、Al属于单质;
2
(2)大部分含碳元素的化合物为有机物,但CO、CO、HCO 及其盐、HCN及其盐、HSCN及其盐、
2 2 3
CaC 等和无机物结构和性质相似,不属于有机物,所以属于有机物的是CHCHOH和CH;
2 3 2 4
(3)由两种元素组成,其中一种是氧元素的化合物属于氧化物,则属于氧化物的是CaO、Fe O、CO、
2 3 2
CO;
(4)电离出来的阳离子全部是氢离子的化合物属于酸,则属于酸的是HNO、HSO 、HPO 、HCO;
3 2 4 3 4 2 3
(5)电离出来的阴离子全部是氢氧根离子的化合物属于碱,则属于碱的是Ba(OH) 、Cu(OH) 、NaOH;
2 2
(6)由金属阳离子或铵根离子跟酸根离子组成的化合物属于盐,则属于盐的是NaHSO、CuSO 、
4 4
MgCl 、MgSO ;
2 4
(7)由两种或多种物质组成的物质属于混合物,则属于混合物的是浑浊的河水、空气。
17.(12分)现有甲、乙、丙三名同学分别进行Fe(OH) 胶体的制备实验。
3
甲同学:向1 mol·L-1的氯化铁溶液中加入少量3 mol·L-1的NaOH溶液。
乙同学:向25 mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至液体呈红褐色,停止加热。
3
丙同学:向沸水中滴加饱和FeCl 溶液,为了使反应进行充分,待液体呈红褐色后继续煮沸10分钟。
3
试回答下列问题:
(1)其中操作正确的同学是 ,该反应原理的离子方程式为 。
(2)证明有Fe(OH) 胶体生成的实验操作是 ,利用了胶体的 性质。
3(3)在胶体中加入电解质溶液或带有相反电荷的胶体微粒能使胶体微粒沉淀出来。丁同学利用所制得的
Fe(OH) 胶体进行下列实验:
3
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现靠近阴极(和电源负极相连)区附
近的颜色逐渐变深,这表明Fe(OH) 胶体粒子带 (填“正”或“负”)电荷。
3
②现有橘红色的硫化锑(Sb S)胶体,装入U型管,插入石墨电极后通直流电,发现阳极附近橘红色加深,
2 3
若把硫化锑(Sb S)胶体与Fe(OH) 胶体混合,看到的现象是 。
2 3 3
【答案】(1) 乙 Fe3+ + 3H O Fe (OH) (胶体) + 3H+
2 3
(2) 用一束光通过得到的液体,从侧面观察能看到一条光亮的“通路” 丁达尔效应
(3) 正 有沉淀生成
【解析】(1)氢氧化铁胶体制备的方法为:向25 mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸
3
至液体呈红褐色,停止加热,故乙同学的操作正确;该反应原理的离子方程式为Fe3+ + 3H O Fe (OH)
2 3
(胶体) + 3H+;
(2)丁达尔效应是胶体独有的现象,证明有Fe(OH) 胶体生成的实验操作是用一束光通过得到的液体,从
3
侧面观察能看到一条光亮的“通路”;利用了胶体的丁达尔效应;
(3)①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现靠近阴极(和电源负极相连)
区附近的颜色逐渐变深,这表明Fe(OH) 胶体粒子带正电荷;②现有橘红色的硫化锑(Sb S)胶体,装入U
3 2 3
型管,插入石墨电极后通直流电,发现阳极附近橘红色加深,说明硫化锑(Sb S)胶粒带负电, 硫化锑
2 3
(Sb S)与Fe(OH) 胶体混合,看到的现象是有沉淀生成,异种电荷会发生聚沉。
2 3 3
18.(12分)下图是依据一定的分类标准,对某些物质与水反应的情况进行分类的分类图。回答下列问题:
(1)上述第一级分类标准(分成A、B组的依据)是 。
(2)A组物质中属于电解质的是 (填化学式)。
(3)B组物质中的NaO 中含有的化学键类型是 ;NO 与HO的反应中,氧化剂与还原剂的物质
2 2 2 2
的量之比为 。
(4)C组中的物质与F组中的一种单质在水中反应生成两种强酸,该反应的化学方程式为 。
(5)B组→E组反应的离子方程式为 。
【答案】 是否为氧化还原反应(或反应中是否有化合价变化、反应中是否有电子转移) CaO、
NaO 离子键、共价键 1∶2
2
【分析】C组物质的水溶液呈酸性,故C组物质为SO ,D组物质为NH 、CaO、NaO;E组物质为Na,F
2 3 2
组物质为Cl、NO 、NaO;
2 2 2 2
【详解】(1)第一级分类标准是按物质与水反应是否是氧化还原反应(或反应中是否有化合价变化、反应中
是否有电子转移);
(2)NH 、SO 本身熔融态不能导电,溶于水中本身不能电离,是非电解质;CaO、NaO的熔融态都能导
3 2 2
电,故答案为:CaO、NaO;
2
(3)Na O 中Na+与 间是离子键, 中O与O是共价键,故答案为:离子键、共价键;
2 2
(4)C组物质为SO ,F组物质为Cl、NO 、NaO,符合C组中的物质与F组中的一种单质在水中反应生成
2 2 2 2 2
两种强酸的是SO 和Cl,故反应的化学方程式为: ;
2 2
(5)E组物质为Na,则B组→E组反应的离子方程式为: 。
19.(17分)Ⅰ.现有以下物质:①NaCl溶液 ②NH ③冰醋酸(纯净的醋酸) ④铜 ⑤KSO 固体 ⑥蔗
3 2 4
糖 ⑦酒精 ⑧熔融的MgO ⑨盐酸 ⑩铁
(1)其中能导电的是 (填序号,下同);属于电解质的是 ,属于非电解质的是
。
(2)写出物质⑤溶于水的电离方程式 。
(3)写出物质⑨和物质⑩反应的化学方程式 。Ⅱ.甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,
“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO、O 作用产生的,其化学式为Cu (OH) CO,“铜
2 2 2 2 3
绿”能跟酸反应生成铜盐、CO 和HO。回答下列问题:
2 2
(4)CO 属于 氧化物。(填“酸性”或“碱性”)
2
(5)从物质分类标准看,“铜绿”属于哪类物质___________。(填选项)
A.酸 B.碱 C.盐 D.氧化物
(6)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:
反应Ⅰ: ,
反应Ⅱ: 。
①反应Ⅰ中,氧化产物是 ,还原产物是 。
②反应Ⅱ中,Cu O的作用是 。(填“氧化剂”“还原剂”或“氧化剂和还原剂”)
2
【答案】(1) ①④⑧⑨⑩ ③⑤⑧ ②⑥⑦
(2)
(3)
(4)酸性
(5)C
(6) SO 氧化剂
2
【详解】(1)导电的物质包括金属、电解质溶液和熔融的电解质,故导电的物质包括①④⑧⑨⑩,电解
质包括酸、碱、盐和活泼金属氧化物,非电解质包括大部分非金属氧化物、非金属氢化物和部分有机物,
故可知属于电解质的有③⑤⑧,属于非电解质的有②⑥⑦。单质和混合物既不属于电解质也不属于非电解
质。
(2)KSO 是强电解质,其电离方程式为 。
2 4
(3)铁和盐酸发生置换反应: 。
(4)二氧化碳与碱反应生成盐和水,故属于酸性氧化物。
(5)Cu (OH) CO 属于碱式盐。
2 2 3(6) 中S化合价升高,故SO 属于氧化产物,O化合价降低,还原产物为
2
。Cu O中Cu化合价降低,被还原,做氧化剂。
2