文档内容
专题讲座(五) “位-构-性”综合推断题的解题方法
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·山东济宁市·高三二模)常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物
溶液(浓度均为0.01mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法错误的是
A.非金属性:W>Z>Y>X
B.简单离子的半径:Y>Z>W>X
C.W的氢化物空间构型不一定是三角锥形
D.Z的单质具有强氧化性和漂白性
【答案】D
【解析】W、Z的最高价氧化物对应的水化物溶液(浓度均为0.01 mol/L)的pH均为2,则两种元素最高价
氧化物对应的水化物均为一元强酸,则应为HNO 和HClO,Z的的原子序数和原子半径均大于W,则W为N
3 4
元素,Z为Cl元素;X的最高价氧化物对应的水化物溶液(浓度均为0.01 mol/L)的pH为12,为一元强碱,
且原子半径大于Cl,则X为Na元素;Y位于Na和Cl之间,且最高价氧化物对应的水化物溶液(浓度均为
0.01 mol/L)的pH<2,应为二元强酸,则Y为S元素。A.同周期元素,第一电离能呈增大趋势,半径越
小,越不容易失去电子,第一电离能越大,则第一电离能:W>Z>Y> X,故A正确;B.电子层数越大离子半
径越大,电子层数相同核电荷数越小离子半径越大,所以简单离子半径:S2->Cl->N3->Na+,即Y>Z>W>
X,故B正确;C.W为N元素,其气态氢化物有NH、NH 等,NH 是三角锥形,NH 不是三角锥形,故C正
3 2 4 3 2 4
确;D.Z为Cl,Cl 本身并不具有漂白性,D错误。故选D。
2
2.(2021·浙江高三二模)A、B、C、D四种短周期元素,原子序数依次增大,其元素特征信息如下表所示:
元素编
元素特征信息
号
A 单质常温下为气体,被人们看做理想的“绿色能源”
B 地壳范围内含量最多的元素
C 焰色反应显黄色
D C、D同周期,该周期中D的简单离子半径最小
下列说法不正确的是
A.113号元素与D同主族
B.原子半径D>C>B>A
C.C单质与水反应所得的强碱性溶液中含有两种电子数相同的阴、阳离子
D.C、D的最高价氧化物水化物之间能发生反应,生成一种正四面体构型的离子
【答案】B
【解析】A、B、C、D四种短周期元素,原子序数依次增大,A单质常温下为气体,被人们看做理想的“绿
色能源”,则A为H;B是地壳范围内含量最多的元素,则B为O;C的颜色反应显黄色,则C为Na;C、D
同周期,该周期中D的简单离子半径最小,则D为Al。A.113号元素原子的电子层结构为2、8、18、32、
32、18、3,该元素位于第七周期,IIIA族,与Al同主族,故A正确;B.同周期元素,原子半径随核电
荷数增大而减小,故原子半径:Na>Al,故B错误;C.Na单质与水反应得到氢氧化钠溶液,其中钠离子和
氢氧根离子电子数目都为10,故C正确;D.C、D的最高价氧化物水化物分别为NaOH和Al(OH),反应生
3
成[Al(OH)₄]-,是一种正四面体构型的离子,故D正确。故选B。
3.(2021·浙江高三三模)如图, 、 、 、 四种短周期元素的原子最外层电子数之和为 。下
列说法正确的是
A.原子半径( ):
B. 的氢化物一定比 的氢化物的沸点要低
C. 、 、 均有熔点高、硬度大的特性D.某病毒 链中有 元素,可能是 取代了普通 链中的 元素
【答案】D
【解析】设X的最外层电子数为a,则Y、W、Z的最外层电子数分别为(a+2)、a、(a+3),从而得出a+
(a+2)+a+(a+3)=21,a=4,故X、Y、W、Z分别为C、O、Si、Cl,则T的电子排布为2、8、18、5,其为As
元素。A.X、Y、Z分别为C、O、Cl,C、O为同周期元素,C在O的左边,则原子半径( ): ,
A不正确;B.X、Y分别为C、O,若X的氢化物中碳原子数比较多(如石蜡),常温下呈固态,则其沸点可
能比 的氢化物(HO)的沸点要高,B不正确;C.SiCl 在固态时形成分子晶体,其熔点较低、硬度较小,
2 4
C不正确;D.某病毒 链中有As元素,As与P属于同主族元素,可能是As取代了普通 链中的
P元素生成的,D正确;故选D。
4.(2021·吉林松原市·高三其他模拟)短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形
成的化合物结构如图所示。在元素周期表中元素W是原子半径最小的元素,Z原子的最外层电子数是周期
数的3倍,且W与X、Y、Z均可形成电子数相等的分子。下列说法正确的是
A.简单气态氢化物稳定性:Z<X
B.由W、Y、Z三种元素组成的化合物均是共价化合物
C.YF 分子中的原子均是稳定的8电子结构
3
D.X元素的最高价氧化物对应的水化物为强酸
【答案】C
【解析】由在元素周期表中元素W是原子半径最小的元素可知,W是H元素;Z原子的最外层电子数是周期
数的3倍,则Z是O元素;W与X、Y、Z均可形成电子数相等的分子,由化合物的结构可知,Y能形成3个
共价键、X能形成4个共价键,则Y是N元素、X是C元素。A.同周期元素,从左到右元素非金属性依次
增强,最简单气态氢化物的稳定性依次增强,则HO的稳定性大于NH,故A错误;B.H、N、O三种元素能
2 3
形成共价化合物硝酸或亚硝酸,也能形成离子化合物硝酸铵,故B错误;C.NF 分子中N原子和F原子最
3
外层均为8电子的稳定结构,故C正确;D.C元素的最高价氧化物对应的水化物为HCO,HCO 为二元弱
2 3 2 3
酸,故D错误;故选C。5.(2021·浙江金华市·高三二模)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。元素X、
Y、Q的单质在常温下呈气态,元素Y的最高正价和最低负价之和为2,元素Z在同周期的主族元素中原子
半径最大,元素M是地壳中含最多的金属元素。下列说法不正确的是
A.元素X、Y可以形成YX、YX 等化合物
3 2 4
B.简单离子半径:Y<Z
C.元素Z、M的最高价氧化物对应的水化物能相互反应
D.M、Q两种元素形成的化合物的水溶液呈酸性
【答案】B
【解析】元素Y的最高正价与最低负价之和为2,推测该元素最高价为+5,最低价为-3价,则Y可能为N
或P,又其单质常温下呈气态,故Y为N,Z在同周期中原子半径最大,又Z原子序数比Y大,故Z只能为
第三周期的Na,M元素为地壳中含量最多的金属元素,故M为Al,Al后面的同周期主族元素对应单质常温
下呈气态的只有Cl对应的Cl,故Q为Cl,N元素之前的主族元素中对应单质常温为气态的只有H对应的
2
H,故X为H。A.X为H,Y为N,可形成NH、NH 等化合物,A正确;B.Y3-(N3-)与Z+(Na+)电子层均为两
2 3 2 4
层,但Na的核电荷数大于N,故离子半径:Na+<N3-,B错误;C.Z、M最高价氧化物对应水化物分别为
NaOH、Al(OH),Al(OH) 有两性,可以与NaOH反应生成NaAlO,C正确;D.M、Q形成化合物AlCl,由于
3 3 2 3
Al3+水解,故AlCl 溶液显酸性,D正确;故答案选B。
3
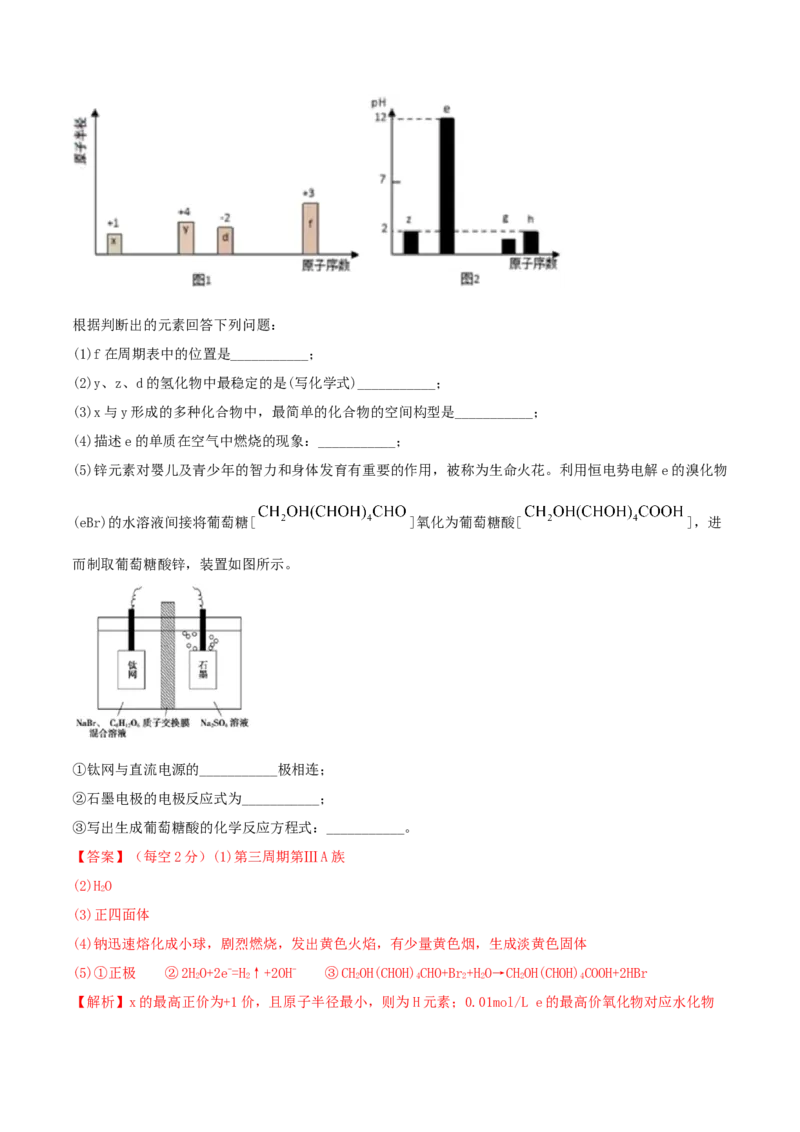
6.(2021·山东滨州市·高三二模)短周期主族元素W、X、Y、Z的原子序数依次增大,W的一种核素没
有中子,Y原子中L层电子数与K层电子数三倍。a、b、c、d均是由以上四种元素中的两种组成的二元化
合物,且d是淡黄色固体;25℃时,0.1mol/L e的水溶液pH=13。上述物质的转化关系如图所示。
下列说法正确的是
A.沸点:a>c
B.元素的非金属性:X>W
C.f溶液中存在c(H+)+c(HCO-)+c(HCO)=c(OH-)
3 2 3
D.简单阴离子的还原性:Y>W
【答案】B
【解析】短周期主族元素W、X、Y、Z的原子序数依次增大,W的一种核素没有中子,则W为H元素;Y原
子中L层电子数与K层电子数三倍,Y原子只能有2个电子层,K层2个电子,则L层有6个电子,故Y为O
元素;a、b、c、d均是由以上四种元素中的两种组成的二元化合物,且d是淡黄色固体,d为NaO;c跟
2 2d反应生成e和m,25℃时,0.1mol/Le的水溶液pH=13,则e为NaOH,则c为HO,m为O;b跟d反应生
2 2
成f和m,则b为CO,f为NaCO;a跟m反应生成c和d,则a为甲烷等烃,因此X为C元素,Z为Na元
2 2 3
素。A.a为甲烷等烃,c为HO,常温下,水为液体,沸点:HO>CH,故A错误;B.W为H元素,X为C
2 2 4
元素,元素的非金属性:X>W,故B正确;C.f为NaCO,质子守恒表达式应为c(H+)+c(HCO-)
2 3 3
+c(HCO)=c(OH-),故C错误;D.Y为O元素,W为H元素,非金属性O>H,故阴离子的还原性:Y<W,故
2 3
D错误;故选B。
7.(2021·浙江高三一模)根据物质的组成、结构等信息可以预测其性质或用途。下列预测中,明显不
合理的是
A.根据化合价预测,高铜酸钠( )与 可生成硫酸盐
B.根据组成预测,铝酸三钙( )溶于足量盐酸,生成白色沉淀
C.根据在周期表中位置预测,单质砷(第ⅤA族)是重要的半导体材料
D.根据结构预测,葡萄糖[ ]溶液中加入新制氢氧化铜,溶液呈绛蓝色
【答案】B
【解析】A.高铜酸钠( )中铜元素的化合价为+3价,具有氧化性,二氧化硫具有还原性,所以二
者反应可生成硫酸盐,故A合理;B.铝酸三钙( )溶于足量盐酸,反应生成氯化钙、氯化铝,不
能生成白色沉淀,B不合理;C.根据在周期表中位置预测,砷在金属和非金属的分界线附近,所以单质砷
(第ⅤA族)是重要的半导体材料,C合理;D.根据结构预测,葡萄糖[ ]为多羟基
醛,多羟基的物质溶液中加入新制氢氧化铜,溶液呈绛蓝色,D合理;故选B。
8.(2020·浙江绍兴市·高三一模)氮化镓(GaN)是第三代半导体核心材料,镓(Ga) 与铝位于同一主族,
微量分散于铝土矿中,其熔点为29.8 ℃,沸点为2403℃。下列说法不正确的是
A.室温下合成氮化镓的普遍方法为:2Ga+N =2GaN
2
B.GaO 具有两性,既能与酸反应,又能与碱反应
2 3
C.从铝土矿提取Al的废液中电解提取Ga,阴极反应为: Ga(OH) +3e- =Ga +4OH-
D.由于液态镓的宽温度范围,故Ga可以用于制作高温温度计的材料
【答案】A【解析】A.由题干信息可知,镓(Ga)与铝位于同一主族,N 的化学性质很稳定,故在室温下很难用Ga和
2
N 合成氮化镓,合成氮化镓的普遍方法为利用镓与NH 在1000℃高温下合成,A不正确;B.由题干信息可
2 3
知,镓(Ga)与铝位于同一主族,AlO 具有两性,故GaO 具有两性,既能与酸反应,又能与碱反应,B正确;
2 3 2 3
C.由题干信息可知,镓(Ga)与铝位于同一主族,微量分散于铝土矿中,故从铝土矿提取Al的废液中含有
Ga的化合物Ga(OH) ,故从中电解提取Ga,阴极反应为:Ga(OH) +3e- =Ga +4OH-,C正确;D.由题干信
息可知,Ga的熔点为29.8 ℃,沸点为2403℃,故液态镓的宽温度范围,Ga可以用于制作高温温度计的材
料,D正确;故答案为:A。
9.(2021·北京高三二模)下表是周期表中5种元素的相关信息,其中Q、W、X位于同一周期。
元素 信息 元素 信息
Q 位于周期表的第3周期第ⅢA族 Y 焰色反应为紫色
W 最高正化合价为+7价
Z 原子结构示意图为
X 本周期中原子半径最大
下列说法正确的是
A.Q在地壳中含量最高
B.元素的金属性:
C.气态氢化物的稳定性:
D.Q的最高价氧化物对应的水化物既能与NaOH反应,又能与HCl反应
【答案】D
【解析】Q位于周期表的第3周期第ⅢA族,则Q为Al,Q、W、X位于同一周期,W最高正化合价为+7价,
则W为Cl,X在本周期中原子半径最大,则X为Na,Y的焰色反应为紫色,则Y为K,由Z的原子结构示意
图知,Z为Br。A.氧元素在地壳中含量最高,A错误;B. 钠、钾位于同主族,钾位于钠的下方,钾的金
属性大于钠,B错误;C. 非金属性越强,气态氢化物越稳定:氯、溴位于同主族,溴位于氯的下方,氯
的非金属性大于溴,C错误;D. Q的最高价氧化物对应的水化物即氢氧化铝是两性氢氧化物,既能与
NaOH反应,又能与HCl反应,D正确;答案选D。
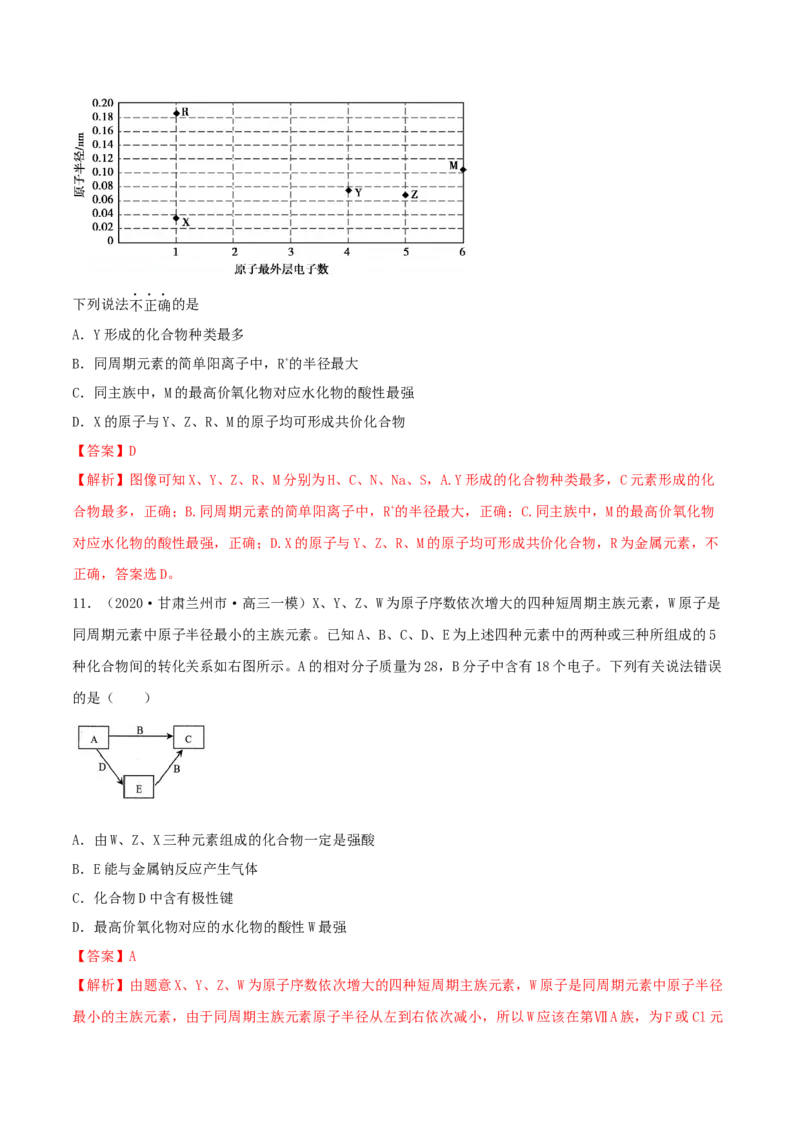
10.(2021·北京高三模拟)X、Y、Z、R、M为原子序数依次增大的短周期元素,其原子的最外层电子数
与原子半径的关系如图所示。下列说法不正确的是
A.Y形成的化合物种类最多
B.同周期元素的简单阳离子中,R+的半径最大
C.同主族中,M的最高价氧化物对应水化物的酸性最强
D.X的原子与Y、Z、R、M的原子均可形成共价化合物
【答案】D
【解析】图像可知X、Y、Z、R、M分别为H、C、N、Na、S,A.Y形成的化合物种类最多,C元素形成的化
合物最多,正确;B.同周期元素的简单阳离子中,R+的半径最大,正确;C.同主族中,M的最高价氧化物
对应水化物的酸性最强,正确;D.X的原子与Y、Z、R、M的原子均可形成共价化合物,R为金属元素,不
正确,答案选D。
11.(2020·甘肃兰州市·高三一模)X、Y、Z、W为原子序数依次增大的四种短周期主族元素,W原子是
同周期元素中原子半径最小的主族元素。已知A、B、C、D、E为上述四种元素中的两种或三种所组成的5
种化合物间的转化关系如右图所示。A的相对分子质量为28,B分子中含有18个电子。下列有关说法错误
的是( )
A.由W、Z、X三种元素组成的化合物一定是强酸
B.E能与金属钠反应产生气体
C.化合物D中含有极性键
D.最高价氧化物对应的水化物的酸性W最强
【答案】A
【解析】由题意X、Y、Z、W为原子序数依次增大的四种短周期主族元素,W原子是同周期元素中原子半径
最小的主族元素,由于同周期主族元素原子半径从左到右依次减小,所以W应该在第ⅦA族,为F或Cl元素,A相对原子质量为28的两种或三种元素组成化合物,容易想到一氧化碳和乙烯,而B分子有18个电子
的化合物,容易想到氯化氢、硫化氢、磷化氢、硅烷、乙烷、甲醇等,但要根据图中信息要发生反应容易
想到A为乙烯,B为氯化氢,C为氯乙烷,D为水,E为乙醇,从而X、Y、Z、W分别为H、C、O、Cl。A. 由
W、Z、X三种元素组成的化合物,有HClO、HClO、HClO 等,其中HClO为弱酸,A错误;B. E为乙醇,含
3 4
有羟基,能与金属钠反应产生氢气,B正确;C. 化合物D为水,水的结构式为 ,含有氢氧极性键,
C正确;D. 最高价氧化物对应的水化物有HCO、HClO,酸性HCO O2->Na+ >H+
(2)C SiH
4
(3)HClO> HSO >HCO > HSiO
4 2 4 2 3 2 3(4)离子键和共价键
(5) H++ HSO-=SO↑+HO SO+2HO+Cl=2HCl+HSO
3 2 2 2 2 2 2 4
【解析】现有A、B、C、D、E、F、G七种短周期主族元素,D是短周期中原子半径最大的,D为Na;B、E
最外层电子数是最内层电子数的2倍,B为C,E为Si;已知A、D位于同一主族;C、F的最外层电子数相
等,且C、F的原子序数之和为A、D原子序数之和的两倍,C的原子序数小于D,F的原子序数大于D,所
以A 为H,C为O,F为S;G为Cl;
(1)离子的电子层数越多,半径越大,电子层结构相同的离子,核电荷数越大,离子半径越小;因此离子
半径由大到小的顺序是:S2-> O2->Na+ >H+;综上所述,答案是:S2-> O2->Na+ >H+。
(2) B、C、E、F、G形成的气态氢化物数目最多的是C,它可以与氢形成烷烃、烯烃、炔烃等(碳数小于等
于4)、芳香烃等;根据同周期从左到右元素的非金属增强,气态氢化物的稳定性增强,同主族从上到下
元素的非金属性减弱,气态氢化物的稳定性减弱,硅的非金属性最弱,其所形成的气态氢化物SiH 是最不
4
稳定的;综上所述,答案是:C、SiH。
4
(3)B、E、F、G最高氧化物对应的水化物为:HCO 、 HSiO 、 HSO 、HClO ;元素的非金属性越强,
2 3 2 3 2 4 4
最高价含氧酸的酸性就越强,因为非金属性:Cl>S>C>Si,所以最高价含氧酸酸性由强到弱的顺序是:
HClO> HSO >HCO > HSiO ;综上所述,答案是:HClO> HSO >HCO > HSiO。
4 2 4 2 3 2 3 4 2 4 2 3 2 3
(4)由A、C、D形成的化合物为NaOH,它属于离子化合物,所含的化学键类型有离子键和共价键;综上所
述,答案是:离子键和共价键。
(5) A、C、D、F四种元素组成化合物M和N分别为:NaHSO 和 NaHSO,它们在溶液中相互反应的离子方
4 3
程式是:H++ HSO-=SO↑+HO;二氧化硫通入氯气的水溶液中发生反应生成硫酸和盐酸,化学方程式为:
3 2 2
SO+2HO+Cl=2HCl+HSO;综上所述,答案是:H++ HSO-=SO↑+HO;SO+2HO+Cl=2HCl+HSO;
2 2 2 2 4 3 2 2 2 2 2 2 4
15.(2021·上海高三一模)(12分)2019年1月3日一吨多重的嫦娥四号探测器首次实现人类飞行器在
月球背面的软着陆,它所搭载的“玉兔二号”月球车通过砷化镓 太阳能电池提供能量开展工作。
下表是As、Ga等元素所在元素周期表中的一部分。回答下列问题:
Al Si P
Ga Ge As
(1)上表中,原子半径最小的是_________元素(填元素名称),元素周期表中镓的位置是_________。从原
子结构角度解释磷与砷的非金属性强弱:_______________。
(2)GaAs可以用浓硝酸溶解,生成HAsO 和Ga(NO)。配平反应的化学方程式,并标出电子转移方向和数目:
3 4 3 3
GaAs+HNO→Ga(NO)+NO↑+HAsO+HO,_________
3 3 3 2 3 4 2(3)GaN、GaAs、GaP都是良好的半导体材料,晶体类型与晶体硅相同,它们的熔点如表。
晶体 GaN GaAs GaP
熔点/℃ 1700 1238 1480
解释它们熔点变化的原因______________。
(4)亚磷酸(HPO)与NaOH反应只能生成NaHPO 和NaHPO 两种盐,这两种盐溶液均呈碱性。根据以上信息
3 3 2 3 2 3
判断,亚磷酸应属于____________________酸,NaHPO 溶液中阴离子浓度由大到小的次序为_______。
2 3
【答案】(除标注外,每空2分)(1)磷(1分) 第四周期第IIIA族(1分) 磷原子和砷原子的最
外层电子数相同,但磷原子比砷原子少一层电子,原子半径小,得电子能力强,所以磷的非金属性强于砷
(2)
(3)GaN、GaP、GaAs都是原子晶体,原子半径N<P<As,键长Ga−N<Ga−P<Ga−As,键能Ga−N>Ga−P>
Ga−As,故GaN、GaP、GaAs的熔点依次降低
(4)二元弱 >OH->
【解析】(1)上表中,根据层多径小,同电子层结构核多径小原则,则原子半径最小的是磷元素,Al在周
期表中是第三周期第IIIA族,Al和Ga是同族,因此元素周期表中镓的位置是第四周期第IIIA族。磷原子
和砷原子的最外层电子数相同,但磷原子比砷原子少一层电子,原子半径小,得电子能力强,所以磷的非
金属性强于砷;故答案为:磷;第四周期第IIIA族;磷原子和砷原子的最外层电子数相同,但磷原子比砷
原子少一层电子,原子半径小,得电子能力强,所以磷的非金属性强于砷。
(2)GaAs可以用浓硝酸溶解,生成HAsO 和Ga(NO)。配平反应的化学方程式,并标出电子转移方向和数目:
3 4 3 3
GaAs中As化合价由−3价升高到+5价,升高8个价态,HNO 中N化合价降低到NO,由+5价降低到+4价,
3 2
降低1个价态,根据升降守恒得到NO 系数为8,GaAs系数为1,HAsO 系数为1,Ga(NO) 系数为1,HNO
2 3 4 3 3 3
系数为11,HO系数为4,根据O守恒检验,因此得到GaAs+11HNO = Ga(NO)+8NO↑+HAsO+4HO,其单
2 3 3 3 2 3 4 2
线桥法为 ;故答案为:
。
(3)从图中熔点变化分析出GaN、GaP、GaAs都是原子晶体,原子半径N<P<As,键长Ga−N<Ga−P<
Ga−As,键能Ga−N>Ga−P>Ga−As,故GaN、GaP、GaAs的熔点依次降低;故答案为:GaN、GaP、GaAs都
是原子晶体,原子半径N<P<As,键长Ga−N<Ga−P<Ga−As,键能Ga−N>Ga−P>Ga−As,故GaN、GaP、
GaAs的熔点依次降低。(4)根据信息,说明亚磷酸(HPO)与足量NaOH反应生成NaHPO,说明亚磷酸应属于二元弱酸,NaHPO 溶液
3 3 2 3 2 3
显碱性,说明 水解大于电离,因此溶液中阴离子浓度由大到小的次序为 >OH-> ;
故答案为:二元弱; >OH-> 。