文档内容
主题七 化学实验测试(二)
(考试时间:75 分钟 试卷满分:100 分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共 45 分)
一、选择题(本题共 15 个小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1.李时珍的《本草纲目》中记载了纯净 KNO 的制备过程。志曰:“此即地霜也。所在山泽,冬月地上
3
有霜,扫取以水淋汁,后乃煎炼而成”,时珍曰:“……货者苟且,多不洁净,须再以水煎化,倾盆中,一夜
结成。”根据上述描述,下列说法错误的是( )
A.“冬月地上有霜”说明 KNO 的溶解度随温度的降低而降
3
低
B.“以水淋汁”和“煎炼而成”涉及了溶解和蒸发操作
C.实验室中进行“煎炼而成”过程应使用到 和
D.“再以水煎化,倾盆中,一夜结成”是重结晶操作
【答案】C
【解析】A 项,冬月温度降低,KNO 溶解度降低,以晶体形式析出,说明 KNO 的溶解度随温度降低
3 3
而降低,A 正确;B 项,以水淋汁是加水溶解,煎炼而成是蒸发结晶,B 正确;C 项,蒸发过程应使用
,而非 ,C 错误;D 项,根据“货者苟且,多不洁净”,说明 KNO 不纯,需进行重结
3
晶
操作,D 正确; 故选 C。
2.下列说法不正确的是( )
A.为除去乙酸乙酯中的乙醇,可向其中加入水进行多次萃取分液
B.“静置”也是一种必要的实验操作,比如:淀粉和硫酸加热水解实验后需静置冷却后才能滴加碘水
来
检验水解程度,滴定管读数前、移液管移取液体、萃取分液时等
C.如果不慎将苯酚沾到皮肤上,应立即先用酒精洗涤,再用水冲洗
D.测 NaClO 溶液 pH: 用干燥洁净的玻璃棒蘸取溶液,滴到放在表面皿上的 pH 试纸中部,变色后
与标准比色卡比对
原创精品资源学科网1独 / 1家7享有版权,侵权必究!【答案】D
【解析】A 项,乙醇与水互溶,水与乙酸乙酯分层,且乙醇易溶于水,则除去乙酸乙酯中的乙醇,可
向其中加入水进行多次萃取分液,A 正确;B 项,“静置”时可充分反应或充分混合、分层等,所以“静置”
也
是一种必要的实验操作,B 正确;C 项,苯酚有毒,其浓溶液对皮肤有强烈的腐蚀性,使用时要小心,如果
不慎沾到皮肤上,应立即用酒精洗涤,再用水冲洗,C 正确;D 项,次氯酸钠溶液具有漂白性,会漂白试纸,
不能用 pH 试纸测定其 pH,D 错误;故选 D。
3.下列有关实验基本操作不能达到目的的是( )
A.配制 10%CuSO 溶液:称取 5. 0 g CuSO •5H O,加入 27.0 g 水,搅拌溶解
4 4 2
B.在实验室中,采用加热氯酸钾和二氧化锰混合物的方法制取氧气。我们可以用溶解、过滤、洗涤、
干燥的方法从反应产物中得到二氧化锰
C.可以用酒精灯、玻璃棒、坩埚、泥三角这些仪器从食盐水中获取 NaCl 晶体
D.配制 100 mL 1 mol·Lˉ1 的 Na CO 溶液可将固体放于天平左盘称其质量
2 3
【答案】C
【解析】A 项,5. 0gCuSO •5H O 中所含 CuSO 的质量为: ,,加入 27.0g 水,所得
4 2 4
溶液的溶质质量分数= ,故 A 正确;B 项,氯酸钾和二氧化锰混合加热后,氯酸
钾分解成氯化钾和氧气,二氧化锰不反应且不溶于水,因此将反应后混合物溶解、过滤、洗涤、干燥后可
得到二氧化锰,故 B 正确;C 项,从食盐水中获取 NaCl 晶体需要通过蒸发结晶的方法,蒸发需用到蒸发皿,
故 C 错误;D 项,托盘天平的使用“左物右码”,所成药品在左盘中称量,故 D 正确;故选 C。
4.化学实验操作是进行科学实验的基础。下列操作正确的是( )
A.碱式滴定管排气泡 B.溶液加热 C.制备并收集少量氨气 D.吸收多余的 气体
【答案】A
【解析】A 项,碱式滴定管排气泡时,把橡皮管向上弯曲,出口上斜,轻轻挤压玻璃珠附近的橡皮管
原创精品资源学科网2独 / 1家7享有版权,侵权必究!可以使溶液从尖嘴涌出,气泡即可随之排出,A 正确;B 项,用试管加热溶液时,试管夹应夹在距离管口的
1/3 处,B 错误;C 项,实验室制备少量氨气,应用氯化铵和熟石灰共热,C 错误;D 项,HCl 气体极易溶
于水,用水吸收多余的 HCl 气体,要注意放倒吸,应采用倒扣的漏斗代替长导管,D 错误;故选 A。
5.下列图示对应的操作规范的是( )
A.称量 B.过滤 C.将剩余钠放回试剂瓶 D.转移溶液
【答案】C
【解析】A 项,称量时应该左物右码,氢氧化钠具有腐蚀性,应该在小烧杯中称量,操作不规范,故 A
不选;B 项,过滤时需要用玻璃棒引流,故 B 不选;C 项,钠的性质非常活泼,随意丢弃易发生事故,实
验中剩余的钠,需要放回试剂瓶,操作规范,故 C 选;D 项,转移溶液时玻璃棒下端应该靠在容量瓶颈部
刻度线以下,操作不规范,故 D 不选;故选 C。
6.某研究小组通过实验探究 Cu 及其化合物的性质,操作正确且能达到实验目的的是( )
A.将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察 CuCl 的生成
2
C.将 CuCl 溶液在蒸发皿中加热蒸干,得到无水 CuCl 固体
2 2
D.将表面有铜绿[Cu (OH) CO ]的铜器放入盐酸中浸泡,除去铜绿
2 2 3
【答案】D
【解析】A 项,浓硫酸溶于水放热,正确的操作应该将铜丝插入浓硫酸中加热,反应后取一定量的反
应液加入盛有水的烧杯中,A 错误;B 项,应该用红热的铜丝,B 错误;C 项,Cu2+水解,加热 CuCl 溶液
2
不能得到 CuCl 固体,C 错误;D 项,铜绿溶于盐酸而铜不溶于盐酸,故可用盐酸除去铜器表面的铜绿,D
2
正确。故选 D。
7.某废催化剂含 SiO 、ZnS、CuS 及少量的 Fe O 。某实验小组以该废催化剂为原料,回收锌和铜,
2 3 4
设计实验流程如图:
原创精品资源学科网3独 / 1家7享有版权,侵权必究!下列说法不正确的是( )
A.滤渣 2 的主要成分 S、SiO
2
B.检验滤液 1 中是否含有 Fe3+可以选用 KSCN 溶液
C.步骤②操作中,应先加 6%H O ,然后不断搅拌下缓慢加入 1.0mol·L-1H SO
2 2 2
4
D.步骤③、④操作是蒸发浓缩至出现晶膜时停止加热,冷却结晶,过滤
【答案】C
【解析】废催化剂含 SiO 、ZnS、CuS 及少量的 Fe O ,加入硫酸后,发生反应 ZnS
2 3 4
+H SO =ZnSO +H S↑、Fe O +4H SO =FeSO +Fe (SO ) +4H O,得到的滤液 1 中含 ZnSO 、FeSO 、Fe
2 4 4 2 3 4 2 4 4 2 4 3 2 4 4
2
(SO ) ,滤渣 1 中含 SiO 、CuS,向滤渣 1 中加入 H SO 和 H O 溶液,会得到 CuSO 、S,则滤液 2 中含
4 3 2 2 4 2 2 4
CuSO
,滤渣 2 中含 S、SiO 。A 项,滤渣 2 的主要成分为 S、SiO ,故 A 正确;B 项,铁离子遇到 KSCN 溶液4
2 2
显
红色,可以用 KSCN 检验,故 B 正确;C 项,H O 在酸性条件下能氧化 CuS,步骤②操作中,应先加入硫
2 2
酸,再加入 6%H O ,故 C 错误;D 项,两步均为从溶液到晶体的过程,操作正确,故 D 正确;故选 C。
2 2
8.海带富含碘元素,从海带中提取碘的实验过程如图所示,其中没有涉及的实验操作是( )
A. B. C. D.
【答案】C
【解析】海带在坩埚中灼烧生成海带灰,用热水浸泡得到海带灰的悬浊液,再过滤得到含碘离子的溶
液,用双氧水在酸性条件下氧化得到含单质碘的溶液,用四氯化碳萃取分液,再蒸馏得到单质碘。步骤①
原创精品资源学科网4独 / 1家7享有版权,侵权必究!是灼烧,步骤③是悬浊液到溶液,其操作是过滤, 步骤⑤是从碘的水溶液到碘的四氯化碳溶液,操作是分
液,没有涉及到的操作是配溶液,故答案为 C。
9.侯德榜将氨碱法制取碳酸钠和合成氨联合起来,将制碱技术发展到新的水平。氨碱法的反应原理为
NaCl+NH +CO +H O=NaHCO ↓+NH Cl,过滤所得 NaHCO 可用于制纯碱。现对过滤所得滤液进行如下实
3 2 2 3 4 3
验,所得结论正确的是( )
A.用铂丝蘸取少量滤液进行焰色反应,观察到火焰呈黄色,说明滤液中含有 Na+
B.取少量滤液于试管中,加热试管,将湿润的红色石蕊试纸置于试管口,试纸未变蓝,说明滤液中不
含 NH 4+
C.取少量滤液,向其中加入足量稀盐酸,再加入硝酸银溶液,观察到有白色沉淀生成,说明滤液中含
有 Cl-
D.取少量滤液,向其中加入适量澄清石灰水,观察到有白色沉淀生成,说明滤液中含有 CO2-
3
【答案】A
【解析】A 项,钠元素的焰色试验是黄色,滤液中钠元素是以钠离子形式存在,A 正确;B 项,滤液中
含 NH Cl,取少量滤液于试管中,直接加热试管,生成的氨气与氯化氢会重新结合生成氯化铵,检验不到
4
氨气,而应取样于试管中加入浓氢氧化钠加热,观察是否产生能使湿润的红色石蕊试纸变蓝的气体判断,B
错误;C 项,取少量滤液,向其中加入足量稀盐酸后引入了氯离子,对原滤液中是否含氯离子有干扰,C 错
误;D 项,若滤液中含碳酸氢根离子,遇澄清石灰水也会出现白色沉淀,则上述操作不能证明是否含碳酸
根离子,D 错误;故选 A。
10.实验室以磷石膏[主要成分为 CaSO ,含少量 SiO 、Ca (PO ) 等杂质]为原料制备轻质 CaCO ,流程
4 2 3 4 2 3
如下图。下列说法错误的是( )
A.“转化”中,包含反应 CaSO+ CO2-3===SO2-4+
4
CaCO
3
B.“滤液”的 pH 约为 6.5,阴离子主要是 SO2-4 和 CO2-
3C.“高温煅烧”需要的仪器有酒精喷灯、坩埚、坩埚钳、泥三角、三脚架等
D.“浸取”时,适当升高温度有利于 Ca2+的浸
出
【答案】B
【解析】A 项,“转化”时,通入二氧化碳,生成碳酸根离子,将硫酸钙转化为碳酸钙,A 项正确;B 项,
原创精品资源学科网5独 / 1家7享有版权,侵权必究!pH 约为 6.5,呈酸性,碳酸根不可能大量存在,B 项错误;C 项,“高温煅烧”需要的仪器有酒精喷灯、坩埚、
坩埚钳、泥三角、三脚架等,C 项正确;D 项,氯化钙的溶解度随着温度的升高而增大,所以适当升高温度
有利于 Ca2+的浸出,D 项正确;故选 B。
11.已知相关氢氧化物沉淀的 pH 范围:Fe(OH) 为 5.85---8.35,Fe(OH) 为 1.14----3.0,Cu(OH) 为 4.2
2 3 2
----6.7。孔雀石的主要成分是 Cu (OH) CO ,还含有少量 SiO 、FeCO 等杂质,实验室以孔雀石为原料制备
2 2 3 2 3
硫酸铜晶体流程如下:
下列说法正确的是( )
A.滤液 1 中含有的金属阳离子有 Cu2+、Fe2+、H+
B.步骤②中所用的试剂 X 可是 H O 、Cl 或氯水
2 2 2
C.步骤③中加入 CuO,可以用 Cu(OH) 、CuCO 等代替
2 3
D.由滤液 3 得到硫酸铜晶体,需要经过的步骤把溶液蒸发至大量晶体析出,过滤等。
【答案】C
【解析】A 项,H+ 不是金属阳离子,A 错误;B 项,步骤②中所用的试剂 X 是氧化剂,以双氧水为最佳,
Cl 或氯水能把亚铁离子氧化,但会引入氯离子,故 B 错误;C 项,步骤③中加入 CuO 的目的是调节溶液
2
的 pH,使 Fe3+沉淀的同时不引入新的杂质,可以用 Cu(OH) 、CuCO 等代替,故 C 正确;D 项,由滤液 3
2 3
得到硫酸铜晶体,需要经过的步骤依次有:蒸发浓缩、降温结晶、过滤等,故 D 错误。
12.某同学设计如图装置探究 H O 、SO 、I 的氧化性强弱。首先用 N 排净装置内空气,然后通入 SO
2 2 2 2 2
2
,甲中蓝色溶液褪色,乙中产生不溶于盐酸的白色沉淀;关闭弹簧夹,打开甲中分液漏斗活塞,逐滴滴加
H O 溶液,开始时颜色无明显变化,继续滴加 H O 溶液,混合液逐渐变成蓝色。下列说法错误的是( )
2 2 2 2
原创精品资源学科网6独 / 1家7享有版权,侵权必究!A.甲中蓝色溶液褪色说明 SO 将 I 氧化
2 2
B.乙中反应的离子方程式是 SO
2
+Ba2++H
2
O
2
=BaSO
4
↓+2H+
C.实验中“开始时颜色无明显变化”的原因是 SO 与 H O 反
2 2 2
应
D.由实验可知 H O 、SO 、I 氧化性由强到弱的顺序是 H O >I >SO
2 2 2 2 2 2 2
2
【答案】A
【解析】如图,向甲中通入二氧化硫气体,因碘单质与二氧化硫反应使得溶液褪色,说明氧化性:碘
单质>二氧化硫;多余的二氧化硫进入装置乙,被双氧水氧化生成硫酸根离子,再与钡离子反应生成不溶于
盐酸的硫酸钡;向已经褪色的装置甲中加入双氧水,刚开始与溶于水的二氧化硫反应颜色无变化,然后再
与碘离子反应生成碘单质,溶液变为蓝色,说明氧化性:双氧水>碘单质;装置丙为尾气吸收装置。A 项,
甲中蓝色溶液褪色说明单质与二氧化硫反应使得溶液褪色,说明氧化性:碘单质>二氧化硫,故 A 错误;B
项,根据题意,乙中反应的离子方程式是 SO
2
+Ba2++H
2
O
2
=BaSO
4
↓+2H+ ,故 B 正确;C 项,实验中“开始时
颜色无明显变化”的原因是 SO 还原性比碘离子强,SO 先与 H O 反应,故 C 正确;D 项,根据分析可知,
2 2 2 2
H O 、SO 、I 氧化性由强到弱的顺序:H O >I >SO ,故 D 正确;故选 A。
2 2 2 2 2 2 2 2
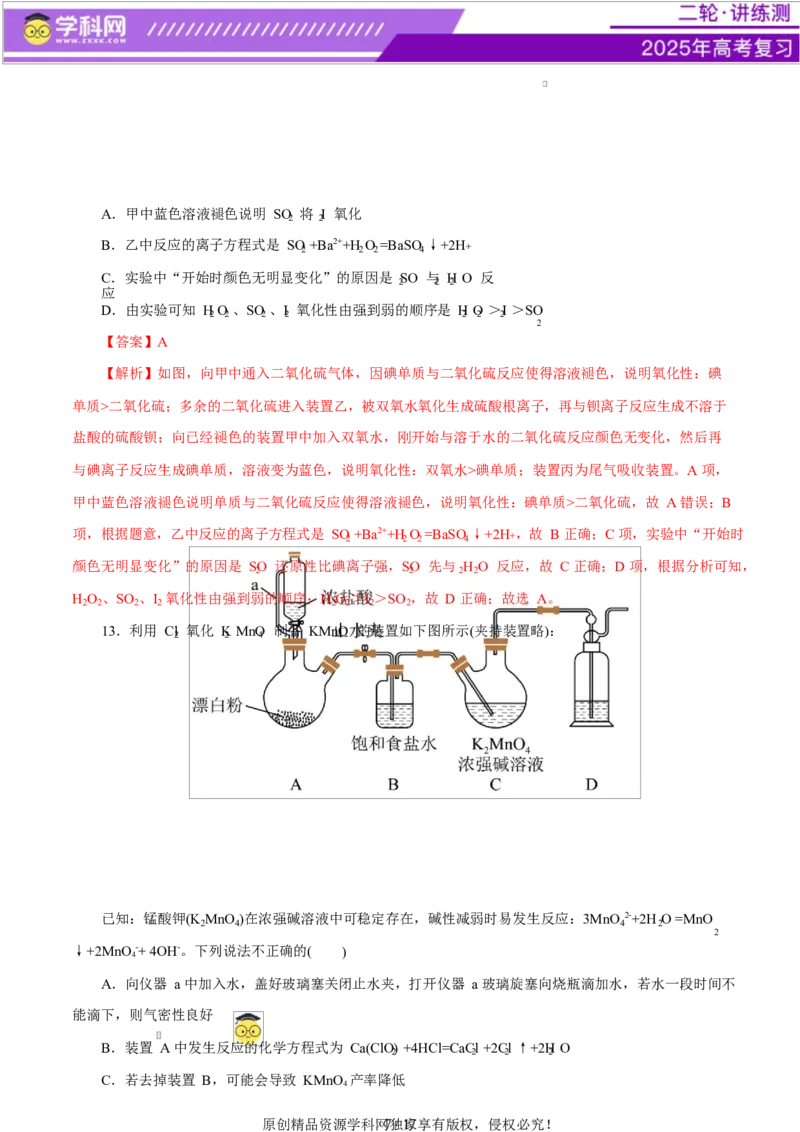
13.利用 Cl 氧化 K MnO 制备 KMnO 的装置如下图所示(夹持装置略):
2 2 4 4
已知:锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO 2-+2H O =MnO
2 4 4 2
2
↓+2MnO-+ 4OH-。下列说法不正确的( )
4
A.向仪器 a 中加入水,盖好玻璃塞关闭止水夹,打开仪器 a 玻璃旋塞向烧瓶滴加水,若水一段时间不
能滴下,则气密性良好
B.装置 A 中发生反应的化学方程式为 Ca(ClO) +4HCl=CaCl +2Cl ↑+2H O
2 2 2 2
C.若去掉装置 B,可能会导致 KMnO 产率降低
4
原创精品资源学科网7独 / 1家7享有版权,侵权必究!D.装置 D 中的作用是除去过量的氯气,以免污染环境
【答案】A
【解析】A 项,仪器 a 为恒压滴液漏斗,无论装置气密性是否良好,打开活塞,液体都能顺利流下,不
能检查装置的气密性,A 错误;B 项,装置 A 中的漂白粉,与浓盐酸反应,方程式为:Ca
(ClO) +4HCl=CaCl +2Cl ↑+2H O,B 正确;C 项,装置 B 中饱和食盐水是为了除去 Cl 中的 HCl,若去掉
2 2 2 2 2
装置 B,溶液在酸性条件下,会使 KMnO 产率降低 ,C 正确;D 项,Cl 有毒,会污染空气,用 NaOH 溶
4 2
液进行尾气处理,D 正确; 故选 A。
14.某化学小组同学通过实验研究 FeCl 溶液与 Cu 粉发生的氧化还原反应,实验记录如下表所示:已
3
知:Cu2++Cu+4Cl- =2 [CuCl ]-,[CuCl ]- CuCl↓(白色)+Cl-。
2 2
序号 Ⅰ Ⅱ Ⅲ
实验
步骤
充分振荡,加入 2mL 充分振荡,加入 2mL 蒸馏 充分振荡,加入 2mL 蒸
馏
水 水
蒸馏水
铜粉消失,溶液黄色 铜粉有剩余,溶液黄色褪 铜粉有剩余,溶液黄色褪去,
实验
变浅,加入蒸馏水后 去,加入蒸馏水后生成白 变成蓝色,加入蒸馏水后无
现象
无明显现象 色沉淀 白色沉淀
下列说法错误的是( )
A.实验Ⅰ中加入铜粉充分反应后,溶液中铜以[CuCl ]-的形式存在
2
B.实验Ⅰ、Ⅱ、Ⅲ中, 均被还原
C.实验Ⅱ中所得白色沉淀能溶于饱和 NaCl 溶液
D.向实验Ⅱ反应后的溶液中加入饱和 NaCl 溶液可能出现白色沉淀
【答案】A
【解析】实验 I:少量铜粉加入 1mL 0.1mol/L 氯化铁溶液,充分振荡,加 2mL 蒸馏水,铜粉消失,溶
液黄色变浅,加入蒸馏水后无明显现象,说明铁离子氧化铜生成铜离子。实验Ⅱ:过量铜粉加入 1mL 0.1mol/L
氯化铁溶液,充分振荡,加 2mL 蒸馏水,铜粉有剩余,溶液黄色褪去,铁离子全部和铜反应,加入蒸馏水
后生成白色沉淀说明铜被氧化的产物有亚铜离子,生成 CuCl 白色沉淀。实验Ⅲ:过量铜加入 1mL 0.05 mol/L
原创精品资源学科网8独 / 1家7享有版权,侵权必究!硫酸铁溶液,充分振荡,加 2mL 蒸馏水,铜粉有剩余,溶液黄色褪去,加入蒸馏水后无白色沉淀,说明铁
离子反应完全,生成的溶液中可能含铜离子和亚铜离子。A 项,实验 I 中所加铜粉少量,Cu 与 Fe3+反应生
成 Fe2+、Cu2+,Cu 被全部消耗,因此无法完成 Cu2++Cu+4Cl- =2 [CuCl ]-反应,故 A 项错误;B 项,由实验
2
Ⅰ、Ⅱ、Ⅲ中向等体积、铁离子浓度相同的溶液中加入铜粉,充分反应后溶液黄色变浅或溶液黄色褪去可知,
铜与溶液中铁离子反应生成 Fe2+,反应中 Fe3+被铜还原生成 Fe2+,故 B 项正确;C 项,由题干信息可知,
实验Ⅱ中所得白色沉淀为 CuCl,由[CuCl ]- CuCl↓(白色)+Cl-可知,增大溶液中 Cl-浓度能使平衡向
2
沉淀溶解方向移动,使得沉淀溶解,故 C 项正确;D 项,实验Ⅱ反应后的溶液中含有亚铜离子,因此向溶
液中加入饱和 NaCl 溶液可能出现白色沉淀 CuCl,故 D 项正确;故选 A。
15.为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计、现象
和结论都正确的是( )
影响因素 方案设计 现象 结论
向 1mol·L-1 FeCl 溶 液 中 滴 加
3
溶液颜色变 增大反应物浓度,平衡向正反应方向
A 浓度 溶液,溶液呈红色,反应
深 移动
达到平衡后继续滴加 KSCN 溶液
对于反应前后气体总体积会变化的可
一定温度下,压缩装有 NO 和 气体颜色变
2
B 压强 逆反应,增大压强,平衡向正反应方
N O 容器的体积 浅
2 4
向移动
分 别 向 盛 有 5mL0.1mol·
热水中的试
L-1Na S O 溶液的两支试管中同
2 2 3
C 温度 管先出现浑 升高温度,可加快反应速率
时加入等体积、等浓度的稀硫酸,
浊和气泡
混合后再分别放入冷水和热水中
单位时间内
向 和稀硫酸正在反应的溶液 使用合适的催化剂可使平衡向正反应
D 催化剂 产生的气体
中滴加少量 CuSO 溶液 方向移动
4
增多
【答案】A
【解析】A 项,向 1mol·L-1 FeCl 溶液中滴加 KSCN 溶液,溶液呈红色,反应达到平衡后继续滴加 KSCN
3
溶液,反应物浓度增大,平衡向正反应方向移动,溶液颜色加深,故 A 正确;B 项,一定温度下,压缩装
原创精品资源学科网9独 / 1家7享有版权,侵权必究!有 NO 和 N O 容器的体积,NO 、N O 浓度均增大,气体颜色加深,故 B 错误;C 项,为控制反应温度,
2 2 4 2 2 4
将盛有 5mL0.1mol·L-1Na S O 溶液的两支试管和装有等体积、等浓度的稀硫酸的溶液的两支试管分别放入
2 2 3
冷水和热水中,等溶液到一定温度后再混合,故 C 错误;D 项,催化剂不能使平衡移动,且 CuSO 表示锌
4
和硫酸反应的催化剂,故 D 错误;故选 A。
第 II 卷(非选择题 共 55
分)
二、填空题(本题共 4 小题,共 55 分)
16.(13 分)亚硝酸钠(NaNO )是一种常见的食品添加剂。某实验小组制备 NaNO 并对其性质进行探究。
2 2
资料:Ag+ 与 NO
2
-反应,可生产 AgNO
2
白色沉淀或无色络合离子。
Ⅰ. NaNO 的制取(夹持装置略)
2
实验 i:
向装置 A 中通入一段时间 N ,再通入 NO 和 NO 混合气体,待 Na CO 反应完全后,将所得溶液经
2 2 2 3
系
列操作,得到 NaNO 白色固体。
2
(1)仪器 a 的名称是_______。
(2)制取 NaNO 的离子方程式是_______。
2
(3)小组成员推测 HNO 是弱酸。为证实推测,向 NaNO 溶液中加入试剂 X,“实验现象”证实该推
2 2
测合
理,加入的试剂及现象是_______。
Ⅱ. NaNO 性质探究
2
将实验 i 制取的 NaNO 固体配成约 0.1mol/L NaNO 溶液,进行实验 ii 和
2 2
iii。
实验 ii:
原创精品资源学科网10独 / 家17享有版权,侵权必究!(4)由实验 ii 的现象得出结论:白色沉淀的生成与_______有关。仅用实验 ii 的试剂,设计不同实验方案
进一步证实了上述结论,实验操作及现象是_______。
(5)酸性条件下,NO -氧化 I-的离子方程式是_______。
2
实验 iii:
(6)甲同学认为,依据实验 iii 的现象可以得出结论:该条件下,NO 能氧化 I-。乙同学却提出了质疑,
他质疑的理由是_______。
【答案】(1)分液漏斗(1 分)
(2)NO+NO +CO 2-=2NO -+CO (2 分)
2 3 2 2
(3)酚酞试液,溶液会变成浅红色(2 分)
(4) AgNO 溶液和 NaNO 溶液的相对用量(2 分) 向 AgNO 溶液中逐滴滴加 NaNO 溶液,先有白色沉
3 2 3 2
淀生成,后沉淀逐渐溶解(2 分)
(5)2NO
2
-+2I-+4H+=2NO↑+I
2
+2H
2
O(2 分)
(6)A 装置中制取的 NaNO 可能含有副产物 NaNO (2 分)
2 3
【解析】由实验装置图可知,制备亚硝酸钠时,先向盛有碳酸钠溶液的三颈烧瓶中通入一段时间氮气,
排尽装置中的空气后,再通入一氧化氮和二氧化氮混合气体,一氧化氮和二氧化氮在碳酸钠溶液中反应生
成亚硝酸钠和二氧化碳,盛有酸性高锰酸钾溶液的洗气瓶用于吸收一氧化氮,防止污染空气。(1)根据仪器 a
的结构特点可知其为分液漏斗;(2)一氧化氮和二氧化氮在碳酸钠溶液中反应生成亚硝酸钠和二氧化碳,反
应的离子方程式为 NO+NO +CO 2-=2NO -+CO ;(3)若亚硝酸为弱酸,亚硝酸钠会在溶液中水解使溶液呈碱
2 3 2 2
性,则向亚硝酸钠溶液中滴加酚酞试液,若溶液会变成浅红色,说明亚硝酸为弱酸;(4)由实验现象可知,
向 NaNO 溶液中滴加 AgNO 溶液时,先没有白色沉淀生成,后有白色沉淀生成,说明白色沉淀的生成与
2 3
原创精品资源学科网11独 / 家17享有版权,侵权必究!AgNO 溶液和 NaNO 溶液的相对用量有关;因沉淀的生成与二者用量有关,所以可以互滴进行进一步验证,
3 2
具体操作为:向 AgNO 溶液中滴加 NaNO 溶液时,先有白色沉淀生成,后沉淀逐渐溶解;(5)由实验现象
3 2
可知,向亚硝酸钠溶液中滴加淀粉碘化钾溶液无明显现象,滴加稀硫酸后,溶液变蓝色,有无色气体生成,
说明酸性条件下,亚硝酸钠溶液与碘化钾溶液发生氧化还原反应生成硫酸钠、硫酸钾、碘、一氧化氮和水,
反应的离子方程式为 2NO
2
-+2I-+4H+=2NO↑+I
2
+2H
2
O;(6)NO
2
与碳酸钠溶液反应可以生成 NaNO
3
,即 A 装
置中制取的 NaNO 可能含有副产物硝酸钠,酸性环境中硝酸根具有氧化性,所以仅凭实验ⅲ不能得出上述
2
结论。
17.(13 分)烟酸又称维生素 B3,实验室可用 3-甲基吡啶为原料来制备。
已知:烟酸在冷水中微溶,随温度升高,溶解度逐渐增大。
实验步骤:
1.氧化:在如图所示的装置中加入 2.40g 3-甲基吡啶、70mL 水,分次加入 10.0g 高锰酸钾,加热控制
温度在 85~90℃,搅拌反应 60min,反应过程中有难溶物 MnO 生成。
2
2.合成粗产品
3.重结晶:将粗产品用热水溶解,加活性炭脱色,趁热过滤、冷却结晶、过滤、洗涤、干燥,得纯品。
4.纯度测定:取提纯后产品 0.500g 溶于水,配成 100mL 的溶液,每次取 25.00mL 溶液于锥形瓶中,
滴加几滴酚酞试液,用 0.0500molL 氢氧化钠溶液滴定,平均消耗氢氧化钠溶液 20.00mL。
请回答:
原创精品资源学科网12独 / 家17享有版权,侵权必究!(1)仪器 A 的名称是 。
(2)①从下列选项中选出合理的操作并排序,完善合成粗产品实验步骤:a→(______)→(______)→
(______)→(______)→干燥、称量粗产品 。
a.将反应液转移至蒸馏烧瓶中,常压下 144℃蒸馏
b.用浓盐酸酸化至 pH 为 3.8~4.0
c.趁热过滤,用热水洗涤滤渣
d.冷却、过滤、冷水洗涤
e.合并洗涤液与滤液
②上述合成粗产品的实验步骤中,下列有关说法正确的是 。
A.蒸馏的目的是为了除去未反应完的 3-甲基吡啶;
B.用浓盐酸酸化时,可用广泛 pH 试纸测定
C.趁热过滤后,若滤液呈紫红色,可加入适量乙醇,再重新过滤
D.若未用冷水洗涤,则粗产品的产率偏高
(3)重结晶过程中,趁热过滤的目的是 。
(4)纯度测定中,滴定终点的现象是 ,产品的纯度为 [M(烟酸)=123g·molˉ1],若滴定前仰
视读数,滴定后俯视读数,则测定的结果 (填“偏大”、“偏小”或“无影
响”)。
【答案】(1)(球形)冷凝管(1 分)
(2) cebd(2 分) ACD(2 分)
(3)滤去活性炭等不溶性物质,防止烟酸晶体析出(2 分)
(4) 加入半滴氢氧化钠溶液后,溶液变为粉红色,且半分钟内不变色(2 分) 98.4%(2 分) 偏小(2 分)
【解析】3-甲基吡啶被高锰酸钾氧化先生成烟酸钾,再经过盐酸酸化得到烟酸粗产品,粗产品经过重结
晶得到纯品,纯品用氢氧化钠溶液滴定测定其纯度。(1)仪器 A 的名称是球形冷凝管;(2)合成粗产品先将反
应液转移至蒸馏烧瓶中,常压下 144℃蒸馏,除去未反应的 3-甲基吡啶,再趁热过滤除去生成物中的 MnO ,
2
用热水洗涤滤渣,同时可以防止产品析出,合并洗涤液与滤液,再用盐酸酸化至 pH 为 3.8~4.0,最后冷却、
过滤、冷水洗涤得到烟酸产品,故实验步骤为 acebd;A 项,蒸馏的目的是为了除去未反应完的 3-甲基吡啶,
A 正确;B 项,广泛 pH 试纸测定值只能是整数值,B 错误;C 项,趁热过滤后,若滤液呈紫红色,说明高
锰酸钾过量,可加入适量乙醇除去高锰酸钾,再重新过滤,C 正确;D 项,若未用冷水洗涤,产品中混有可
溶性杂质,则粗产品的产率偏高,D 正确;故选 ACD;(3)由于烟酸在冷水中微溶,随温度升高,溶解度逐
原创精品资源学科网13独 / 家17享有版权,侵权必究!渐增大,重结晶过程中,趁热过滤的目的是:滤去活性炭等不溶性物质,防止烟酸晶体析出;(4)NaOH 滴
定烟酸,用酚酞做指示剂,达到终点的现象是:加入半滴氢氧化钠溶液后,溶液变为粉红色,且半分钟内
不变色;烟酸是一元酸,与 NaOH 反应物质的量之比为 1:1,消耗 NaOH 的物质的量为:0.0500molL×20.00
×10-3L=1×10-3mol,烟酸的质量为 1×10-3mol×123g/mol× =0.492g,纯度为 98.4%;若滴
定前仰视读数,滴定后俯视读数,读出的 NaOH 体积偏小,则测定的结果偏小。
18.(14 分)某研究性学习小组利用下列有关装置制备 SO ,并对 SO 的性质进行探究(装置的气密性已
2 2
检查)。已知:NaHSO 溶液显酸性。
3
Ⅰ.探究 SO 与可溶性钡的强酸盐是否反应(接口 a 接 b)
2
(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间 N,再关闭弹簧夹,此操作的目的是_______。
2
(2)实验过程中装置 B 中没有明显变化,装置 C 中有白色沉淀生成,该沉淀不溶于稀盐酸。据 B 中现象
得出的结论是_______,装置 C 中反应的离子方程式是_______。
(3)装置 D 中 NaOH 全部转化为 NaHSO 的标志为_______。
3
Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口 a 接 c)
(4)将少量装置 A 中生成的气体直接通入装置 G 中,不能根据 G 中现象判断亚硫酸与次氯酸的酸性强弱,
理由是_______(用化学反应方程式表示)。
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置 E 中药品是_______,其作用是
_______,通过_______现象即可证明亚硫酸的酸性强于次氯酸。
【答案】(1)排出装置中的空气,防止二氧化硫被氧气氧化为 SO 2-,干扰实验(2 分)
4
(2) 二氧化硫和 BaCl
2
溶液不反应(2 分) 3SO +2NO -+3Ba2++2H O=3BaSO ↓+2NO↑+4H+(2 分)
2 3 2 4
(3)溶液褪色(1 分)
(4)Ca(ClO) +2SO +2H O= CaSO ↓+H SO +2HCl(2 分)
2 2 2 4 2 4
原创精品资源学科网14独 / 家17享有版权,侵权必究!(5)碳酸氢钠溶液(1 分) 证明亚硫酸酸性大于碳酸,制取二氧化碳,吸收二氧化硫(2 分)
F 中品红溶液不褪色、G 中溶液变浑浊(2 分)
【解析】次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚
硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比 HClO 强判断;A 装置制备二氧
化硫,通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用品红溶液检验二氧化碳中不含二氧化硫,再
把二氧化碳通入漂白粉溶液中证明碳酸的酸性大于次氯酸。(1)为防止二氧化硫被氧气氧化为 SO 2-,干扰实
4
验,滴加浓硫酸之前,打开弹簧夹,通入一段时间 N ,排出装置中的空气。(2)二氧化硫通入 BaCl 溶液中,
2 2
没有明显变化,说明二氧化硫和 BaCl 不反应,装置 C 中有白色沉淀生成,该沉淀不溶于稀盐酸,说明二
2
氧化硫被硝酸根离子氧化生成硫酸钡沉淀,装置 C 中反应的离子方程式是 3SO
2
+2NO
3
-+3Ba2++2H
2
O=3BaSO
4
↓+2NO↑+4H+ 。(3)二氧化硫能使品红溶液褪色,装置 D 中 NaOH 全部转化为
NaHSO 的标志为溶液褪色;(4)次氯酸具有强氧化性、二氧化硫具有还原性,二氧化硫被次氯酸钙氧化为硫
3
酸钙,反应方程式为 Ca(ClO) +2SO +2H O= CaSO ↓+H SO +2HCl,所以不能根据 G 中生成沉淀判断亚硫
2 2 2 4 2 4
酸与次氯酸的酸性强弱。(5)为了验证亚硫酸与次氯酸的酸性强弱,需要证明酸性:亚硫酸>碳酸>次氯酸,
二氧化硫和碳酸氢钠反应生成亚硫酸氢钠和二氧化碳,所以装置 E 中盛放碳酸氢钠溶液证明亚硫酸酸性大
于碳酸、制取二氧化碳、吸收二氧化硫,通过 F 中品红溶液不褪色、G 中溶液变浑浊即可证明亚硫酸的酸
性强于次氯酸。
19.(15 分)某学习小组对 Cu 与 HNO 的反应进行了研究。
3
(1)铜与稀硝酸反应的化学方程式是_______。
(2)利用下图装置完成 Cu 与 HNO 制取氮氧化物的反应。实验可观察到装置 B 中液面上方为无色气体,
3
C 中液面上为红棕色气体。
①盛稀硝酸的仪器名称_______。
②为排尽整套装置内的空气,先打开弹簧夹,通入_______(填化学式),一段时间后关闭弹簧夹。
③C 中液面上为红棕色气体,其原因是_______(用化学方程式表示)。
原创精品资源学科网15独 / 家17享有版权,侵权必究!(3)下图是学习小组在做铜与硝酸反应的实验时的操作和现象。图中溶液 A 遇铜片立即产生气泡,而相
同条件下 稀硝酸(溶液 B)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。分析溶液 A
的成分后,学习小组探究溶液 A 与铜片能够立即发生反应的原因。
①假设 1:_______(填化学式)对该反应有催化作用。
实验验证:向溶液 B 中加入少量硝酸铜固体,溶液呈浅蓝色,放入铜片,没有明显变化。
结论:假设 1 不成立。
②假设 2:NO 对该反应有催化作用。
2
方案 1:向放有铜片的溶液 B 中通入少量 NO ,铜片表面立即产生气泡,反应持续进行。有同学认为
2
应补充对比实验:另取一份放有铜片的溶液 B,向其中加入数滴 5mol·L—1 硝酸,无明显变化。补充该实验
的目的是_______。
方案 2:向 A 中鼓入 N 数分钟得溶液 C.相同条件下,铜片与 A、C 溶液的反应速率分别为 、
2
,当 _______ 。(填“>”、“=”、“<”)时,实验能够证明假设 2 成立。
③经检验,A 溶液中还含有少量亚硝酸 HNO。
2
设计实验证明 HNO 也对该反应有催化作用。操作和预期现象是:向含有铜片的 B 溶液中_______。
2
最后结论:NO 和 HNO 对铜与硝酸的反应都有催化作用。
2 2
【答案】(1)3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O(2 分)
3 3 2 2
(2)分液漏斗或滴液漏斗(1 分) N 、CO 、稀有气体等(2 分)
2 2
NO+2HNO (浓)=3NO +H O(2 分)
3 2 2
(3) Cu2+或 Cu(NO ) (2 分) 排除通 NO 带来的硝酸浓度增大的影响(2 分)
3 2 2
>(2 分) 加入少量的固体 NaNO ,B 中铜片上立即生成气泡,反应持续进行(2 分)
2
【解析】(1)稀硝酸是氧化剂,铜是还原剂,铜和稀硝酸反应生成硝酸铜、一氧化氮和水,配平后方程
式为 3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O;(2)装置 A 中稀硝酸和铜反应生成 NO,装置 B 除去 NO
3 3 2 2
中
的硝酸,装置 C 中 NO 和浓硝酸反应生成了 NO ,装置 D 除去尾气,避免污染空气。①根据装置图,可得
2
盛稀硝酸的仪器名称为分液漏斗或滴液漏斗;②为了排除装置内的空气,需要通入不与产生气体反应的气体,
原创精品资源学科网16独 / 家17享有版权,侵权必究!可通入 N 、CO 、稀有气体等;③根据装置 B 中为无色气体,可知通入 C 中的气体为 NO,装置 C 中液
2 2
面
上为红棕色气体,可知 NO 和浓硝酸反应生成了 NO ,所以方程式为 NO+2HNO (浓)=3NO +H O;(3)①由
2 3 2 2
验证性实验加少量硝酸铜固体可得,该假设是探究 Cu2+或 Cu(NO ) 对该反应有催化作用;②因为 NO 会和
3 2 2
水反应产生硝酸,致使硝酸浓度增大,避免浓度对反应的影响,故需增加对照实验;向 A 中鼓入 N 数分钟,
2
使得溶液中 NO 的浓度下降,得溶液 C,当 > 时,实验能够证明假设 2 成立;③欲设计实验证明
2
HNO 也对该反应有催化作用,只需证明往含有铜片的 B 溶液中加入少量的固体 NaNO 比没加的速率快就
2 2
行。
原创精品资源学科网17独 / 家17享有版权,侵权必究!