文档内容
绝密★启用前
2025 年高考考前信息必刷卷 04(北京专用)
化 学
考情速递
高考·新动向:近年来高考化学试卷总体呈现回归教材、回归课标的特点,2025年可能会继续延续这一
趋势。这意味着每一道题在考纲上都会有相应的考点对应,不管题型、考法、侧重点如何变化,都会
基于教材本身展开。
高考·新考法:对中学化学基础知识能正确复述、再现、识别,并能融会贯通;将实际问题分解,通过
运用有关知识,采用分析、综合的方法,处理简单化学问题;对常规考点的新设问或知识融合,对非
常规考点的创新糅合等。
高考·新情境:继续考查高中化学主干内容,强调化学与科技、生产、生活的亲密联系。高考化学学科
的改革旨在贴近社会与生活,强调课程标准的教育理念。改革后,试题将更加紧密地结合生活生产环
境,体现教育与实践的融合。命题会精选试题情境,发挥学科育人价值。情境素材可能来源于生活实
际、科研成果、社会热点等
命题·大预测:化学试题将继续体现综合性,即一道试题可能涉及多个知识点的综合考查。例如,在一
道工业流程题中,可能同时考查化学反应原理、元素化合物知识、化学实验操作等多个方面的内容,
要求考生能够将所学的化学知识融会贯通。题目的呈现方式可能会有创新,例如采用图表、数据等多
种形式呈现信息,增加信息的密度,测试考生在阅读理解、知识提炼、信息整合及书面表达等方面的
综合能力。考生需要能够快速捕捉关键信息、精准分析并有效传达信息,像根据图表中的数据变化趋
势分析化学平衡的移动方向等。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 Li-7 Be-9 B-11 C-12 N-14 O-16 Na-23 Mg-24 Al-27
Si-28 S-32 Cl-35.5 K-39 Fe-56 Co-59 Cu-64
第一部分
一、选择题(本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的
一项。)
1.我国科学家通过机械化学方法,在氢化镧(LaH )晶格中制造大量的缺陷和纳米微晶,研发出首
1.95~3个室温环境下超快氢负离子(H−)导体。下列说法不正确的是( )
A.电负性:La > H B.氢属于s区元素
C.H−具有还原性 D.超快氢负离子导体有望用于新型电池研发
2.下列表示不正确的是( )
A.As原子的简化电子排布式:[Ar] 4s24p6 3
B.SO 2-的VSEPR模型:
3
C.N,N'-二甲基苯甲酰胺的结构简式:
D.用电子云轮廓图表示乙烯分子中的 键:
3.表面皿中都装有混合了饱和食盐水、酚酞和铁氰化钾溶液的琼脂,分别将缠有铜丝的铁钉(图A)和
缠有锌皮的铁钉(图 )放置其中,如图所示。下列说法不正确的是( )
A.图 中铁钉受锌皮保护,为牺牲阳极的阴极保护法
B.图 中铁钉上的电极反应式:2HO+2e-=H↑+2OH-
2 2
C.离子在半凝固态的琼脂内可定向移动
D.图 中,会出现蓝、红、蓝三个色块
4.下列说法不正确的是( )
A.工业上大量使用的乙酸是通过石油化学工业人工合成的
B.我国化学工作者第一次人工合成结晶牛胰岛素,它是一种结构复杂的氨基酸
C.乙炔可燃(氧炔焰温度可达3000℃以上),氧炔焰常用于焊接或切割金属
D.淀粉经酯化后可用于生产食品添加剂、表面活性剂和可降解塑料等
4.下列说法正确的是( )
A.含氨基甲酸酯的有机合成农药不慎触及皮肤用肥皂水清洗
B.重金属盐一定能使蛋白质变性C.同系物性质一定相似
D.纤维素、蚕丝、淀粉、牛油都属于天然有机高分子
5.下列反应的离子方程式的正确是( )
A.磁铁矿溶于稀硝酸:3Fe2++4H++NO-=3Fe3++NO↑+2HO
3 2
B.将NaAlO 溶液与NaHCO 溶液混合:AlO-+HCO-+H O=Al(OH) ↓+CO 2-
2 3 2 3 2 3 3
C.在亚硫酸中加入过量的次氯酸钠溶液:HSO + ClO-=Cl-+2H++SO2-
2 3 4
D.往硫酸氢铵溶液滴加过量NaOH溶液:H++OH-=H O
2
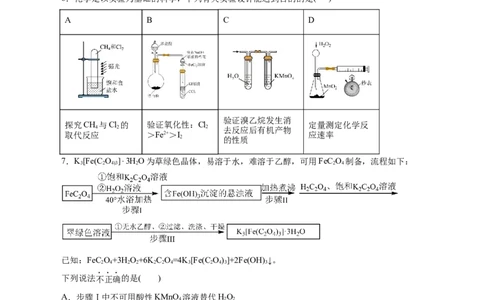
6.化学是以实验为基础的科学,下列有关实验设计能达到目的的是( )
A B C D
验证溴乙烷发生消
探究CH 与Cl 的 验证氧化性:Cl 定量测定化学反
4 2 2 去反应后有机产物
取代反应 >Fe2+>I 应速率
2 的性质
7.K[Fe(C O ]⋅3HO为草绿色晶体,易溶于水,难溶于乙醇,可用FeC O 制备,流程如下:
3 2 4)3 2 2 4
已知:FeC O+3H O+6K C O=4K [Fe(C O)]+2Fe(OH) ↓。
2 4 2 2 2 2 4 3 2 4 3 3
下列说法不正确的是( )
A.步骤Ⅰ中不可用酸性KMnO 溶液替代HO
4 2 2
B.步骤Ⅱ中加热煮沸是为了除去多余的HO
2 2
C.步骤Ⅲ中加入无水乙醇是为了降低三草酸合铁酸钾的溶解度
D.可用亚铁氰化钾溶液来检验翠绿色溶液中是否还有 未被氧化
8.羟胺(NH OH)是一种重要的物质,下面有关羟胺的说法中,不正确的是( )
2
A.因为羟胺可以与醛或酮反应生成肟,并且能与烷基化试剂发生反应,因此羟胺应属于一种有机物
B.羟胺可以与氧化铜发生氧化还原反应,化学方程式为:4CuO+2NH OH=2Cu O+NO↑+3HO
2 2 2 2C.羟胺属于一种亲核试剂,可以与金属原子之间形成配位键,羟胺中N原子与O原子都能进行配位
D.羟胺的碱性比氨更弱,这是因为羟基氧的电负性比氢更大
9.工业上常用NaOH溶液吸收NO ,发生反应:2NO +2NaOH=NaNO +NaNO +H O,下列说法不正
2 2 2 3 2
确的是( )
A.NaNO 是强电解质 B.NaNO 有毒,不可用于食品添加剂
3 2
C.N元素位于元素周期表p区 D.NaNO 溶液中通入O,溶液pH降低
2 2
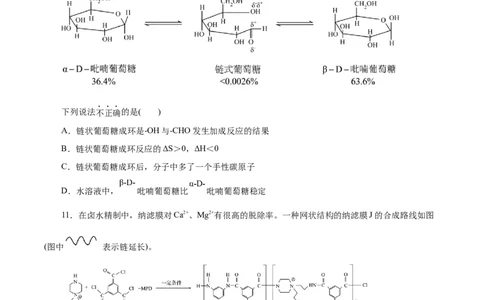
10.在葡萄糖水溶液中,链状结构与环状结构的平衡关系及百分含量如下:
下列说法不正确的是( )
A.链状葡萄糖成环是-OH与-CHO发生加成反应的结果
B.链状葡萄糖成环反应的ΔS>0,ΔH<0
C.链状葡萄糖成环后,分子中多了一个手性碳原子
D.水溶液中, 吡喃葡萄糖比 吡喃葡萄糖稳定
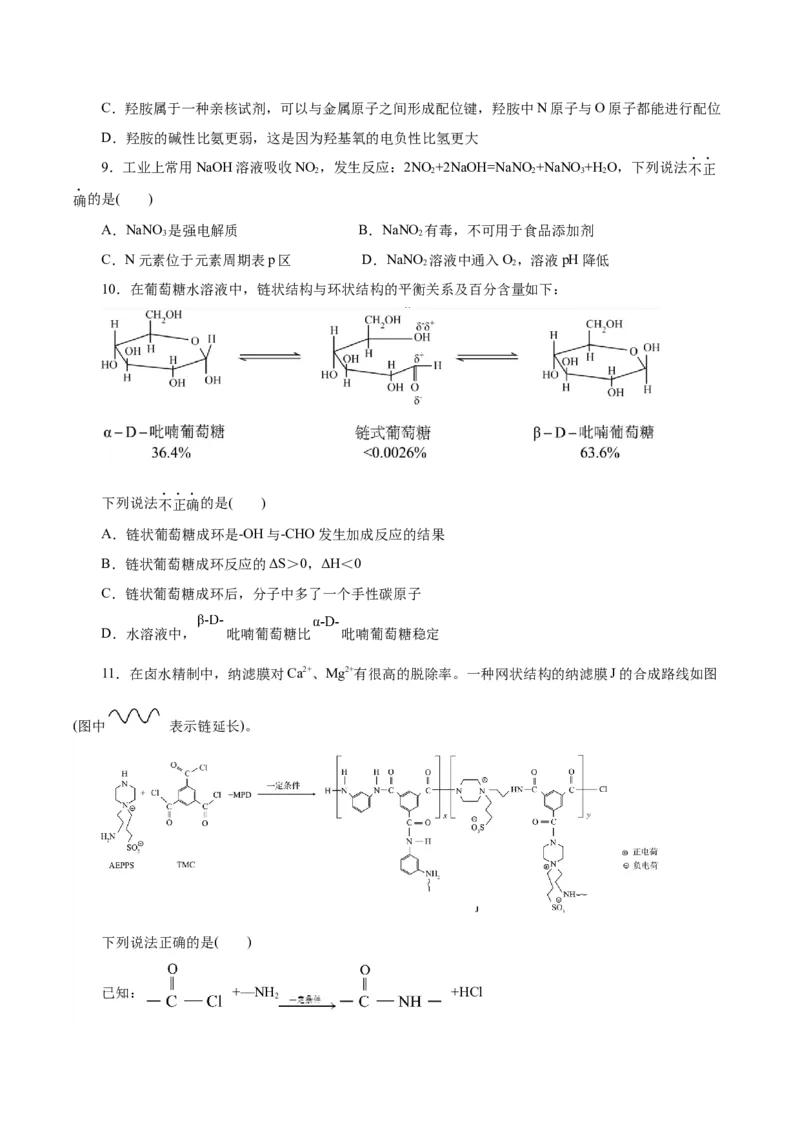
11.在卤水精制中,纳滤膜对Ca2+、Mg2+有很高的脱除率。一种网状结构的纳滤膜J的合成路线如图
(图中 表示链延长)。
下列说法正确的是( )
已知: +—NH +HCl
2A.J能脱除 、 可能与其存在阴离子有关
B.MPD的核磁共振氢谱有5组峰
C.J具有网状结构仅与单体AEPPS的结构有关
D.合成J的反应为加聚反应
12.下列关于物质的结构或性质的描述及解释都正确的是( )
A.键角:HO+>HO,是由于HO+中O上孤电子对数比HO分中O上的少
3 2 3 2
B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强
C.溶解度:O 在水中溶解度比在CCl 中溶解度更大,是由于O 是弱极性分子
3 4 3
D.酸性:CHClCOOH>CHCOOH,是由于CHClCOOH的羧基中羟基极性更小
2 3 2
13.已知基元反应的速率符合质量作用定律,如基元反应 , (k为速率常
数)。卤代烃RX发生水解反应有两种历程,能量变化如下图所示,下列说法不正确的是( )
A.若RX的水解速率 ,则反应按历程1进行
B.调节NaOH浓度,观察分层现象消失的用时变化,可确定RX的水解历程
C.相同条件下,按反应历程2,碘代烷(CH)CI水解速率要快于氯代烷(CH)CCl
3 3 3 3
D.取水解液,加AgNO 溶液,根据沉淀颜色可判断卤代烃RX中的卤素原子
3
14.同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同的不同金属片,加热,
用生成气体进行下表实验操作并记录实验现象。
实验现象
实验操作
金属为铜 金属为锌 金属为铝
点燃 不燃烧 燃烧 燃烧
通入KMnO 酸性溶液 褪色 褪色 褪色
4
无明显变
通入CuSO 溶液 无明显变化 出现黑色沉淀
4 化通入品红溶液 褪色 褪色 不褪色
已知:CuSO +H S= CuS↓+H SO (CuS为黑色固体);HS可燃
4 2 2 4 2
下列说法不正确的是( )
A.加入铜片的实验中,使KMnO 酸性溶液褪色的气体是SO
4 2
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含HS
2
C.加入锌片的实验中,生成的气体一定是混合气体
D.金属与浓硫酸反应的还原产物与金属活动性强弱有关
第二部分
二、非选择题(本部分共5题,共58分。)
15.(9分)氮及其化合物在生产生活中有重要用途。回答下列问题:
(1)基态N原子核外有 种不同能量的电子,其价层电子的轨道表示式为 。
(2)已知NH+的空间结构为正四面体形,请画出NH+的结构式(要求画出配位键) 。
4 4 4 4
(3)下列说法不正确的是___________。
A.[Cu(NH )]2+的中心离子为sp3杂化
3 4
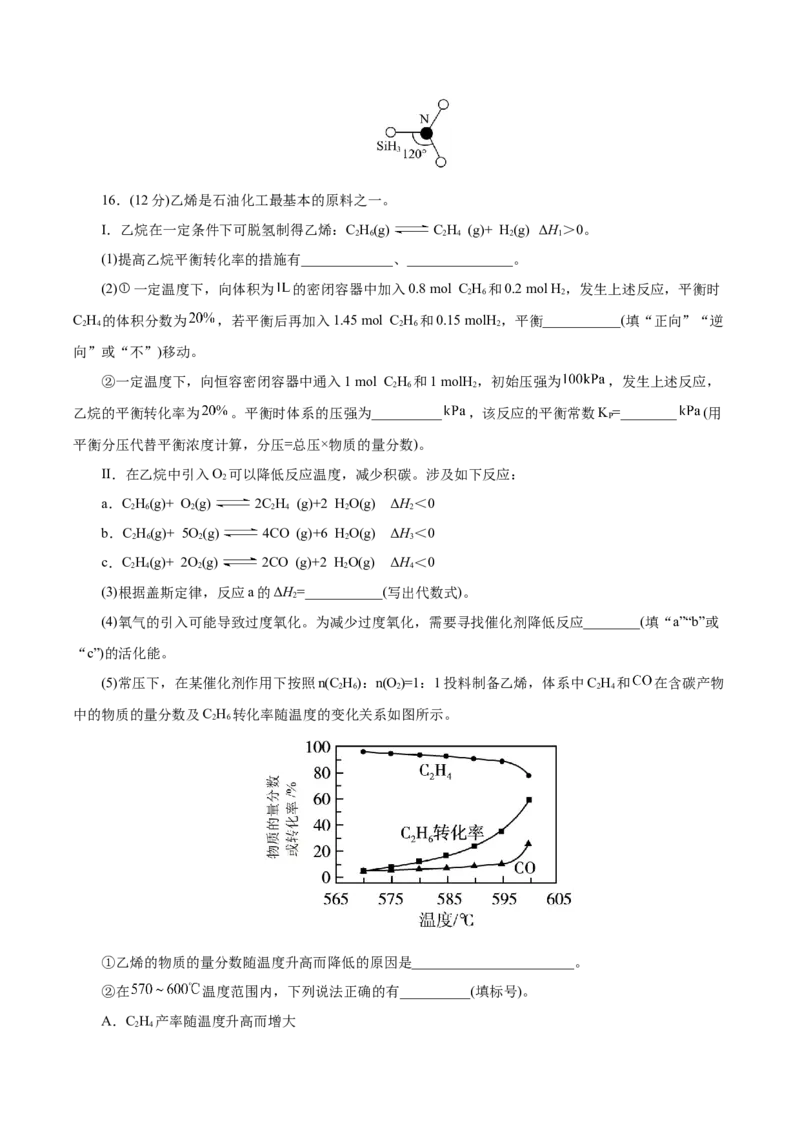
B.一种配离子的结构如图所示,该配离子中 的键角大于单个水分子中 的键角
C.分子的极性:NCl 比PCl 的大
3 3
D.氧化性:Fe3+>Fe(SCN)
3
(4)铁和氮形成一种物质,其晶胞结构如右图所示, 原子的配位数(紧邻的Fe原子)为 。
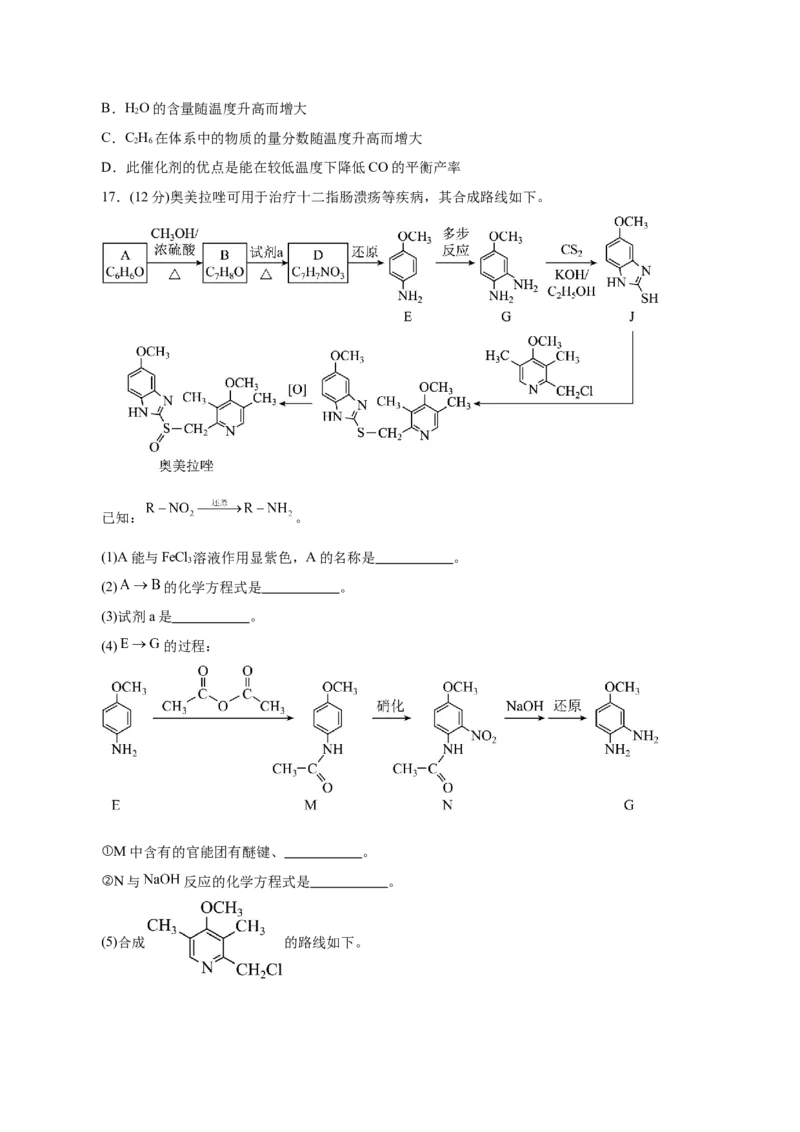
(5)有一种观点认为:由于硅的价层有可以利用的空 轨道,部分含硅化合物的性质与结构会与硅的3d
空轨道有关。化合物N(SiH ) 为平面结构,如右图所示。该物质中 原子的杂化方式为 ;
3 3
N(SiH ) 与H+形成配位键的能力 于(填“强”或“弱”)于N(CH )。
3 3 3 316.(12分)乙烯是石油化工最基本的原料之一。
I.乙烷在一定条件下可脱氢制得乙烯:C H(g) C H (g)+ H(g) ΔH>0。
2 6 2 4 2 1
(1)提高乙烷平衡转化率的措施有_____________、_______________。
(2)①一定温度下,向体积为 的密闭容器中加入0.8 mol C H 和0.2 mol H,发生上述反应,平衡时
2 6 2
C H 的体积分数为 ,若平衡后再加入1.45 mol C H 和0.15 molH ,平衡___________(填“正向”“逆
2 4 2 6 2
向”或“不”)移动。
②一定温度下,向恒容密闭容器中通入1 mol C H 和1 molH,初始压强为 ,发生上述反应,
2 6 2
乙烷的平衡转化率为 。平衡时体系的压强为__________ ,该反应的平衡常数K =________ (用
P
平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
II.在乙烷中引入O 可以降低反应温度,减少积碳。涉及如下反应:
2
a.C H(g)+ O(g) 2C H (g)+2 HO(g) ΔH<0
2 6 2 2 4 2 2
b.C H(g)+ 5O(g) 4CO (g)+6 HO(g) ΔH<0
2 6 2 2 3
c.C H(g)+ 2O(g) 2CO (g)+2 HO(g) ΔH<0
2 4 2 2 4
(3)根据盖斯定律,反应a的ΔH=___________(写出代数式)。
2
(4)氧气的引入可能导致过度氧化。为减少过度氧化,需要寻找催化剂降低反应________(填“a”“b”或
“c”)的活化能。
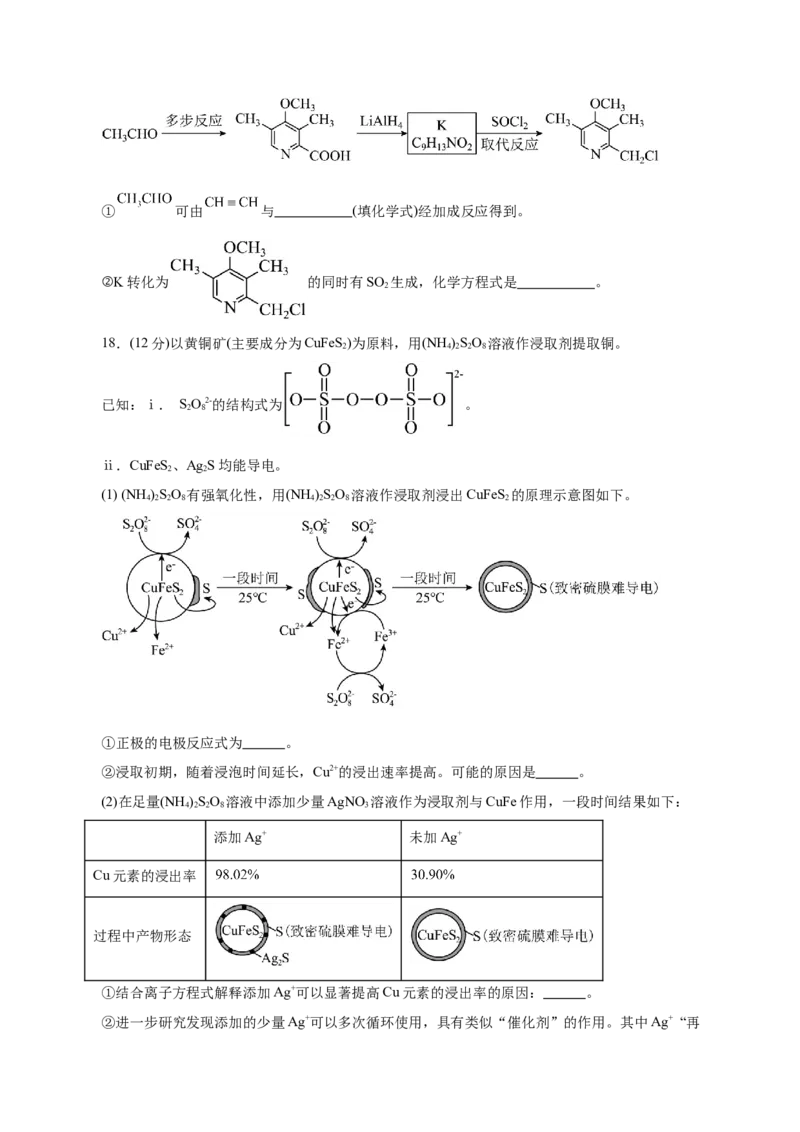
(5)常压下,在某催化剂作用下按照n(C H):n(O )=1:1投料制备乙烯,体系中C H 和 在含碳产物
2 6 2 2 4
中的物质的量分数及C H 转化率随温度的变化关系如图所示。
2 6
①乙烯的物质的量分数随温度升高而降低的原因是_______________________。
②在 温度范围内,下列说法正确的有__________(填标号)。
A.C H 产率随温度升高而增大
2 4B.HO的含量随温度升高而增大
2
C.C H 在体系中的物质的量分数随温度升高而增大
2 6
D.此催化剂的优点是能在较低温度下降低CO的平衡产率
17.(12分)奥美拉唑可用于治疗十二指肠溃疡等疾病,其合成路线如下。
已知: 。
(1)A能与FeCl 溶液作用显紫色,A的名称是 。
3
(2) 的化学方程式是 。
(3)试剂a是 。
(4) 的过程:
①M中含有的官能团有醚键、 。
②N与 反应的化学方程式是 。
(5)合成 的路线如下。① 可由 与 (填化学式)经加成反应得到。
②K转化为 的同时有SO 生成,化学方程式是 。
2
18.(12分)以黄铜矿(主要成分为CuFeS)为原料,用(NH )SO 溶液作浸取剂提取铜。
2 4 2 2 8
已知:ⅰ. SO2-的结构式为 。
2 8
ⅱ.CuFeS、Ag S均能导电。
2 2
(1) (NH )SO 有强氧化性,用(NH )SO 溶液作浸取剂浸出CuFeS 的原理示意图如下。
4 2 2 8 4 2 2 8 2
①正极的电极反应式为 。
②浸取初期,随着浸泡时间延长,Cu2+的浸出速率提高。可能的原因是 。
(2)在足量(NH )SO 溶液中添加少量AgNO 溶液作为浸取剂与CuFe作用,一段时间结果如下:
4 2 2 8 3
添加Ag+ 未加Ag+
Cu元素的浸出率
过程中产物形态
①结合离子方程式解释添加Ag+可以显著提高Cu元素的浸出率的原因: 。
②进一步研究发现添加的少量Ag+可以多次循环使用,具有类似“催化剂”的作用。其中Ag+ “再生”的离子方程式为: 。
(3)进一步从浸出液中提取铜并使(NH )SO 再生的流程示意图如下。
4 2 2 8
①在空气中焙烧FeC O 得到铁红,反应的化学方程式为 。
2 4
②由滤液B电解(Pt作电极)生成(NH )SO 的总反应的离子方程式为 ;
4 2 2 8
③从能源及物质利用的角度,说明电解滤液B而不直接电解滤液A的优点: 。
19.(13分)某小组探究KCr O 的制备。
2 2 7
已知:i. Cr O(绿色,不溶于水)、Cr3+(绿色)、Cr(OH) (灰绿色,不溶于水)、
2 3 3
[Cr(NO )]3-(玫瑰红色)、Cr O2-(橙色)、CrO2-(黄色)
2 6 2 7 4
ii.HNO 是一种弱酸,易分解:3 HNO =HNO +2NO↑+HO
2 2 3 2
将7.60gCr O 固体和15.15gKNO 固体(物质的量之比为1:3)与过量的KCO 固体混合,高温煅烧得含
2 3 3 2 3
KCrO 的黄色固体,反应如下:Cr O+3KNO +2K CO 2KCrO+2 CO↑+3KNO 。
2 4 2 3 3 2 3 2 4 2 2
(1)KNO 受热分解转化为KNO,反应的化学方程式是 。
3 2
(2) K CrO 转化为KCr O,进行实验Ⅰ:
2 4 2 2 7
①加入HSO ,CrO2-转化为Cr O2-反应的离子方程式是 。
2 4 4 2 7
②无色气泡中的气体有 。
③资料显示溶液变为棕黑色是Cr3+与Cr O2-混合所致。设计实验:取少量棕黑色溶液于试管中,逐滴
2 7
加入NaOH溶液,生成灰绿色沉淀,溶液变为黄色,至不再生成沉淀时,静置,取上清液 (填操作
和现象),证实溶液中存在Cr3+与Cr O2-。
2 7
(3)探究Cr3+的来源
来源1:……
来源2:酸性环境中,Cr O2-与NO -发生氧化还原反应生成Cr3+。
2 7 2
①来源1: 。
②进行实验Ⅱ证实来源2成立,实验操作及现象如下:实验操作 实验现象
溶液由橙色逐渐变为棕黑色,进而变为绿色,过程中无红棕色气体产生。
继续加入NaNO 溶液,溶液变为玫瑰红色,加入1mL1mol·L-1HSO 溶液后,溶
2 2 4
液恢复绿色。
溶液由橙色变为绿色、绿色变为玫瑰红色的反应的离子方程式: 、 。
从平衡移动的角度解释溶液由玫瑰红色变为绿色的原因: 。
(4)为避免KCrO 转化为KCr O 的过程中产生Cr3+,进行实验Ⅲ。
2 4 2 2 7
将煅烧后的黄色固体浸泡于100mL水中,过滤后向滤液中加入醋酸溶液,调至pH=5,溶液变为橙色。
实验Ⅲ中溶液的颜色与实验Ⅰ中的不同的原因可能是 。