文档内容
微专题 03 以物质的量为中心的计算
1.(2023·浙江·高考真题)关于反应 ,下列说
法正确的是
A.生成 ,转移 电子 B. 是还原产物
C. 既是氧化剂又是还原剂 D.若设计成原电池, 为负极产物
【答案】A
【解析】A.由方程式可知,反应生成1mol一氧化二氮,转移4mol电子,故A正确;
B.由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,故B错误;
2
C.由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,铁元素
2
的化合价降低被还原,铁离子是反应的氧化剂,故C错误;
D.由方程式可知,反应中铁元素的化合价降低被还原,铁离子是反应的氧化剂,若设计
成原电池,铁离子在正极得到电子发生还原反应生成亚铁离子,亚铁离子为正极产物,故
D错误;
故选A。
2.(2022·全国·高考真题) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
【答案】C
【解析】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质
资料收集整理【淘宝店铺:向阳百分百】 1
学科网(北京)股份有限公司的量,故A错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于
3 3
2.0N ,故B错误;
A
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生
成7molCO ,则0.2mol苯甲酸完全燃烧生成1.4molCO ,数目为1.4N ,故C正确;
2 2 A
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的
2
重量为Cu的质量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的
物质的量为0.2mol,数目为0.2N ,故D错误;
A
答案选C。
3.(2022·浙江·统考高考真题)某同学设计实验确定Al(NO ) ·xH O的结晶水数目。称取样
3 3 2
品7.50g,经热分解测得气体产物中有NO 、O 、HNO 、H O,其中H O的质量为3.06g;残
2 2 3 2 2
留的固体产物是Al O ,质量为1.02g。计算:
2 3
(1)x=_______(写出计算过程)。
(2)气体产物中n(O )_______mol。
2
【答案】(1)9
(2)0.0100
【解析】(1)Al(NO ) ·xH O的摩尔质量为(213+18x)g/mol,根据固体产物氧化铝的质量为
3 3 2
1.02g,可知样品中n(Al)= ,则 ,解得
x=9。
(2)气体产物中n(H O)=3.06g÷18g/mol=0.17mol,则n(HNO )=0.02×9×2-0.17×2=0.02mol,
2 3
根据氮元素守恒,n(NO )=样品中N的物质的量-HNO 中N的物质的量=0.02×3-
2 3
0.02=0.04mol,根据氧元素守恒,n(O )=(0.02×18-0.17-0.02×3-0.04×2-0.03)÷2=0.0100mol。
2
化学计算中的四种常用方法
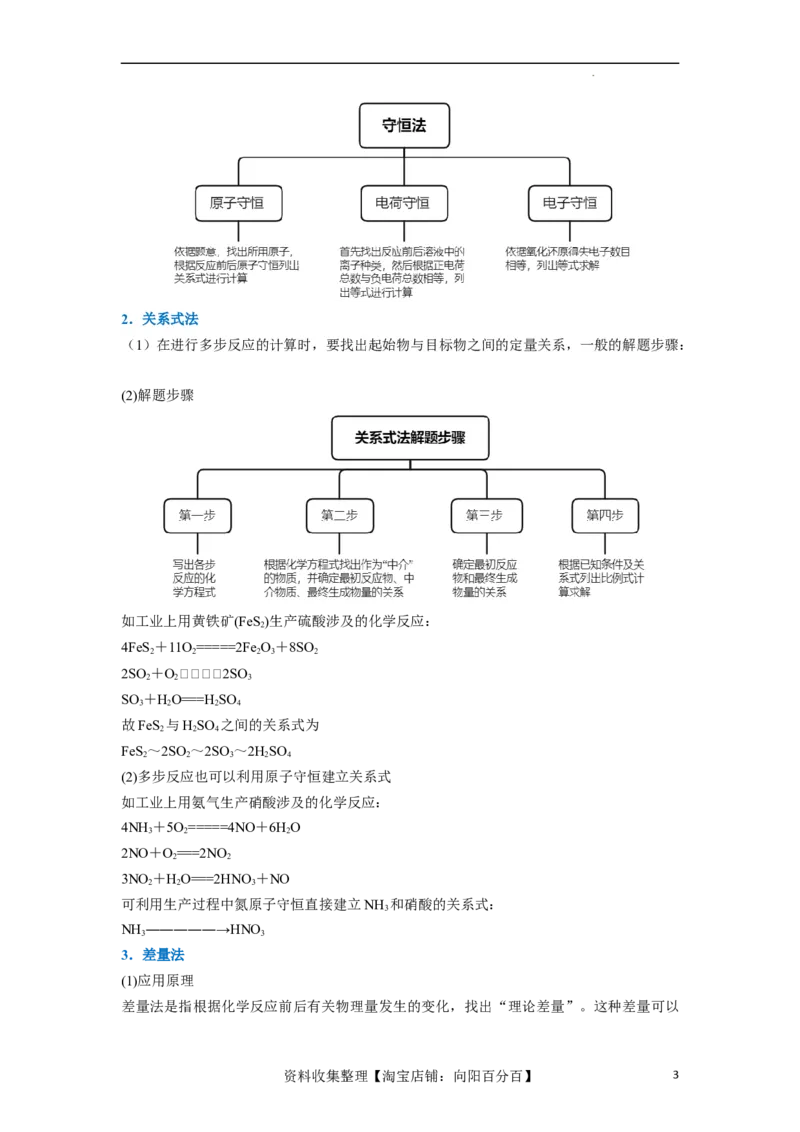
1.守恒法
资料收集整理【淘宝店铺:向阳百分百】 2
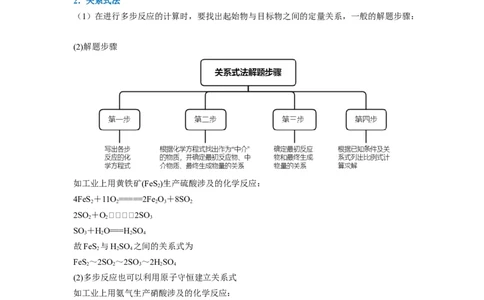
学科网(北京)股份有限公司2.关系式法
(1)在进行多步反应的计算时,要找出起始物与目标物之间的定量关系,一般的解题步骤:
(2)解题步骤
如工业上用黄铁矿(FeS )生产硫酸涉及的化学反应:
2
4FeS+11O=====2Fe O+8SO
2 2 2 3 2
2SO +O2SO
2 2 3
SO +HO===H SO
3 2 2 4
故FeS 与HSO 之间的关系式为
2 2 4
FeS~2SO ~2SO ~2HSO
2 2 3 2 4
(2)多步反应也可以利用原子守恒建立关系式
如工业上用氨气生产硝酸涉及的化学反应:
4NH +5O=====4NO+6HO
3 2 2
2NO+O===2NO
2 2
3NO +HO===2HNO +NO
2 2 3
可利用生产过程中氮原子守恒直接建立NH 和硝酸的关系式:
3
NH ―――――→HNO
3 3
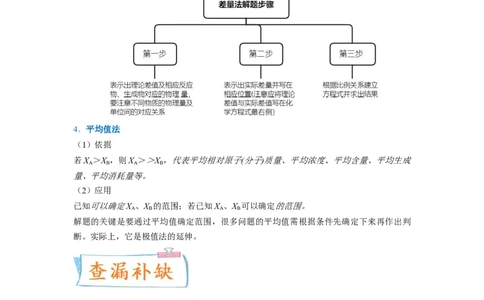
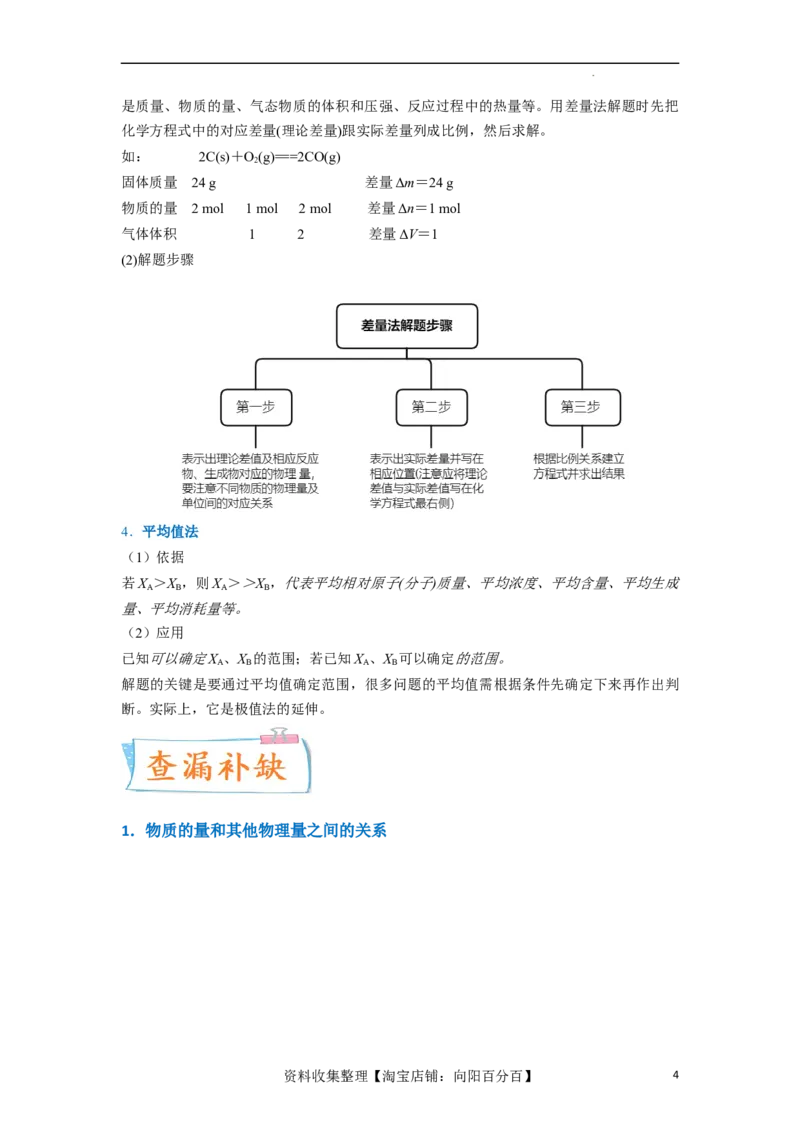
3.差量法
(1)应用原理
差量法是指根据化学反应前后有关物理量发生的变化,找出“理论差量”。这种差量可以
资料收集整理【淘宝店铺:向阳百分百】 3
学科网(北京)股份有限公司是质量、物质的量、气态物质的体积和压强、反应过程中的热量等。用差量法解题时先把
化学方程式中的对应差量(理论差量)跟实际差量列成比例,然后求解。
如: 2C(s)+O(g)===2CO(g)
2
固体质量 24 g 差量Δm=24 g
物质的量 2 mol 1 mol 2 mol 差量Δn=1 mol
气体体积 1 2 差量ΔV=1
(2)解题步骤
4.平均值法
(1)依据
若X >X ,则X >>X ,代表平均相对原子(分子)质量、平均浓度、平均含量、平均生成
A B A B
量、平均消耗量等。
(2)应用
已知可以确定X 、X 的范围;若已知X 、X 可以确定的范围。
A B A B
解题的关键是要通过平均值确定范围,很多问题的平均值需根据条件先确定下来再作出判
断。实际上,它是极值法的延伸。
1.物质的量和其他物理量之间的关系
资料收集整理【淘宝店铺:向阳百分百】 4
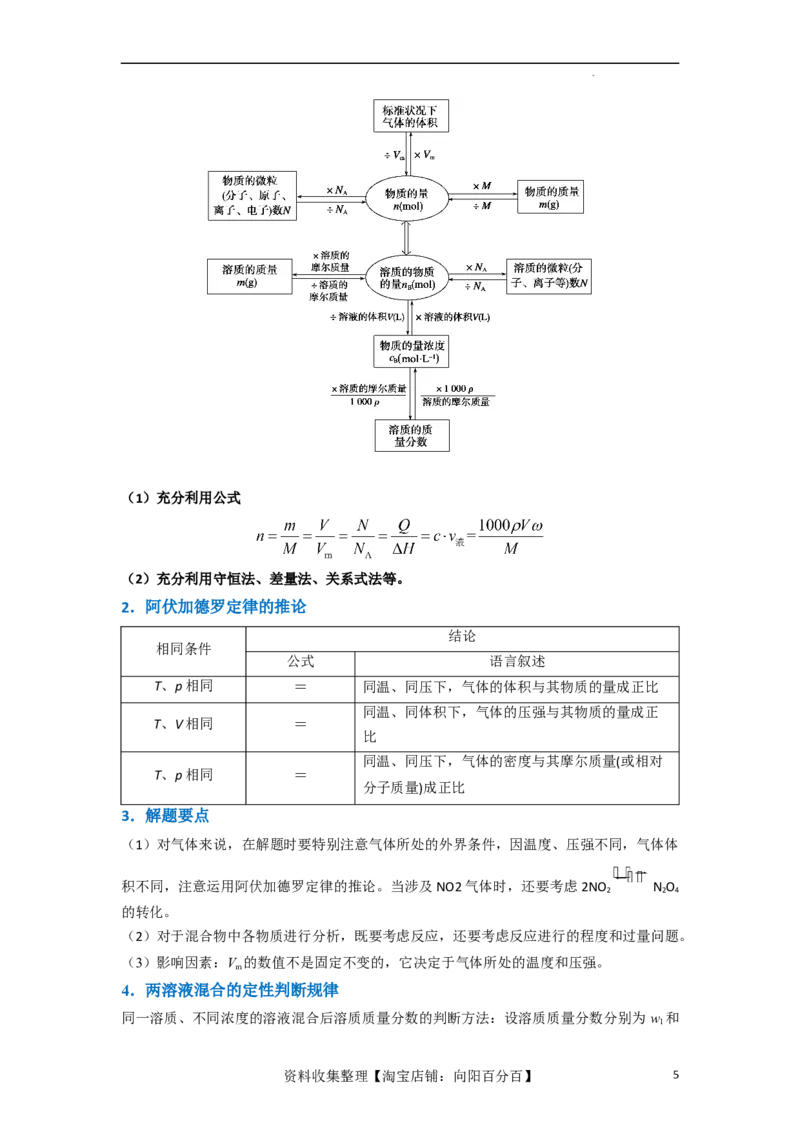
学科网(北京)股份有限公司(1)充分利用公式
(2)充分利用守恒法、差量法、关系式法等。
2.阿伏加德罗定律的推论
结论
相同条件
公式 语言叙述
T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
同温、同体积下,气体的压强与其物质的量成正
T、V相同 =
比
同温、同压下,气体的密度与其摩尔质量(或相对
T、p相同 =
分子质量)成正比
3.解题要点
(1)对气体来说,在解题时要特别注意气体所处的外界条件,因温度、压强不同,气体体
积不同,注意运用阿伏加德罗定律的推论。当涉及NO2气体时,还要考虑2NO N O
2 2 4
的转化。
(2)对于混合物中各物质进行分析,既要考虑反应,还要考虑反应进行的程度和过量问题。
(3)影响因素:V 的数值不是固定不变的,它决定于气体所处的温度和压强。
m
4.两溶液混合的定性判断规律
同一溶质、不同浓度的溶液混合后溶质质量分数的判断方法:设溶质质量分数分别为 w 和
1
资料收集整理【淘宝店铺:向阳百分百】 5
学科网(北京)股份有限公司w 的两溶液混合后所得溶液溶质的质量分数为w。
2
(1)两溶液等质量混合:w=。
(2)两溶液等体积混合
①若溶液的密度大于溶剂的密度,则w>,如HSO 溶液。
2 4
②若溶液的密度小于溶剂的密度,则w<,如氨水、酒精溶液。
5.溶液配制操作的注意事项
(1)仪器的选用要注意思维有序,从配制步骤角度排查还需要的仪器。
(2)用玻璃棒引流时,玻璃棒末端应插入刻度线以下并接触瓶壁,但玻璃棒不能接触瓶口。
(3)溶液配制过程中,若有任何引起误差的操作均应重新配制。
(4)导致溶液浓度偏低的错误操作:NaOH在称量纸上称量;左码右物(用游码);洗涤或转移
时溶液溅出;未洗涤烧杯及玻璃棒;超过刻度线时用胶头滴管吸出液体;定容时仰视;定
容摇匀后发现液面低于刻度线再加水。
(5)导致溶液浓度偏高的错误操作:砝码生锈;定容时俯视;未等溶液冷却至室温就定容。
1.(2022·浙江·统考高考真题)关于反应4CO +SiH 4CO+2H O+SiO ,下列说法
2 4 2 2
正确的是
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
【答案】D
【解析】A.根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A错
误;
B.硅元素化合价由-4价升为+4价,故SiH 发生氧化反应,B错误;
4
C.反应中氧化剂为二氧化碳,还原剂为SiH ,,则氧化剂与还原剂的物质的量之比为
4
4:1,C错误;
D.根据反应方程式可知,Si元素的化合价由-4价升高至+4价,因此生成1molSiO 时,转
2
移8mol电子,D正确;
答案选D。
2.(2022·浙江·统考高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
资料收集整理【淘宝店铺:向阳百分百】 6
学科网(北京)股份有限公司【答案】A
【解析】A.1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量0.01mol/L
2
1L=0.01mol,OH-的数目为0.01N ,A正确;
A
B.1.8g重水(D O)的物质的量为:0.09mol,所含质子数为0.9N ,B错误;
2 A
C.足量的浓盐酸与8.7gMnO (0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数目为
2
0.2N ,C错误;
A
D.甲醇的结构简式为:CH OH,32g (1mol)的分子中含有C—H键的数目为3N ,D错误;
3 A
答案选A。
3.(2022·辽宁·统考高考真题)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为0.01N
A
【答案】A
【解析】A.1个 原子中含有10个中子, 的物质的量为 ,故
中含有中子的物质的量为 ,中子数为 ,故A正确;
B.乙烯分子的结构式为 ,1个乙烯分子中含有5个 键, 的物
质的量为 ,所以 分子中含有的 键数目为 ,B错误;
C. 是共价化合物, 分子中不存在 ,故C错误;
D.没有给出 溶液的体积,无法计算 的 溶液中 的数目,故D错
误;
选A。
一、与物质的量有关的计算
(1)根据 进行相关的计算
1.(2023·广东·模拟预测)我国科学家发现了用 介导苯胺氢解生成苯和氨气的化学链
循环方法,其过程如图所示。设阿伏加德罗常数的值为 ,下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】 7
学科网(北京)股份有限公司A. 苯胺中 键数目为 B.反应 电子转移数目为
C. 中约含电子数目为 D.生成 苯需消耗 分子数目为
【答案】B
【解析】A. 苯胺中含有1mol-NH ,含有的 键数目为 ,A错误;
2
B.LiH中H显-1价,反应时生成H ,故反应 电子转移数目为 ,B正确;
2
C.-NH 含有9个电子, 中约含电子数目为 ,C错误;
2
D.计量气体体积时,需要说明温度与压强,D错误;
故选B。
2.(2022秋·重庆万州·高三校考阶段练习)有以下四种气体:①3.01×1023个HCl分子;
②13.6gH S;③2gD ;④0.2molNH 。下列关系正确的是
2 2 3
A.质量:②>①>④>③
B.分子个数:①>③>②>④
C.物质的量:③>①>②>④
D.氢原子数:③>②>④>①
【答案】D
【解析】①3.01×1023个HCl分子的物质的量为0.5mol;②13.6gH S为0.4mol;③2gD 为
2 2
0.5mol;④0.2molNH 。
3
A.①3.01×1023个HCl分子;②13.6gH S;③2gD ;④0.2molNH 的质量分别为18.25g、
2 2 3
13.6g、2g、3.4g,故质量:①>②>④>③,故A错误;
B.四者的物质的量分别为0.5mol、0.4mol、0.5mol、0.2mol,分子个数:①=③>②>④,
故B错误;
C.由分析可知,物质的量:①=③>②>④,故C正确;
D.四者所含的氢原子的物质的量分别为0.5mol、0.8mol、1.0mol、0.6mol,氢原子数:
③>②>④>①,故D正确。
故选D。
(2)结合气体物质与N 的计算
A
3.(2023春·河北沧州·高三校联考期中)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.14g乙烯和丙烯的混合气体中含有 键和 键的总数为3N
A
资料收集整理【淘宝店铺:向阳百分百】 8
学科网(北京)股份有限公司B.1molCl 溶于水,充分反应后转移电子的数目为N
2 A
C.2molCO 与3molNaOH在水中完全反应,溶液中 的数目为N
2 A
D.标准状况下,11.2LNO和5.6LO 充分混合后,所得分子的数目为0.5N
2 A
【答案】A
【解析】A.已知乙烯分子中含有5个 键和1个 键,丙烯分子中含有8个 键和1 键,
设14g乙烯和丙烯的混合气体中乙烯为xg,则丙烯为(14-x)g中含有 键和 键的总数为
=3N ,A正确;
A
B.已知Cl 溶于水后只有部分Cl 与水反应,故无法计算1molCl 溶于水,充分反应后转移
2 2 2
电子的数目,B错误;
C.根据反应2NaOH+CO =Na CO +H O、NaOH+CO =NaHCO 可知,2molCO 与3molNaOH在
2 2 3 2 2 3 2
水中完全反应生成1molNa CO 和1molNaHCO ,由于碳酸根离子的水解程度大于碳酸氢根
2 3 3
离子的电离程度,故溶液中 的数目大于N ,C错误;
A
D.标准状况下,11.2L即 =0.5molNO和5.6L即 =0.25molO 充分混合
2
后,由反应2NO+O =2NO ,2NO N O 可知所得分子的数目小于0.5N ,D错误;
2 2 2 2 4 A
故答案为:A。
4.(2023·天津·模拟预测)设 为阿伏加德罗常数的值。下列叙述正确的是
A.4℃时, 中含有氢离子数为
B.一定温度下, 和 混合气体中含有的电子数为
C.标准状况下, 通入水中充分反应,生成的 为
D. 与足量 反应生成 时,转移电子数为
【答案】B
【解析】A.18 mL水的质量为18g,物质的量为 ,水是弱电解质,
无法完全电离,含有的氢离子数小于 ,A错误;
B. 和 的相对分子质量都为44,且都是 分子,所以无论以何种比例混合,
和 混合气体的物质的量为 ,含有的电子总数均为
,B正确;
C.标准状况下, 不是气体,无法用气体摩尔体积计算物质的量,C错误;
D.根据关系式: [提示: ],生成 的
资料收集整理【淘宝店铺:向阳百分百】 9
学科网(北京)股份有限公司物质的量为 时,转移电子数应为 ,D错误;
故选:B。
(3)根据 进行相关计算
5.(2023春·河北保定·高三河北安国中学校联考阶段练习) 是阿伏加德罗常数的值,
下列说法正确的是
A.25℃、101kPa下,67.2L 溶于水后,转移的电子数为2
B.常温下,1 溶液中含有的阳离子数为
C.42g 中含有非极性共价键的数目可能为3
D.2.2g 中含有的中子数为
【答案】C
【解析】A.25℃、101kPa不是标准状况,67.2L 的物质的量不是3mol,溶于水后,
转移的电子数不是2 ,故A错误;
B.未说明1 溶液的体积,无法计算溶液中含有的阳离子数,故B错误;
C.42g 的物质的量为 =1mol,若 为环丙烷,其中含有3个非极性共价键,
则1mol 中含有非极性共价键的数目可能为3 ,故C正确;
D. 中含有12个中子,2.2g 的物质的量为 =0.1mol,含有的中子数
为1.2 ,故D错误;
故选C。
6.(2023春·湖北宜昌·高三统考期中)设 为阿伏加德罗常数的值,下列说法错误的是
A.常温常压下,3.2g甲醇( )中含有的 键数目为
B.4g氘化锂( )含中子数为
C. 溴化铵水溶液中 与 离子数之和大于
D.3mol的 与 完全反应时转移的电子数为
【答案】D
【解析】A. 中C原子和O原子都是sp3杂化, 中含有4个 键,3.2g
甲醇的物质的量为 =0.1mol,含有的 键数目为 ,A正确;
资料收集整理【淘宝店铺:向阳百分百】 10
学科网(北京)股份有限公司B. 中含有1+6-3=4个中子,4g氘化锂( )的物质的量为 =0.5mol,含中子数
为 ,B正确;
C. 溴化铵水溶液中c(Br-)=1mol/L,该溶液中存在电荷守恒c( )+c( )=c(Br-)
+c(OH-)>1mol/L,则 与 离子数之和大于 ,C正确;
D. 与 反应的化学方程式为: ,该反应消耗3个
分子转移的电子数为2个,则有3mol的 参与反应时,转移的电子数为2 ,D错误;
故选D。
(4)结合氧化还原反应知识与N 的相关计算
A
7.(2023秋·福建龙岩·高三校联考期末)电催化 还原制氨是一种很有吸引力的替代方
法,它可以在较温和的条件下实现氨的合成(反应表达式为: )。
设 为阿伏加德罗常数的值,下列说法正确的是
A.电催化还原制氨实现化学能向电能转变
B.每产生34 g , 得到的电子数为
C.1 L 1 mol·L 氨水中, 分子数数为
D.消耗11.2 L 时,产生的 分子数为
【答案】B
【解析】A.电催化还原制氨实现电能向化学能转变,A错误;
B.每产生34 g ,表示有2摩尔氮原子由零价降低到-3价,所以 得到的电子数为
,B正确;
C.1 L 1 mol·L 氨水中, 发生部分电离,分子数小于 ,C错误;
D.标准状况下,消耗11.2 L 时,产生的 分子数为 ,D错误;
故选B。
8.(2023秋·辽宁朝阳·高三校联考期末)黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例
混合而成的,爆炸时的反应为 。下列说法正确的是
A.该反应的氧化剂是C,还原剂是 、S
B.当有 参加反应时,生成 的体积为
C.当有 生成时,转移电子数约为
D.当有 参加反应时,被 氧化生成的 为
【答案】D
资料收集整理【淘宝店铺:向阳百分百】 11
学科网(北京)股份有限公司【解析】A.根据元素化合价的变化可知,该反应的氧化剂是 、S,还原剂是C,A错
误;
B.末指明是否为标准状况,不能根据标准状况下气体摩尔体积计算气体的体积,B错误;
C.当有 生成时,有 电子转移,即转移电子数为 ,C错误;
D.当有 参加反应时,有 参加反应,即得到 电子,根据得失电子守
恒,被 氧化生成的二氧化碳为 ,D正确;
故选D。
(5)结合物质结构基础知识与N 的相关计算
A
9.(2023·湖南娄底·统考模拟预测) 为阿伏加德罗常数的值。硫、氟及其化合物在生
产、生活中有广泛应用。下列有关叙述正确的是
A.0.2mol 和0.3mol 混合反应转移电子数最多为
B.标准状况下,11.2LHF含原子总数为
C.1mol (如图所示)分子含 键数为
D.32g 、 、 的混合物中含S原子数为
【答案】A
【解析】A. ,0.2mol 与0.3mol 完全反应,转移0.4mol电
子,A项正确;
B.标准状况下,HF为液体,不确定其物质的量,B项错误;
C.1个 分子含6个单键,则1mol (如图所示)分子含 键数为 ,C项错误;
D.32g硫的单质含1molS,含S原子数为 ,D项错误。
故选A。
10.(2023·全国·高三专题练习)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.14 g C H 和CO的混合气体中所含质子总数等于8N
2 4 A
B.1 mol P S ( )中所含P—S键的数目为6N
4 3 A
资料收集整理【淘宝店铺:向阳百分百】 12
学科网(北京)股份有限公司C.常温下,将5.6 g铁块投入足量浓硝酸中,转移0.3N 电子
A
D.11.2 L Cl 与足量乙烷在光照条件下反应产生HCl分子的总数为0.5N
2 A
【答案】B
【解析】A.乙烯和一氧化碳的相对分子质量都为28,但是一个乙烯分子中含有16个质子,
而一个一氧化碳分子中含有14个质子,故质子总数不能计算,A错误;
B.从图分析,一个分子中含有6个磷硫键,故1mol该物质含有6mol磷硫键,B正确;
C.常温下铁在浓硝酸中钝化,不能计算,C错误;
D.未指明状态,不能计算氯气的物质的量,D错误;
故选B。
(6)以 为中心有关基本粒子的计算
11.(2023·全国·统考模拟预测)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.28.0gN 和足量的H 反应生成NH 的数目为2N
2 2 3 A
B.13.2gCrO (Cr元素的化合价为+6)分子中含过氧键的数目为0.2N
5 A
C.4.6gC H O中含有C-H键的数目为0.6N
2 6 A
D.标准状况下,11.2LHF含有的分子数为0.5N
A
【答案】B
【解析】A.28.0g 的物质的量为1mol, 与 生成 的反应为可逆反应,反应生成
的数目小于 ,A项错误;
B. 中Cr元素的化合价为+6,则 可写成 ,13.2g 的物质的量为
0.1mol,其中含过氧键的数目为 ,B项正确;
C.4.6g 的物质的量是0.1mol, 表示的物质可能是乙醇,也可能是二甲醚,
也可能是二者的混合物,因此含有C—H键的数目为 ,C项错误;
D.标准状况下HF不是气体,不能根据标准状况下的气体摩尔体积计算,D项错误;
故选B。
12.(2023·辽宁葫芦岛·统考一模)设 为阿伏加德罗常数的值,下列说法正确的是
A.室温下34.2 g蔗糖完全水解形成的葡萄糖分子数为
B.70 g 的烃分子中含有 键的数目一定为
C.1 mol 与足量的 反应,转移的电子数为
D.2.0 g 中所含质子数为
【答案】A
【解析】A.蔗糖相对分子质量为342,每摩尔蔗糖完全水解生成1mol葡萄糖和1mol果糖,
资料收集整理【淘宝店铺:向阳百分百】 13
学科网(北京)股份有限公司34.2g蔗糖物质的量为0.1mol, 完全水解生成的葡萄糖分子数为0.1N ,A正确;
A
B.70g该分子物质的量为1mol,该分子可能是不饱和的烯烃,含有C-C 键4N ,也可能
A
是饱和的环烷烃,含有C-C 键5N ,B错误;
A
C. 与 反应生成 为可逆反应,1mol 与足量 反应时转移的电子数小于2N ,
A
C错误;
D.1个 分子含有10个质子, 的相对分子质量为22,2.0g 中含有的质子
数为: ,D错误;
故选A。
(7)化学方程式计算中物质的量的运用
13.(2023春·上海宝山·高三上海市行知中学校考阶段练习)汽车剧烈碰撞时,安全气囊
中发生反应10NaN +2KNO →K O+5Na O+16N ↑。若氧化物比还原物多 1.75mol,则下列判
3 3 2 2 2
断正确的是
A.生成40.32 LN (标准状况) B.有0.250molKNO 被氧化
2 3
C.转移电子的物质的量为1.75mol D.被氧化的N 原子的物质的量为3.75mol
【答案】D
【解析】根据分析16mol氮气中有15mol氮气是氧化产物,有1mol氮气是还原产物,则氧
化产物比还原产物多14mol,若氧化物比还原物多 1.75mol,则说明生成氮气2mol。
A.根据前面分析生成氮气2mol即标准状况44.8 LN ,故A错误;
2
B.KNO 中氮化合价降低,是KNO 被还原,故B错误;
3 3
C.根据方程式分析转移10mol电子,得到的氧化产物比还原产物多14mol,若氧化物比还
原物多 1.75mol,则转移电子的物质的量为1.25mol,故C错误;
D.根据方程式分析被氧化的N原子物质的量为30mol,得到的氧化产物比还原产物多
14mol,若氧化物比还原物多 1.75mol,则被氧化的N 原子的物质的量为3.75mol,故D正
确。
综上所述,答案为D。
14.(2023·全国·高三专题练习)镁带在空气中燃烧生成的固体产物主要是氧化镁和氮化镁。
将燃烧后的固体产物溶解在60mL浓度为2.0mol/L的盐酸溶液中,(氮化镁和盐酸反应的化
学方程式为:Mg N +8HCl=3MgCl +2NH Cl)以20mL0.5mol/L的氢氧化钠溶液中和多余的盐酸,
3 2 2 4
然后在此溶液中加入过量的碱,把氨全部蒸发出来,用稀盐酸吸收,稀盐酸增重0.17g。镁
带的质量为
A.0.6g B.1.2g C.2.4g D.3.6g
【答案】B
【解析】加入氢氧化钠溶液中和多余的盐酸后,溶液中仅有MgCl 、NH Cl和NaCl,根电荷
2 4
资料收集整理【淘宝店铺:向阳百分百】 14
学科网(北京)股份有限公司守恒的原理:n(NH +)+n(Na+)+2n(Mg2+)=n(Cl-),n(Mg2+)= (0.06L×2.0mol/L-
4
-0.02L×0.5mol/L)=0.05mol,m(Mg)=0.05mol×24g/mol=1.2g。
二、与物质的量浓度有关的计算
(1)依据物质的量浓度公式的基本计算
15.(2023·广东湛江·统考二模)设 为阿伏加德罗常数的值。下列说法正确的是
A.50℃, 的 溶液中含有 的数目为
B. 的 溶液中含 分子的数目为
C. 和 于密闭容器中充分反应后,分子总数为
D.浓度均为 的 溶液和 溶液中, 数目均为
【答案】A
【解析】A. 的 溶液中c(H+)=10-12mol/L, 的数目为1L×10-12mol/
L×N mol-1= ,故A正确;
A
B. 溶液中HCl完全电离,没有HCl分子,故B错误;
C. 和 发生反应:2 + =2NO , 和 于密闭容器中充分反应后,
2
生成0.2mol NO ,但NO 中存在2NO N O ,因此充分反应后,分子物质的量小于
2 2 2 2 4
0.2mol,故C错误;
D.未说明溶液的体积,无法计算 数目,故D错误;
故选A。
16.(2023·上海宝山·统考二模)标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,
溶液pH先增大后减小,当通入SO 112mL时,溶液pH最大,则原氢硫酸溶液的物质的量
2
浓度为_____mol·L-1。
A.0.1 B.0.05 C.0.01 D.0.005
【答案】A
【解析】H S水溶液中存在H S的电离而显酸性,起始pH<7,将SO 气体通入H S水溶液中
2 2 2 2
时先发生2H S+SO = S↓+2H O,该过程中H S的浓度不断减小,酸性减弱,pH增大,当完
2 2 2 2
全反应时,溶液呈中性、溶液pH最大,继续通入SO ,生成亚硫酸,PH减小。. 通入
2
SO 112mL时,SO 的物质的量为 =5 10-3 mol,则H S的物质的量为2×5 10-3
2 2 2
mol=10-2 mol,则氢硫酸溶液的物质的量浓度为 =0.1mol/L,A项正确;
答案选A。
(2)与溶质成分有关的计算
资料收集整理【淘宝店铺:向阳百分百】 15
学科网(北京)股份有限公司17.(2023·重庆九龙坡·重庆市育才中学校考三模)设 为阿伏加德罗常数的值。下列说
法正确的是
A. 石墨中含有的 键电子数为
B. 的 溶液中含有的阴离子总数为
C. 羟基和 中含有的质子数均为
D. 的浓硫酸与足量铜反应转移的电子数为
【答案】C
【解析】A.石墨是由碳原子构成的六边形平面网状结构,其中C原子以sp2杂化轨道与邻
近的3个C原子形成无限的六边形平面网状结构。每个C原子还有1个与碳环平面垂直的
未杂化的p轨道,并含有1个未成对电子,因此能够形成大 键。 石墨中含有的碳原
子数为,因此 键电子数为 ,故A错误;
B.缺少溶液体积,无法计算微粒数目,故B错误;
C.羟基和 中含有的质子数均为9, 羟基和 的物质的量均为0.1mol,则含
有的质子数均为 ,故C正确;
D.随着反应的进行,浓硫酸变成稀硫酸,稀硫酸与铜不反应,故转移的电子数小于
,故D错误;
故答案选C。
18.(2021秋·新疆阿克苏·高三校考阶段练习)物质的量浓度相同的NaCl、MgCl 、AlCl 三
2 3
种溶液,当溶液体积比为3∶2∶1时,三种溶液中Cl-的物质的量浓度之比为
A.1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.3∶4∶3
【答案】B
【解析】NaCl溶液中c(Cl-)=c(NaCl),MgCl 溶液中c(Cl-)=2c(MgCl ),AlCl 溶液中
2 2 3
c(Cl-)=3c(AlCl ),而c(NaCl)=c(MgCl )=c(AlCl ),则NaCl、MgCl 、AlCl 三种溶液中Cl-的物质的
3 2 3 2 3
量浓度之比为1:2:3,故答案为:B。
(3)溶液配制有关计算
19.(2020·天津河东·高三统考学业考试)实验室需用 的 溶液,现
选用 的容量瓶配制该溶液,下列方法可行的是
A.称取 ,加入 水
B.称取 ,加入 水
C.称取 ,加水配成 溶液
D.称取 ,加水配成 溶液
【答案】C
资料收集整理【淘宝店铺:向阳百分百】 16
学科网(北京)股份有限公司【解析】需要n(CuSO )=n(CuSO •5H O)=0.10mol/L×0.5L=0.05mol,如果称量的是硫酸铜,则
4 4 2
m(CuSO )=0.05mol×160g/mol=8.0g,如果称量的是胆矾,则
4
m(CuSO •5H O)=0.05mol×250g/mol=12.5g,
4 2
A.称取8.0gCuSO ,加入500mL水,则溶液的体积大于500mL,故A错误;
4
B.需要配制的是500mL溶液,故应将8.0gCuSO 溶于水使溶液的体积为500mL,而不是加
4
入到480mL水中,故B错误;
C.需要胆矾的质量为12.5g,且胆矾溶于水中,使所配溶液体积是500mL,故C正确;
D.需要配制的是500mL溶液,故应将12.50g胆矾溶于水使溶液的体积为500mL,而不是
将12.0g胆矾加入到480mL水中,故D错误;
故选:C。
20.(2022·全国·高三专题练习)下列有关溶液配制说法不正确的是
A.在溶液配制过程中,定容时俯视会导致所配溶液浓度偏高
B.取58.5gNaCl固体溶于1L水中,所得溶液物质的量浓度为1mol·L-1
C.取16.0gCuSO 固体溶于水并加水稀释至500mL,所得溶液物质的量浓度为0.2mol·L-1
4
D.10mL5mol·L-1Na SO 溶液加水稀释至100mL,所得溶液浓度为0.5mol·L-1
2 4
【答案】B
【解析】A.在溶液配制过程中,定容时俯视会导致所配溶液的体积偏小,则所配溶液的
浓度偏高,A项正确;
B.58.5gNaCl物质的量为 =1mol,水的体积为1L,所配溶液的体积不等于1L,所
配溶液物质的量浓度不为1mol/L,B项错误;
C.16.0gCuSO 物质的量为 =0.1mol,所配溶液的体积为500mL,则所配CuSO 溶
4 4
液的物质的量浓度为 =0.2mol/L,C项正确;
D.根据稀释前后Na SO 物质的量不变,0.01L 5mol/L=0.1L c(Na SO ) ,解得c(Na SO )
2 4 2 4 后 2 4 后
=0.5mol/L,D项正确;
× ×
答案选B。
(4)溶液稀释的有关计算
21.(2021·全国·高三专题练习)将10mL1.0mol/L 溶液加水稀释至100mL, 物
质的量浓度变为
A.0.1mol/L B.0.2mol/L C.1.0mol/L D.0.5mol/L
【答案】B
【解析】稀释溶液,溶质的物质的量不变,稀释前 物质的量为n=cV=2×10×10-3 L×1.0
资料收集整理【淘宝店铺:向阳百分百】 17
学科网(北京)股份有限公司mol/L =0.02mol,稀释后 物质的量浓度为 =0.2mol/L,故选B。
22.(2022秋·海南省直辖县级单位·高三校考阶段练习)VmL 溶液中含有
mg,取V/4 mL该溶液用水稀释至4VmL,则 物质的量浓度为
A. mol/L B. mol/L C. mol/L D. mol/L
【答案】A
【解析】VmLAl (SO ) 溶液中含有Al3+mg,则 的物质的量为 mol,取 mL该溶液稀
2 4 3
释至4VmL,则 的物质的量为 mol,则其物质的量浓度为 mol÷(4V×10-3)L=
,故答案选A。
(5)溶液混合的有关计算
23.(2022秋·辽宁沈阳·高三辽宁实验中学校考期中)下列叙述中正确的是
A.溶质质量分数为23%和10%的氨水等质量混合,混合液的溶质质量分数小于16.5%
B.同种溶质不同浓度的两种溶液混合,计算时可将体积直接加和
C.若溶质质量分数为 的乙醇溶液的物质的量浓度为 ,则将其加水稀释至溶质
质量分数为 ,所得稀溶液物质的量浓度大于
D.某溶液密度为 ,溶质摩尔质量为 ,若物质的量浓度为 ,则该溶液
的溶质质量分数为
【答案】C
【解析】A.溶质质量分数为23%和10%的氨水等质量混合,假设质量均为m,则混合液的
溶质质量分数 ,故A错误;
B.构成物质的微粒之间有间隔,且同种溶质不同浓度的两种溶液的密度不同,两者混合,
计算时不可将体积直接加和,故B错误;
C.由 可知,c=2y= ,铜离子稀释后c= ,
1 2
, ,乙醇密度小于水,则 ,故 ,故C正确;
D.由 可知,某溶液密度为 ,溶质摩尔质量为 ,若物质的量浓度
资料收集整理【淘宝店铺:向阳百分百】 18
学科网(北京)股份有限公司为 ,则该溶液的溶质质量分数为 ,故D错误;
故选C。
24.(2022·全国·高三专题练习)向200mL0.6mol•L-1Na SO 溶液中加入
2 4
200mL0.2mol•L-1Al (SO ) 溶液(忽略溶液体积的变化),取出100mL混合后溶液加热浓缩至
2 4 3
40mL,浓缩后溶液中c(SO )为
A.1.5mol•L-1 B.1.25mol•L-1 C.1.35mol•L-1 D.2.5mol•L-1
【答案】A
【解析】向 溶液中加入 溶液,混
合后,溶液中硫酸根离子的物质的量为 ,取出
混合后溶液加热浓缩至 ,浓缩后,硫酸根离子的物质的量不变,则此时溶液
中 ,故A正确;
故选A。
1.(2022·浙江·统考高考真题)关于反应 ,下
列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
【答案】B
【解析】A.H SO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发
2 4
生还原反应,A说法不正确;
B.Na S O 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧化
2 2 3 2
剂又是还原剂,B说法正确;
C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的量之比为1:1,
2
C说法不正确;
D.根据其中S元素的化合价变化情况可知,1mol Na S O 发生反应,要转移2 mol电子,D
2 2 3
说法不正确。
综上所述,本题选B。
资料收集整理【淘宝店铺:向阳百分百】 19
学科网(北京)股份有限公司2.(2022·浙江·统考高考真题) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
【答案】C
【解析】A. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子,
的物质的量为0.1mol,因此,其中只含有 个阳离子,A说法不正确;
B.没有指明气体的温度和压强,无法确定 乙烷和丙烯的混合气体的物质的量是多少,
因此,无法确定其中所含碳氢键的数目,B说法不正确;
C. 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为
,C说法正确;
D. 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此,
和 于密闭容器中充分反应后, 分子总数小于 ,D说法不正确。
综上所述,本题选C。
3.(2022·海南·统考高考真题)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿
A
伏加德罗常数的值,下列说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
【答案】A
【解析】2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为
0.3mol,两者发生反应后,Fe完全溶解,而盐酸过量。
A.Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;
B.HCl溶液中Cl-的物质的量为0.3mol,因此,Cl-数为0.3N ,B不正确;
A
C.56Fe 的质子数为26、中子数为30,2.8g56Fe的物质的量为0.05mol,因此,2.8g56Fe含有
的中子数为1.5N ,C不正确;
A
D.反应生成H 的物质的量为0.05mol,在标准状况下的体积为1.12L ,D不正确;
2
综上所述,本题A。
4.(2022·河北·高考真题)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和Mg N ,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
资料收集整理【淘宝店铺:向阳百分百】 20
学科网(北京)股份有限公司D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
【答案】B
【解析】A.过氧化钠与水反应生成氢氧化钠和氧气,则3.9g过氧化钠与足量水反应,转
移电子个数为 ×1×N mol-1=0.05N ,故A错误;
A A
B.镁在空气中燃烧无论生成氧化镁,还是氮化镁,镁均转化为镁离子,则1.2gMg在空气
中燃烧生成氧化镁和氮化镁时,转移电子个数为 ×2×N mol-1=0.1N ,故B正确;
A A
C.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,则2.7g铝与足量氢氧化钠溶液反应生成
氢气的个数为 × ×N mol-1=0.15N ,故C错误;
A A
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠在溶液中发生水解反应,则由
原子个数守恒可知,6.0g二氧化硅与足量氢氧化钠溶液反应所得溶液中硅酸根离子的个数
小于 ×N mol-1=0.1N ,故D错误;
A A
故选B。
5.(2022·福建·统考高考真题)常温常压下,电化学还原制氨气的总反应方程式:
,设 为阿伏加德罗常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
【答案】D
【解析】A.H O分子中孤电子对数为 =2, H O的物质的量为 =0.5mol,
2 2
含有的孤电子对数为 ,故A错误;
B.该反应中N 中N元素化合价由0价下降到-3价,34g 的物质的量为
2
=2mol,每产生 , 得到6mol电子,数目为6N ,故B错误;
A
C.氨水的体积未知,无法计算 的分子数,故C错误;
D. 的物质的量为0.5mol,由方程式可知,消耗0.5mol ,产生的0.75mol ,
数目为 ,故D正确;
资料收集整理【淘宝店铺:向阳百分百】 21
学科网(北京)股份有限公司故选D。
6.(2022·重庆·统考高考真题)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,
2 2 3 A
下列说法正确的是
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
【答案】B
【解析】A.由方程式可知,消耗14g氮气生成氨气的分子数为 ×2×N mol—1=N ,
A A
故A错误;
B.由方程式可知,消耗1mol氢气生成N-H键数为1mol× ×3×N mol—1=2N ,故B正确;
A A
C.由方程式可知,生成标准状况下22.4L氨气,反应电子转移数为 ×3×N mol—
A
1=3N ,故C错误;
A
D.由得失电子数目守恒可知,1mol氨气与氧气反应生成一氧化氮,需氧气分子数为
1mol× ×N mol—1=1.25N ,故D错误;
A A
故选B。
7.(2022·浙江·统考高考真题)联合生产是化学综合利用资源的有效方法。煅烧石灰石反
应: ,石灰石分解需要的能量由焦炭燃烧
提供。将石灰石与焦炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成
,其热量有效利用率为50%。石灰窑中产生的富含 的窑气通入氨的氯化钠饱和溶
液中,40%的 最终转化为纯碱。已知:焦炭的热值为 (假设焦炭不含杂质)。请
回答:
(1)每完全分解 石灰石(含 ,杂质不参与反应),需要投料_______kg焦炭。
(2)每生产106kg纯碱,同时可获得_______ (列式计算)。
【答案】(1)10.8
(2)70
【解析】(1)完全分解 石灰石(含 ,杂质不参与反应),需要吸收的热量
是 =162000kJ,已知:焦炭的热值为 (假设焦炭不含杂
质),其热量有效利用率为50%,所以需要投料焦炭的质量是 =10800g=
资料收集整理【淘宝店铺:向阳百分百】 22
学科网(北京)股份有限公司10.8kg。
(2)根据(1)中计算可知消耗焦炭的物质的量是 =900mol,参加反应的碳酸钙
的物质的量是900mol,这说明参加反应的碳酸钙和焦炭的物质的量之比为1:1,所以根据
原子守恒可知生成氧化钙的质量是 =70kg。
8.(2021·辽宁·高考真题)下列说法正确的是
A. (标准状况)与水充分反应转移 电子
B. 和 均可通过化合反应得到
C.将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D. 与 溶液反应:
【答案】B
【解析】A.由于溶于水中的Cl 只有部分与H O反应,故 (标准状况)与水充分反应
2 2
转移电子数目小于 ,A错误;
B.根据反应:SO +H O=H SO ,Cu+Cl CuCl ,故 和 均可通过化合反应得
3 2 2 4 2 2
到,B正确;
C.将蘸有浓氨水和浓盐酸或浓硝酸的玻璃棒相互靠近,有白烟产生,由于浓硫酸难挥发,
故不能形成白烟,C错误;
D.由于ClO-具有强氧化性,SO 具有强还原性,故 与 溶液反应:
2
,D错误;
故答案为:B。
9.(2021·广东·高考真题)设 为阿伏加德罗常数的值。下列说法正确的是
A. 含有 键的数目为
B. 的盐酸含有阴离子总数为
C. 与 混合后的分子数目为
D. 与足量 反应生成的 分子数目为
【答案】A
【解析】A.1个 分子中含有3个 键,微粒个数与物质的量成正比,故
含有3mol 键, 键的数目为 ,A正确;
B.盐酸为氯化氢的水溶液,氯化氢会全部电离出阴离子Cl-,水会部分电离出阴离子OH-,
水的质量及电离程度未知,故无法计算 的盐酸含有阴离子总数,B错误;
资料收集整理【淘宝店铺:向阳百分百】 23
学科网(北京)股份有限公司C.未提到具体的温度、压强(如标况下),故无法计算 与 混合后的分
子数目,C错误;
D. 为1mol,钠与足量的水反应生成氢气的关系式为: ,故1mol Na应对
应生成0.5mol H , 分子数目应为0.5 ,D错误;
2
故选A。
10.设N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,18gH O中含有的原子总数为3N
2 A
B.标准状况下,0.1molCl 溶于水,转移的电子数目为0.1N
2 A
C.标准状况下,11.2LCH CH OH中含有的分子数目为0.5N
3 2 A
D.常温常压下,2.24LCO和CO 混合气体中含有的碳原子数目为0.1N
2 A
【答案】A
【解析】A.常温常压下,18gH O的物质的量为1mol,一个分子中含有3个原子,则含有
2
的原子总数为3N ,A说法正确;
A
B.标准状况下,0.1molCl 溶于水,少量的氯气与水反应,则转移的电子数目无法确定,B
2
说法错误;
C.标准状况下,CH CH OH为液体,则11.2LCH CH OH的物质的量大于0.5mol,则含有的
3 2 3 2
分子数目大于0.5N ,C说法错误;
A
D.常温常压下,气体摩尔体积大于22.4L/mol,则2.24LCO和CO 混合气体的物质的量小于
2
0.1mol,则含有的碳原子数目小于0.1N ,D说法错误;
A
答案为A。
11.(2021·全国·高考真题) 为阿伏加德罗常数的值。下列叙述正确的是
A. 重水( )中含有的质子数为
B. 的 与 完全反应时转移的电子数为
C. 环状 ( )分子中含有的 键数为
D. 的 溶液中 离子数为
【答案】C
【解析】A. 的质子数为10,18g 的物质的量为 0.9mol, 则 重水(
)中所含质子数为 ,A错误;
B. 与 反应的化学方程式为:3NO +H O=2HNO +NO,该反应消耗3个NO 分子转
2 2 3 2
移的电子数为2个,则有3mol的NO 参与反应时,转移的电子数为 ,B错误;
2
资料收集整理【淘宝店铺:向阳百分百】 24
学科网(北京)股份有限公司C.一个 ( )分子中含有的 键数为8个,32gS 的物质的量为
8
mol,则含有的 键数为 ,C正确;
D.酸性 溶液中存在: ,含Cr元素微粒有 和 ,
则 的 溶液中 离子数应小于 ,D错误;
故选C。
12.(2022·浙江·高考真题)某同学设计实验确定Al(NO ) ·xH O的结晶水数目。称取样品
3 3 2
7.50g,经热分解测得气体产物中有NO 、O 、HNO 、H O,其中H O的质量为3.06g;残留
2 2 3 2 2
的固体产物是Al O ,质量为1.02g。计算:
2 3
(1)x=_______(写出计算过程)。
(2)气体产物中n(O )_______mol。
2
【答案】(1)9
(2)0.0100
【解析】(1)Al(NO ) ·xH O的摩尔质量为(213+18x)g/mol,根据固体产物氧化铝的质量为
3 3 2
1.02g,可知样品中n(Al)= ,则 ,解得
x=9。
(2)气体产物中n(H O)=3.06g÷18g/mol=0.17mol,则n(HNO )=0.02×9×2-0.17×2=0.02mol,根据
2 3
氮元素守恒,n(NO )=样品中N的物质的量-HNO 中N的物质的量=0.02×3-0.02=0.04mol,根
2 3
据氧元素守恒,n(O )=(0.02×18-0.17-0.02×3-0.04×2-0.03)÷2=0.0100mol。
2
资料收集整理【淘宝店铺:向阳百分百】 25
学科网(北京)股份有限公司