文档内容
选择题突破三 A 组 基础巩固练
题组一 离子方程式的正误判断与离子共存
1.(2024·安徽淮北一模)下列离子方程式错误的是 ( )
A.氯化银溶于氨水:AgCl+2NH [Ag(NH)]++Cl-
3 3 2
B.铜与浓硝酸反应:3Cu+8H++2NO-
3Cu2++2NO↑+4H O
3 2 2
C.漂白粉用于环境消毒的原理:Ca2++2ClO-+CO +H O CaCO ↓+2HClO
2 2 3
D.铁上镀锌的阴极反应:Zn2++2e- Zn
2.(2024·湖南名校联盟联考)室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 H SO
溶液:Mg2+、K+、F-、NO-
2 4 3
B.0.1 mol·L-1 Na[Al(OH)
]溶液:Al3+、Na+、Cl-、SO2-
4 4
C.0.1 mol·L-1 Fe (SO )
溶液:Na+、K+、I-、CO2-
2 4 3 3
D.通入大量CO 的溶液中:Na+、Ba2+、CHCOO-、Br-
2 3
3.(2024·广西北海一模)下列过程中的化学反应,相应的离子方程式正确的是( )
A.Fe2+在碱性环境中被空气氧化:4Fe2++O +2H O+8OH- 4Fe(OH) ↓
2 2 3
B.氢氧化铁加入氢碘酸溶液中:Fe(OH) +3H+ Fe3++3H O
3 2
C.用铁作阳极电解氯化镁溶液:Mg2++2Cl-+2H O Mg(OH) ↓+H ↑+Cl↑
2 2 2 2
D.碳酸钙加入乙酸溶液中:CaCO +2H+ Ca2++H O+CO↑
3 2 2
4.(2024·广东名校4月联考)下列日常生产生活涉及的化学反应的离子方程式或电极反应式书写不正
确的是( )
选项 生产生活事实 离子方程式
志愿服务:用“84”消毒液对小区公
A 消毒液生效原理:ClO-+CO +H O
HClO+HCO-
2 2 3
共区域消毒
B 家务劳动:炒完菜的铁锅洗净并擦干 铁锅电化学腐蚀的负极反应:Fe-3e- Fe3+
工业生产:将TiCl 加入大量水中制
4
C TiCl +(x+2)H O TiO ·xHO↓+4H++4Cl-
4 2 2 2
备TiO
2
自主探究:利用氯化铁溶液和覆铜板
D 涉及反应:2Fe3++Cu 2Fe2++Cu2+
制作图案
5.(2024·福建福州二模)常温下,下列各组离子能在指定溶液中大量共存的是( )
A.0.1 mol·L-1 NaHCO
溶液:NH+ 、CO2-
、OH-
3 4 3
B.0.1 mol·L-1 H SO 溶液:Mg2+、ClO-、CHCOO-
2 4 3C.pH=12的氨水:NO-
、Na+、Cl-
3
D.SO
饱和溶液:K+、MnO-
、Ca2+
2 4
6.(2024·辽宁葫芦岛一模)下列方程式能准确解释事实的是( )
A.海水提溴中用SO 水溶液富集溴:SO+Br +2H O
4H++SO2-
+2Br-
2 2 2 2 4
B.以石墨为电极电解饱和食盐水时阳极的电极反应:2H O+2e- 2OH-+H ↑
2 2
C.向苯酚钠溶液通入CO 后变浑浊:
2
2 +H O+CO 2 +Na CO
2 2 2 3
D.三价铁腐蚀铜板:2Fe3++3Cu 2Fe+3Cu2+
7.(2024·辽宁沈阳一模)下列离子方程式书写正确的是( )
A.向酸性高锰酸钾溶液中滴加过氧化氢:2MnO-
+H O+6H+ 2Mn2++3O ↑+4H O
4 2 2 2 2
B.NiSO 溶于氨水形成硫酸六氨合镍溶液:Ni2++6NH·H O [Ni(NH )]2++6H O
4 3 2 3 6 2
C.将水垢中CaSO 转化为CaCO
的原理:Ca2++CO2-
CaCO ↓
4 3 3 3
D.向盐酸中滴加少量碳酸钠溶液:CO2-
+H+
HCO-
3 3
8.(2024·安徽马鞍山一模)某溶液仅由NO- 、Cl-、SO2- 、CO2- 、NH+
、Fe3+和K+中的若干种离子组
3 4 3 4
成,且各离子浓度相等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,得到固体并产生无色气体;
②将①中所得混合物过滤,再将得到的固体洗涤、灼烧又得到固体a;
③向上述滤液中加足量BaCl 溶液,产生白色沉淀。
2
根据以上实验,下列推断错误的是( )
A.根据操作①,推断一定存在NH+
4
B.②中得到固体a为氧化铁
C.原溶液中一定不存在CO2-
,可能含有K+
3
D.说明原溶液中一定存在NO- 、Cl-、SO2- 、NH+
、Fe3+
3 4 4
题组二 氧化还原反应的概念与规律
9.(2024·安徽淮北一模)下列物质的应用与性质不对应的是( )
A.维生素C作抗氧化剂——还原性
B.ClO 作自来水消毒剂——氧化性
2
C.SO 作葡萄酒保鲜剂——漂白性
2
D.Na CO 溶液作除污剂——碱性
2 3
10.(2024·浙江宁波二模)酸性条件下NaS和NaSO 发生反应:2Na S+Na SO +3H SO
2 2 3 2 2 3 2 4
3NaSO +3S↓+3H O,下列说法不正确的是( )(设N 为阿伏加德罗常数的值)
2 4 2 A
A.生成24 g S转移电子的数目为N
AB.Na S是还原剂,发生氧化反应
2
C.Na SO 是氧化产物
2 4
D.碱性条件下S2-和SO2-
可以大量共存
3
11.(2024·浙江衢州模拟)KNO 具有强氧化性,可发生反应:2KNO +2NHCl 2N↑+O ↑+4H O+2KCl,
3 3 4 2 2 2
下列说法不正确的是( )(设N 为阿伏加德罗常数的值)
A
A.N 既是氧化产物,又是还原产物
2
B.KNO 仅作氧化剂
3
C.生成1 mol N 转移电子的数目为5N
2 A
D.每生成36 g水,能产生33.6 L气体(在标准状况下)
12.(2024·浙江嘉兴二模)高铁酸钠(Na FeO)是一种新型绿色消毒剂,主要用于饮用水处理,制备高铁酸
2 4
钠的一种方法是3ClO-+2Fe3++10OH-
2FeO2-
+3Cl-+5H O,下列说法不正确的是( )
4 2
A.Fe3+是还原剂
B.H O既不是还原产物也不是氧化产物
2
C.生成1 mol
FeO2-
时转移6 mol电子
4
D.氧化产物与还原产物的物质的量之比为2∶3
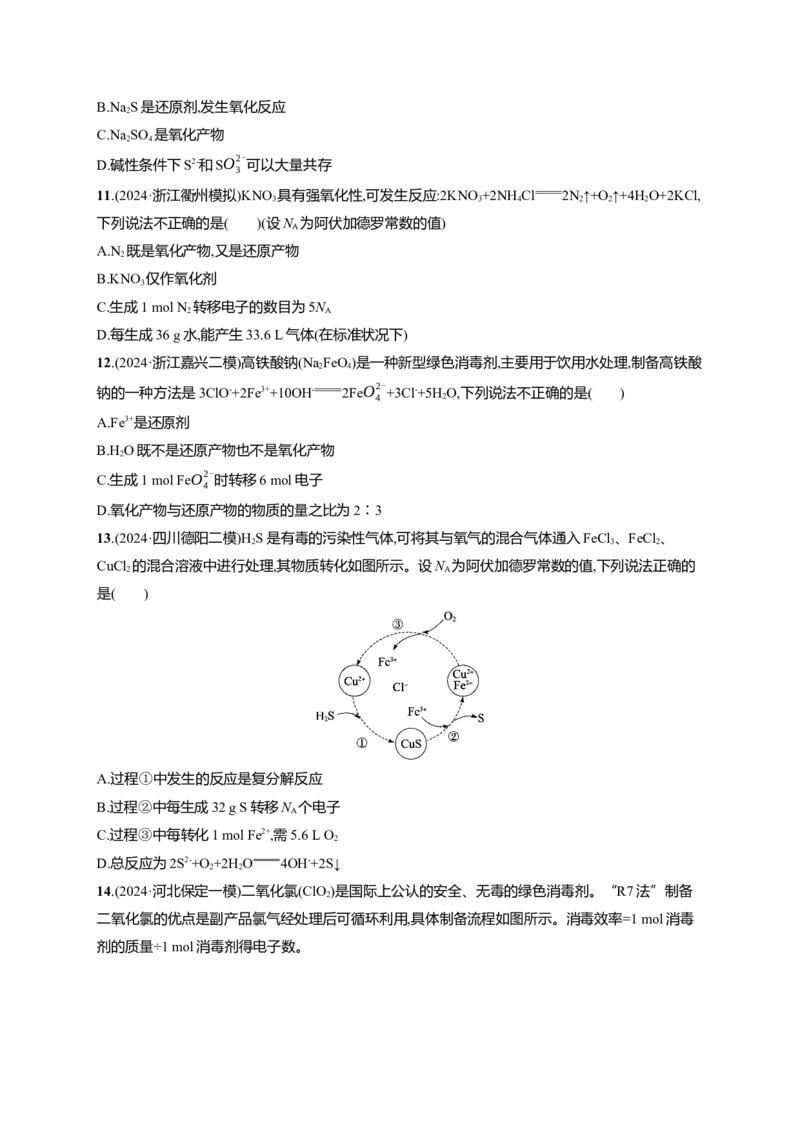
13.(2024·四川德阳二模)H S是有毒的污染性气体,可将其与氧气的混合气体通入FeCl 、FeCl 、
2 3 2
CuCl 的混合溶液中进行处理,其物质转化如图所示。设N 为阿伏加德罗常数的值,下列说法正确的
2 A
是( )
A.过程①中发生的反应是复分解反应
B.过程②中每生成32 g S转移N 个电子
A
C.过程③中每转化1 mol Fe2+,需5.6 L O
2
D.总反应为2S2-+O +2H O 4OH-+2S↓
2 2
14.(2024·河北保定一模)二氧化氯(ClO )是国际上公认的安全、无毒的绿色消毒剂。“R7法”制备
2
二氧化氯的优点是副产品氯气经处理后可循环利用,具体制备流程如图所示。消毒效率=1 mol消毒
剂的质量÷1 mol消毒剂得电子数。下列说法正确的是( )
A.ClO 和Cl 的消毒效率之比为71∶18
2 2
B.反应①生成ClO
的离子方程式:2ClO-
+2Cl-+4H+ 2ClO ↑+2H O+Cl ↑
2 3 2 2 2
C.反应①消耗的硫酸与反应②生成的硫酸的物质的量相等
D.反应②中SO 作还原剂,物质X为HSO
2 2 4
选择题突破三 A 组 基础巩固练
题组一 离子方程式的正误判断与离子共存
1.(2024·安徽淮北一模)下列离子方程式错误的是 ( )
A.氯化银溶于氨水:AgCl+2NH [Ag(NH)]++Cl-
3 3 2
B.铜与浓硝酸反应:3Cu+8H++2NO-
3Cu2++2NO↑+4H O
3 2 2
C.漂白粉用于环境消毒的原理:Ca2++2ClO-+CO +H O CaCO ↓+2HClO
2 2 3
D.铁上镀锌的阴极反应:Zn2++2e- Zn
答案:B
解析:氯化银溶于氨水生成[Ag(NH)]Cl溶液,[Ag(NH )]Cl发生完全电离:AgCl+2NH
3 2 3 2 3
[Ag(NH)]++Cl-,A正确;铜与浓硝酸反应生成Cu(NO )、NO
等,正确的离子方程式为Cu+4H++2NO-
3 2 3 2 2 3
Cu2++2NO↑+2H O,B错误;漂白粉用于环境消毒时,与空气中的CO、HO反应生成CaCO 和
2 2 2 2 3
HClO:Ca2++2ClO-+CO +H O CaCO ↓+2HClO,C正确;铁上镀锌时,在阴极上溶液中的Zn2+得电子
2 2 3
生成Zn,Zn附着在铁镀件表面,则阴极反应为Zn2++2e- Zn,D正确。
2.(2024·湖南名校联盟联考)室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 H SO
溶液:Mg2+、K+、F-、NO-
2 4 3
B.0.1 mol·L-1 Na[Al(OH)
]溶液:Al3+、Na+、Cl-、SO2-
4 4
C.0.1 mol·L-1 Fe (SO )
溶液:Na+、K+、I-、CO2-
2 4 3 3
D.通入大量CO 的溶液中:Na+、Ba2+、CHCOO-、Br-
2 3
答案:D
解析:A项,HF是弱酸,F-能与H+结合生成HF;B项,Al3+与[Al(OH) ]-可发生完全水解反应生成Al(OH)
4 3
沉淀;C项,Fe3+能与I-发生氧化还原反应,Fe3+能与CO2-
发生相互促进的水解反应生成Fe(OH) 沉淀和
3 3
CO 气体。答案选D。
2
3.(2024·广西北海一模)下列过程中的化学反应,相应的离子方程式正确的是( )A.Fe2+在碱性环境中被空气氧化:4Fe2++O +2H O+8OH- 4Fe(OH) ↓
2 2 3
B.氢氧化铁加入氢碘酸溶液中:Fe(OH) +3H+ Fe3++3H O
3 2
C.用铁作阳极电解氯化镁溶液:Mg2++2Cl-+2H O Mg(OH) ↓+H ↑+Cl↑
2 2 2 2
D.碳酸钙加入乙酸溶液中:CaCO +2H+ Ca2++H O+CO↑
3 2 2
答案:A
解析:Fe2+被氧气氧化为Fe3+,Fe3+在碱性环境中生成Fe(OH) 沉淀,A正确;氢氧化铁加入氢碘酸溶液中,
3
反应的离子方程式为2Fe(OH) +6H++2I- 2Fe2++I +6H O,B错误;电解池的阳极材料为铁时,铁失去
3 2 2
电子,反应的离子方程式为Fe+2H O Fe(OH) +H ↑,C错误;碳酸钙加入乙酸溶液中,反应的离子方
2 2 2
程式为CaCO +2CH COOH 2CHCOO-+Ca2++H O+CO↑,D错误。
3 3 3 2 2
4.(2024·广东名校4月联考)下列日常生产生活涉及的化学反应的离子方程式或电极反应式书写不正
确的是( )
选项 生产生活事实 离子方程式
志愿服务:用“84”消毒液对小区公
A 消毒液生效原理:ClO-+CO +H O
HClO+HCO-
2 2 3
共区域消毒
B 家务劳动:炒完菜的铁锅洗净并擦干 铁锅电化学腐蚀的负极反应:Fe-3e- Fe3+
工业生产:将TiCl 加入大量水中制
4
C TiCl +(x+2)H O TiO ·xHO↓+4H++4Cl-
4 2 2 2
备TiO
2
自主探究:利用氯化铁溶液和覆铜板
D 涉及反应:2Fe3++Cu 2Fe2++Cu2+
制作图案
答案:B
解析:“84”消毒液的漂白原理,离子方程式为ClO-+CO +H O
HClO+HCO-
,A正确;钢铁电化学腐
2 2 3
蚀的负极反应为Fe-2e- Fe2+,B错误;TiCl 水解生成TiO ·xHO,将TiCl 加入水中反应的离子方程
4 2 2 4
式为TiCl +(x+2)H O TiO ·xHO↓+4H++4Cl-,C正确;氯化铁溶液腐蚀覆铜板的离子方程式为2Fe3+
4 2 2 2
+Cu 2Fe2++Cu2+,D正确。
5.(2024·福建福州二模)常温下,下列各组离子能在指定溶液中大量共存的是( )
A.0.1 mol·L-1 NaHCO
溶液:NH+ 、CO2-
、OH-
3 4 3
B.0.1 mol·L-1 H SO 溶液:Mg2+、ClO-、CHCOO-
2 4 3
C.pH=12的氨水:NO-
、Na+、Cl-
3
D.SO
饱和溶液:K+、MnO-
、Ca2+
2 4
答案:C解析:A项,HCO- 、NH+
均不能与OH-大量共存;B项,ClO-、CHCOO-都是弱酸的酸根离子,不能与氢
3 4 3
离子大量共存;C项,碱性条件下,各离子之间不相互反应,可以大量共存;D项,MnO-
有强氧化性,二氧
4
化硫有还原性,两者会发生氧化还原反应;故选C。
6.(2024·辽宁葫芦岛一模)下列方程式能准确解释事实的是( )
A.海水提溴中用SO 水溶液富集溴:SO+Br +2H O
4H++SO2-
+2Br-
2 2 2 2 4
B.以石墨为电极电解饱和食盐水时阳极的电极反应:2H O+2e- 2OH-+H ↑
2 2
C.向苯酚钠溶液通入CO 后变浑浊:
2
2 +H O+CO 2 +Na CO
2 2 2 3
D.三价铁腐蚀铜板:2Fe3++3Cu 2Fe+3Cu2+
答案:A
解析:溴单质与二氧化硫在溶液中反应生成强酸硫酸和HBr,A正确;以石墨为电极电解饱和食盐水,
阳极发生氧化反应,氯离子被氧化生成氯气,阳极的电极反应式为2Cl--2e- Cl↑,B错误;向苯酚钠溶
2
液通入CO 后变浑浊,反应生成苯酚和碳酸氢钠,反应的化学方程式为 +H O+CO
2 2 2
+NaHCO,C错误;三价铁腐蚀铜板生成的是二价铁,离子方程式为2Fe3++Cu 2Fe2+
3
+Cu2+,D错误。
7.(2024·辽宁沈阳一模)下列离子方程式书写正确的是( )
A.向酸性高锰酸钾溶液中滴加过氧化氢:2MnO-
+H O+6H+ 2Mn2++3O ↑+4H O
4 2 2 2 2
B.NiSO 溶于氨水形成硫酸六氨合镍溶液:Ni2++6NH·H O [Ni(NH )]2++6H O
4 3 2 3 6 2
C.将水垢中CaSO 转化为CaCO
的原理:Ca2++CO2-
CaCO ↓
4 3 3 3
D.向盐酸中滴加少量碳酸钠溶液:CO2-
+H+
HCO-
3 3
答案:B
解析:酸性KMnO 溶液可氧化HO
生成O,离子方程式为2MnO-
+5H O+6H+ 2Mn2+
4 2 2 2 4 2 2
+5O ↑+8H O,A错误;NiSO 溶于氨水形成硫酸六氨合镍溶液,离子方程式为Ni2++6NH·H O
2 2 4 3 2
[Ni(NH )]2++6H O,B正确;将水垢中的CaSO 转化为CaCO 属于沉淀的转化,离子方程式为CaSO+C
3 6 2 4 3 4
O2-
CaCO
↓+SO2- ,C错误;向盐酸中滴加少量碳酸钠溶液生成水和二氧化碳,离子方程式为CO2-
3 3 4 3
+2H+ HO+CO↑,D错误。
2 2
8.(2024·安徽马鞍山一模)某溶液仅由NO- 、Cl-、SO2- 、CO2- 、NH+
、Fe3+和K+中的若干种离子组
3 4 3 4
成,且各离子浓度相等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,得到固体并产生无色气体;
②将①中所得混合物过滤,再将得到的固体洗涤、灼烧又得到固体a;③向上述滤液中加足量BaCl 溶液,产生白色沉淀。
2
根据以上实验,下列推断错误的是( )
A.根据操作①,推断一定存在NH+
4
B.②中得到固体a为氧化铁
C.原溶液中一定不存在CO2-
,可能含有K+
3
D.说明原溶液中一定存在NO- 、Cl-、SO2- 、NH+
、Fe3+
3 4 4
答案:C
解析:加入过量的碱产生的气体为NH
,说明溶液中有NH+
。由信息②知加入过量的碱产生了
3 4
Fe(OH)
沉淀,溶液中有Fe3+,由于CO2- 与Fe3+不能共存,则溶液中不存在CO2-
。由信息③知溶液中有
3 3 3
SO2- 。由上述分析可知溶液中一定有NH+
,A正确;Fe(OH) 受热分解生成Fe O,B正确;溶液中一定
4 4 3 2 3
有NH+ 、Fe3+及SO2- ,由于溶液中各离子浓度相同,根据电荷守恒可知,溶液中一定还有Cl-和NO-
。
4 4 3
溶液中一定不存在CO2- 和K+,C错误;由C项分析可知溶液中一定存在NH+ 、Fe3+、SO2-
、Cl-和N
3 4 4
O-
,D正确。
3
题组二 氧化还原反应的概念与规律
9.(2024·安徽淮北一模)下列物质的应用与性质不对应的是( )
A.维生素C作抗氧化剂——还原性
B.ClO 作自来水消毒剂——氧化性
2
C.SO 作葡萄酒保鲜剂——漂白性
2
D.Na CO 溶液作除污剂——碱性
2 3
答案:C
解析:维生素C具有还原性,可作抗氧化剂;ClO 具有氧化性,可作自来水消毒剂;SO 可以杀菌消毒,能
2 2
作为葡萄酒的保鲜剂,与漂白性无关;Na CO 溶液呈碱性,可作除污剂;故选C。
2 3
10.(2024·浙江宁波二模)酸性条件下NaS和NaSO 发生反应:2Na S+Na SO +3H SO
2 2 3 2 2 3 2 4
3NaSO +3S↓+3H O,下列说法不正确的是( )(设N 为阿伏加德罗常数的值)
2 4 2 A
A.生成24 g S转移电子的数目为N
A
B.Na S是还原剂,发生氧化反应
2
C.Na SO 是氧化产物
2 4
D.碱性条件下S2-和SO2-
可以大量共存
3
答案:C
解析:硫化钠中硫元素的化合价由-2价变为0价,亚硫酸钠中硫元素的化合价由+4价变为0价,生成3
mol S时转移电子为4 mol,则生成24 g S时转移1 mol电子,数目为N ,A正确;Na S是还原剂,发生氧
A 2化反应,B正确;Na SO
为硫酸生成的,不是氧化产物,C错误;碱性条件下S2-和SO2-
不反应,可以大量
2 4 3
共存,D正确。
11.(2024·浙江衢州模拟)KNO 具有强氧化性,可发生反应:2KNO +2NHCl 2N↑+O ↑+4H O+2KCl,
3 3 4 2 2 2
下列说法不正确的是( )(设N 为阿伏加德罗常数的值)
A
A.N 既是氧化产物,又是还原产物
2
B.KNO 仅作氧化剂
3
C.生成1 mol N 转移电子的数目为5N
2 A
D.每生成36 g水,能产生33.6 L气体(在标准状况下)
答案:B
解析:KNO 中N元素化合价由+5价变为0价,NHCl中N元素化合价由-3价变为0价,则N 既是氧化
3 4 2
产物,又是还原产物,A正确;KNO 中N元素的化合价由+5价变为0价,O元素化合价由-2价变为0价,
3
则KNO 既是氧化剂又是还原剂,B错误;KNO 中N元素的化合价由+5价变为0价,反应消耗2 mol
3 3
KNO 生成2 mol N ,转移10 mol 电子,则生成1 mol N 转移电子的数目为5N ,C正确;由反应可知,每
3 2 2 A
36 g
生成4 mol水产生3 mol气体(N 和O),36 g水的物质的量为 =2 mol,生成2 mol H O
2 2 18 g·mol-1 2
时产生1.5 mol 气体,气体在标准状况下的体积为1.5 mol×22.4 L·mol-1=33.6 L,D正确。
12.(2024·浙江嘉兴二模)高铁酸钠(Na FeO)是一种新型绿色消毒剂,主要用于饮用水处理,制备高铁酸
2 4
钠的一种方法是3ClO-+2Fe3++10OH-
2FeO2-
+3Cl-+5H O,下列说法不正确的是( )
4 2
A.Fe3+是还原剂
B.H O既不是还原产物也不是氧化产物
2
C.生成1 mol
FeO2-
时转移6 mol电子
4
D.氧化产物与还原产物的物质的量之比为2∶3
答案:C
解析:反应中Fe3+的化合价升高到+6价,故Fe3+是还原剂,A正确;反应中H和O的化合价均未改变,故
HO既不是还原产物也不是氧化产物,B正确;反应中Fe3+的化合价升高到+6价,则生成1 mol
FeO2-
2 4
时转移3
mol电子,C错误;反应中FeO2-
是氧化产物,Cl-是还原产物,故氧化产物与还原产物的物质的
4
量之比为2∶3,D正确。
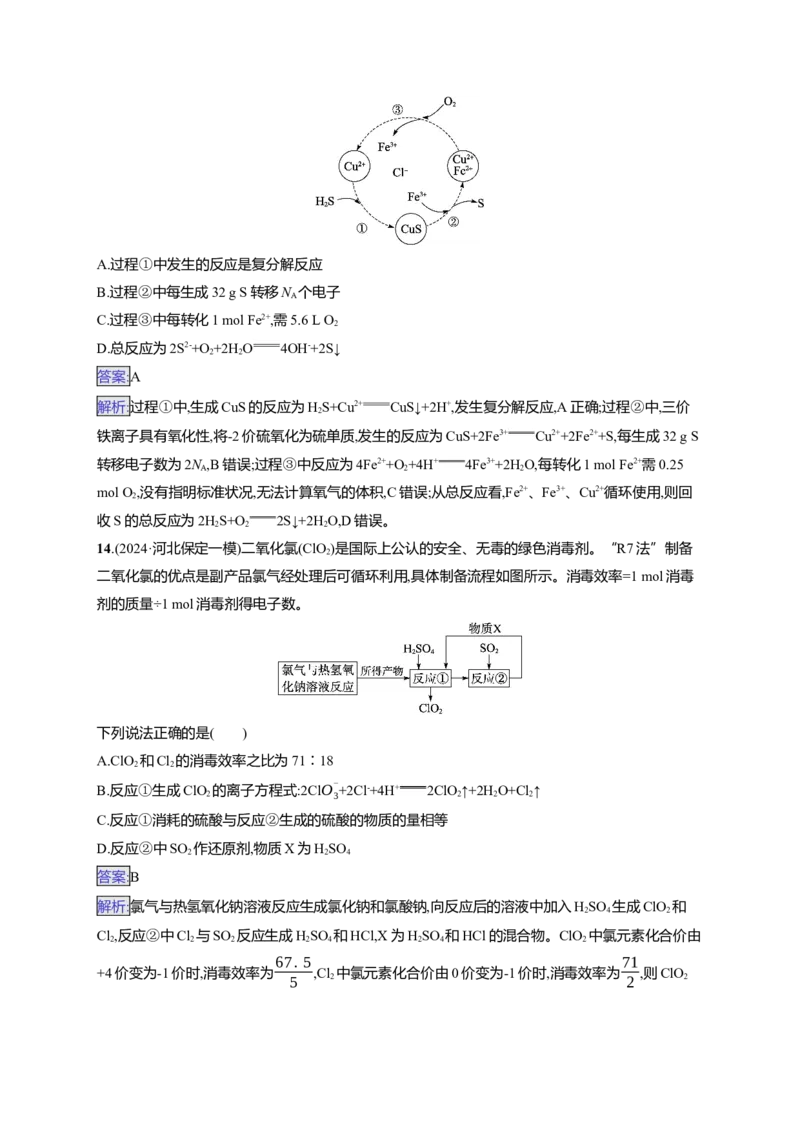
13.(2024·四川德阳二模)H S是有毒的污染性气体,可将其与氧气的混合气体通入FeCl 、FeCl 、
2 3 2
CuCl 的混合溶液中进行处理,其物质转化如图所示。设N 为阿伏加德罗常数的值,下列说法正确的
2 A
是( )A.过程①中发生的反应是复分解反应
B.过程②中每生成32 g S转移N 个电子
A
C.过程③中每转化1 mol Fe2+,需5.6 L O
2
D.总反应为2S2-+O +2H O 4OH-+2S↓
2 2
答案:A
解析:过程①中,生成CuS的反应为HS+Cu2+ CuS↓+2H+,发生复分解反应,A正确;过程②中,三价
2
铁离子具有氧化性,将-2价硫氧化为硫单质,发生的反应为CuS+2Fe3+ Cu2++2Fe2++S,每生成32 g S
转移电子数为2N ,B错误;过程③中反应为4Fe2++O +4H+ 4Fe3++2H O,每转化1 mol Fe2+需0.25
A 2 2
mol O,没有指明标准状况,无法计算氧气的体积,C错误;从总反应看,Fe2+、Fe3+、Cu2+循环使用,则回
2
收S的总反应为2HS+O 2S↓+2HO,D错误。
2 2 2
14.(2024·河北保定一模)二氧化氯(ClO )是国际上公认的安全、无毒的绿色消毒剂。“R7法”制备
2
二氧化氯的优点是副产品氯气经处理后可循环利用,具体制备流程如图所示。消毒效率=1 mol消毒
剂的质量÷1 mol消毒剂得电子数。
下列说法正确的是( )
A.ClO 和Cl 的消毒效率之比为71∶18
2 2
B.反应①生成ClO
的离子方程式:2ClO-
+2Cl-+4H+ 2ClO ↑+2H O+Cl ↑
2 3 2 2 2
C.反应①消耗的硫酸与反应②生成的硫酸的物质的量相等
D.反应②中SO 作还原剂,物质X为HSO
2 2 4
答案:B
解析:氯气与热氢氧化钠溶液反应生成氯化钠和氯酸钠,向反应后的溶液中加入HSO 生成ClO 和
2 4 2
Cl,反应②中Cl 与SO 反应生成HSO 和HCl,X为HSO 和HCl的混合物。ClO 中氯元素化合价由
2 2 2 2 4 2 4 2
67.5 71
+4价变为-1价时,消毒效率为 ,Cl 中氯元素化合价由0价变为-1价时,消毒效率为 ,则ClO
5 2 2 267.5 71
和Cl 的消毒效率之比为 ∶ =27∶71,A错误;反应①中氯化钠和氯酸钠在酸性条件下发生氧
2 5 2
化还原反应生成ClO
和Cl,根据得失电子守恒和电荷守恒配平离子方程式为2ClO-
+2Cl-+4H+
2 2 3
2ClO ↑+2H O+Cl ↑,B正确;反应②中Cl 和SO 反应生成HSO ,根据得失电子守恒和质量守恒配平化
2 2 2 2 2 2 4
学方程式为Cl+SO+2H O HSO +2HCl,当反应①生成1 mol Cl 时消耗2 mol H SO ,反应②消耗
2 2 2 2 4 2 2 4
1 mol Cl 时生成1 mol H SO ,C错误;反应②为Cl+SO+2H O HSO +2HCl,S元素化合价上
2 2 4 2 2 2 2 4
升,SO 作还原剂,物质X为HSO 和HCl的混合物,D错误。
2 2 4