文档内容
8.新型化学电源及分析
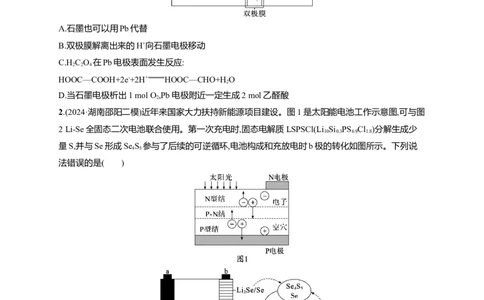
1.(2024·广东佛山质检一)如图装置可合成重要的化工中间体乙醛酸,双极膜中的HO能解离为H+和
2
OH-,下列说法正确的是( )
A.石墨也可以用Pb代替
B.双极膜解离出来的H+向石墨电极移动
C.H C O 在Pb电极表面发生反应:
2 2 4
HOOC—COOH+2e-+2H+ HOOC—CHO+H O
2
D.当石墨电极析出1 mol O ,Pb电极附近一定生成2 mol乙醛酸
2
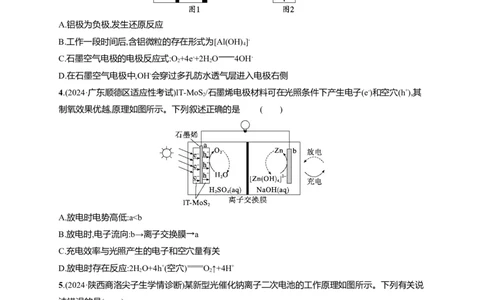
2.(2024·湖南邵阳二模)近年来国家大力扶持新能源项目建设。图1是太阳能电池工作示意图,可与图
2 Li-Se全固态二次电池联合使用。第一次充电时,固态电解质LSPSCl(Li Si PS Cl )分解生成少
10 0.3 6.9 1.8
量S,并与Se形成Se S 参与了后续的可逆循环,电池构成和充放电时b极的转化如图所示。下列说
4 5
法错误的是( )
A.P电极是太阳能电池的正极
B.Li-Se全固态电池放电时Li+向b电极移动
C.Li-Se全固态电池放电时,a电极质量每减少14 g,理论上外电路转移电子数为2N
A
D.电池充电时,b电极与N电极相连,其电极反应有5LiS+4LiSe-18e- 18Li++Se S
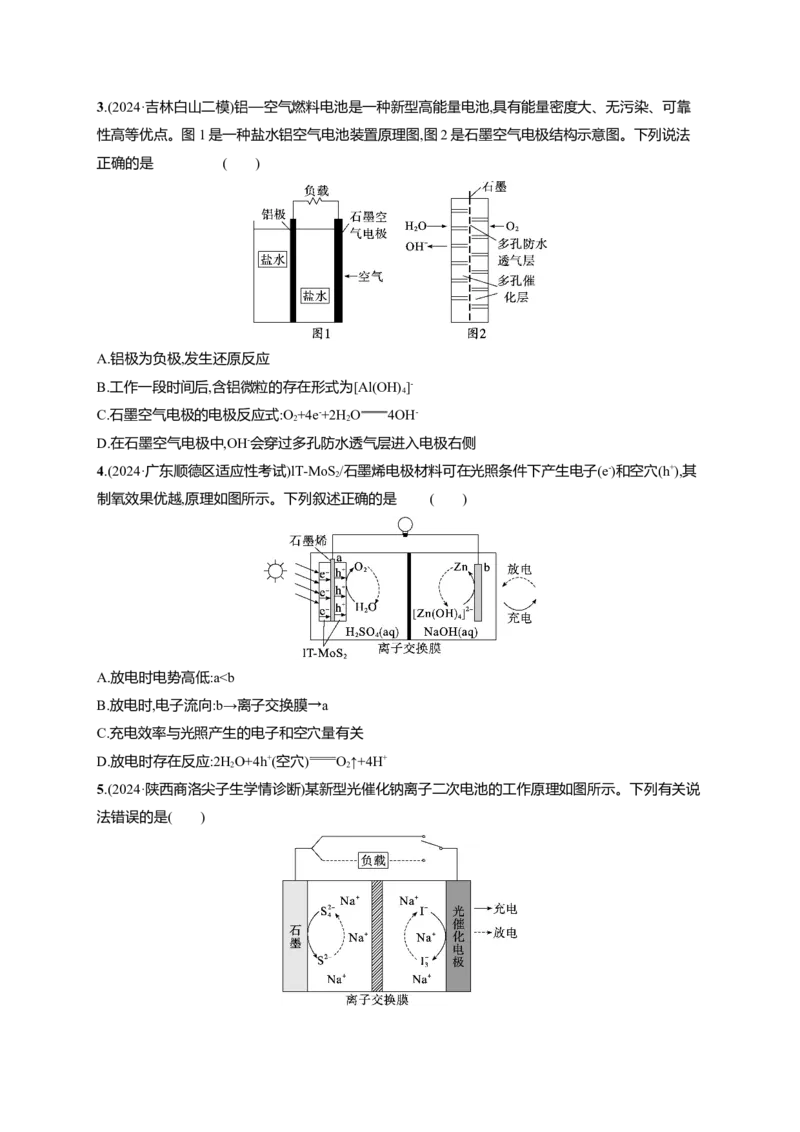
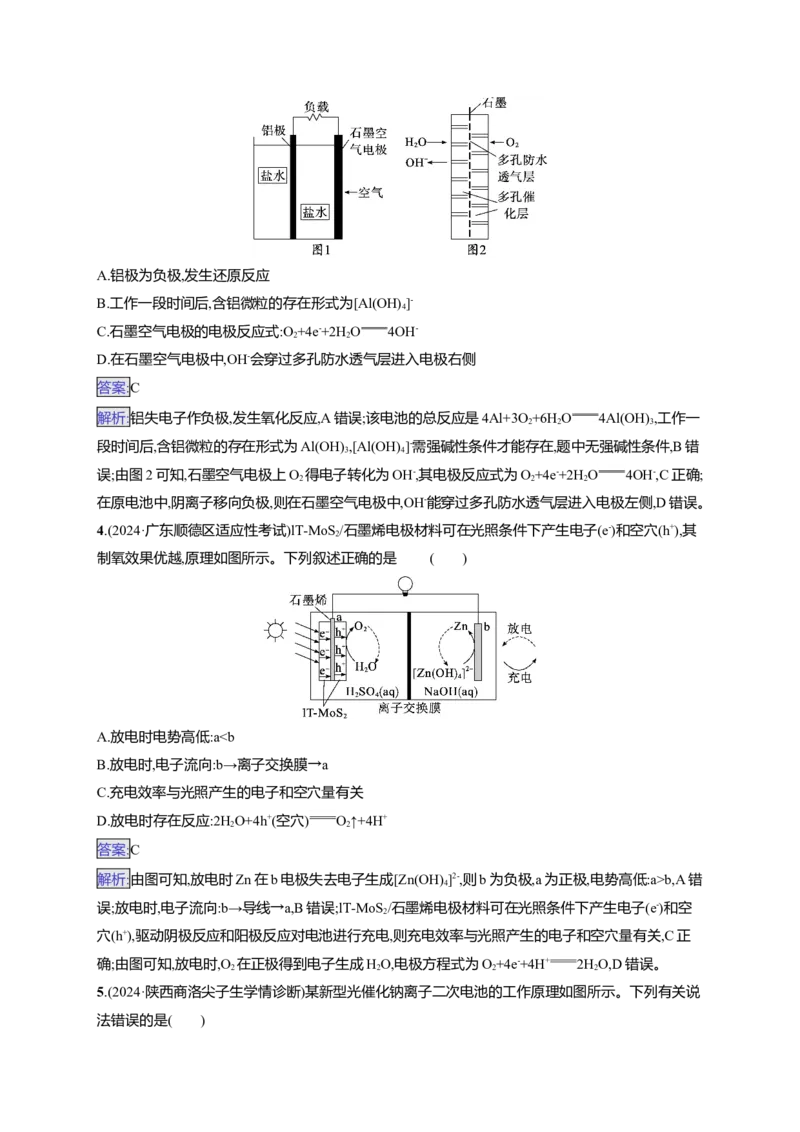
2 2 4 53.(2024·吉林白山二模)铝—空气燃料电池是一种新型高能量电池,具有能量密度大、无污染、可靠
性高等优点。图1是一种盐水铝空气电池装置原理图,图2是石墨空气电极结构示意图。下列说法
正确的是 ( )
A.铝极为负极,发生还原反应
B.工作一段时间后,含铝微粒的存在形式为[Al(OH) ]-
4
C.石墨空气电极的电极反应式:O +4e-+2H O 4OH-
2 2
D.在石墨空气电极中,OH-会穿过多孔防水透气层进入电极右侧
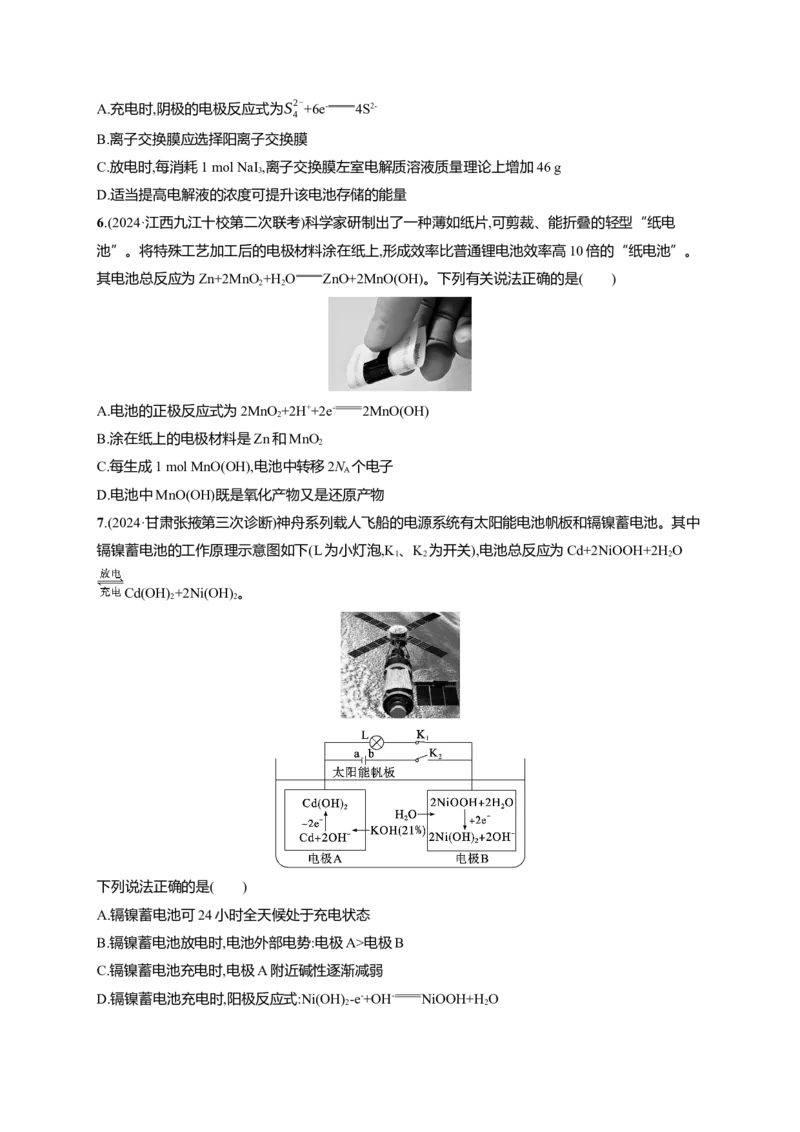
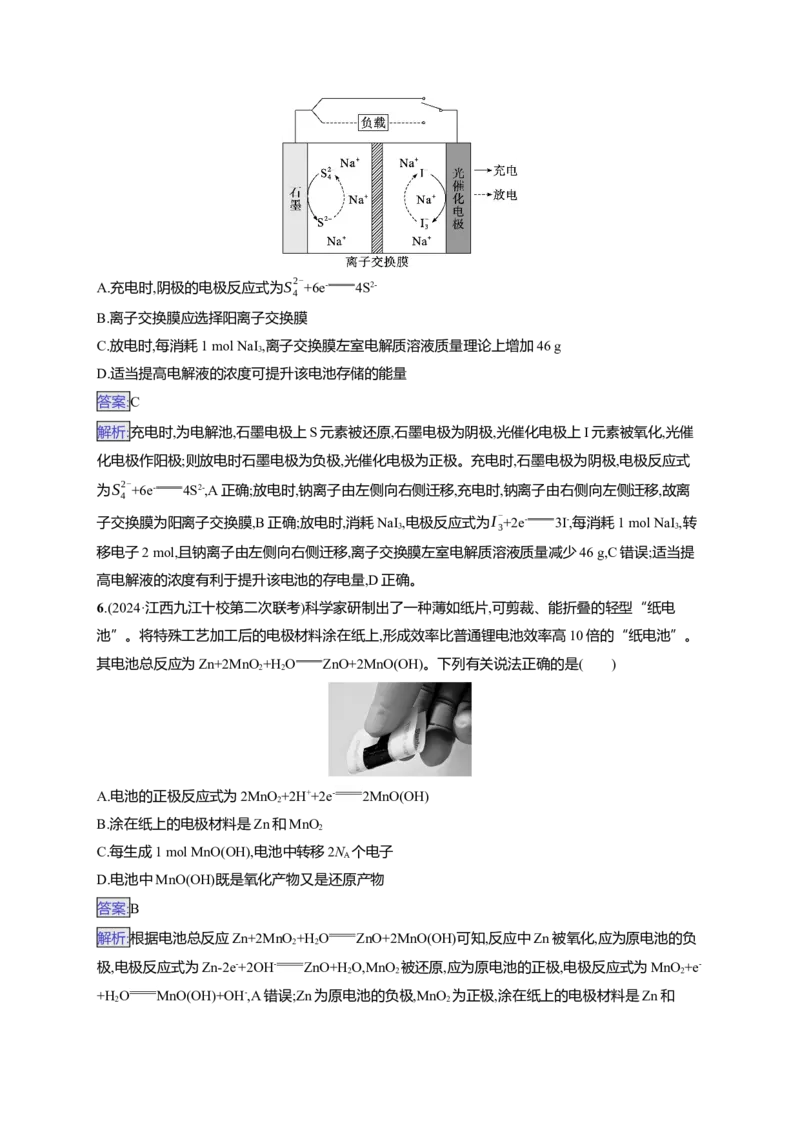
4.(2024·广东顺德区适应性考试)lT-MoS /石墨烯电极材料可在光照条件下产生电子(e-)和空穴(h+),其
2
制氧效果优越,原理如图所示。下列叙述正确的是 ( )
A.放电时电势高低:a电极B
C.镉镍蓄电池充电时,电极A附近碱性逐渐减弱
D.镉镍蓄电池充电时,阳极反应式:Ni(OH) -e-+OH- NiOOH+H O
2 28.(2024·甘肃白银名校联合调研)一种将酸—碱双电解液分开且具有双溶解沉积反应的酸碱混合高电
压水系可充电电池的充电过程如图。下列说法中错误的是( )
A.充电时,电极a与电源的负极相连
B.放电时,在电极a区加入KOH溶液作电解质溶液
C.放电时,电极b的电极反应式为MnO +4H++2e- Mn2++2H O
2 2
D.充电时,当电极a处生成6.5 g Zn时,有0.1 mol K+通过交换膜N
8.新型化学电源及分析
1.(2024·广东佛山质检一)如图装置可合成重要的化工中间体乙醛酸,双极膜中的HO能解离为H+和
2
OH-,下列说法正确的是( )
A.石墨也可以用Pb代替
B.双极膜解离出来的H+向石墨电极移动
C.H C O 在Pb电极表面发生反应:
2 2 4
HOOC—COOH+2e-+2H+ HOOC—CHO+H O
2
D.当石墨电极析出1 mol O ,Pb电极附近一定生成2 mol乙醛酸
2
答案:C
解析:由图可知,铅电极为电解池的阴极,水在阴极得到电子发生还原反应生成氢气和氢氧根离子,酸
性条件下草酸在阴极得到电子发生还原反应生成乙醛酸和水,石墨电极为阳极,水在阳极失去电子发
生氧化反应生成氧气和氢离子,双极膜解离出来的氢氧根离子进入阳极区、氢离子进入阴极区。若
用铅电极代替石墨电极,铅会在阳极失去电子发生氧化反应生成铅离子,所以不能用铅电极代替石墨
电极,A错误;由分析可知,铅电极为电解池的阴极,石墨电极为阳极,双极膜解离出来的氢氧根离子进入阳极区、氢离子进入阴极区,B错误;铅电极为电解池的阴极,酸性条件下草酸在阴极得到电子发生
还原反应生成乙醛酸和水,电极反应式为HOOC—COOH+2e-+2H+ HOOC—CHO+H O,C正确;铅
2
电极为电解池的阴极,水在阴极得到电子发生还原反应生成氢气和氢氧根离子,酸性条件下草酸在阴
极得到电子发生还原反应生成乙醛酸和水,则石墨电极析出1 mol氧气时,无法计算铅电极附近生成
乙醛酸的物质的量,D错误。
2.(2024·湖南邵阳二模)近年来国家大力扶持新能源项目建设。图1是太阳能电池工作示意图,可与图
2 Li-Se全固态二次电池联合使用。第一次充电时,固态电解质LSPSCl(Li Si PS Cl )分解生成少
10 0.3 6.9 1.8
量S,并与Se形成Se S 参与了后续的可逆循环,电池构成和充放电时b极的转化如图所示。下列说
4 5
法错误的是( )
A.P电极是太阳能电池的正极
B.Li-Se全固态电池放电时Li+向b电极移动
C.Li-Se全固态电池放电时,a电极质量每减少14 g,理论上外电路转移电子数为2N
A
D.电池充电时,b电极与N电极相连,其电极反应有5LiS+4LiSe-18e- 18Li++Se S
2 2 4 5
答案:D
解析:由图1可知,有太阳光时,电池处于充电状态,电子移向N极,即N为负极,P为正极,A正确;Li-Se
全固态电池放电时b电极为正极,Li+向b电极移动,B正确;Li-Se全固态电池放电时,a电极的电极反应
式为Li-e- Li+,质量每减少14 g即有2 mol Li+产生,理论上外电路转移电子数为2N ,C正确;电池
A
充电时,b电极与P电极相连,其电极反应有:5LiS+4LiSe-18e- 18Li++Se S,D错误。
2 2 4 5
3.(2024·吉林白山二模)铝—空气燃料电池是一种新型高能量电池,具有能量密度大、无污染、可靠
性高等优点。图1是一种盐水铝空气电池装置原理图,图2是石墨空气电极结构示意图。下列说法
正确的是 ( )A.铝极为负极,发生还原反应
B.工作一段时间后,含铝微粒的存在形式为[Al(OH) ]-
4
C.石墨空气电极的电极反应式:O +4e-+2H O 4OH-
2 2
D.在石墨空气电极中,OH-会穿过多孔防水透气层进入电极右侧
答案:C
解析:铝失电子作负极,发生氧化反应,A错误;该电池的总反应是4Al+3O +6H O 4Al(OH) ,工作一
2 2 3
段时间后,含铝微粒的存在形式为Al(OH) ,[Al(OH) ]-需强碱性条件才能存在,题中无强碱性条件,B错
3 4
误;由图2可知,石墨空气电极上O 得电子转化为OH-,其电极反应式为O+4e-+2H O 4OH-,C正确;
2 2 2
在原电池中,阴离子移向负极,则在石墨空气电极中,OH-能穿过多孔防水透气层进入电极左侧,D错误。
4.(2024·广东顺德区适应性考试)lT-MoS /石墨烯电极材料可在光照条件下产生电子(e-)和空穴(h+),其
2
制氧效果优越,原理如图所示。下列叙述正确的是 ( )
A.放电时电势高低:ab,A错
4
误;放电时,电子流向:b→导线→a,B错误;lT-MoS /石墨烯电极材料可在光照条件下产生电子(e-)和空
2
穴(h+),驱动阴极反应和阳极反应对电池进行充电,则充电效率与光照产生的电子和空穴量有关,C正
确;由图可知,放电时,O 在正极得到电子生成HO,电极方程式为O+4e-+4H+ 2HO,D错误。
2 2 2 2
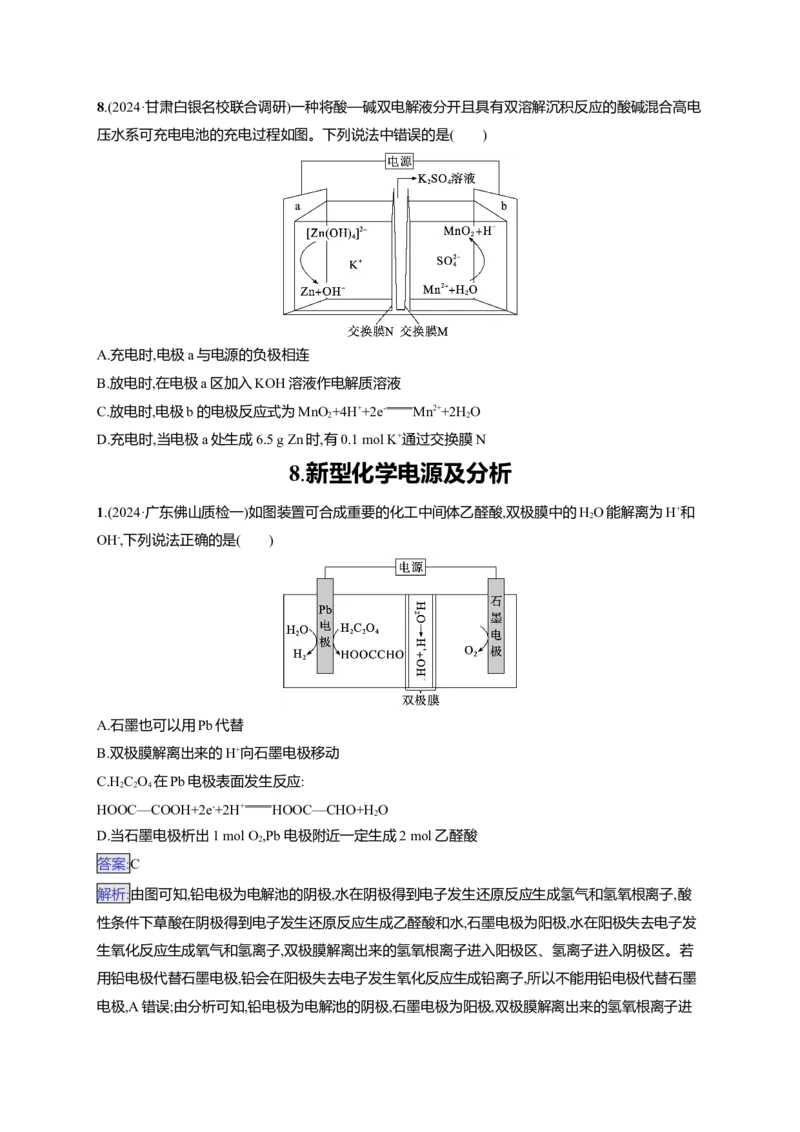
5.(2024·陕西商洛尖子生学情诊断)某新型光催化钠离子二次电池的工作原理如图所示。下列有关说
法错误的是( )A.充电时,阴极的电极反应式为S2-
+6e- 4S2-
4
B.离子交换膜应选择阳离子交换膜
C.放电时,每消耗1 mol NaI ,离子交换膜左室电解质溶液质量理论上增加46 g
3
D.适当提高电解液的浓度可提升该电池存储的能量
答案:C
解析:充电时,为电解池,石墨电极上S元素被还原,石墨电极为阴极,光催化电极上I元素被氧化,光催
化电极作阳极;则放电时石墨电极为负极,光催化电极为正极。充电时,石墨电极为阴极,电极反应式
为S2-
+6e- 4S2-,A正确;放电时,钠离子由左侧向右侧迁移,充电时,钠离子由右侧向左侧迁移,故离
4
子交换膜为阳离子交换膜,B正确;放电时,消耗NaI
,电极反应式为I-
+2e- 3I-,每消耗1 mol NaI ,转
3 3 3
移电子2 mol,且钠离子由左侧向右侧迁移,离子交换膜左室电解质溶液质量减少46 g,C错误;适当提
高电解液的浓度有利于提升该电池的存电量,D正确。
6.(2024·江西九江十校第二次联考)科学家研制出了一种薄如纸片,可剪裁、能折叠的轻型“纸电
池”。将特殊工艺加工后的电极材料涂在纸上,形成效率比普通锂电池效率高10倍的“纸电池”。
其电池总反应为Zn+2MnO +H O ZnO+2MnO(OH)。下列有关说法正确的是( )
2 2
A.电池的正极反应式为2MnO +2H++2e- 2MnO(OH)
2
B.涂在纸上的电极材料是Zn和MnO
2
C.每生成1 mol MnO(OH),电池中转移2N 个电子
A
D.电池中MnO(OH)既是氧化产物又是还原产物
答案:B
解析:根据电池总反应Zn+2MnO +H O ZnO+2MnO(OH)可知,反应中Zn被氧化,应为原电池的负
2 2
极,电极反应式为Zn-2e-+2OH- ZnO+H O,MnO 被还原,应为原电池的正极,电极反应式为MnO +e-
2 2 2
+H O MnO(OH)+OH-,A错误;Zn为原电池的负极,MnO 为正极,涂在纸上的电极材料是Zn和
2 2MnO ,B正确;由MnO +e-+H O MnO(OH)+OH-,每生成1 mol MnO(OH)转移1 mol电子,电池中转
2 2 2
移N 个电子,C错误;Zn元素化合价升高,ZnO是氧化产物,MnO 被还原,MnO(OH)是还原产物,D错误。
A 2
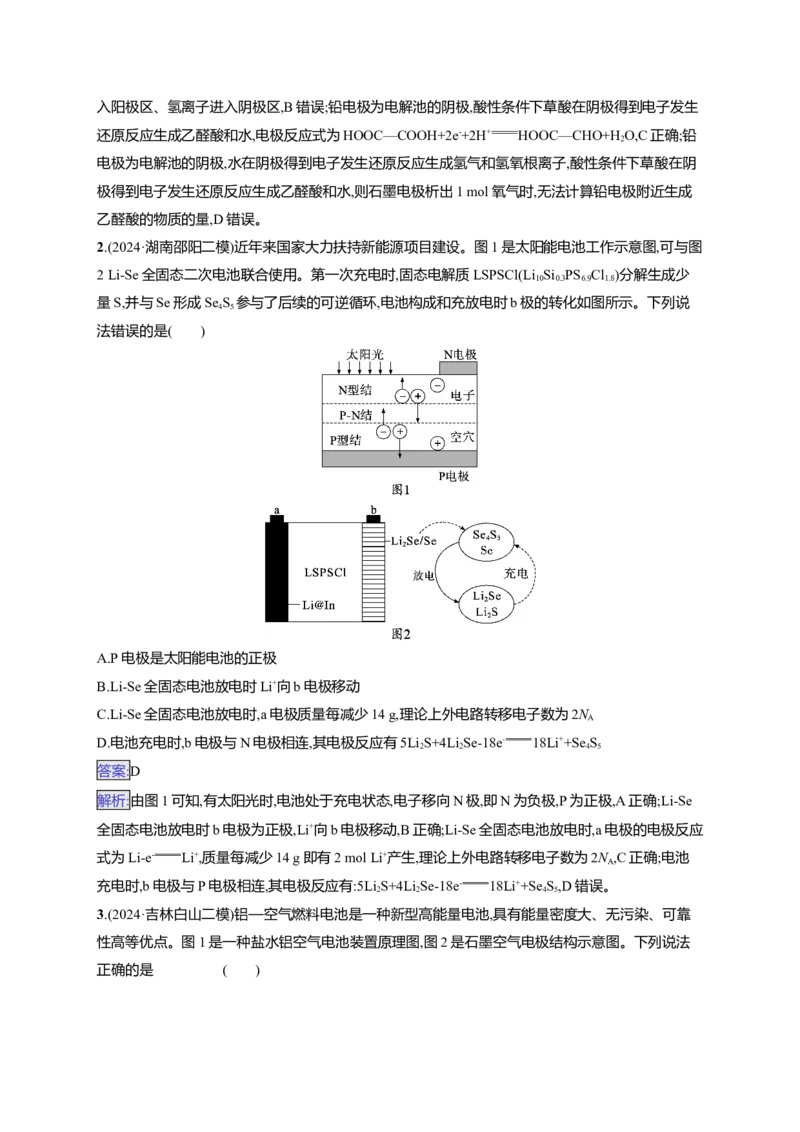
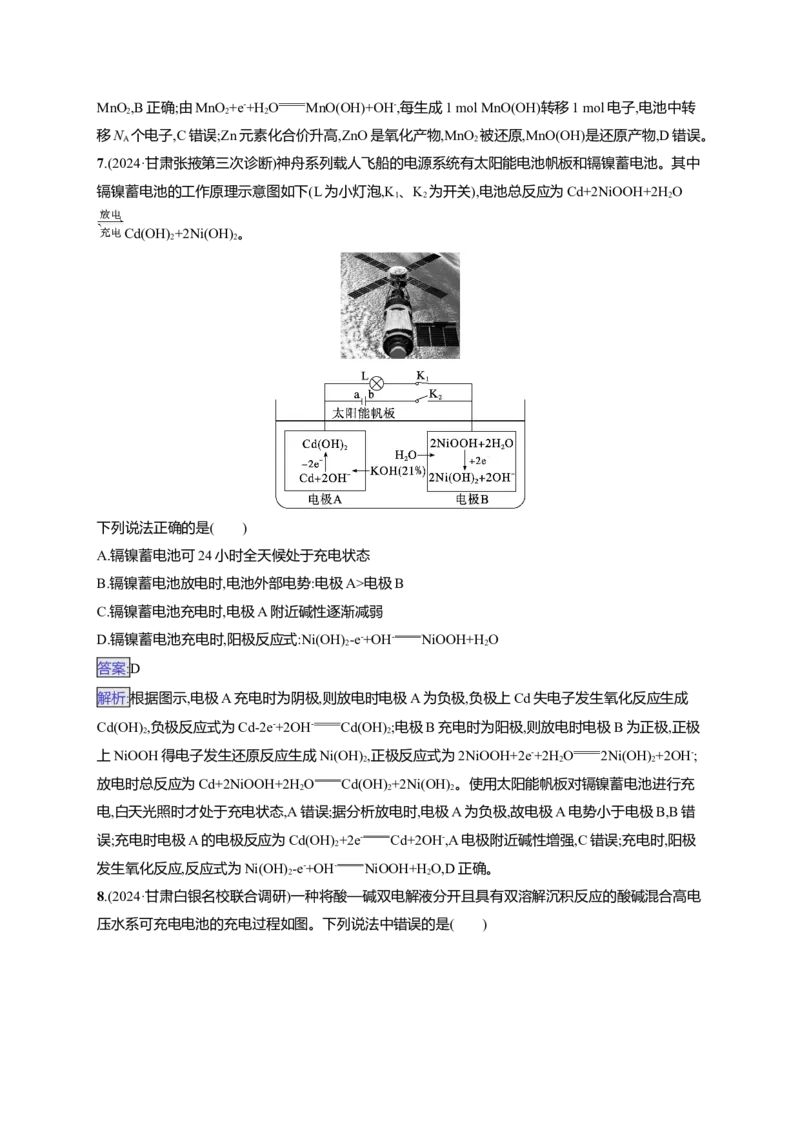
7.(2024·甘肃张掖第三次诊断)神舟系列载人飞船的电源系统有太阳能电池帆板和镉镍蓄电池。其中
镉镍蓄电池的工作原理示意图如下(L为小灯泡,K 、K 为开关),电池总反应为Cd+2NiOOH+2H O
1 2 2
Cd(OH) +2Ni(OH) 。
2 2
下列说法正确的是( )
A.镉镍蓄电池可24小时全天候处于充电状态
B.镉镍蓄电池放电时,电池外部电势:电极A>电极B
C.镉镍蓄电池充电时,电极A附近碱性逐渐减弱
D.镉镍蓄电池充电时,阳极反应式:Ni(OH) -e-+OH- NiOOH+H O
2 2
答案:D
解析:根据图示,电极A充电时为阴极,则放电时电极A为负极,负极上Cd失电子发生氧化反应生成
Cd(OH) ,负极反应式为Cd-2e-+2OH- Cd(OH) ;电极B充电时为阳极,则放电时电极B为正极,正极
2 2
上NiOOH得电子发生还原反应生成Ni(OH) ,正极反应式为2NiOOH+2e-+2H O 2Ni(OH) +2OH-;
2 2 2
放电时总反应为Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) 。使用太阳能帆板对镉镍蓄电池进行充
2 2 2
电,白天光照时才处于充电状态,A错误;据分析放电时,电极A为负极,故电极A电势小于电极B,B错
误;充电时电极A的电极反应为Cd(OH) +2e- Cd+2OH-,A电极附近碱性增强,C错误;充电时,阳极
2
发生氧化反应,反应式为Ni(OH) -e-+OH- NiOOH+H O,D正确。
2 2
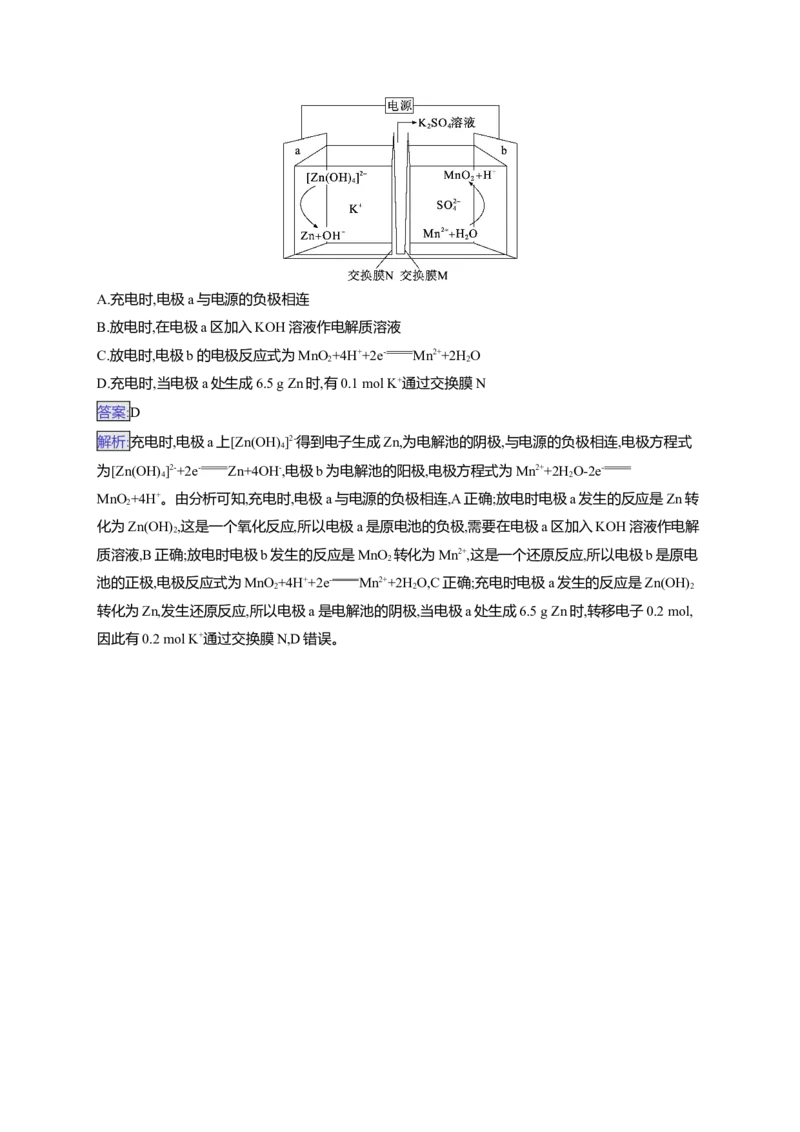
8.(2024·甘肃白银名校联合调研)一种将酸—碱双电解液分开且具有双溶解沉积反应的酸碱混合高电
压水系可充电电池的充电过程如图。下列说法中错误的是( )A.充电时,电极a与电源的负极相连
B.放电时,在电极a区加入KOH溶液作电解质溶液
C.放电时,电极b的电极反应式为MnO +4H++2e- Mn2++2H O
2 2
D.充电时,当电极a处生成6.5 g Zn时,有0.1 mol K+通过交换膜N
答案:D
解析:充电时,电极a上[Zn(OH) ]2-得到电子生成Zn,为电解池的阴极,与电源的负极相连,电极方程式
4
为[Zn(OH) ]2-+2e- Zn+4OH-,电极b为电解池的阳极,电极方程式为Mn2++2H O-2e-
4 2
MnO +4H+。由分析可知,充电时,电极a与电源的负极相连,A正确;放电时电极a发生的反应是Zn转
2
化为Zn(OH) ,这是一个氧化反应,所以电极a是原电池的负极,需要在电极a区加入KOH溶液作电解
2
质溶液,B正确;放电时电极b发生的反应是MnO 转化为Mn2+,这是一个还原反应,所以电极b是原电
2
池的正极,电极反应式为MnO +4H++2e- Mn2++2H O,C正确;充电时电极a发生的反应是Zn(OH)
2 2 2
转化为Zn,发生还原反应,所以电极a是电解池的阴极,当电极a处生成6.5 g Zn时,转移电子0.2 mol,
因此有0.2 mol K+通过交换膜N,D错误。