文档内容
第 74 讲 以性质为主的探究类综合实验
[复习目标] 1.能根据不同情景、不同类型实验特点评价或设计解决问题的简单方案。2.建
立解答探究类综合实验的思维模型。
类型一 物质性质的探究
1.物质性质探究类实验的类型
(1)根据物质性质设计实验方案
(2)根据物质的结构(或官能团)设计实验方案
2.物质性质探究类实验的常见操作及原因
操作 目的或原因
沉淀水洗 除去××(可溶于水)杂质
a.减小固体的溶解度;b.除去固体表面吸附的杂
沉淀用乙醇洗涤
质;c.乙醇挥发带走水分,使固体快速干燥
防止××蒸气逸出脱离反应体系;提高××物质
冷凝回流
的转化率
防止××离子水解;防止××离子沉淀;确保
控制溶液pH
××离子沉淀完全;防止××溶解等
“趁热过滤”后,有时先向滤液中
稀释溶液,防止降温过程中杂质析出,提高产品
加入少量水,加热至沸腾,然后再
的纯度
“冷却结晶”
加过量A试剂 使B物质反应完全(或提高B物质的转化率等)
温度过高××物质分解(如HO、浓硝酸、
2 2
NH HCO 等)或××物质挥发(如浓硝酸、浓盐酸)
4 3
温度不高于××℃
或××物质氧化(如NaSO 等)或促进××物质水
2 3
解(如AlCl 等)
3减小压强,使液体沸点降低,防止××物质受热
减压蒸馏(减压蒸发)
分解(如HO、浓硝酸、NH HCO 等)
2 2 4 3
抑制××离子的水解(如加热蒸发AlCl 溶液时需
3
蒸发、反应时的气体氛围 在HCl气流中进行,加热MgCl ·6H O制MgCl
2 2 2
时需在HCl气流中进行等)
配制某溶液前先煮沸水 除去溶解在水中的氧气,防止××物质被氧化
反应容器中用玻璃管和大气相通 指示容器中压强大小,避免反应容器中压强过大
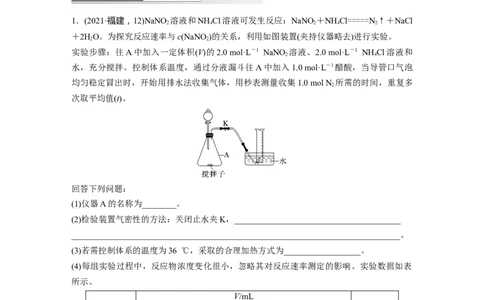
1.(2021·福建,12)NaNO 溶液和NH Cl溶液可发生反应:NaNO +NH Cl=====N↑+NaCl
2 4 2 4 2
+2HO。为探究反应速率与c(NaNO )的关系,利用如图装置(夹持仪器略去)进行实验。
2 2
实验步骤:往A中加入一定体积(V)的2.0 mol·L-1 NaNO 溶液、2.0 mol·L-1 NH Cl溶液和
2 4
水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0 mol·L-1醋酸,当导管口气泡
均匀稳定冒出时,开始用排水法收集气体,用秒表测量收集1.0 mol N 所需的时间,重复多
2
次取平均值(t)。
回答下列问题:
(1)仪器A的名称为________。
(2)检验装置气密性的方法:关闭止水夹K,_______________________________________
_____________________________________________________________________________。
(3)若需控制体系的温度为36 ℃,采取的合理加热方式为__________________。
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如表
所示。
V/mL
实验编号 t/s
NaNO 溶液 NH Cl溶液 醋酸 水
2 4
1 4.0 V 4.0 8.0 334
1
2 V 4.0 4.0 V 150
2 3
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
①V=________,V=________。
1 3
②该反应的速率方程为v=k·cm(NaNO )·c(NH Cl)·c(H+),k为反应速率常数。利用实验数据
2 4计算得m=________(填整数)。
③醋酸的作用是________________________________________________________________。
(5)如果用同浓度的盐酸代替醋酸进行实验 1,NaNO 与盐酸反应生成HNO ,HNO 分解产
2 2 2
生等物质的量的两种气体,反应结束后,A中红棕色气体逐渐变浅,装置中还能观察到的现
象有____________________________________________________________________________。
HNO 分解的化学方程式为_______________________________________________________
2
______________________________________________________________________________。
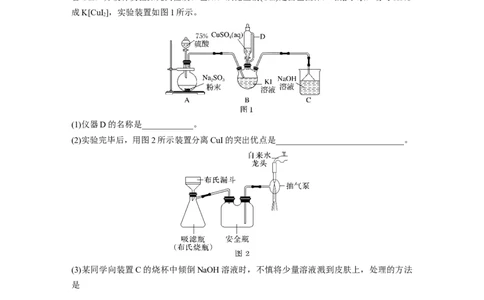
2.(2023·江西上饶统考一模)碘化亚铜(CuI)是重要的有机催化剂。某学习小组用如图装置制
备CuI,并设计实验探究其性质。已知:碘化亚铜(CuI)是白色固体,难溶于水,易与KI形
成K[CuI ],实验装置如图1所示。
2
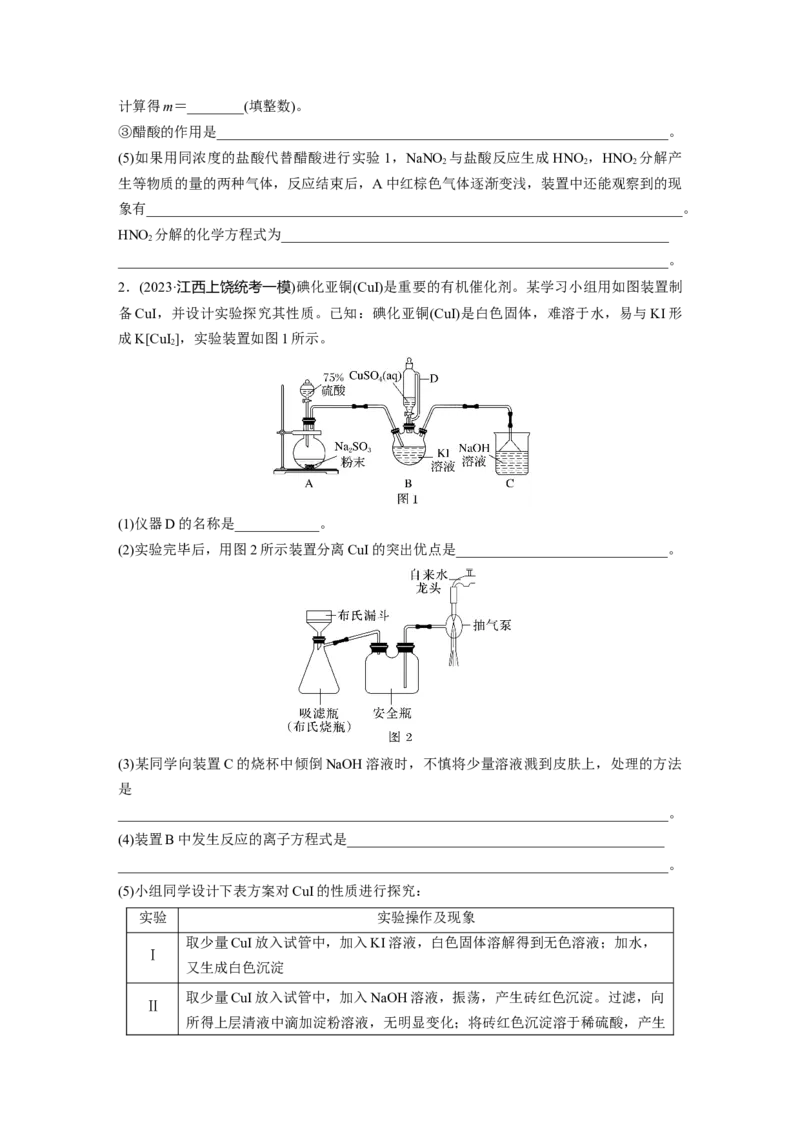
(1)仪器D的名称是____________。
(2)实验完毕后,用图2所示装置分离CuI的突出优点是______________________________。
(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法
是
______________________________________________________________________________。
(4)装置B中发生反应的离子方程式是_____________________________________________
______________________________________________________________________________。
(5)小组同学设计下表方案对CuI的性质进行探究:
实验 实验操作及现象
取少量CuI放入试管中,加入KI溶液,白色固体溶解得到无色溶液;加水,
Ⅰ
又生成白色沉淀
取少量CuI放入试管中,加入NaOH溶液,振荡,产生砖红色沉淀。过滤,向
Ⅱ
所得上层清液中滴加淀粉溶液,无明显变化;将砖红色沉淀溶于稀硫酸,产生红色固体和蓝色溶液
①在实验 Ⅰ 中“加水,又生成白色沉淀”的原理是________________________________
______________________________________________________________________________。
②根据实验 Ⅱ ,CuI与NaOH溶液反应的化学方程式是____________________________
______________________________________________________________________________。
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入
足量的酸化的双氧水,滴几滴淀粉溶液,用b mol·L-1NaSO 标准溶液滴定至终点,消耗
2 2 3
NaSO 溶液的体积为V mL[已知:滴定反应为I +2SO===SO(无色)+2I-]。该样品纯度为
2 2 3 2 2 4
________(用含a、b、V的代数式表示)。如果其他操作均正确,仅滴定前盛标准溶液的滴定
管用蒸馏水洗净后没有用标准溶液润洗,测得结果________(填“偏高”“偏低”或“无影
响”)。
类型二 反应产物、反应机理的探究
1.解答产物确定题的思路分析
由性质确定反应产物是解此类题目的根本思路,而题目中所涉及的物质,一般分为两类。
要注意物质的特殊性质,比如颜色、状态、气味、溶解性等
常见的熟悉
第一类 物理性质,或能与哪些物质反应生成特殊的沉淀、气体等化
物质
学性质
虽然平时接触不多,但其某种组成成分、结构成分(如离子、
能类比迁移
第二类 原子团、官能团等)必然学过,则可以考虑与其结构相似的物
的陌生物质
质的性质,进而推断其具体组成
2.文字表述题的各种答题规范
(1)沉淀洗涤是否完全的检验答题模板
取少许最后一次洗涤液,滴入少量……溶液(试剂),若……(现象),表示已经洗涤完全。
解答此类题目要注意四个得分点:取样+试剂+现象+结论。
取样 要取“少许最后一次”洗涤液
试剂 选择合理的试剂
现象 须有明显的现象描述
结论 根据现象得出结论
(2)实验操作的原因、目的、作用的答题要点明确实验目的:做什么
答题要素 明确操作目的:为什么这样做
明确结论:这样做会有什么结果?理由是什么
操作:怎么“做”,为什么这样“做”
得分点及关键词
作用:须有明确的结论、判断、理由
(3)实验现象的准确、全面描述
现象描述要全面:看到的、听到的、触摸到的、闻到的
现象描述要准确:如A试管中……B处有……
答题要素
按“现象+结论”格式描述,忌现象结论不分、由理论推现象、指出具体
生成物的名称
溶液中:颜色由……变成……,液面上升或下降(形成液面差),溶液变浑
浊,生成(产生)……沉淀,溶液发生倒吸,产生大量气泡(或有气体从溶液
中逸出),有液体溢出等
得分点及
固体:表面产生大量气泡,逐渐溶解,体积逐渐变小,颜色由……变成……
关键词
等
气体:生成……色(味)气体,气体由……色变成……色,先变……后……
(加深、变浅、褪色)等
(4)试剂的作用的答题模板
答题要素 试剂的作用是什么?要达到的目的是什么
作用类:“除去”“防止”“抑制”“使……”等,回答要准确
得分点及
作用—目的类:“作用”是“……”,“目的”是“……”,回答要准
关键词
确全面
1.(2023·北京,19)资料显示,I 可以将Cu氧化为Cu2+。某小组同学设计实验探究Cu被I
2 2
氧化的产物及铜元素的价态。
已知:I 易溶于KI溶液,发生反应I+I-I(红棕色);I 和I氧化性几乎相同。
2 2 2
(1)将等体积的KI溶液加入到m mol铜粉和n mol I (n>m)的固体混合物中,振荡。
2
实验记录如下:
c(KI) 实验现象
极少量I 溶解,溶液为淡红色;充分反应后,红色的铜粉转
2
实验 Ⅰ 0.01 mol·L-1
化为白色沉淀,溶液仍为淡红色
部分I 溶解,溶液为红棕色;充分反应后,红色的铜粉转化
2
实验 Ⅱ 0.1 mol·L-1
为白色沉淀,溶液仍为红棕色I 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完
2
实验 Ⅲ 4 mol·L-1
全溶解,溶液为深红棕色
①初始阶段,Cu被氧化的反应速率:实验 Ⅰ________(填“>”“<”或“=”)实验 Ⅱ。
②实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有[Cu(H O) ]2+(蓝色)或[CuI]-(无色),
2 4 2
进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入CCl ,多次萃取、分液。
4
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是______________________________________________________________。
ⅱ.查阅资料,2Cu2++4I-===2CuI↓+I ,[Cu(NH )]+(无色)容易被空气氧化。用离子方程
2 3 2
式解释步骤b的溶液中发生的变化:________________________________________________
______________________________________________________________________________
______________________________________________________________________________。
③结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是CuI,实验Ⅰ中铜被氧化的化学方程式
是____________________________________________________________________________。
分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓 KI 溶液,
________________________________(填实验现象),观察到少量红色的铜。分析铜未完全反
应的原因是____________________________________________________________________。
(2)上述实验结果,I 仅将Cu氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了I
2 2
能将Cu氧化为Cu2+。装置如图所示,a、b分别是____________________________________
______________________________________________________________________________。
(3)运用氧化还原反应规律,分析在上述实验中 Cu被I 氧化的产物中价态不同的原因:
2
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________。
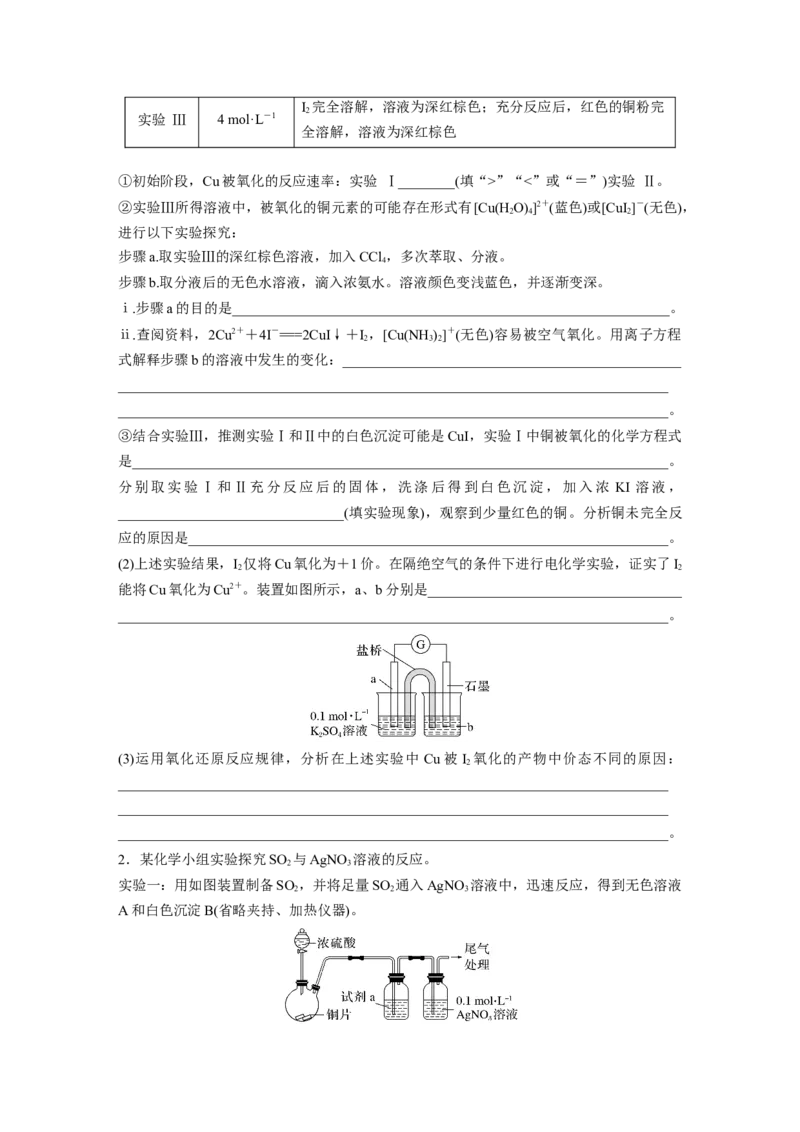
2.某化学小组实验探究SO 与AgNO 溶液的反应。
2 3
实验一:用如图装置制备SO ,并将足量SO 通入AgNO 溶液中,迅速反应,得到无色溶液
2 2 3
A和白色沉淀B(省略夹持、加热仪器)。(1)制备的SO 中会混有少量的SO ,原因可能为____________________________________。
2 3
为了排除SO 的干扰,试剂a可以为________(填字母)。
3
a.浓硫酸
b.饱和NaSO 溶液
2 3
c.饱和NaHS溶液
d.饱和NaHSO 溶液
3
实验二:验证白色沉淀B的成分。
分析:沉淀B可能为Ag SO 、Ag SO 或两者混合物。滴加氨水可释出其阴离子,便于后续
2 3 2 4
检验。
相关反应为①Ag SO +4NH ·H O===2[Ag(NH)]++SO+4HO;
2 3 3 2 3 2 2
②Ag SO +4NH ·H O===2[Ag(NH)]++SO+4HO。
2 4 3 2 3 2 2
流程如下:
(2)欲检验溶液C中加入的Ba(NO ) 是否已经过量,请简述实验方法:_________________
3 2
______________________________________________________________________________。
(3)沉淀D中主要含BaSO,理由是_______________________________________________
3
______________________________________________________________________________。
向滤液E中加入HO 溶液,产生的现象是________________________________________
2 2
______________________________________________________________________________,
可进一步证实B中含Ag SO 。
2 3
实验三:探究SO的产生途径。
猜想1:实验一中,SO 在AgNO 溶液中被氧化生成Ag SO ,随沉淀B进入D。
2 3 2 4
猜想2:实验二中,SO被氧化为SO进入D。
(4)取少量溶液A,滴加过量盐酸,产生白色沉淀。静置后,取上层清液再滴加BaCl 溶液,
2
未出现白色沉淀,可判断猜想1不合理。理由是____________________________________
______________________________________________________________________________。
(5)不同反应的速率也有所不同。将实验一所得混合物放置一段时间,也会有 SO生成,同时
生成单质Ag。请从化学反应速率的角度分析原因:_______________________________
______________________________________________________________________________。
(6)实验探究可知,SO在________(填“酸性”“中性”或“碱性”)溶液中更易被氧化为
SO。反应机理类探究性实验解题流程