文档内容
微专题突破14 物质制备与实验方案设计考点透视一
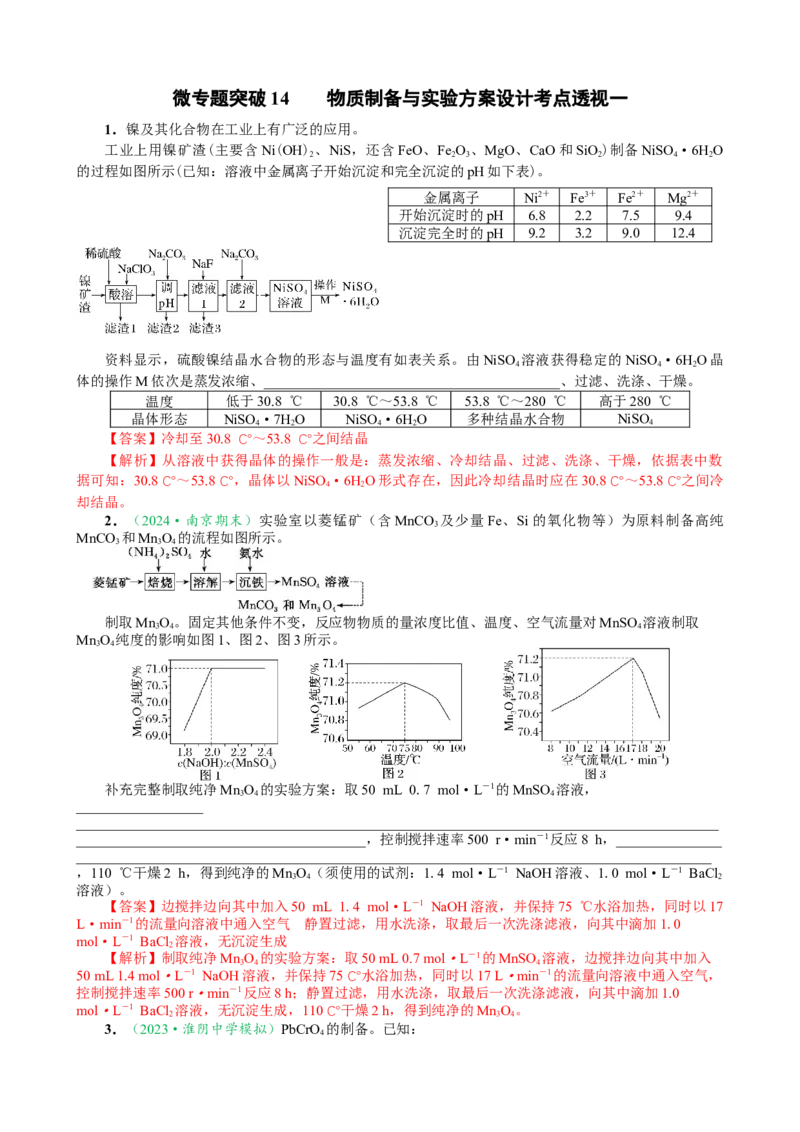
1.镍及其化合物在工业上有广泛的应用。
工业上用镍矿渣(主要含Ni(OH) 、NiS,还含FeO、Fe O 、MgO、CaO和SiO)制备NiSO ·6HO
2 2 3 2 4 2
的过程如图所示(已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表)。
金属离子 Ni2+ Fe3+ Fe2+ Mg2+
开始沉淀时的pH 6.8 2.2 7.5 9.4
沉淀完全时的pH 9.2 3.2 9.0 12.4
资料显示,硫酸镍结晶水合物的形态与温度有如表关系。由NiSO 溶液获得稳定的NiSO ·6HO晶
4 4 2
体的操作M依次是蒸发浓缩、__________________________________________、过滤、洗涤、干燥。
温度 低于30.8 ℃ 30.8 ℃~53.8 ℃ 53.8 ℃~280 ℃ 高于280 ℃
晶体形态 NiSO ·7HO NiSO ·6HO 多种结晶水合物 NiSO
4 2 4 2 4
【答案】冷却至30.8 ℃~53.8 ℃之间结晶
【解析】从溶液中获得晶体的操作一般是:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,依据表中数
据可知:30.8 ℃~53.8 ℃,晶体以NiSO ·6HO形式存在,因此冷却结晶时应在30.8 ℃~53.8 ℃之间冷
4 2
却结晶。
2.(2024·南京期末)实验室以菱锰矿(含MnCO 及少量Fe、Si的氧化物等)为原料制备高纯
3
MnCO 和MnO 的流程如图所示。
3 3 4
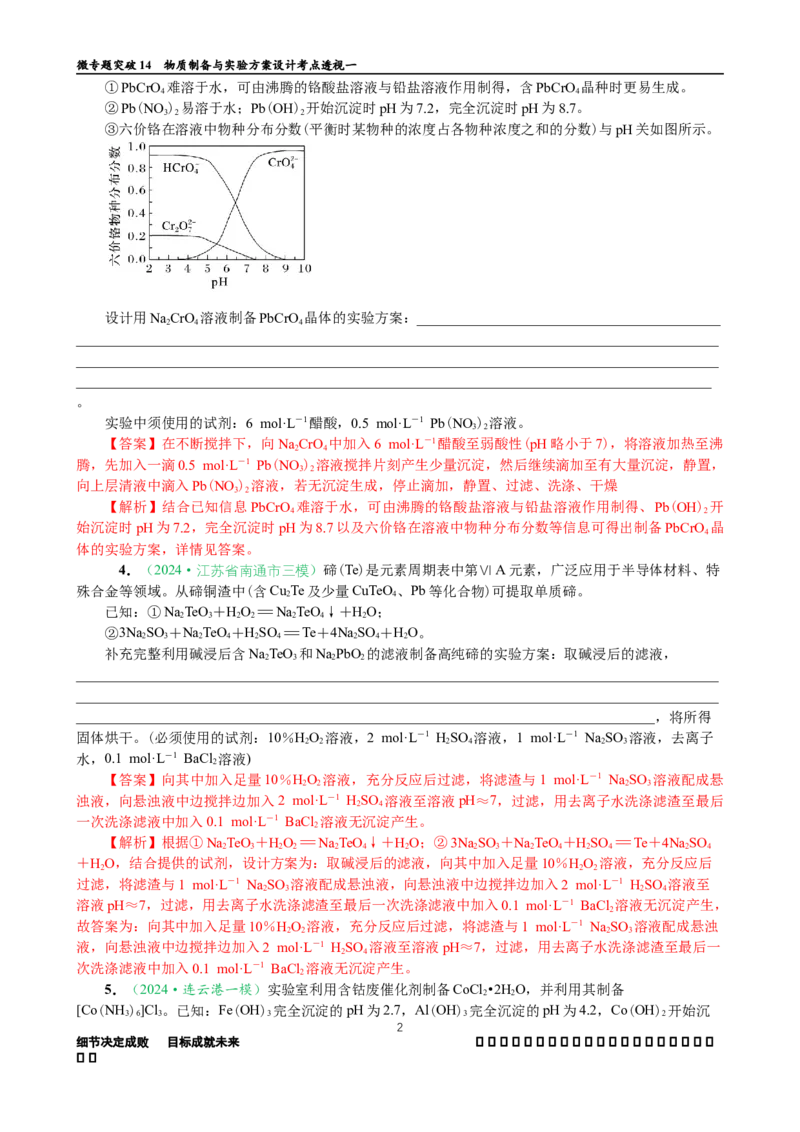
制取MnO。固定其他条件不变,反应物物质的量浓度比值、温度、空气流量对MnSO 溶液制取
3 4 4
MnO 纯度的影响如图1、图2、图3所示。
3 4
补充完整制取纯净MnO 的实验方案:取50 mL 0.7 mol·L-1的MnSO 溶液,
3 4 4
__________________
___________________________________________________________________________________________
_________________________________________,控制搅拌速率500 r·min-1反应8 h,_______________
__________________________________________________________________________________________
,110 ℃干燥2 h,得到纯净的MnO(须使用的试剂:1.4 mol·L-1 NaOH溶液、1.0 mol·L-1 BaCl
3 4 2
溶液)。
【答案】边搅拌边向其中加入50 mL 1.4 mol·L-1 NaOH溶液,并保持75 ℃水浴加热,同时以17
L·min-1的流量向溶液中通入空气 静置过滤,用水洗涤,取最后一次洗涤滤液,向其中滴加1.0
mol·L-1 BaCl 溶液,无沉淀生成
2
【解析】制取纯净MnO 的实验方案:取50 mL 0.7 mol·L-1的MnSO 溶液,边搅拌边向其中加入
3 4 4
50 mL 1.4 mol·L-1 NaOH溶液,并保持75 ℃水浴加热,同时以17 L·min-1的流量向溶液中通入空气,
控制搅拌速率500 r·min-1反应8 h;静置过滤,用水洗涤,取最后一次洗涤滤液,向其中滴加1.0
mol·L-1 BaCl 溶液,无沉淀生成,110 ℃干燥2 h,得到纯净的MnO。
2 3 4
3.(2023·淮阴中学模拟)PbCrO 的制备。已知:
4微专题突破14 物质制备与实验方案设计考点透视一
①PbCrO 难溶于水,可由沸腾的铬酸盐溶液与铅盐溶液作用制得,含PbCrO 晶种时更易生成。
4 4
②Pb(NO ) 易溶于水;Pb(OH) 开始沉淀时pH为7.2,完全沉淀时pH为8.7。
3 2 2
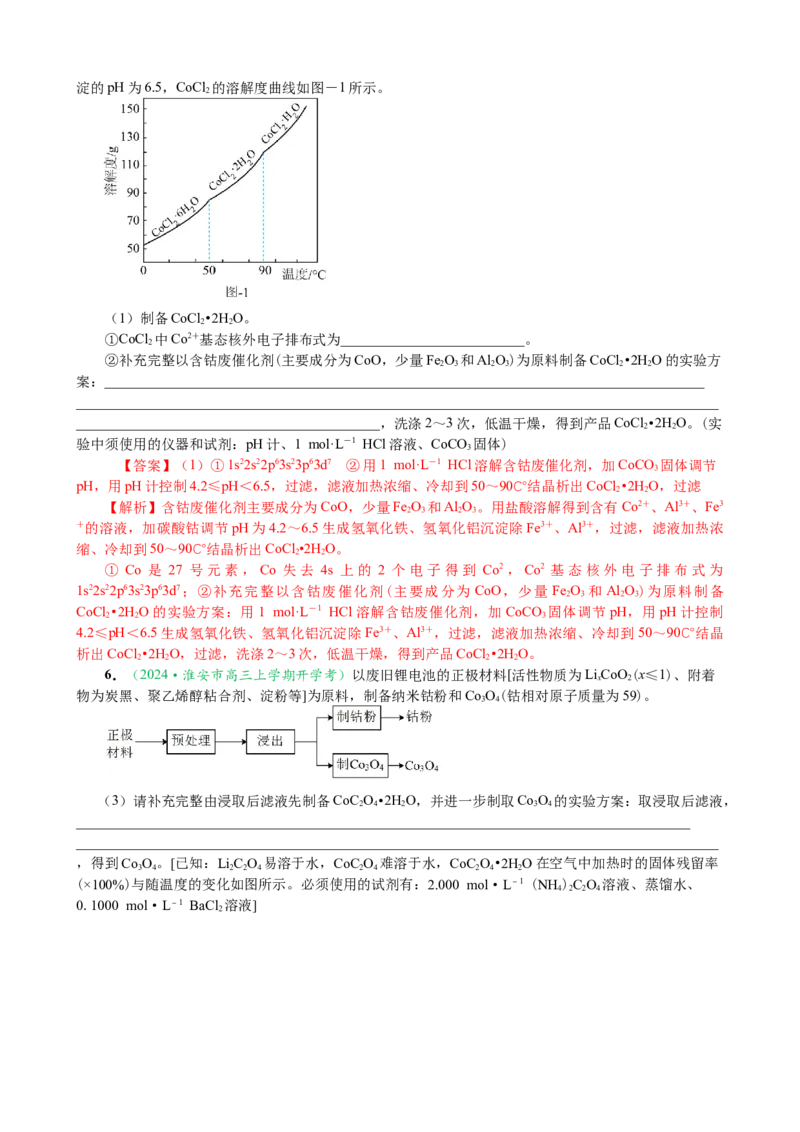
③六价铬在溶液中物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH关如图所示。
设计用NaCrO 溶液制备PbCrO 晶体的实验方案:___________________________________________
2 4 4
___________________________________________________________________________________________
___________________________________________________________________________________________
__________________________________________________________________________________________
。
实验中须使用的试剂:6 mol·L-1醋酸,0.5 mol·L-1 Pb(NO ) 溶液。
3 2
【答案】在不断搅拌下,向NaCrO 中加入6 mol·L-1醋酸至弱酸性(pH略小于7),将溶液加热至沸
2 4
腾,先加入一滴0.5 mol·L-1 Pb(NO ) 溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,静置,
3 2
向上层清液中滴入Pb(NO ) 溶液,若无沉淀生成,停止滴加,静置、过滤、洗涤、干燥
3 2
【解析】结合已知信息PbCrO 难溶于水,可由沸腾的铬酸盐溶液与铅盐溶液作用制得、Pb(OH) 开
4 2
始沉淀时pH为7.2,完全沉淀时pH为8.7以及六价铬在溶液中物种分布分数等信息可得出制备PbCrO 晶
4
体的实验方案,详情见答案。
4.(2024·江苏省南通市三模)碲(Te)是元素周期表中第ⅥA元素,广泛应用于半导体材料、特
殊合金等领域。从碲铜渣中(含Cu Te及少量CuTeO 、Pb等化合物)可提取单质碲。
2 4
已知:①NaTeO+HO=NaTeO↓+HO;
2 3 2 2 2 4 2
②3NaSO+NaTeO+HSO =Te+4NaSO +HO。
2 3 2 4 2 4 2 4 2
补充完整利用碱浸后含NaTeO 和NaPbO 的滤液制备高纯碲的实验方案:取碱浸后的滤液,
2 3 2 2
___________________________________________________________________________________________
___________________________________________________________________________________________
__________________________________________________________________________________,将所得
固体烘干。(必须使用的试剂:10%HO 溶液,2 mol·L-1 HSO 溶液,1 mol·L-1 NaSO 溶液,去离子
2 2 2 4 2 3
水,0.1 mol·L-1 BaCl 溶液)
2
【答案】向其中加入足量10%HO 溶液,充分反应后过滤,将滤渣与1 mol·L-1 NaSO 溶液配成悬
2 2 2 3
浊液,向悬浊液中边搅拌边加入2 mol·L-1 HSO 溶液至溶液pH≈7,过滤,用去离子水洗涤滤渣至最后
2 4
一次洗涤滤液中加入0.1 mol·L-1 BaCl 溶液无沉淀产生。
2
【解析】根据①NaTeO+HO=NaTeO↓+HO;②3NaSO+NaTeO+HSO =Te+4NaSO
2 3 2 2 2 4 2 2 3 2 4 2 4 2 4
+HO,结合提供的试剂,设计方案为:取碱浸后的滤液,向其中加入足量10%HO 溶液,充分反应后
2 2 2
过滤,将滤渣与1 mol·L-1 NaSO 溶液配成悬浊液,向悬浊液中边搅拌边加入2 mol·L-1 HSO 溶液至
2 3 2 4
溶液pH≈7,过滤,用去离子水洗涤滤渣至最后一次洗涤滤液中加入0.1 mol·L-1 BaCl 溶液无沉淀产生,
2
故答案为:向其中加入足量10%HO 溶液,充分反应后过滤,将滤渣与1 mol·L-1 NaSO 溶液配成悬浊
2 2 2 3
液,向悬浊液中边搅拌边加入2 mol·L-1 HSO 溶液至溶液pH≈7,过滤,用去离子水洗涤滤渣至最后一
2 4
次洗涤滤液中加入0.1 mol·L-1 BaCl 溶液无沉淀产生。
2
5.(2024·连云港一模)实验室利用含钴废催化剂制备CoCl •2HO,并利用其制备
2 2
[Co(NH )]Cl 。已知:Fe(OH) 完全沉淀的pH为2.7,Al(OH) 完全沉淀的pH为4.2,Co(OH) 开始沉
3 6 3 3 3 2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
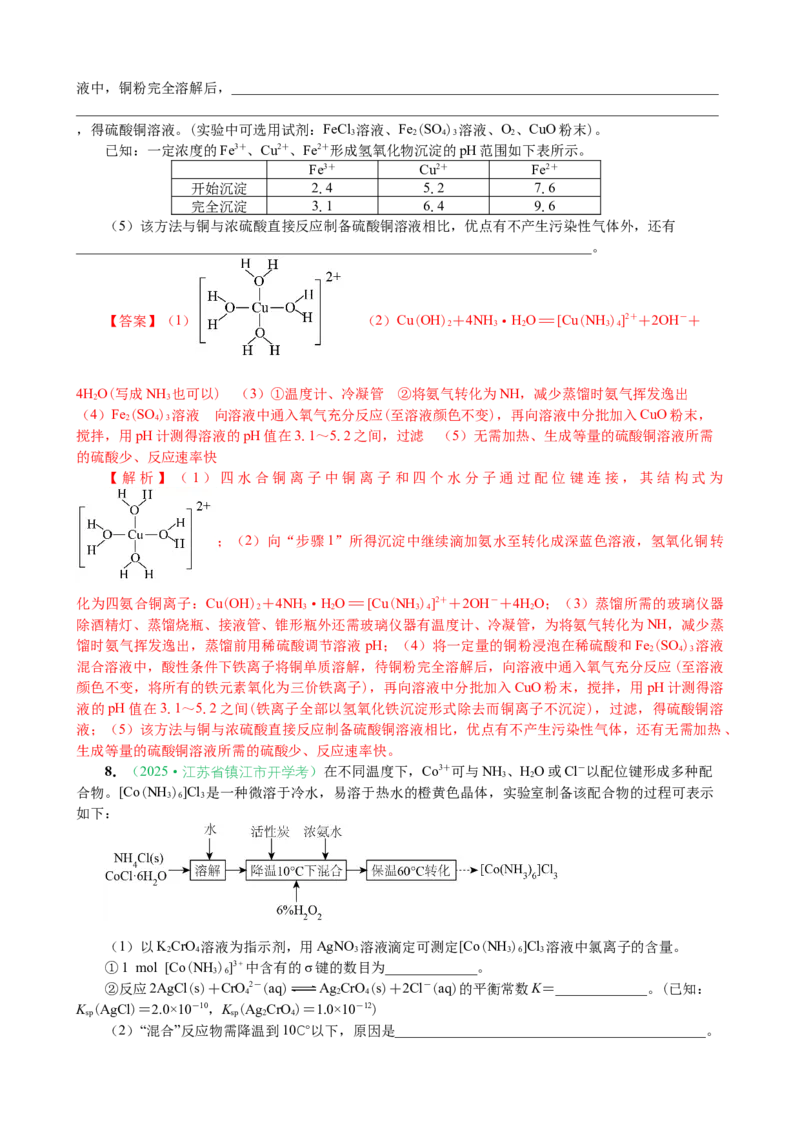
找找淀的pH为6.5,CoCl 的溶解度曲线如图-1所示。
2
(1)制备CoCl •2HO。
2 2
①CoCl 中Co2+基态核外电子排布式为__________________________。
2
②补充完整以含钴废催化剂(主要成分为CoO,少量Fe O 和Al O)为原料制备CoCl •2HO的实验方
2 3 2 3 2 2
案:_____________________________________________________________________________________
___________________________________________________________________________________________
___________________________________________,洗涤2~3次,低温干燥,得到产品CoCl •2HO。(实
2 2
验中须使用的仪器和试剂:pH计、1 mol·L-1 HCl溶液、CoCO 固体)
3
【答案】(1)①1s22s22p63s23p63d7 ②用1 mol·L-1 HCl溶解含钴废催化剂,加CoCO 固体调节
3
pH,用pH计控制4.2≤pH<6.5,过滤,滤液加热浓缩、冷却到50~90℃结晶析出CoCl •2HO,过滤
2 2
【解析】含钴废催化剂主要成分为CoO,少量Fe O 和Al O 。用盐酸溶解得到含有Co2+、Al3+、Fe3
2 3 2 3
+的溶液,加碳酸钴调节pH为4.2~6.5生成氢氧化铁、氢氧化铝沉淀除Fe3+、Al3+,过滤,滤液加热浓
缩、冷却到50~90℃结晶析出CoCl •2H O。
2 2
① Co 是 27 号元素,Co 失去 4s 上的 2 个电子得到 Co2,Co2 基态核外电子排布式为
1s22s22p63s23p63d7;②补充完整以含钴废催化剂(主要成分为 CoO,少量 Fe O 和 Al O)为原料制备
2 3 2 3
CoCl •2HO的实验方案:用1 mol·L-1 HCl溶解含钴废催化剂,加CoCO 固体调节pH,用pH计控制
2 2 3
4.2≤pH<6.5生成氢氧化铁、氢氧化铝沉淀除Fe3+、Al3+,过滤,滤液加热浓缩、冷却到50~90℃结晶
析出CoCl •2HO,过滤,洗涤2~3次,低温干燥,得到产品CoCl •2HO。
2 2 2 2
6.(2024·淮安市高三上学期开学考)以废旧锂电池的正极材料[活性物质为LiCoO(x≤1)、附着
x 2
物为炭黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和Co O(钴相对原子质量为59)。
3 4
(3)请补充完整由浸取后滤液先制备CoC O•2HO,并进一步制取Co O 的实验方案:取浸取后滤液,
2 4 2 3 4
_______________________________________________________________________________________
___________________________________________________________________________________________
,得到Co O。[已知:LiC O 易溶于水,CoC O 难溶于水,CoC O•2HO在空气中加热时的固体残留率
3 4 2 2 4 2 4 2 4 2
(×100%)与随温度的变化如图所示。必须使用的试剂有:2.000 mol·L-1 (NH )C O 溶液、蒸馏水、
4 2 2 4
0.1000 mol·L-1 BaCl 溶液]
2微专题突破14 物质制备与实验方案设计考点透视一
【答案】边搅拌边加入2.000 mol·L-1 (NH )C O 溶液,当静置后向上层清液中加入(NH )C O 溶
4 2 2 4 4 2 2 4
液不再产生沉淀时,停止滴加,过滤,用蒸馏水洗涤至取最后一次洗涤滤液加入 0.1000 mol·L-1 BaCl
2
溶液时无沉淀生成,将固体在400~800℃下加热,当残余固体质量不再发生变化后停止加热
【解析】由题给流程可知,将正极材料研磨成粉末后进行高温煅烧除去附着物炭黑、聚乙烯醇粘合
剂、淀粉等,煅烧后的粉末与稀硫酸混合后,在75℃条件下加入过氧化氢溶液,将钴酸锂转化为硫酸锂、
硫酸钴,过滤得到含有硫酸锂、硫酸钴的浸出液;向浸出液中加入氢氧化钠溶液调节溶液的pH后,加入
一水合肼将溶液中的钴元素转化为单质钴,过滤得到钴粉;向浸出液中加入可溶的草酸盐溶液,将钴离
子转化为二水草酸钴,过滤得到二水草酸钴;二水草酸钴在空气中加热制得四氧化三钴。
浸取后得到得到LiSO 、CoSO 和硫酸的混合溶液。变搅拌边加入2.000 mol·L-1 (NH )C O,使
2 4 4 4 2 2 4
Co2+反应转化为CoC O•2HO沉淀。静置,向上层清液中加入(NH )C O 溶液不再产生沉淀时,说明
2 4 2 4 2 2 4
Co2+反应完全,停止滴加(NH )C O 溶液。过滤,用蒸馏水洗涤后,取最后一次洗涤液加入0.1000
4 2 2 4
mol·L-1 BaCl 溶液时无沉淀生成,说明固体已经洗涤干净。根据Co元素守恒,100 g CoC O•2HO完
2 2 4 2
全转化为Co O 时固体质量m(Co O)=××241 g·mol-1=43.90 g,因此当固体残留率为43.90%时,
3 4 3 4
CoC O•2HO完全转化为Co O。因此将固体在400~800℃下加热,当残余固体质量不再发生变化后停
2 4 2 3 4
止加热,得到Co O。故答案为:边搅拌边加入2.000 mol·L-1 (NH )C O 溶液,当静置后向上层清液
3 4 4 2 2 4
中加入(NH )C O 溶液不再产生沉淀时,停止滴加,过滤,用蒸馏水洗涤至取最后一次洗涤滤液加入
4 2 2 4
0.1000 mol·L-1 BaCl 溶液时无沉淀生成,将固体在400~800℃下加热,当残余固体质量不再发生变化
2
后停止加热。
7.(2024·南通市海门市第一次调研)一水硫酸四氨合铜[Cu(NH )SO •HO]是一种易溶于水的晶
3 4 4 2
体,可作高效安全的广谱杀菌剂。
I.利用硫酸铜溶液制备少量一水硫酸四氨合铜晶体并回收乙醇,实验步骤如下:
步骤1:向硫酸铜溶液中滴加1 mol·L-1氨水至产生蓝色絮状沉淀。
步骤2:向“步骤1”所得沉淀中继续滴加氨水至转化成深蓝色溶液。
步骤3:向“步骤2”所得溶液中加入稍过量的乙醇溶液,析出深蓝色晶体,过滤。
步骤4:向“步骤3”所得的滤液中加入稀硫酸调节溶液的pH至5左右后蒸馏。
(1)画出[Cu(HO)]2+结构式___________________________________。
2 4
(2)“步骤2”中主要反应的离子方程式为_______________________________________________。
(3)“步骤4”中蒸馏所需的玻璃仪器除酒精灯、蒸馏烧瓶、承接管、锥形瓶外还需玻璃仪器有
_____________________________。蒸馏前用稀硫酸调节溶液pH的目的是___________________________
_____________________________。
Ⅱ、工业上常用Fe3+、铜粉来制备硫酸铜溶液。
(4)补充完整制取硫酸铜溶液的实验方案:将一定量的铜粉浸泡在稀硫酸和_____________混合溶
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找液中,铜粉完全溶解后,_____________________________________________________________________
___________________________________________________________________________________________
,得硫酸铜溶液。(实验中可选用试剂:FeCl 溶液、Fe (SO ) 溶液、O、CuO粉末)。
3 2 4 3 2
已知:一定浓度的Fe3+、Cu2+、Fe2+形成氢氧化物沉淀的pH范围如下表所示。
Fe3+ Cu2+ Fe2+
开始沉淀 2.4 5.2 7.6
完全沉淀 3.1 6.4 9.6
(5)该方法与铜与浓硫酸直接反应制备硫酸铜溶液相比,优点有不产生污染性气体外,还有
_________________________________________________________________________。
【答案】(1) (2)Cu(OH)+4NH ·HO=[Cu(NH )]2++2OH-+
2 3 2 3 4
4HO(写成NH 也可以) (3)①温度计、冷凝管 ②将氨气转化为NH,减少蒸馏时氨气挥发逸出
2 3
(4)Fe (SO ) 溶液 向溶液中通入氧气充分反应(至溶液颜色不变),再向溶液中分批加入CuO粉末,
2 4 3
搅拌,用pH计测得溶液的pH值在3.1~5.2之间,过滤 (5)无需加热、生成等量的硫酸铜溶液所需
的硫酸少、反应速率快
【解析】(1)四水合铜离子中铜离子和四个水分子通过配位键连接,其结构式为
;(2)向“步骤1”所得沉淀中继续滴加氨水至转化成深蓝色溶液,氢氧化铜转
化为四氨合铜离子:Cu(OH) +4NH ·HO=[Cu(NH )]2++2OH-+4HO;(3)蒸馏所需的玻璃仪器
2 3 2 3 4 2
除酒精灯、蒸馏烧瓶、接液管、锥形瓶外还需玻璃仪器有温度计、冷凝管,为将氨气转化为NH,减少蒸
馏时氨气挥发逸出,蒸馏前用稀硫酸调节溶液pH;(4)将一定量的铜粉浸泡在稀硫酸和Fe (SO ) 溶液
2 4 3
混合溶液中,酸性条件下铁离子将铜单质溶解,待铜粉完全溶解后,向溶液中通入氧气充分反应(至溶液
颜色不变,将所有的铁元素氧化为三价铁离子),再向溶液中分批加入CuO粉末,搅拌,用pH计测得溶
液的pH值在3.1~5.2之间(铁离子全部以氢氧化铁沉淀形式除去而铜离子不沉淀),过滤,得硫酸铜溶
液;(5)该方法与铜与浓硫酸直接反应制备硫酸铜溶液相比,优点有不产生污染性气体,还有无需加热、
生成等量的硫酸铜溶液所需的硫酸少、反应速率快。
8.(2025·江苏省镇江市开学考)在不同温度下,Co3+可与NH 、HO或Cl-以配位键形成多种配
3 2
合物。[Co(NH )]Cl 是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示
3 6 3
如下:
(1)以KCrO 溶液为指示剂,用AgNO 溶液滴定可测定[Co(NH )]Cl 溶液中氯离子的含量。
2 4 3 3 6 3
①1 mol [Co(NH )]3+中含有的σ键的数目为_____________。
3 6
②反应2AgCl(s)+CrO2-(aq) Ag CrO(s)+2Cl-(aq)的平衡常数K=_____________。(已知:
4 2 4
K (AgCl)=2.0×10-10,K (Ag CrO)=1.0×10-12)
sp sp 2 4
(2)“混合”反应物需降温到10℃以下,原因是____________________________________________。微专题突破14 物质制备与实验方案设计考点透视一
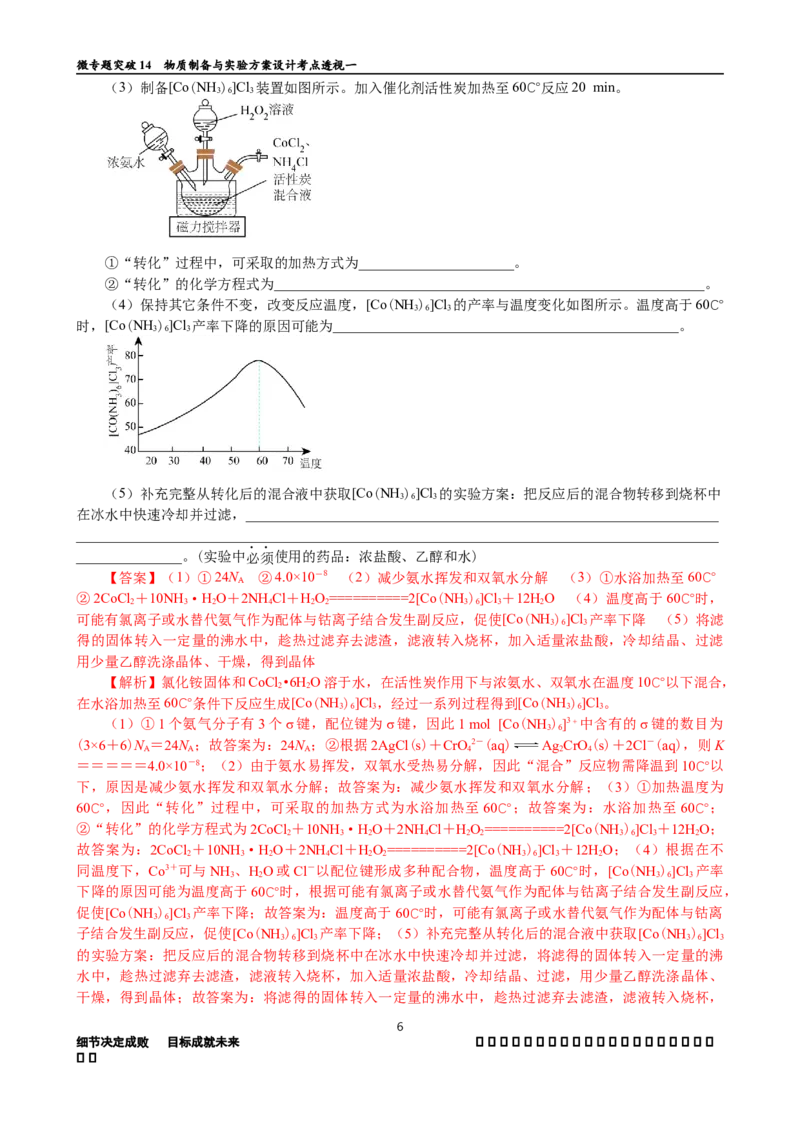
(3)制备[Co(NH )]Cl 装置如图所示。加入催化剂活性炭加热至60℃反应20 min。
3 6 3
①“转化”过程中,可采取的加热方式为______________________。
②“转化”的化学方程式为_____________________________________________________________。
(4)保持其它条件不变,改变反应温度,[Co(NH )]Cl 的产率与温度变化如图所示。温度高于60℃
3 6 3
时,[Co(NH )]Cl 产率下降的原因可能为_________________________________________________。
3 6 3
(5)补充完整从转化后的混合液中获取[Co(NH )]Cl 的实验方案:把反应后的混合物转移到烧杯中
3 6 3
在冰水中快速冷却并过滤,___________________________________________________________________
___________________________________________________________________________________________
_______________。(实验中必须使用的药品:浓盐酸、乙醇和水)
【答案】(1)①24N ②4.0×10-8 (2)减少氨水挥发和双氧水分解 (3)①水浴加热至60℃
A
②2CoCl +10NH ·HO+2NH Cl+HO==========2[Co(NH )]Cl +12HO (4)温度高于60℃时,
2 3 2 4 2 2 3 6 3 2
可能有氯离子或水替代氨气作为配体与钴离子结合发生副反应,促使[Co(NH )]Cl 产率下降 (5)将滤
3 6 3
得的固体转入一定量的沸水中,趁热过滤弃去滤渣,滤液转入烧杯,加入适量浓盐酸,冷却结晶、过滤
用少量乙醇洗涤晶体、干燥,得到晶体
【解析】氯化铵固体和CoCl •6HO溶于水,在活性炭作用下与浓氨水、双氧水在温度10℃以下混合,
2 2
在水浴加热至60℃条件下反应生成[Co(NH )]Cl,经过一系列过程得到[Co(NH )]Cl。
3 6 3 3 6 3
(1)①1个氨气分子有3个σ键,配位键为σ键,因此1 mol [Co(NH )]3+中含有的σ键的数目为
3 6
(3×6+6)N =24N ;故答案为:24N ;②根据2AgCl(s)+CrO2-(aq) Ag CrO(s)+2Cl-(aq),则K
A A A 4 2 4
=====4.0×10-8;(2)由于氨水易挥发,双氧水受热易分解,因此“混合”反应物需降温到10℃以
下,原因是减少氨水挥发和双氧水分解;故答案为:减少氨水挥发和双氧水分解;(3)①加热温度为
60℃,因此“转化”过程中,可采取的加热方式为水浴加热至 60℃;故答案为:水浴加热至 60℃;
②“转化”的化学方程式为2CoCl +10NH ·HO+2NH Cl+HO==========2[Co(NH )]Cl +12HO;
2 3 2 4 2 2 3 6 3 2
故答案为:2CoCl +10NH ·HO+2NH Cl+HO==========2[Co(NH )]Cl +12HO;(4)根据在不
2 3 2 4 2 2 3 6 3 2
同温度下,Co3+可与NH 、HO或Cl-以配位键形成多种配合物,温度高于60℃时,[Co(NH )]Cl 产率
3 2 3 6 3
下降的原因可能为温度高于60℃时,根据可能有氯离子或水替代氨气作为配体与钴离子结合发生副反应,
促使[Co(NH )]Cl 产率下降;故答案为:温度高于60℃时,可能有氯离子或水替代氨气作为配体与钴离
3 6 3
子结合发生副反应,促使[Co(NH )]Cl 产率下降;(5)补充完整从转化后的混合液中获取[Co(NH )]Cl
3 6 3 3 6 3
的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,将滤得的固体转入一定量的沸
水中,趁热过滤弃去滤渣,滤液转入烧杯,加入适量浓盐酸,冷却结晶、过滤,用少量乙醇洗涤晶体、
干燥,得到晶体;故答案为:将滤得的固体转入一定量的沸水中,趁热过滤弃去滤渣,滤液转入烧杯,
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找加入适量浓盐酸,冷却结晶、过滤,用少量乙醇洗涤晶体、干燥,得到晶体。