文档内容
微考点 晶胞计算
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 晶胞模型与切割法计算...............................................................................................................2
考法02 晶胞参数计算...............................................................................................................................6
考法03 原子分数坐标、投影图.............................................................................................................10
...........................................................................................................................................13
1.高考真题考点分布
考点内容 考点分布
晶胞模型与切割法 2024·湖南卷,3分;2024·湖南卷,3分;2024·湖北卷,3分;2024·辽宁卷 ,3
计算 分;
2024·甘肃卷,3分;2023·辽宁卷,3分;2023·湖北卷,3分;2023·湖南卷,3
分;
2022·湖北卷,3分;
晶胞参数计算 2024·河北卷,3分;2024·辽宁卷,3分;2023·辽宁卷,3分;2023·湖北卷 ,3
分;
2023·湖南卷,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,晶胞粒子和化学式的计算、晶胞密度计算、晶胞参数计算仍是高考
命题的热点。
【备考策略】宏观晶体密度与微观晶胞参数的关系【命题预测】
预计2025年高考会以新的情境载体考查晶胞化学式的计算、晶胞密度计算、晶胞参数计算等知识,题目难
度一般较大。
考法01 晶胞模型与切割法计算
1.晶胞的概念及其判断
(1)概念:描述晶体结构的基本单元。
(2)晶体中晶胞的排列——无隙、并置
A.无隙:相邻晶胞之间没有任何间隙。
B.并置:所有晶胞平行排列、取向相同。
(3)晶胞的判断
晶胞是8个顶角相同、三套各4根平行棱分别相同、三套各两个平行面分别相同的最小平行六面体。
2.晶胞中微粒数的计算方法——切割法
(1)原则
晶胞任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份额就是。
(2)实例
①平行六面体晶胞中不同位置的粒子数的计算
②其他晶体结构的计算(以六棱柱晶体结构为例)3.晶胞中粒子配位数的计算
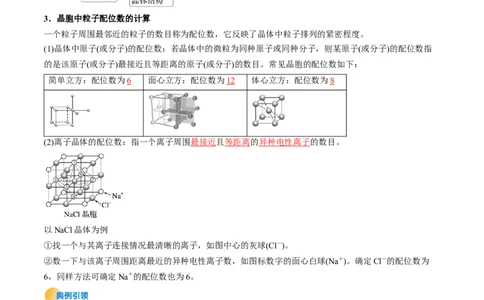
一个粒子周围最邻近的粒子的数目称为配位数,它反映了晶体中粒子排列的紧密程度。
(1)晶体中原子(或分子)的配位数:若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配位数指
的是该原子(或分子)最接近且等距离的原子(或分子)的数目。常见晶胞的配位数如下:
简单立方:配位数为6 面心立方:配位数为12 体心立方:配位数为8
(2)离子晶体的配位数:指一个离子周围最接近且等距离的异种电性离子的数目。
以NaCl晶体为例
①找一个与其离子连接情况最清晰的离子,如图中心的灰球(Cl-)。
②数一下与该离子周围距离最近的异种电性离子数,如图标数字的面心白球(Na+)。确定Cl-的配位数为
6,同样方法可确定Na+的配位数也为6。
考向01 切割法计算微粒数目
【例1】(2024·河北衡水·一模)如图为高温超导领域里的一种化合物(钙钛矿)结构中的最小重复单元。该
化合物中,每个钛离子周围与它最接近且距离相等的钛离子有 a个,元素氧、钛、钙的原子个数比为 b。
则a、b是( )A.6,3∶1∶1 B.24,10∶8∶1
C.12,5∶4∶1 D.3,3∶2∶1
【答案】A
【解析】由晶胞结构可知,晶胞顶角上相邻的钛离子相距最近,则钛离子周围与它最接近且距离相等的钛
离子有6个,a=6;晶胞中钛原子个数为8×=1,氧原子个数为12×=3,钙原子个数为1,则氧、钛、钙
的原子个数比为 3∶1∶1,故选A。
考向02 配位数的计算
【例2】(2024·江苏南京·二模)已知Cu S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中
2
心。
S2-的配位数为________。
【答案】8
【解析】在Cu S晶胞中,正四面体中心共有8个,每个正四面体中心均分布着一个Cu+,每个S2-周围有
2
8个Cu+,故S2-的配位数为8。
【对点1】(2024·湖北·一模)下图是氮化镓的一种晶体结构, 表示阿伏加德罗常数的值。下列说法正
确的是
A.每个 原子周围距离最近的 原子数目为4
B.氮化镓分子式为
C.a、b原子坐标参数依次为 、 、则c原子坐标参数为
D.已知该晶体密度为 ,则镓氮原子间最短距离为
【答案】C
【解析】A.每个 原子周围距离最近的 原子数目为12,A项错误;
B.氮化镓为共价晶体,没有分子,每个晶胞中Ga的个数为 ,N的个数为4,则其化学式为
,B项错误;C.根据a、b原子坐标参数依次为 、 ,判断c原子坐标参数为 ,C项正确;
D.由B项分析知,每个晶胞中含有4个 ,则晶胞的边长为 ,则镓氮原子间最短距离
为体对角线的 ,为 ,D项错误;
故选C。
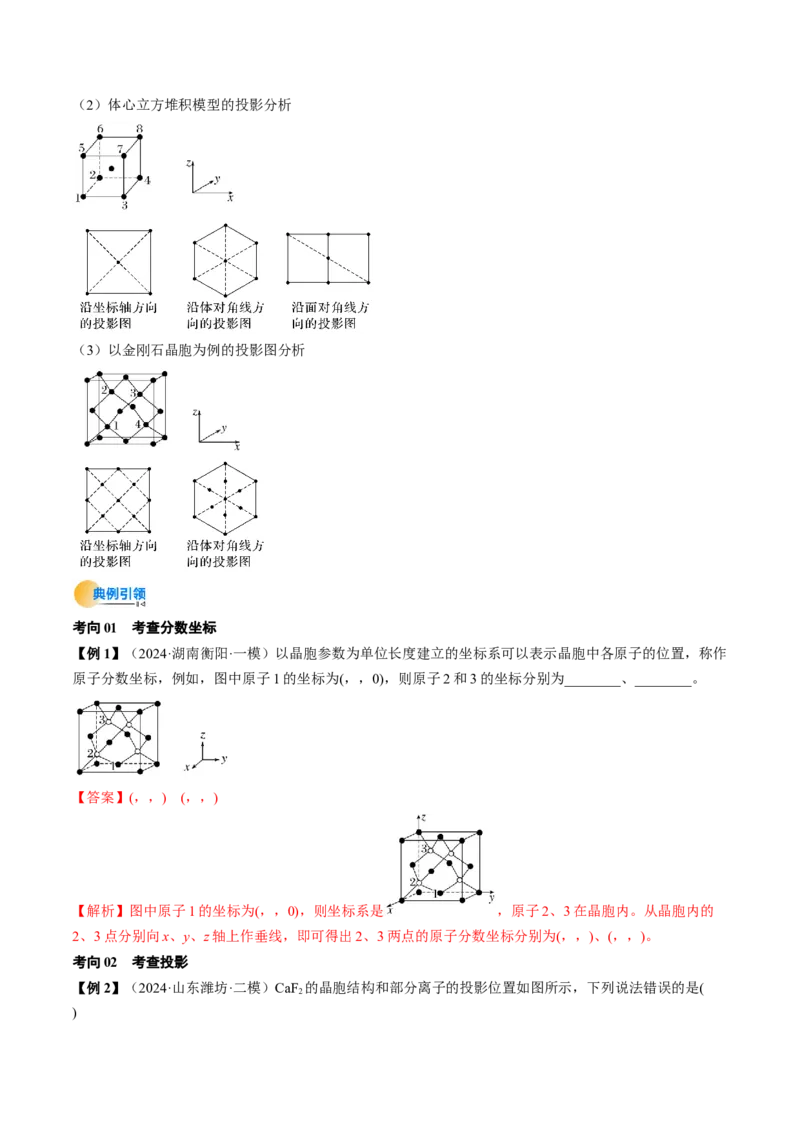
【对点2】(2024·湖南·模拟预测)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示。晶胞
2
参数为apm,阿伏加德罗常数的值为 。下列说法错误的是
A.Y代表的离子是
B.X离子的配位数为8
C.若坐标取向不变,将m点Y离子平移至原点,则n点Y离子位于晶胞xy面的面心
D.该晶体的摩尔体积为
【答案】A
【解析】A.根据萤石晶胞结构,浅色X离子分布在晶胞的顶点和面心上,则1个晶胞中浅色X离子共有
个,深色Y离子分布在晶胞内部,则1个晶胞中共有8个深色Y离子,因此该晶胞的化学式
应为XY ,结合萤石的化学式可知,X为 ,故A错误;
2
B.X离子的配位离子为Y离子,将晶胞进行平移操作,即可找到与其配位的Y离子有8个,故B正确;
C.根据图中所示坐标系,m点坐标为 ,n点坐标为 ,若将m点Y离子平移至原点,晶
胞中各点坐标均由 变为 ;因此n点坐标变为 ,即晶胞xy面的面心,故
C正确;
D.该晶体的摩尔体积为 , ,
故D正确;
故答案选A。考法02 晶胞参数计算
1.晶胞参数
晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的夹角α、β、γ,
即晶格特征参数,简称晶胞参数。
2.宏观晶体密度与微观晶胞参数的关系
3.空间利用率
空间利用率=×100%,球体积为金属原子的总体积。
(1)简单立方堆积
如图所示,原子的半径为r,立方体的棱长为2r,则V =πr3,V =(2r)3=8r3,空间利用率=×100%=
球 晶胞
×100%≈52%。
(2)体心立方堆积
如图所示,原子的半径为r,体对角线c为4r,面对角线b为a,由(4r)2=a2+b2得a=r。1个晶胞中有2个
原子,故空间利用率=×100%=×100%=×100%≈68%。
(3)六方最密堆积
如图所示,原子的半径为r,底面为菱形(棱长为2r,其中一个角为60°),则底面面积S=2r×r=2r2,h=
r,V =S×2h=2r2×2×r=8r3,1个晶胞中有2个原子,则空间利用率=×100%=×100%≈74%。
晶胞
(4)面心立方最密堆积
如图所示,原子的半径为r,面对角线为4r,a=2r,V =a3=(2r)3=16r3,1个晶胞中有4个原子,则空间
晶胞
利用率=×100%=×100%≈74%。考向01 考查晶体的密度
【例1】(2024·河北保定·模拟)我国科学家研究出一种磷化硼纳米颗粒作为高选择性CO 电化学还原为甲醇
2
的非金属电催化剂,磷化硼晶胞结构如图所示,晶胞的棱边边长为a nm,N 为阿伏加德罗常数的值,下
A
列说法错误的是( )
A.磷化硼晶体中共价键与配位键的数目之比为4∶1
B.若氮化硼与磷化硼具有相似的结构,则BN的熔点比BP高
C.磷化硼晶体中,每个硼原子周围紧邻且距离相等的硼原子共有4个
D.磷化硼晶体密度为g·cm-3
【答案】C
【解析】B原子的价电子数为3,且杂化类型为sp3杂化,其中与3个P原子形成3个共价键,另外一条杂
化轨道无电子,为空轨道,与P原子形成配位键,配位键也属于共价键,磷化硼晶体中共价键与配位键的
数目之比为4∶1,A正确;氮化硼与磷化硼都是共价晶体,原子半径:N