文档内容
押广东卷第 12-13 题
元素周期表与周期律 方程式的正误判断
核心考点 考情统计 考向预测 备考策略
2023·广东卷,14 1.重视元素周期表和周期律的
元素周期表与 考查元素周期表和元素周期
2022·广东卷,7 基础知识,其中物质与结构部
周期律 律,尤其要重视电负性、电
分的必备知识要牢记。
2021·广东卷,13
离能和原子结构,主要体现
2.离子方程式主要掌握正误判
基础性和应用性。
断,其中涉及到量的问题要强
考查离子方程式、化学方程
方程式的正误 2022·广东卷,14 化,重视元素及其化合物的转
式的正误判断,主要体现基
判断 2021·广东卷,15 化关系,并能用化学方程式准
础性。
确表达。
1.(2023广东卷,14)化合物 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,
仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周
期,E在地壳中含量最多。下列说法正确的是
A.元素电负性: B.氢化物沸点:
C.第一电离能: D. 和 的空间结构均为三角锥形
2.(2022广东卷,7)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物
对应的水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
3.(2022广东卷,14)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
4.(2021广东卷,13)一种麻醉剂的分子结构式如图所示。其中, 的原子核只有1个质子;元素 、
、 原子序数依次增大,且均位于 的下一周期;元素 的原子比 原子多8个电子。下列说法不正
确的是
A. 是一种强酸
B.非金属性:
C.原子半径:
D. 中, 的化合价为+2价
5.(2021广东卷,15)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方
程式书写正确的是
A. 放入水中:
B. 通过灼热铁粉:
C.铜丝插入热的浓硫酸中:
D. 通入酸性 溶液中:
一、元素周期表和周期律
知能点1 粒子的结构
1.一个信息丰富的粒子(原子或离子)符号
2.粒子间的“四个”数量关系
(1)质子数=核电荷数=核外电子数=原子序数。
(2)质量数=质子数+中子数。
(3)质子数=阳离子的核外电子数+阳离子所带正电荷数。
(4)质子数=阴离子的核外电子数-阴离子所带负电荷数。3.核外电子排布规律
(1)能量最低原理:基态原子核外电子优先占据能量最低的原子轨道,如Ge:1s22s22p63s23p63d104s24p2。
(2)泡利原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子。
(3)洪特规则:当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋
状态相同。
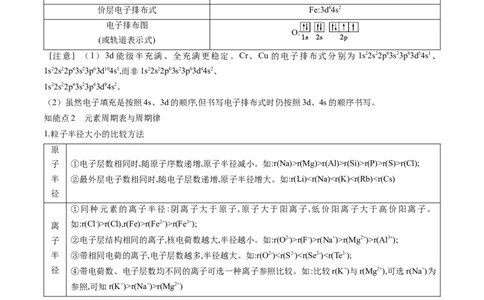
4.核外电子排布的四种表达方式
表示方法 举例
电子排布式 Fe:1s22s22p63s23p63d64s2
简化电子排布式 Fe:[Ar]3d64s2
价层电子排布式 Fe:3d64s2
电子排布图
O:
(或轨道表示式)
[注意] (1)3d 能级半充满、全充满更稳定。Cr、Cu 的电子排布式分别为 1s22s22p63s23p63d54s1、
1s22s22p63s23p63d104s1,而非1s22s22p63s23p63d44s2、
1s22s22p63s23p63d94s2。
(2)虽然电子填充是按照4s、3d的顺序,但书写电子排布式时仍按照3d、4s的顺序书写。
知能点2 元素周期表与周期律
1.粒子半径大小的比较方法
原
子 ①电子层数相同时,随原子序数递增,原子半径减小。如:r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl);
半 ②最外层电子数相同时,随电子层数递增,原子半径增大。如:r(Li)r(Cl),r(Fe)>r(Fe2+)>r(Fe3+);
子 ②电子层结构相同的离子,核电荷数越大,半径越小。如:r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+);
半 ③带相同电荷的离子,电子层数越多,半径越大。如:r(O2-)r(Na+)>r(Mg2+)
2.元素金属性、非金属性强弱的比较
(1)元素金属性强弱的比较。
本质 原子越易失电子,金属性越强
①在金属活动性顺序表中位置越靠前,金属性越强;
判断 ②单质与水或非氧化性酸反应越剧烈,金属性越强;
依据 ③单质还原性越强或离子氧化性越弱,金属性越强;
④最高价氧化物对应水化物的碱性越强,金属性越强;⑤若Xn++Y X+Ym+,则Y金属性比X强
(2)元素非金属性强弱的比较。
本质 原子越易得电子,非金属性越强
①与H 化合越容易,生成的气态氢化物越稳定,非金属性越强;
2
判断 ②单质氧化性越强或阴离子还原性越弱,非金属性越强;
依据 ③最高价氧化物对应水化物的酸性越强,非金属性越强;
④若An-+B Bm-+A,则B非金属性比A强
知能点3 元素第一电离能、电负性的变化规律
1.元素第一电离能的变化规律
一
般 同周期,随着原子序数的增大,元素的第一电离能呈现增大的趋势,稀有气体元素的第一电离能最大,碱
规 金属元素的第一电离能最小;同主族,随着电子层数的增加,元素的第一电离能逐渐减小
律
第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子核外电子排布在能量相等
特
的轨道上形成全空(p0、d0、f0)、半充满(p3、d5、f7)和全充满(p6、d10、f14)结构时,原子的能量较低,该
殊
元素具有较大的第一电离能。如同周期元素,第ⅡA族元素的原子最外层s能级全充满(或p能级全
情
空),第ⅤA族元素的原子最外层p能级半充满,比较稳定,所以其第一电离能大于同周期相邻的主族元
况
素
2.元素电负性的变化规律
(1)同周期元素从左到右,元素的电负性逐渐增大。
(2)同主族元素从上到下,元素的电负性逐渐减小。
(3)元素的非金属性越强,元素的电负性越大。
(4)常常应用化合价及物质类别判断电负性的大小,如O与Cl的电负性比较:HClO中Cl为+1价、O为-2
价,可知O的电负性大于Cl;Al O 是离子化合物、AlCl 是共价化合物,可知O的电负性大于Cl。
2 3 3
二、方程式的正误判断
知能点1 氧化还原反应的“四大规律”及方程式的配平
1.氧化还原反应的规律及其应用2.氧化还原反应方程式的配平流程
知能点2 离子共存
1.有条件的离子共存
条
类型 举例
件
颜
Fe3+(棕黄色)、Fe2+(浅绿色)、Cu2+(蓝色)、MnO-
(紫红色)等有色离
4
无色溶液
色 子不能大量存在
①常温下,pH<7;
a.能与H+大量共存的阴离子只有强酸阴离子(如:Cl-、SO2− 、NO-
②使甲基橙(或石蕊溶液)变红 4 3
酸
、I-、Br-等);
的溶液;
性
K b.不能与 H+大量 共存 的阴离子有 OH-、CO2− 、HCO- 、
条 ③ 常 温 下 , w =1×10-13 3 3
c(H+) CHCOO-、SO2− 、HSO- 、[Al(OH) ]-、SiO2− 、ClO-等;
件 3 3 3 4 3
mol/L; c.在酸性条件下含有NO- 时,Fe2+不能大量存在
3
④0.1 mol/L H SO 溶液;
2 4⑤0.1 mol/L HCl 溶液
①常温下,pH>7;
②使酚酞溶液变红(或石蕊溶
a.能与OH-大量共存的阳离子只有K+、Na+、Ba2+,其余的阳离子
碱
液变蓝)的溶液;
性
(如:H+、NH+
、Ca2+、Mg2+、Fe3+、Fe2+、Cu2+、Al3+、Ag+等)都不
4
c(H+)
条 ③常温下, =1×10-12 能大量存在;
c(OH-)
件 b.弱酸的酸式酸根离子(HCO- 、HSO- )与OH-不能大量共存
的溶液; 3 3
④0.1 mol/L NaOH溶液
酸
①与 Al 反应能放出 H 的溶
2
性
液;
或
HCO-
既不能与H+大量共存又不能与OH-大量共存
3
② 常 温 下 , 水 电 离 的
碱
c(H+)=1×10-13 mol/L 的溶液
性
特 0.1 mol/L FeCl 溶液 OH-、I-、Ag+、SCN-等不能大量共存
3
定 0.1 mol/L K CO 溶液 Ba2+、Ca2+、Al3+、H+、Fe3+、Fe2+等不能大量共存
2 3
物
质
的 0.1 mol/L FeCl 溶液 OH-、ClO-、CO2− 、Ag+等不能大量共存
2 3
溶
液
2.不能大量共存的原因
原因 举例
发生复分解反应(有沉淀、弱电解 Ba2+与 SO2 4 − 、CO 3 2− ,H+与 HCO 3 - 、OH-、CH 3 COO-,Ca2+与 SO2 4 − 、C
质或气体生成) O2− 等不能大量共存
3
Fe2+、NO- (在酸性溶液中),S2-、SO2− (在酸性溶液中),Fe2+与ClO-,Mn
3 3
发生氧化还原反应
O-
、Fe3+与I-不能大量共存
4
有络合物生成的反应 Fe3+与SCN-不能大量共存
水解相互
Al3+与HCO-
,Al3+与[Al(OH) ]-不能大量共存
3 4
促进的反应
知能点3 离子方程式的书写与正误判断
1.建立与“量”有关的离子方程式的书写思维模型2.把握离子方程式正误判断的四个关键点
注意反应环境
如CrO2− 在酸性条件下转化为CrO2− :2CrO2− +2H+ CrO2− +H O
4 2 7 4 2 7 2
审清题意 注意操作顺序
“三注 如把铝盐滴入NaOH溶液中:Al3++4OH- [Al(OH) ]-
4
意” 注意反应物之间量的关系
如 向 NaHSO 溶 液 中 滴 加 Ba(OH) 溶 液 至 SO2− 恰 好 沉 淀 :H++OH-+SO2− +Ba2+
4 2 4 4
BaSO↓+H O
4 2
化学式拆
写 易溶强电解质拆,弱电解质、难溶物不拆;微溶物清拆浊不拆;单质、氧化物不拆;浓硫酸不拆,
“四原 浓盐酸、浓硝酸拆
则”
分析量不同时的产物
如向Ca(OH) 溶液中滴加少量NaHCO
溶液:HCO-
+OH-+Ca2+ CaCO ↓+H O
2 3 3 3 2
反应产物 分析是否漏掉同步反应
“三分 如 Ba(OH) 与硫酸反应:2H++2OH-+SO2− +Ba2+ BaSO↓+2H O,而不是 SO2− +Ba2+
2 4 4 2 4
析”
BaSO↓
4
分析变价元素的产物
如Fe O 与盐酸反应:Fe O+8H+ Fe2++2Fe3++4H O
3 4 3 4 2
方程式遵
循
原子守恒、电荷守恒、电子转移守恒
“三守
恒”
考点一 元素周期表与周期律
1.(2024届广东省梅州一模)Q、R、X、Y是原子序数依次增大的同周期不同主族的非金属元素,Q的基态原子p轨道电子数是s轨道电子数的一半,同周期元素基态原子中R的未成对电子数最多。下列说法
不正确的是
A.简单氢化物的沸点: B.元素电负性:
C.第一电离能: D.简单离子半径:
2.(2024届广东省茂名二模)催化剂(XYZ ME )的组成元素均为主族元素且在每个短周期均有分布,X的
6 5
基态原子p轨道电子总数比s轨道电子总数多1个;仅Y、M、E处于同一周期,原子序数依次增大且相
邻;E在地壳中含量最多。下列说法不正确的是
A.第一电离能:M>E>X B.简单氢化物的稳定性:E>M
C.氧化物的熔点:X>Y>Z D. 和 的空间结构相同
3.(2024届广东省梅州二模)由原子序数依次增大的短周期主族元素X、Y、Z、W构成的离子化合物结
构如下图所示,Y、Z相邻且与X、W均不同周期。下列说法不正确的是
A.元素电负性:
B. 的VSEPR模型为四面体形
C.Y和Z的简单氢化物都是由极性键构成的极性分子
D.第一电离能:
4.(2024届广东省惠州三模)一种因具有成本低廉及反应性质多样等优点被用作有机合成的缩合试剂,
其由4种短周期非金属元素组成,结构如图所示,其中W、X、Y为同一周期,X与Z为同一主族。下列
说法正确的是
A.简单氢化物的沸点:Y>W B.电负性:X>W>Y>Z
C.XW 中元素X为sp3杂化 D.YX 是含极性键的极性分子
2 2
5.(2024届广东省广州市天河区二模)颜料紫是含锰化妆品着色剂,其化学式为 ,X、Y、
Q、Z为原子序数依次增大的短周期元素,其中 对具有正四面体空间结构, 的结构如图所示。下
列说法正确的是A.键角:
B.第一电离能:
C.简单氢化物沸点:
D. 中各原子最外层均为8电子稳定结构
6.(2024届广东省广州一模)化合物 所含的5种元素均为短周期主族元素, 、 和 为同
周期元素,原子序数依次增加, 的基态原子价层电子排布式为 , 的基态原子价层 轨道半充满,
是地壳中含量最多的元素, 是有机分子的骨架元素,下列说法正确的是
A.元素电负性:
B.简单氢化物沸点:
C.第一电离能:
D. 和 的空间结构均为直线形
7.(2024届广东省广州二模)化合物 可作食品膨松剂,W、X、Y、Z为原子序数依次增大的
短周期元素,W的基态原子s能级上的电子总数和p能级上的电子总数相等,W和Z同族,Y是地壳中含
量最多的金属元素,下列说法正确的是
A.第一电离能:X>Y>Z B.简单氢化物沸点:Z>W
C.原子半径:Z>Y>X>W D. 和 的空间结构均为V形
8.(2024届广东省佛山一模) 是一种新型电极材料,所含元素位于前四周期,仅X、E同周期,
E是地壳中含量最多的元素,X可与水反应生成 ,Y的合金用量最大,用途最广,M的基态原子的p轨
道上填充的电子数目满足 ,下列说法错误的是
A.单质的熔点:XE
C. 的构型为正四面体形 D.X和E能形成离子化合物
9.(2024届广东省佛山二模)我国科学家发现,添加 能有效减缓锂离子电池容量衰减,其结
构式如图所示。其中Z原子满足8电子稳定结构,Z、Y、W、X是原子序数依次增大的短周期元素,X、
Y原子核外均有2个未成对电子。下列说法正确的是
A.第一电离能:ZY>Z
C.简单氢化物稳定性:YZ>Y
B.第一电离能:Y>X>W
C.Q的最高价氧化物对应的水化物可能是强酸
D.XW、 的空间结构名称均为三角锥形
3
12.(2024届广东省深圳一模)W、X、Y、Z是原子序数依次增大的主族元素,在前三周期均有分布,基
态X原子有四种不同空间运动状态的电子;Y为地壳中含量最多的元素,其简单离子与Z的简单离子具有
相同电子数;工业上常通过电解Z的氧化物制取其单质,下列说法不正确的是
A.元素电负性: B.简单氢化物的沸点:
C.原子半径: D.Z同周期且第一电离能小于Z的元素有2种
13.(2024届广东省4月名校联考)短周期主族元素X、Y、Z、W的原子半径逐渐增大,它们原子的最
外层电子数之和为15,X原子核外电子总数等于W原子次外层电子数,W与X可形成原子个数比为1∶1的
化合物,Y与Z同主族。下列说法正确的是
A.高温下,ZX 可与WYX 反应
2 2 3
B.X同周期中第一电离能比X小的元素有5种
C.简单氢化物的键角:Y