文档内容
易错类型 04 氧化还原反应
【易错点01】不能正确辨析氧化还原反应有关概念
【易错点02】不能正确判断物质氧化性或还原性强弱
【易错点03】不能利用氧化还原反应规律判断反应能否进行
【易错点04】不能利用氧化还原反应规律判断反应物的反应顺序
【易错点05】不能正确书写陌生的氧化还原反应方程式
【易错点06】不能利用守恒律进行氧化还原反应综合判断与计算
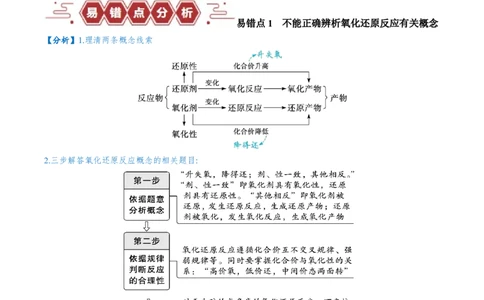
易错点1 不能正确辨析氧化还原反应有关概念
【分析】1.理清两条概念线索
2.三步解答氧化还原反应概念的相关题目:
易错点2 不能正确判断物质氧化性或还原性强弱
【分析】物质的氧化性(或还原性)的强弱与得失电子的难易程度有关,与得失电子的数目无关,但外界因
素(如反应条件、反应物浓度、酸碱性等)也影响物质的氧化性(或还原性)。例如,NO在酸性条件下具有强氧化性,但在中性或碱性条件几乎不表现氧化性。
易错点3 不能利用氧化还原反应规律判断反应能否进行
【分析】含不同价态同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价→
中间价”,而不会出现交叉现象。简记为“两相靠,不相交”。例如,不同价态硫之间可以发生氧化还原
反应的是①②③④。
注:⑤中不会出现HS转化为SO 而HSO 转化为S的情况。
2 2 2 4
易错点4 不能利用氧化还原反应规律判断反应物的反应顺序
【分析】
1.难易律
(1)内容:越易失电子的物质,失去电子后就越难得电子,越易得电子的物质,得到后就越难失电子,一种
氧化剂同时和几种还原剂相遇时,还原性最强的优先发生反应;同理,一种还原剂同时和几种氧化剂相遇
时,氧化性最强的优先发生反应。
可把常见微粒的氧化性、还原性按强弱以位置前后的形式排列:
(2)应用:①判断物质的稳定性;②判断物质反应的先后顺序,即左上方的一种氧化剂可氧化它右下方的还
原性微粒.若有多种,则优先氧化较右下方的微粒;③选择合适的氧化剂或还原剂,如要氧化Fe2+而Br-
不被氧化,则可选择Br ;④判断氧化性微粒、还原性微粒能否共成。虚线所指两种微粒一定能发生反应,
2
故不共存;实线所指微粒能共存.
2.(1)在浓度相差不大的溶液中,若同时含有多种还原剂,加入氧化剂时,将按照物质的还原性由强到弱的
顺序依次发生反应。例如,在FeBr 和FeI 混合液中通入Cl 时,由于还原性:I->Fe2+>Br-,故被Cl 氧
2 2 2 2
化的离子的先后顺序为I-、Fe2+、Br-。
(2) 在浓度相差不大的溶液中,若同时含有多种氧化剂,加入还原剂时,将按照物质的氧化性由强到弱的
顺序依次发生反应。如向含有Fe3+、Cu2+、H+的溶液中加入铁粉,因为氧化性:Fe3+>Cu2+>H+,所以
铁粉先与Fe3+反应,然后依次与Cu2+、H+反应。
3.熟记两串微粒的反应先后顺序
(1)同一还原剂与多种氧化剂发生氧化还原反应的先后顺序:KMnO (H+)>Cl>Br >Fe3+>Cu2+>H+。
4 2 2
(2)同一氧化剂与多种还原剂发生氧化还原反应的先后顺序:S2->SO(或HSO)>I->Fe2+>Br->Cl-。
易错点5 不能正确书写陌生的氧化还原反应方程式
【分析】第1步:根据氧化性、还原性强弱顺序确定氧化性最强的为氧化剂,还原性最强的为还原剂;根
据化合价规律和题给信息及已知元素化合物性质确定相应的还原产物、氧化产物;第2步:根据氧化还原反应的守恒规律确定氧化剂、还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据溶液的酸碱性,通过在反应方程式的两端添加H+或OH-的形式使方程式两端的电荷守恒。
第4步:根据原子守恒(质量守恒),通过在反应方程式两端添加 HO(或其他小分子)使方程式两端的原
2
子守恒。
缺项型氧化还原反应方程式的补项类型、补项原则和组合方式
①补项类型
条件 补项原则
酸性条件下 缺H(氢)或多O(氧)补H+,少O(氧)补HO(水)
2
碱性条件下 缺H(氢)或多O(氧)补HO,少O(氧)补OH-(水)
2
②补项原则
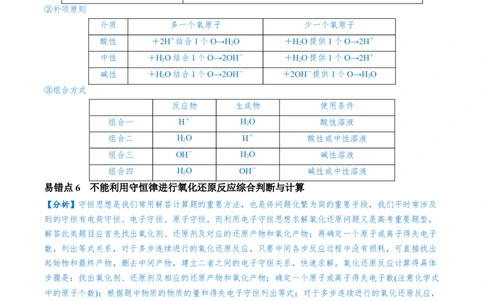
介质 多一个氧原子 少一个氧原子
酸性 +2H+结合1个O→H O +HO提供1个O→2H+
2 2
中性 +HO结合1个O→2OH- +HO提供1个O→2H+
2 2
碱性 +HO结合1个O→2OH- +2OH-提供1个O→H O
2 2
③组合方式
反应物 生成物 使用条件
组合一 H+ HO 酸性溶液
2
组合二 HO H+ 酸性或中性溶液
2
组合三 OH- HO 碱性溶液
2
组合四 HO OH- 碱性或中性溶液
2
易错点6 不能利用守恒律进行氧化还原反应综合判断与计算
【分析】守恒思想是我们常用解答计算题的重要方法,也是将问题化繁为简的重要手段,我们平时常涉及
到的守恒有电荷守恒、电子守恒、原子守恒。而利用电子守恒思想求解氧化还原问题又是高考重要题型,
解答此类题目应首先找出氧化剂、还原剂及对应的还原产物和氧化产物;再确定一个原子或离子得失电子
数,列出等式关系,对于多步连续进行的氧化还原反应,只要中间各步反应过程中没有损耗,可直接找出
起始物和最终产物,删去中间产物,建立二者之间的电子守恒关系,快速求解。氧化还原反应计算得具体
步骤是:找出氧化剂、还原剂及相应的还原产物和氧化产物;确定一个原子或离子得失电子数(注意化学式
中的原子个数);根据题中物质的物质的量和得失电子守恒列出等式;对于多步连续进行的氧化还原反应,
只要中间各步反应过程中没有损耗,可直接找出起始物和最终产物,删去中间产物,建立二者之间的电子
守恒关系,快速求解。
突破1 不能正确辨析氧化还原反应有关概念
【例1】(2022·山东卷)古医典富载化学知识,下述之物见其氧化性者为
A.金(Au):“虽被火亦未熟"
B.石灰(CaO):“以水沃之,即热蒸而解”C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳( ):“色黄,以苦酒(醋)洗刷则白”
【例2】(2022·浙江卷)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
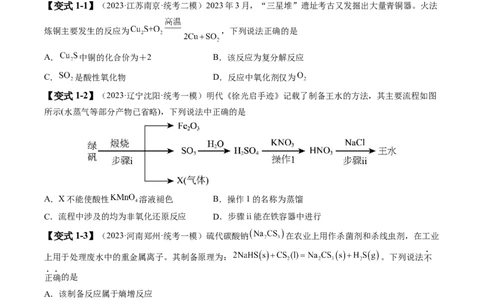
【变式1-1】(2023·江苏南京·统考二模)2023年3月,“三星堆”遗址考古又发掘出大量青铜器。火法
炼铜主要发生的反应为 ,下列说法正确的是
A. 中铜的化合价为+2 B.该反应为复分解反应
C. 是酸性氧化物 D.反应中氧化剂仅为
【变式1-2】(2023·辽宁沈阳·统考一模)明代《徐光启手迹》记载了制备王水的方法,其主要流程如图
所示(水蒸气等部分产物已省略),下列说法中正确的是
A.X不能使酸性 溶液褪色 B.操作1的名称为蒸馏
C.流程中涉及的均为非氧化还原反应 D.步骤ⅱ能在铁容器中进行
【变式1-3】(2023·河南郑州·统考一模)硫代碳酸钠 在农业上用作杀菌剂和杀线虫剂,在工业
上用于处理废水中的重金属离子。其制备原理为: 。下列说法不
正确的是
A.该制备反应属于熵增反应
B. 与 性质相似,不能被氧化
C.制备 的反应属于非氧化还原反应
D. 与盐酸反应,生成NaCl、 和
突破2 不能正确判断物质氧化性或还原性强弱
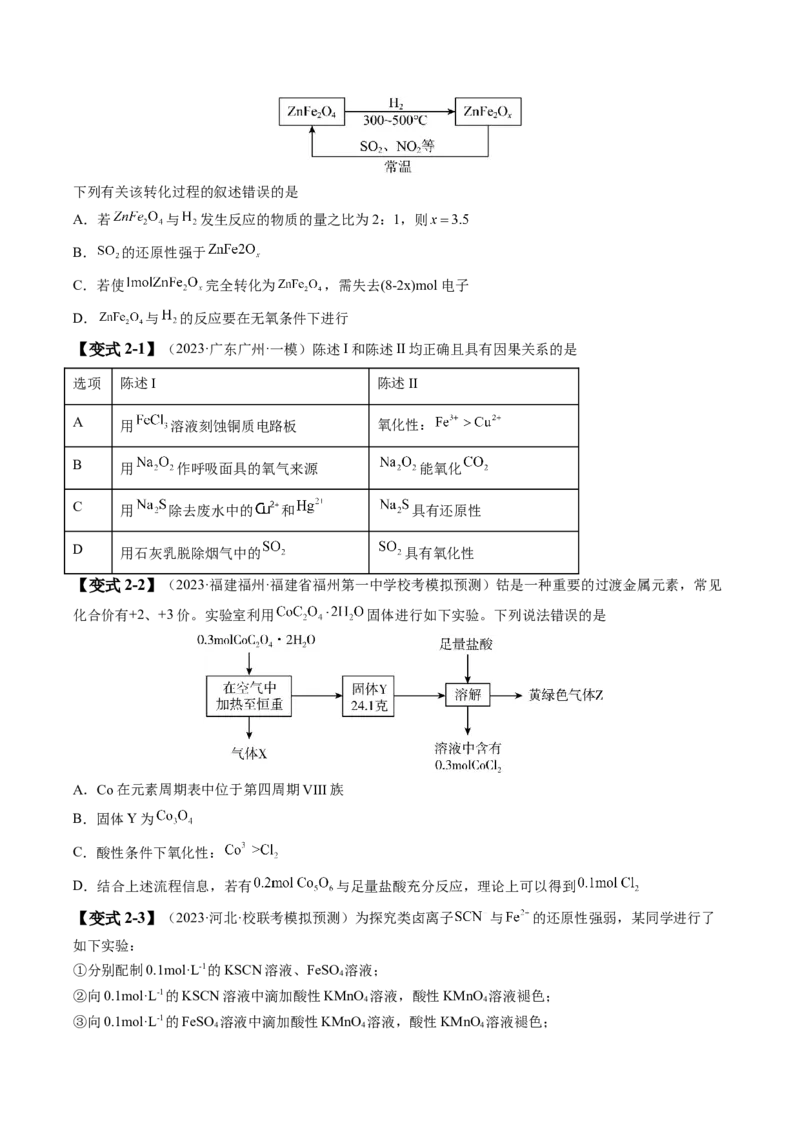
【例3】已知工业上制备氧缺位铁酸盐 的部分流程如图,该方法可实现氮、硫氧化物
的废气利用,转化流程如图所示。下列有关该转化过程的叙述错误的是
A.若 与 发生反应的物质的量之比为2:1,则
B. 的还原性强于
C.若使 完全转化为 ,需失去(8-2x)mol电子
D. 与 的反应要在无氧条件下进行
【变式2-1】(2023·广东广州·一模)陈述I和陈述II均正确且具有因果关系的是
选项 陈述I 陈述II
A 用 溶液刻蚀铜质电路板 氧化性:
B 用 作呼吸面具的氧气来源 能氧化
C 用 除去废水中的 和 具有还原性
D 用石灰乳脱除烟气中的 具有氧化性
【变式2-2】(2023·福建福州·福建省福州第一中学校考模拟预测)钴是一种重要的过渡金属元素,常见
化合价有+2、+3价。实验室利用 固体进行如下实验。下列说法错误的是
A.Co在元素周期表中位于第四周期VIII族
B.固体Y为
C.酸性条件下氧化性:
D.结合上述流程信息,若有 与足量盐酸充分反应,理论上可以得到
【变式2-3】(2023·河北·校联考模拟预测)为探究类卤离子 与 的还原性强弱,某同学进行了
如下实验:
①分别配制0.1mol·L-1的KSCN溶液、FeSO 溶液;
4
②向0.1mol·L-1的KSCN溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4
③向0.1mol·L-1的FeSO 溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4 4④向等体积浓度均为0.1mol·L-1的KSCN和FeSO 混合溶液中滴加酸性KMnO 溶液,溶液先变红后褪色。
4 4
下列说法正确的是
A.实验①中必须用到分液漏斗、锥形瓶等玻璃仪器
B.实验②中 将 还原为
C.实验③中反应的离子方程式为
D.实验④说明还原性:
突破3 不能利用氧化还原反应规律判断反应能否进行
【例4】(2022·辽宁卷)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶液恢
复棕色;加入 ,振荡,静置,液体分层。下列说法正确的是
A.褪色原因为 被 还原
B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈
D.溶液恢复棕色的原因为 被氧化
【变式3-1】已知还原性:Cl-I-。向含a mol KI和a mol KSO 的混合液中通入b mol Cl 充分反应(不
2 3 2
考虑Cl 与I 之间的反应)。下列说法不正确的是( )
2 2
A.当a≥b时,发生的离子反应为SO+Cl+HO===SO+2H++2Cl-
2 2
B.当5a=4b时,发生的离子反应为4SO+2I-+5Cl+4HO===4SO+I+8H++10Cl-
2 2 2
C.当a≤b≤a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol
D.当a