文档内容
模板 03 化学反应速率与平衡图像分析
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明 ·模板构建 答题模板 + 技巧点拨
技法01 速率-时间图像 技法02 含量/转化率-时间-压强/温度图像
技法03 转化率(或含量)—温度/压强图像 技法04 工业生产中的速率和平衡图像
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
化学反应速率和平衡图像题的呈现方式变得越来越新颖,如试题中涉及的图像已不仅仅是速率与简单
的化学平衡,研究体系也已不是单纯的气相体系,往往根据实际工业生产,更多的是研究复杂液相反
应体系,坐标参数也不再局限于时间、温度、压强、速率、转化率、百分含量,而是有更多的变量,
像物质的量之比、气体分压或离子浓度的对数或负对数等,分析投料比、转化率、产率的变化。多变
量图象题是高考考查的一个方向和趋势,它是指在一个图上存在多个变量的图象,此类题的特点是:
一方面信息量大,考查了读图能力;另一方面多变量的存在,考查了分析推理能力,在新课标高考中
受到命题者的青睐。
第一步:仔细审题 阅读题目获取对解题有价值的信息,排除无效信息,并作标记。
第二步:确定变量 明确横、纵轴代表的物理量,确定变量。
第三步:分析图像 分析不同类型的图像的变化趋势,选择不同的特殊点或添加辅助线。
①关注曲线的走向和变化趋势,分析变化的原因;
②关注起点、拐点、交叉点、平衡点、标有具体坐标的点、含量或转化率相
同的点、终点、按化学计量数投料点的含义;
③判断是否要作辅助线,如等温线、等压线、等时间线等。
第四步:综合判断 图表与原理整合,逐项分析图表,根据相关反应原理(特别是影响因素及使
用前提条件等)及题干信息进行分析判断。技法01 速率-时间图像
1.常见图像形式
(1)速率-时间图像
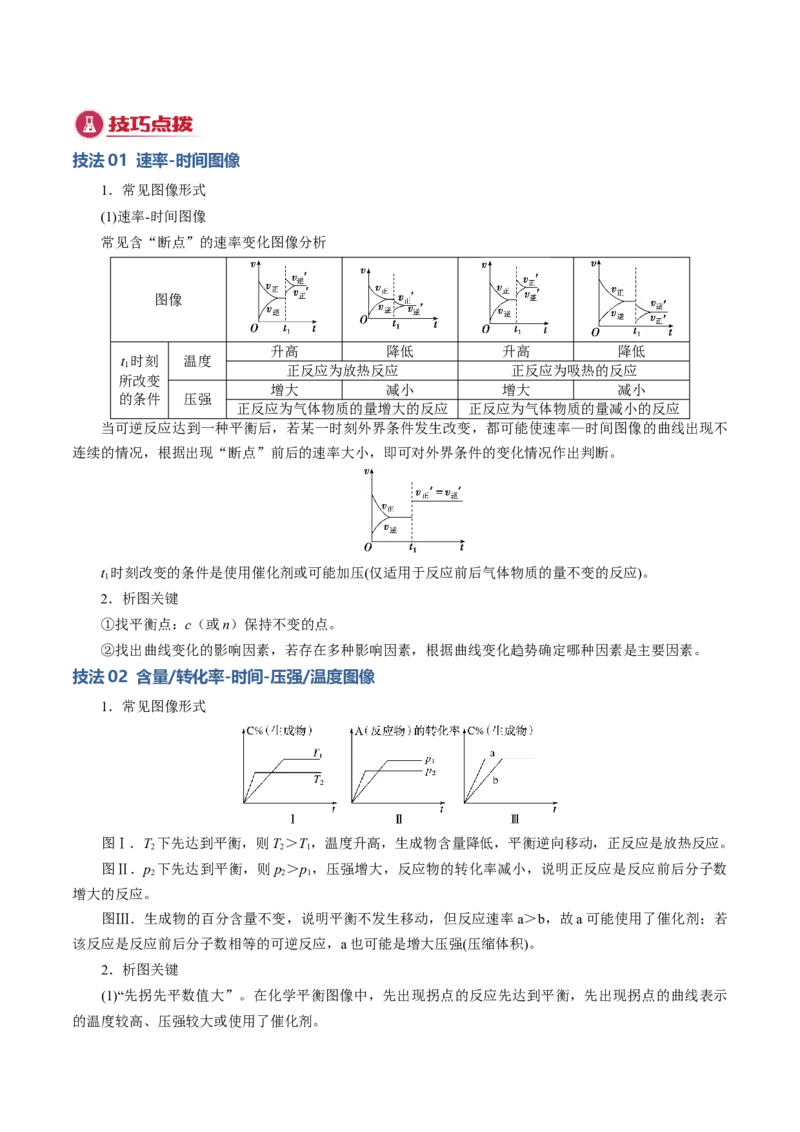
常见含“断点”的速率变化图像分析
图像
升高 降低 升高 降低
t 时刻 温度
1 正反应为放热反应 正反应为吸热的反应
所改变
增大 减小 增大 减小
的条件 压强
正反应为气体物质的量增大的反应 正反应为气体物质的量减小的反应
当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率—时间图像的曲线出现不
连续的情况,根据出现“断点”前后的速率大小,即可对外界条件的变化情况作出判断。
t 时刻改变的条件是使用催化剂或可能加压(仅适用于反应前后气体物质的量不变的反应)。
1
2.析图关键
①找平衡点:c(或n)保持不变的点。
②找出曲线变化的影响因素,若存在多种影响因素,根据曲线变化趋势确定哪种因素是主要因素。
技法02 含量/转化率-时间-压强/温度图像
1.常见图像形式
图Ⅰ.T 下先达到平衡,则T>T,温度升高,生成物含量降低,平衡逆向移动,正反应是放热反应。
2 2 1
图Ⅱ.p 下先达到平衡,则p >p ,压强增大,反应物的转化率减小,说明正反应是反应前后分子数
2 2 1
增大的反应。
图Ⅲ.生成物的百分含量不变,说明平衡不发生移动,但反应速率a>b,故a可能使用了催化剂;若
该反应是反应前后分子数相等的可逆反应,a也可能是增大压强(压缩体积)。
2.析图关键
1“先拐先平数值大”。在化学平衡图像中,先出现拐点的反应先达到平衡,先出现拐点的曲线表示
的温度较高、压强较大或使用了催化剂。2正确掌握图像中反应规律的判断方法。
技法03 转化率(或含量)—温度/压强图像
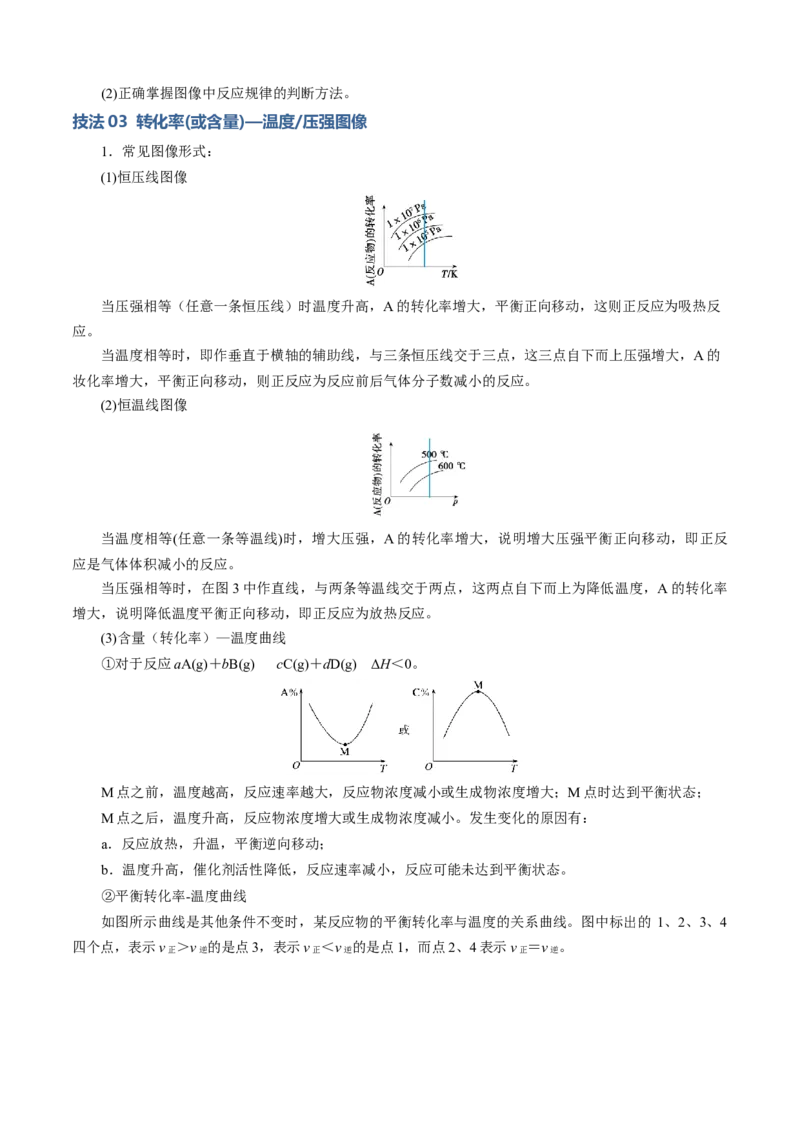
1.常见图像形式:
(1)恒压线图像
当压强相等(任意一条恒压线)时温度升高,A的转化率增大,平衡正向移动,这则正反应为吸热反
应。
当温度相等时,即作垂直于横轴的辅助线,与三条恒压线交于三点,这三点自下而上压强增大,A的
妆化率增大,平衡正向移动,则正反应为反应前后气体分子数减小的反应。
(2)恒温线图像
当温度相等(任意一条等温线)时,增大压强,A的转化率增大,说明增大压强平衡正向移动,即正反
应是气体体积减小的反应。
当压强相等时,在图3中作直线,与两条等温线交于两点,这两点自下而上为降低温度,A的转化率
增大,说明降低温度平衡正向移动,即正反应为放热反应。
(3)含量(转化率)—温度曲线
①对于反应aA(g)+bB(g)cC(g)+dD(g) ΔH<0。
M点之前,温度越高,反应速率越大,反应物浓度减小或生成物浓度增大;M点时达到平衡状态;
M点之后,温度升高,反应物浓度增大或生成物浓度减小。发生变化的原因有:
a.反应放热,升温,平衡逆向移动;
b.温度升高,催化剂活性降低,反应速率减小,反应可能未达到平衡状态。
②平衡转化率-温度曲线
如图所示曲线是其他条件不变时,某反应物的平衡转化率与温度的关系曲线。图中标出的 1、2、3、4
四个点,表示v >v 的是点3,表示v <v 的是点1,而点2、4表示v =v 。
正 逆 正 逆 正 逆图像曲线上的点全为对应条件下的平衡点。
2.析图关键——关注曲线变化趋势,采取“定一议二”法。
在化学平衡图像中,包括纵坐标、横坐标和曲线所表示的三个量。确定横坐标所表示的量,讨论纵坐
标与曲线的关系,或者确定纵坐标所表示的量,讨论横坐标与曲线的关系,即“定一议二”。
技法04 工业生产中的速率和平衡图像
1.含量/转化率—投料比图像
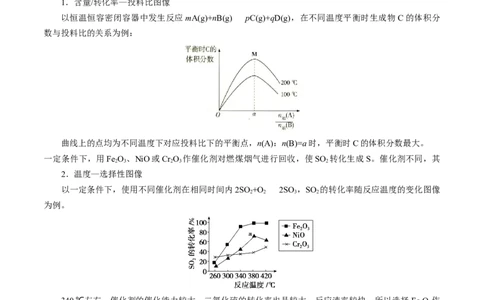
以恒温恒容密闭容器中发生反应mA(g)+nB(g)pC(g)+qD(g),在不同温度平衡时生成物C的体积分
数与投料比的关系为例:
曲线上的点均为不同温度下对应投料比下的平衡点,n(A):n(B)=a时,平衡时C的体积分数最大。
一定条件下,用Fe O 、NiO或Cr O 作催化剂对燃煤烟气进行回收,使SO 转化生成S。催化剂不同,其
2 3 2 3 2
2.温度—选择性图像
以一定条件下,使用不同催化剂在相同时间内2SO +O 2SO ,SO 的转化率随反应温度的变化图像
2 2 3 2
为例。
340 ℃左右,催化剂的催化能力较大,二氧化硫的转化率也是较大,反应速率较快,所以选择 Fe O 作
2 3
催化剂,最适宜温度为340 ℃左右;a点以后,催化剂催化能力需要维持在一定的温度下,温度太高,催化
剂活性可能会降低。
类型01 时间图像
1.(2023·辽宁卷)一定条件下,酸性KMnO 溶液与HC O 发生反应,Mn(Ⅱ)起催化作用,过程中
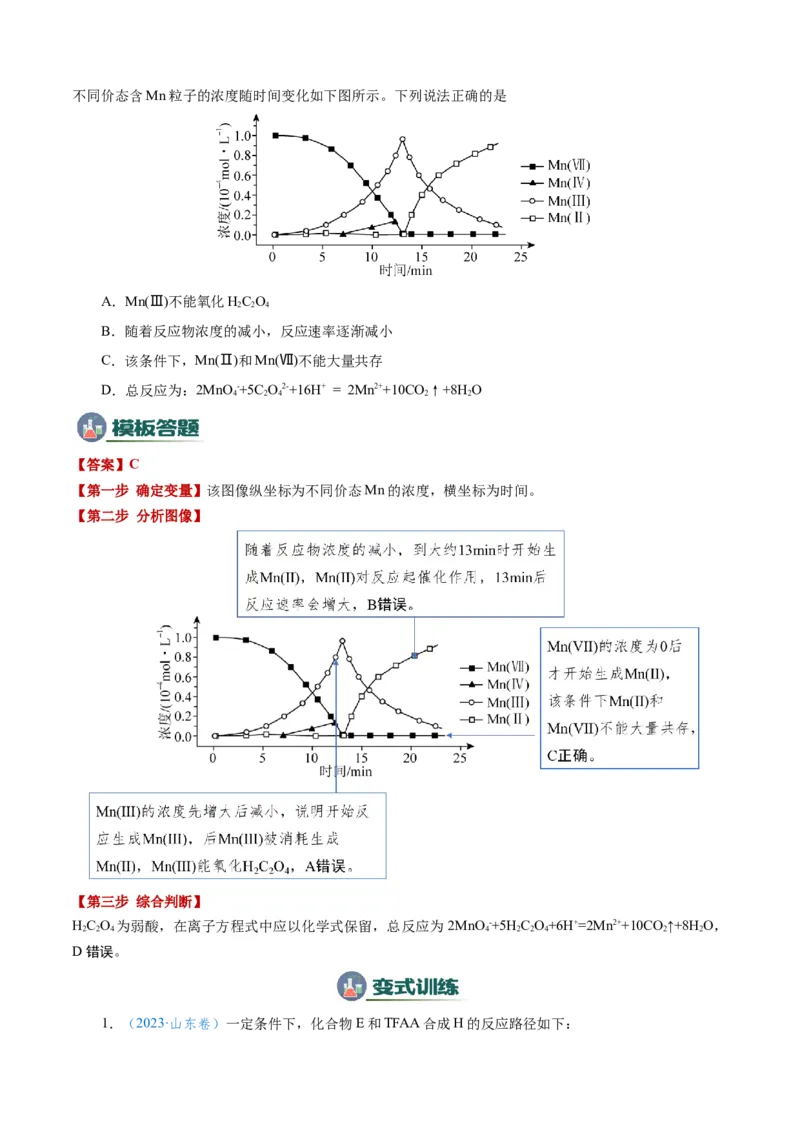
4 2 2 4不同价态含Mn粒子的浓度随时间变化如下图所示。下列说法正确的是
A.Mn(Ⅲ)不能氧化HC O
2 2 4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
D.总反应为:2MnO -+5C O2-+16H+ = 2Mn2++10CO ↑+8H O
4 2 4 2 2
【答案】C
【第一步 确定变量】该图像纵坐标为不同价态Mn的浓度,横坐标为时间。
【第二步 分析图像】
【第三步 综合判断】
HC O 为弱酸,在离子方程式中应以化学式保留,总反应为 2MnO -+5H C O+6H+=2Mn2++10CO ↑+8H O,
2 2 4 4 2 2 4 2 2
D错误。
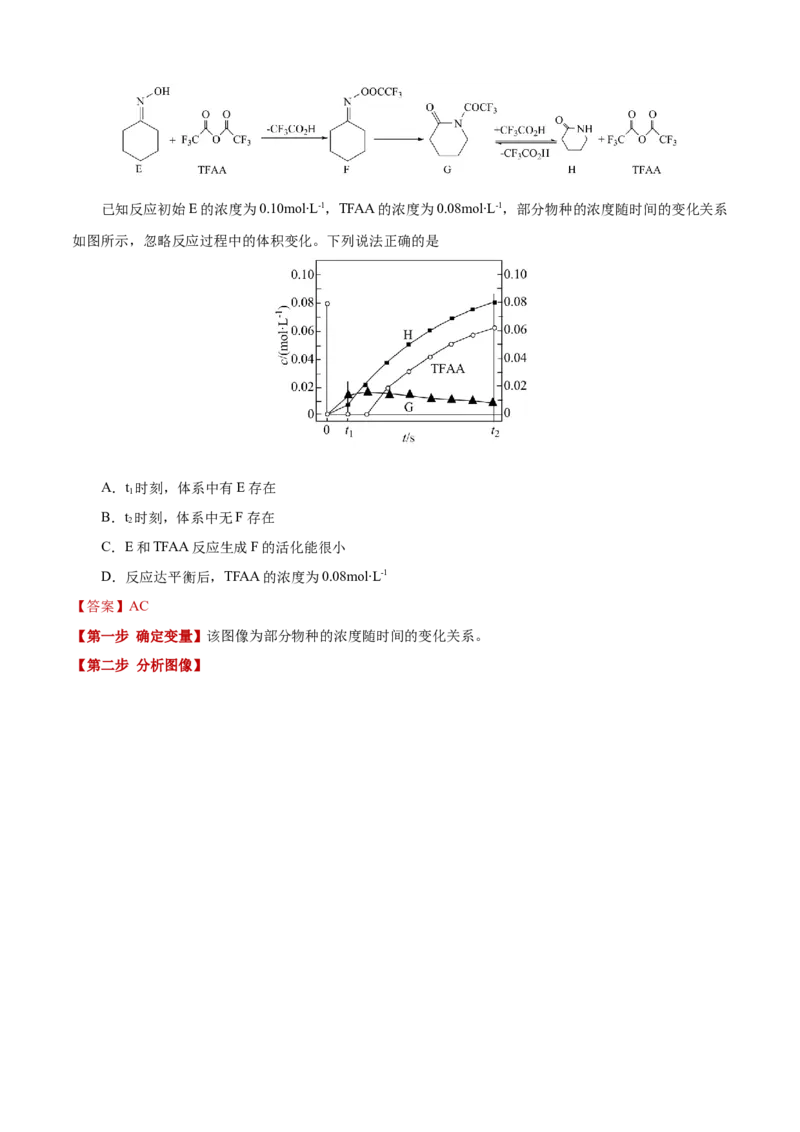
1.(2023·山东卷)一定条件下,化合物E和TFAA合成H的反应路径如下:已知反应初始E的浓度为0.10mol∙L-1,TFAA的浓度为0.08mol∙L-1,部分物种的浓度随时间的变化关系
如图所示,忽略反应过程中的体积变化。下列说法正确的是
A.t 时刻,体系中有E存在
1
B.t 时刻,体系中无F存在
2
C.E和TFAA反应生成F的活化能很小
D.反应达平衡后,TFAA的浓度为0.08mol∙L-1
【答案】AC
【第一步 确定变量】该图像为部分物种的浓度随时间的变化关系。
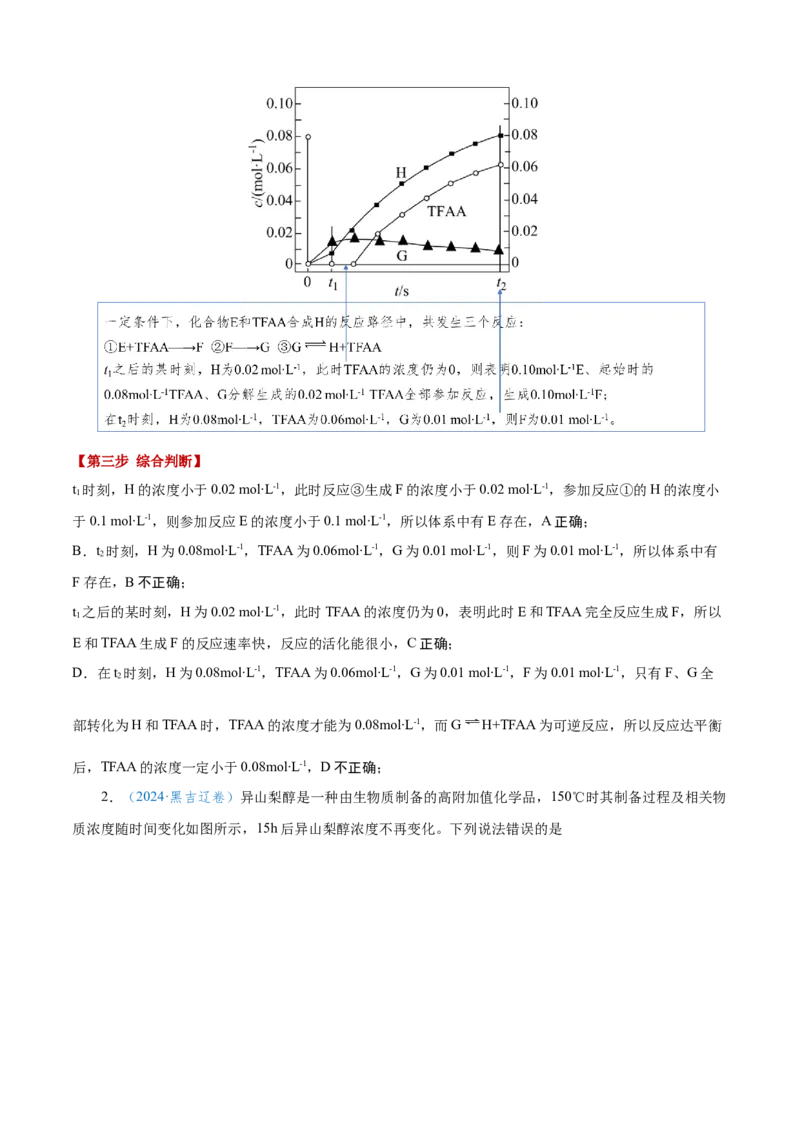
【第二步 分析图像】【第三步 综合判断】
t 时刻,H的浓度小于0.02 mol∙L-1,此时反应③生成F的浓度小于0.02 mol∙L-1,参加反应①的H的浓度小
1
于0.1 mol∙L-1,则参加反应E的浓度小于0.1 mol∙L-1,所以体系中有E存在,A正确;
B.t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,则F为0.01 mol∙L-1,所以体系中有
2
F存在,B不正确;
t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA的浓度仍为0,表明此时E和TFAA完全反应生成F,所以
1
E和TFAA生成F的反应速率快,反应的活化能很小,C正确;
D.在t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,F为0.01 mol∙L-1,只有F、G全
2
部转化为H和TFAA时,TFAA的浓度才能为0.08mol∙L-1,而G H+TFAA为可逆反应,所以反应达平衡
后,TFAA的浓度一定小于0.08mol∙L-1,D不正确;
2.(2024·黑吉辽卷)异山梨醇是一种由生物质制备的高附加值化学品,150℃时其制备过程及相关物
质浓度随时间变化如图所示,15h后异山梨醇浓度不再变化。下列说法错误的是A. 时,反应②正、逆反应速率相等
B.该温度下的平衡常数:①>②
C. 平均速率(异山梨醇)
D.反应②加入催化剂不改变其平衡转化率
【答案】A
【解析】A.由图可知,3小时后异山梨醇浓度继续增大,15h后异山梨醇浓度才不再变化,所以3h时,
反应②未达到平衡状态,即正、逆反应速率不相等,故A错误;
B.图像显示该温度下,15h后所有物质浓度都不再变化,且此时山梨醇转化完全,即反应充分,而1,4-失
水山梨醇仍有剩余,即反应②正向进行程度小于反应①、反应限度小于反应①,所以该温度下的平衡常数:
①>②,故B正确;
C.由图可知,在0~3h内异山梨醇的浓度变化量为0.042mol/kg,所以平均速率(异山梨醇)=
,故C正确;
D.催化剂只能改变化学反应速率,不能改变物质平衡转化率,所以反应②加入催化剂不改变其平衡转化
率,故D正确;
故答案为:A。
类型02 压强/温度图像
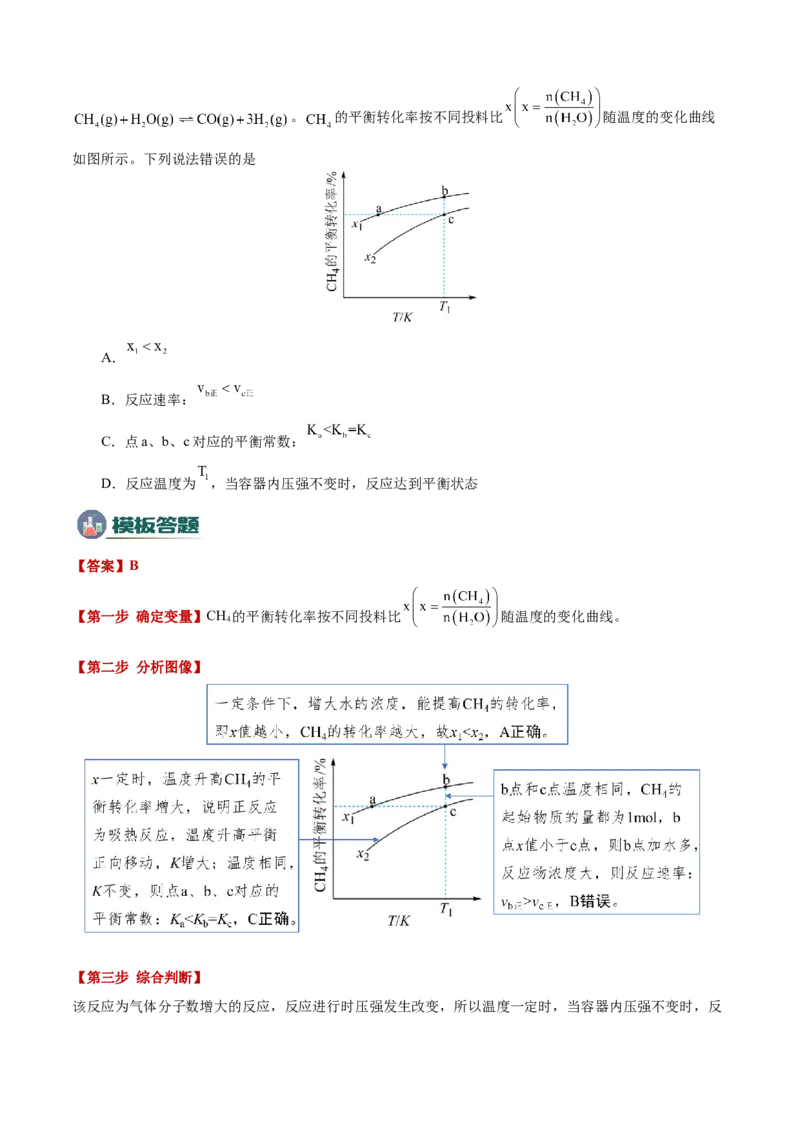
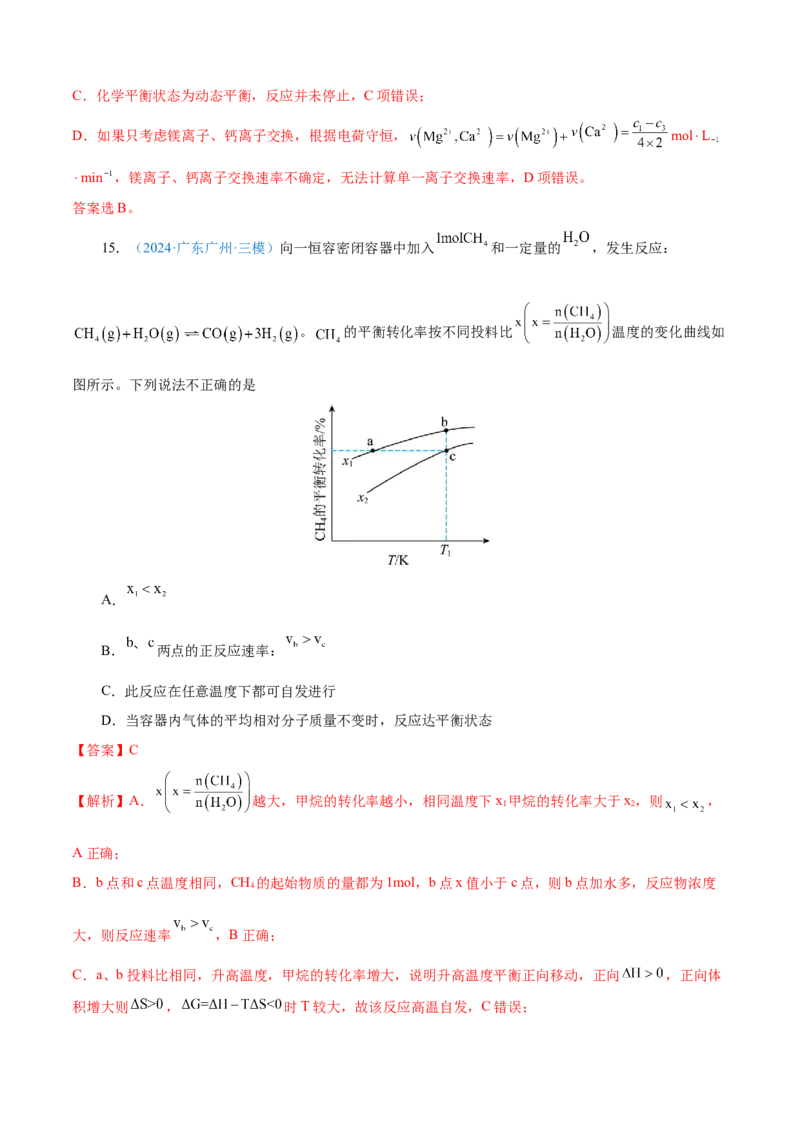
2.(2023·湖南卷)向一恒容密闭容器中加入 和一定量的 ,发生反应:。 的平衡转化率按不同投料比 随温度的变化曲线
如图所示。下列说法错误的是
A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
【答案】B
【第一步 确定变量】CH 的平衡转化率按不同投料比 随温度的变化曲线。
4
【第二步 分析图像】
【第三步 综合判断】
该反应为气体分子数增大的反应,反应进行时压强发生改变,所以温度一定时,当容器内压强不变时,反应达到平衡状态,D正确。
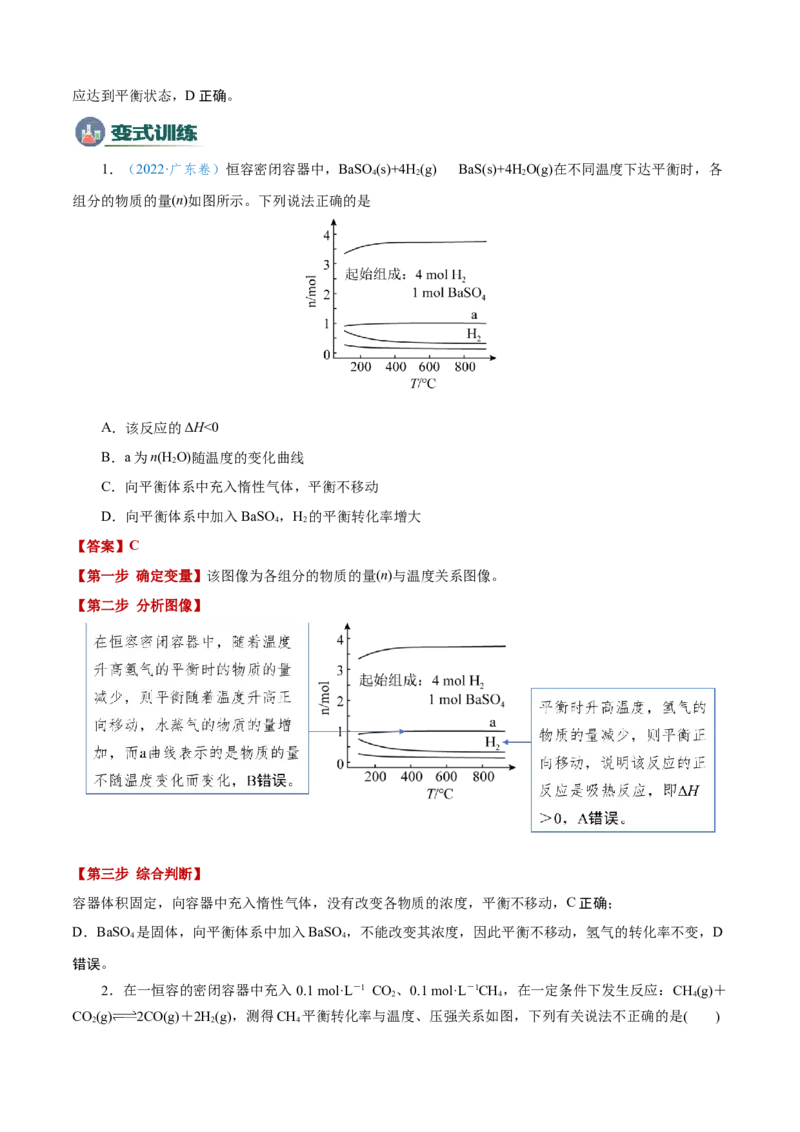
1.(2022·广东卷)恒容密闭容器中,BaSO(s)+4H(g)BaS(s)+4HO(g)在不同温度下达平衡时,各
4 2 2
组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的ΔH<0
B.a为n(H O)随温度的变化曲线
2
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入BaSO,H 的平衡转化率增大
4 2
【答案】C
【第一步 确定变量】该图像为各组分的物质的量(n)与温度关系图像。
【第二步 分析图像】
【第三步 综合判断】
容器体积固定,向容器中充入惰性气体,没有改变各物质的浓度,平衡不移动,C正确;
D.BaSO 是固体,向平衡体系中加入BaSO,不能改变其浓度,因此平衡不移动,氢气的转化率不变,D
4 4
错误。
2.在一恒容的密闭容器中充入0.1 mol·L-1 CO 、0.1 mol·L-1CH ,在一定条件下发生反应:CH(g)+
2 4 4
CO(g) 2CO(g)+2H(g),测得CH 平衡转化率与温度、压强关系如图,下列有关说法不正确的是( )
2 2 4A.上述反应的ΔH<0
B.压强:p>p>p>p
4 3 2 1
C.1 100 ℃时该反应的平衡常数约为1.64
D.压强为p 时,在y点:v >v
4 正 逆
【答案】A
【解析】p、p、p、p 是四条等压线,由图像可知,压强一定时,温度越高,CH 的平衡转化率越高,故
1 2 3 4 4
正反应为吸热反应,ΔH>0,A项错误;该反应为气体分子数增加的反应,压强越高,甲烷的平衡转化率越
小,故压强p>p>p>p,B项正确;压强为p、温度为1 100 ℃时,甲烷的平衡转化率为80.00%,故平衡
4 3 2 1 4
时各物质的浓度分别为c(CH)=0.02 mol·L-1,c(CO)=0.02 mol·L-1,c(CO)=0.16 mol·L-1,c(H )=0.16
4 2 2
mol·L-1,即平衡常数K=≈1.64,C项正确;压强为p 时,y点未达到平衡,此时v >v ,D项正确。
4 正 逆
类型03 工业生产中的速率和平衡图像
3.(2024·湖南卷)恒压下,向某密闭容器中充入一定量的 和 ,发生如下反应:
主反应:
副反应:
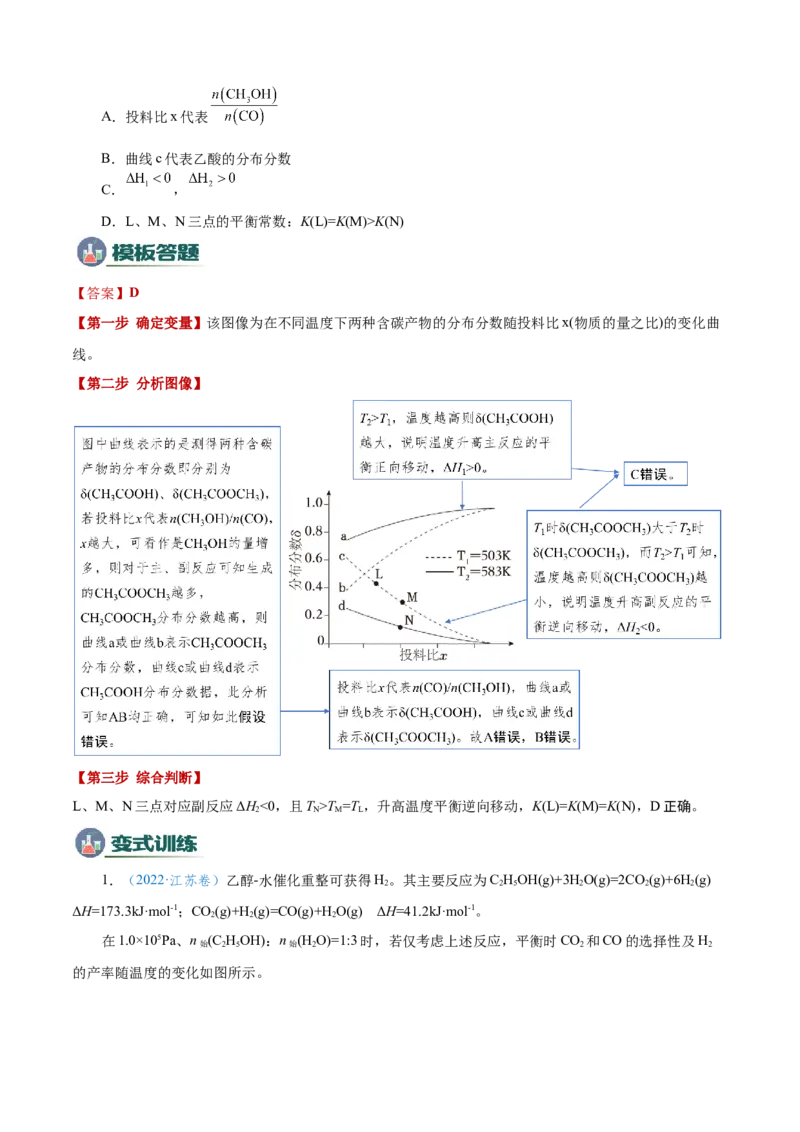
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数
随投料比x(物质的量之比)的变化关系如图所示,下列
说法正确的是A.投料比x代表
B.曲线c代表乙酸的分布分数
C. ,
D.L、M、N三点的平衡常数:K(L)=K(M)>K(N)
【答案】D
【第一步 确定变量】该图像为在不同温度下两种含碳产物的分布分数随投料比x(物质的量之比)的变化曲
线。
【第二步 分析图像】
【第三步 综合判断】
L、M、N三点对应副反应ΔH<0,且T >T =T ,升高温度平衡逆向移动,K(L)=K(M)=K(N),D正确。
2 N M L
1.(2022·江苏卷)乙醇-水催化重整可获得H。其主要反应为C HOH(g)+3H O(g)=2CO(g)+6H(g)
2 2 5 2 2 2
ΔH=173.3kJ·mol-1;CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2kJ·mol-1。
2 2 2
在1.0×105Pa、n (C HOH):n (H O)=1:3时,若仅考虑上述反应,平衡时CO 和CO的选择性及H
始 2 5 始 2 2 2
的产率随温度的变化如图所示。CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时H 产率随温度的变化
2
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时H 产率
2
【答案】B
【分析】根据已知反应① ,反应②
,且反应①的热效应更大,温度升高的时候对反应①影响更
大一些,根据选择性的含义,升温时CO选择性增大,同时CO 的选择性减小,所以图中③代表CO的选
2
择性,①代表CO 的选择性,②代表H 的产率,以此解题。
2 2
【解析】A.由分析可知②代表H 的产率,故A错误;
2
B.由分析可知升高温度,平衡时CO的选择性增大,故B正确;
C.一定温度下,增大 ,可以认为开始时水蒸气物质的量不变,增大乙醇物质的量,乙醇的平
衡转化率降低,故C错误;
D.加入CaO(s)或者选用高效催化剂,不会影响平衡时H 产率,故D错误;
2
故选B。
【答案】D
【第一步 确定变量】该图像为平衡时CO 和CO的选择性及H 的产率随温度的变化。
2 2
【第二步 分析图像】根据已知反应①C HOH(g)+3H O(g)=2CO(g)+6H(g) ΔH=173.3kJ·mol-1;②CO(g)+H(g)=CO(g)+HO(g)
2 5 2 2 2 2 2 2
ΔH=41.2kJ·mol-1。且反应①的热效应更大,温度升高时对反应①影响更大一些,根据选择性的含义,升温
时CO选择性增大,同时CO 的选择性减小,所以图中③代表CO的选择性,①代表CO 的选择性,②代
2 2
表H 的产率。故A错误,B错误。
2
【第三步 综合判断】
一定温度下,增大 ,可以认为开始时水蒸气物质的量不变,增大乙醇物质的量,乙醇的平衡转
化率降低,故C错误;加入CaO(s)或者选用高效催化剂,不会影响平衡时H 产率,故D错误。
2
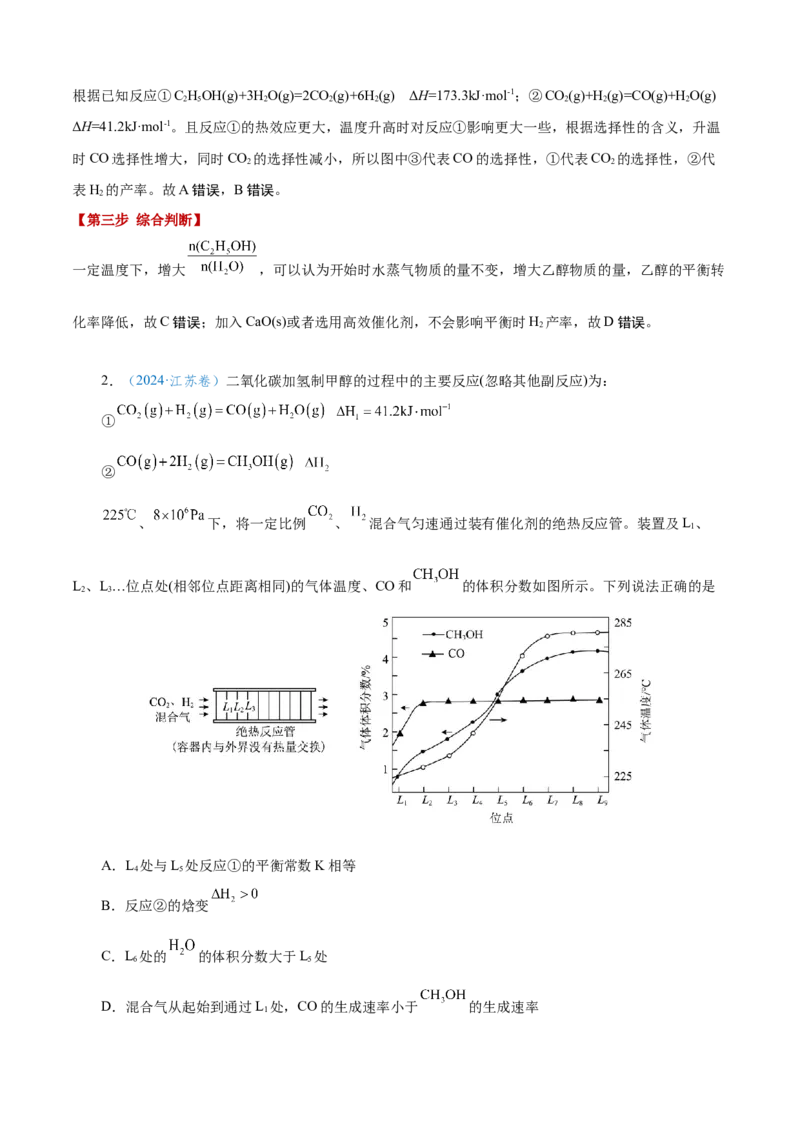
2.(2024·江苏卷)二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①
②
、 下,将一定比例 、 混合气匀速通过装有催化剂的绝热反应管。装置及L、
1
L、L…位点处(相邻位点距离相同)的气体温度、CO和 的体积分数如图所示。下列说法正确的是
2 3
A.L 处与L 处反应①的平衡常数K相等
4 5
B.反应②的焓变
C.L 处的 的体积分数大于L 处
6 5
D.混合气从起始到通过L 处,CO的生成速率小于 的生成速率
1【答案】C
【解析】L 处与L 处的温度不同,故反应①的平衡常数K不相等,A错误;由图像可知,L-L 温度在升
4 5 1 3
高,该装置为绝热装置,反应①为吸热反应,所以反应②为放热反应,ΔH<0,B错误;从L 到L,甲醇
2 5 6
的体积分数逐渐增加,说明反应②在向右进行,反应②消耗 CO,而 CO 体积分数没有明显变化,说明反
应①也在向右进行,反应①为气体分子数不变的反应,其向右进行时,n(H O) 增大,反应②为气体分子
2
数减小的反应,且没有HO的消耗与生成,故 n总减小而n(H₂O)增加,即HO的体积分数会增大,故L
2 2 6
处的 HO的体积分数大于L 处,C正确;L 处CO 的体积分数大于 CHOH,说明生成的 CO 的物质的
2 5 1 3
量大于CHOH,两者反应时间相同,说明CO的生成速率大于 CHOH的生成速率,D错误。
3 3
1.生产硫酸的主要反应:2SO (g)+O(g) 2SO (g) ΔH<0。图中L(L 、L)、X可分别代表压强或
2 2 3 1 2
温度。下列说法正确的是( )
A.X代表压强
B.L>L
1 2
C.A、B两点对应的平衡常数相同
D.一定温度下,当混合气中n(SO )∶n(O )∶n(SO )=2∶1∶2时,反应一定达到平衡
2 2 3
【答案】B
【解析】若X代表压强,则L代表温度,温度相同时,增大压强,平衡正向移动,SO 的平衡转化率增大,
2
与图像不符合,A错误;结合A项分析推知,X代表温度,L代表压强,温度相同时,增大压强,平衡正
向移动,SO 的平衡转化率增大,则压强:L >L ,B正确;A、B两点的温度不同,平衡常数不同,C错
2 1 2
误;温度一定,达到平衡状态时,n(SO )、n(O )和n(SO )均保持不变,但其比值不一定等于对应的化学计
2 2 3
量数之比,D错误。
2.一定条件下合成乙烯:6H(g)+2CO(g) CH===CH (g)+4HO(g);已知温度对CO 的平衡转化
2 2 2 2 2 2
率和催化剂催化效率的影响如图,下列说法不正确的是( )A.该反应的逆反应为吸热反应
B.平衡常数:K >K
M N
C.生成乙烯的速率:v(N)一定大于v(M)
D.当温度高于250 ℃,升高温度,催化剂的催化效率降低
【答案】C
【解析】升高温度,CO 的平衡转化率降低,说明平衡逆向移动,则逆反应为吸热反应,A正确;该反应
2
的正反应是放热反应,升温平衡常数减小,B正确;化学反应速率随温度的升高而加快,催化剂在250 ℃
时催化活性最高,温度继续升高,其催化效率降低,所以v(N)有可能小于v(M),C错误,D正确。
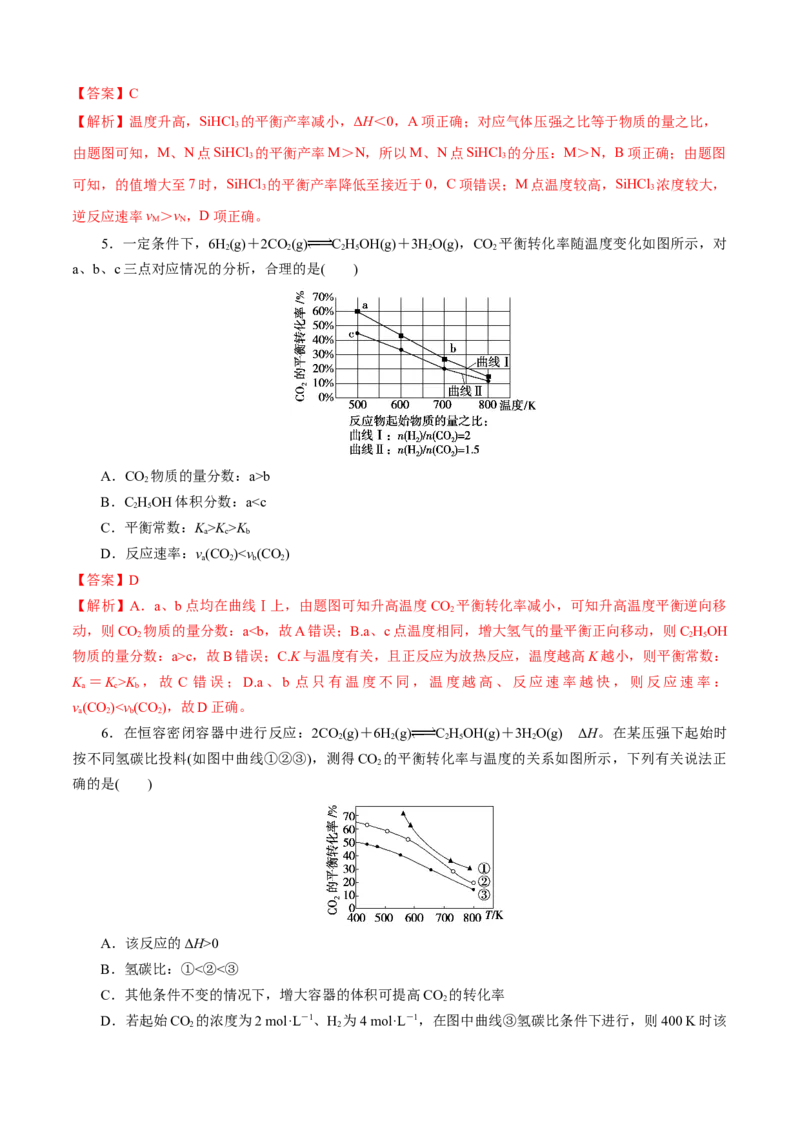
3.一定条件下,用Fe O 、NiO或Cr O 作催化剂对燃煤烟气进行回收,使SO 转化生成S。催化剂不
2 3 2 3 2
同,其他条件相同(浓度、温度、压强)情况下,相同时间内SO 的转化率随反应温度的变化如图,下列说
2
法不正确的是( )
A.不考虑催化剂价格因素,选择Fe O 作催化剂可以节约能源
2 3
B.选择Fe O 作催化剂,最适宜温度为340 ℃左右
2 3
C.a点后SO 的转化率减小的原因可能是温度升高催化剂活性降低
2
D.其他条件相同的情况下,选择Cr O 作催化剂,SO 的平衡转化率最小
2 3 2
【答案】D
【解析】根据图像可知,当温度在340 ℃时,在Fe O 作催化剂条件下,SO 的转化率最大,可以节约能源,
2 3 2
故A正确;340 ℃左右,催化剂的催化能力较大,二氧化硫的转化率也是较大,反应速率较快,所以选择
Fe O 作催化剂,最适宜温度为340 ℃左右,故B正确; 催化剂催化能力需要维持在一定的温度下,温度
2 3
太高,催化剂活性可能会降低,故C正确;催化剂只对速率有影响,对平衡转化率没有影响,故D错误。
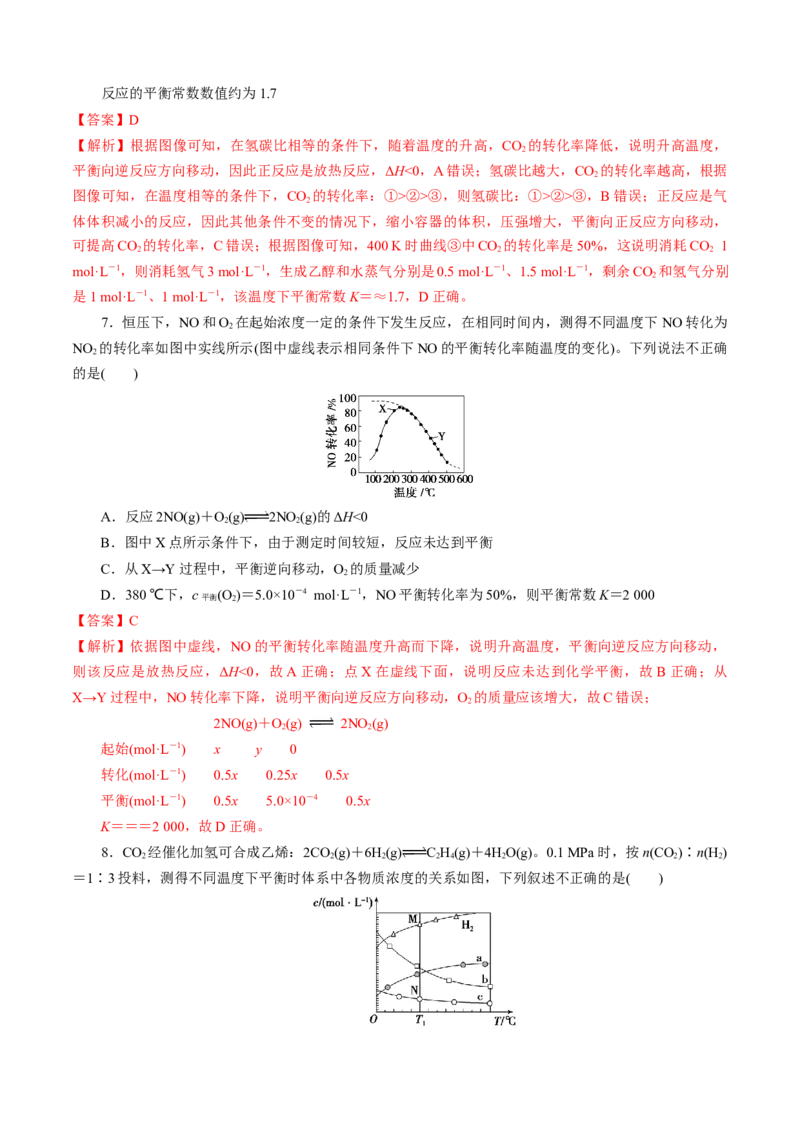
4.反应Si(s)+3HCl(g) SiHCl (g)+H(g) ΔH是工业上制备高纯硅的重要中间过程。一定压强下,
3 2
起始投入原料的值和温度与SiHCl 的平衡产率的变化关系如图所示。下列说法错误的是( )
3
A.该反应为放热反应,ΔH<0
B.M、N点SiHCl 的分压:M>N
3
C.的值越大SiHCl 平衡产率越高
3
D.M、N点的逆反应速率:v >v
M N【答案】C
【解析】温度升高,SiHCl 的平衡产率减小,ΔH<0,A项正确;对应气体压强之比等于物质的量之比,
3
由题图可知,M、N点SiHCl 的平衡产率M>N,所以M、N点SiHCl 的分压:M>N,B项正确;由题图
3 3
可知,的值增大至7时,SiHCl 的平衡产率降低至接近于0,C项错误;M点温度较高,SiHCl 浓度较大,
3 3
逆反应速率v >v ,D项正确。
M N
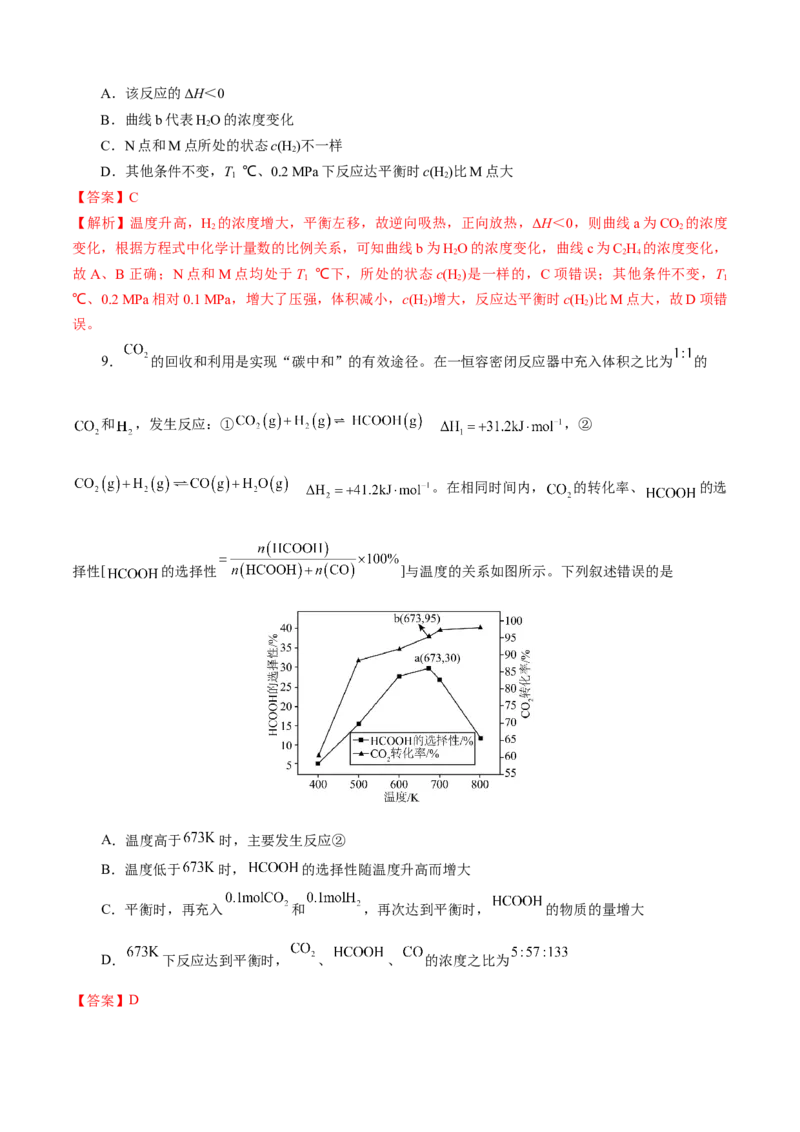
5.一定条件下,6H(g)+2CO(g) C HOH(g)+3HO(g),CO 平衡转化率随温度变化如图所示,对
2 2 2 5 2 2
a、b、c三点对应情况的分析,合理的是( )
A.CO 物质的量分数:a>b
2
B.C HOH体积分数:aK>K
a c b
D.反应速率:v(CO)c,故B错误;C.K与温度有关,且正反应为放热反应,温度越高K越小,则平衡常数:
K =K>K ,故 C 错误;D.a、b 点只有温度不同,温度越高、反应速率越快,则反应速率:
a c b
v(CO)0
B.氢碳比:①<②<③
C.其他条件不变的情况下,增大容器的体积可提高CO 的转化率
2
D.若起始CO 的浓度为2 mol·L-1、H 为4 mol·L-1,在图中曲线③氢碳比条件下进行,则400 K时该
2 2反应的平衡常数数值约为1.7
【答案】D
【解析】根据图像可知,在氢碳比相等的条件下,随着温度的升高,CO 的转化率降低,说明升高温度,
2
平衡向逆反应方向移动,因此正反应是放热反应,ΔH<0,A错误;氢碳比越大,CO 的转化率越高,根据
2
图像可知,在温度相等的条件下,CO 的转化率:①>②>③,则氢碳比:①>②>③,B错误;正反应是气
2
体体积减小的反应,因此其他条件不变的情况下,缩小容器的体积,压强增大,平衡向正反应方向移动,
可提高CO 的转化率,C错误;根据图像可知,400 K时曲线③中CO 的转化率是50%,这说明消耗CO 1
2 2 2
mol·L-1,则消耗氢气3 mol·L-1,生成乙醇和水蒸气分别是0.5 mol·L-1、1.5 mol·L-1,剩余CO 和氢气分别
2
是1 mol·L-1、1 mol·L-1,该温度下平衡常数K=≈1.7,D正确。
7.恒压下,NO和O 在起始浓度一定的条件下发生反应,在相同时间内,测得不同温度下NO转化为
2
NO 的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法不正确
2
的是( )
A.反应2NO(g)+O(g) 2NO (g)的ΔH<0
2 2
B.图中X点所示条件下,由于测定时间较短,反应未达到平衡
C.从X→Y过程中,平衡逆向移动,O 的质量减少
2
D.380 ℃下,c (O )=5.0×10-4 mol·L-1,NO平衡转化率为50%,则平衡常数K=2 000
平衡 2
【答案】C
【解析】依据图中虚线,NO的平衡转化率随温度升高而下降,说明升高温度,平衡向逆反应方向移动,
则该反应是放热反应,ΔH<0,故A正确;点X在虚线下面,说明反应未达到化学平衡,故B正确;从
X→Y过程中,NO转化率下降,说明平衡向逆反应方向移动,O 的质量应该增大,故C错误;
2
2NO(g)+O(g) 2NO (g)
2 2
起始(mol·L-1) x y 0
转化(mol·L-1) 0.5x 0.25x 0.5x
平衡(mol·L-1) 0.5x 5.0×10-4 0.5x
K===2 000,故D正确。
8.CO 经催化加氢可合成乙烯:2CO(g)+6H(g) C H(g)+4HO(g)。0.1 MPa时,按n(CO)∶n(H )
2 2 2 2 4 2 2 2
=1∶3投料,测得不同温度下平衡时体系中各物质浓度的关系如图,下列叙述不正确的是( )A.该反应的ΔH<0
B.曲线b代表HO的浓度变化
2
C.N点和M点所处的状态c(H )不一样
2
D.其他条件不变,T ℃、0.2 MPa下反应达平衡时c(H )比M点大
1 2
【答案】C
【解析】温度升高,H 的浓度增大,平衡左移,故逆向吸热,正向放热,ΔH<0,则曲线a为CO 的浓度
2 2
变化,根据方程式中化学计量数的比例关系,可知曲线b为HO的浓度变化,曲线c为C H 的浓度变化,
2 2 4
故A、B正确;N点和M点均处于T ℃下,所处的状态c(H )是一样的,C项错误;其他条件不变,T
1 2 1
℃、0.2 MPa相对0.1 MPa,增大了压强,体积减小,c(H )增大,反应达平衡时c(H )比M点大,故D项错
2 2
误。
9. 的回收和利用是实现“碳中和”的有效途径。在一恒容密闭反应器中充入体积之比为 的
和 ,发生反应:① ,②
。在相同时间内, 的转化率、 的选
择性[ 的选择性 ]与温度的关系如图所示。下列叙述错误的是
A.温度高于 时,主要发生反应②
B.温度低于 时, 的选择性随温度升高而增大
C.平衡时,再充入 和 ,再次达到平衡时, 的物质的量增大
D. 下反应达到平衡时, 、 、 的浓度之比为
【答案】D【解析】A.根据图像可知,当温度高于673 K时,CO 的转化率增加,但HCOOH的选择性降低,故以发
2
生反应②为主,A正确;
B.根据图像可知,当温度低于673K时,HCOOH的选择性随温度升高而增大,B正确;
C.平衡时再通入0.1molCO 和0.1molH,平衡一定正向移动,HCOOH的物质的量一定增大,C正确;
2 2
D.根据题意,利用转化率和选择性表达式可知,673K时CO 的转化率为95%,其中HCOOH的选择性为
2
30%,那么CO的选择性为70%,设起始时二氧化碳的物质的量为amol,根据化学方程式利用元素守恒,平
衡时二氧化碳0.05amol,HCOOH和CO物质的量之和为0.95amol,那么HCOOH的物质的量为0.95a×30%
=0.285amol,CO的物质的量为0.95a×70%=0.665amol,容密闭容器中CO、HCOOH、CO的浓度之比为
2
10:57:133,故D错误;
故选D。
10.(2024·湖南永州·三模)室温下,在P和Q浓度相等的混合溶液中,同时发生反应①P+Q=X+Z
和反应②P+Q=Y+Z,反应①和②的速率方程分别是v=kc2(P)、v=kc2(P)(k 、k 为速率常数)。反应过程
1 1 2 2 1 2
中,Q、X的浓度随时间变化情况如图所示。下列说法错误的是
A.反应开始后,体系中X和Y的浓度之比保持不变
B.45min时Z的浓度为0.4mol·L-1
C.反应①的活化能比反应②的活化能大
D.如果反应能进行到底,反应结束时,有40%的P转化为Y
【答案】D
【解析】A.根据①和②的速率方程分别是v=kc2(P)、v=kc2(P)(k 、k 为速率常数),反应开始后,体系中
1 1 2 2 1 2
X和Y的浓度之比为 ,保持不变,故A正确;
B.根据反应①P+Q=X+Z和反应②P+Q=Y+Z方程式,可知每消耗1molQ同时生成1molZ,反应到
45min时,Q的浓度降低0.4mol/L, 则Z的浓度为0.4mol·L-1,故B正确;
C.反应到20min时,Q的浓度降低0.3mol/L,反应①中X浓度增大0.12mol/L,则反应②中Y浓度增大
0.18mol/L,反应②的速率大于反应①,所以反应①的活化能比反应②的活化能大,故C正确;D.反应到20min时,Q的浓度降低0.3mol/L,反应①中X浓度增大0.12mol/L,则反应②中Y浓度增大
0.18mol/L,如果反应能进行到底,反应结束时,有60%的P转化为Y,故D错误;
选D。
11.(2024·安徽合肥·三模)已知双环戊二烯解聚成环戊二烯的反应为 。
若将3 mol双环戊二烯通入2L恒容密闭容器中,测得 ℃和 ℃下n(双环戊二烯或环戊二烯)随时间的
变化如图所示, ℃时反应到a点恰好达到平衡。下列有关说法错误的是
A. T>T
1 2
B. ℃时,0~2h内的平均反应速率:v(环戊二烯) mol⋅L ⋅h
C. ℃时,当容器内的气体压强为起始的1.5倍时:v(正) (逆)
D. ℃时,反应恰好达到平衡时:44.8 mol (环戊二烯) mol
【答案】B
【解析】A.由图可知, ℃时,双环戊二烯前1h减少1.8 mol,相当于环戊二烯增加3.6 mol, ℃时,
环戊二烯增加4 mol mol,所以 ,A正确;
B. ℃时,0~2h内的平均反应速率:v(环戊二烯) mol⋅L ⋅h ,B错误;
C.由a点可知, ℃时,平衡时气体总物质的量为2×(3 mol-0.6 mol)+0.6 mol=5.4 mol,是初始3 mol
的1.8倍,气体的压强为起始时的1.5倍时,反应正向进行, (正) (逆),C正确;D.在 ℃时,反应达到平衡,消耗双环戊二烯的物质的量为(3-0.6)mol=2.4mol,此时生成环戊二烯的
物质的量为2.4×2 mol=4.8 mol,因为T₁>T₂,该反应为吸热反应,升高温度,平衡正向移动,则 ℃时n
(环戊二烯) mol,假设双环戊二烯全部反应,则生成环戊二烯的物质的量为6 mol,但该反应为可逆
反应,不能进行到底,因此n(环戊二烯) mol,D正确;
故选B。
12.(2024·北京师范大学附属中学三模)CH 和CO 联合重整能减少温室气体的排放。其主要反应为:
4 2
①
②
其他条件相同时,投料比 为 ,不同温度下反应的结果如图。
下列说法不正确的是
A.由图中信息无法判断反应①、②哪个先达到平衡
B. 始终低于1.0,与反应②有关
C.加压有利于增大CH 和CO 反应的速率但不利于提高二者的平衡转化率
4 2
D.若不考虑其他副反应,体系中存在:
【答案】D
【解析】A.图中横坐标为温度,与时间无关,仅从图中信息无法判断反应①、②哪个先达到平衡,A正
确;
B.从反应①的方程式可知,生成的氢气和CO的物质的量之比为1:1,反应②中消耗氢气生成CO,使得
氢气与CO的物质的量之比小于1.0,与反应②有关,B正确;
C.加压能增大反应速率,有利于增大CH 和CO 的反应速率,但是加压反应①化学平衡逆向移动,CH 和
4 2 4CO 的转化率减小,C正确;
2
D.不妨令初始时CH 物质的量为1mol,CO 物质的量为1.3mol,设反应①消耗COamol,反应②消耗
4 2 2
CObmol,则有 ,
2
,则c(CH)+c(CO)+c(CO )=2.3mol,
4 2
4c(CH)+2c(H )+2c(H O)=4,则有 ,D错
4 2 2
误;
故答案选D。
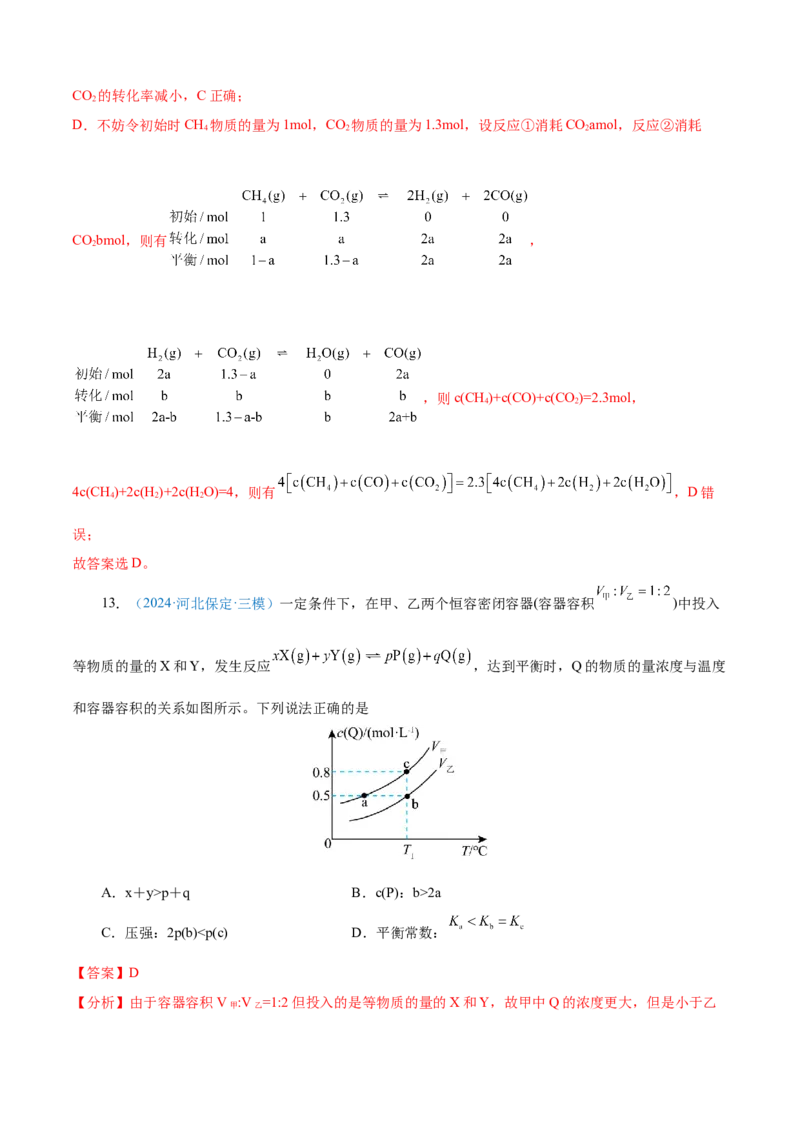
13.(2024·河北保定·三模)一定条件下,在甲、乙两个恒容密闭容器(容器容积 )中投入
等物质的量的X和Y,发生反应 ,达到平衡时,Q的物质的量浓度与温度
和容器容积的关系如图所示。下列说法正确的是
A.x+y>p+q B.c(P):b>2a
C.压强:2p(b)P ,B错误;
1 2
C.随温度升高,CO的平衡选择性接近100%,可知升温后主要发生反应Ⅱ,反应Ⅱ的平衡移动与压强无
关,故随温度升高, 的平衡转化率受压强影响减小,C正确;
D.平衡常数只与温度有关,温度相同平衡常数相同,D错误;
故选C。
17.(2024·重庆·三模)工业制氢,反应Ⅰ:
,反应Ⅱ: 。
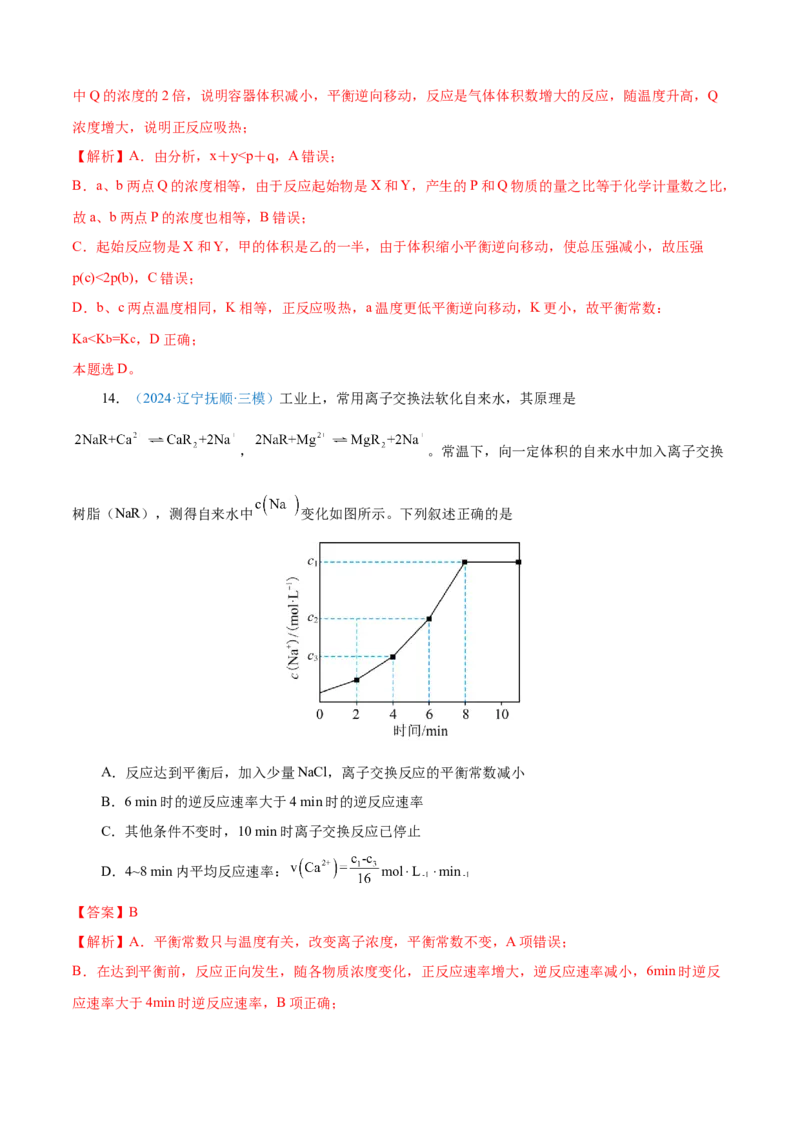
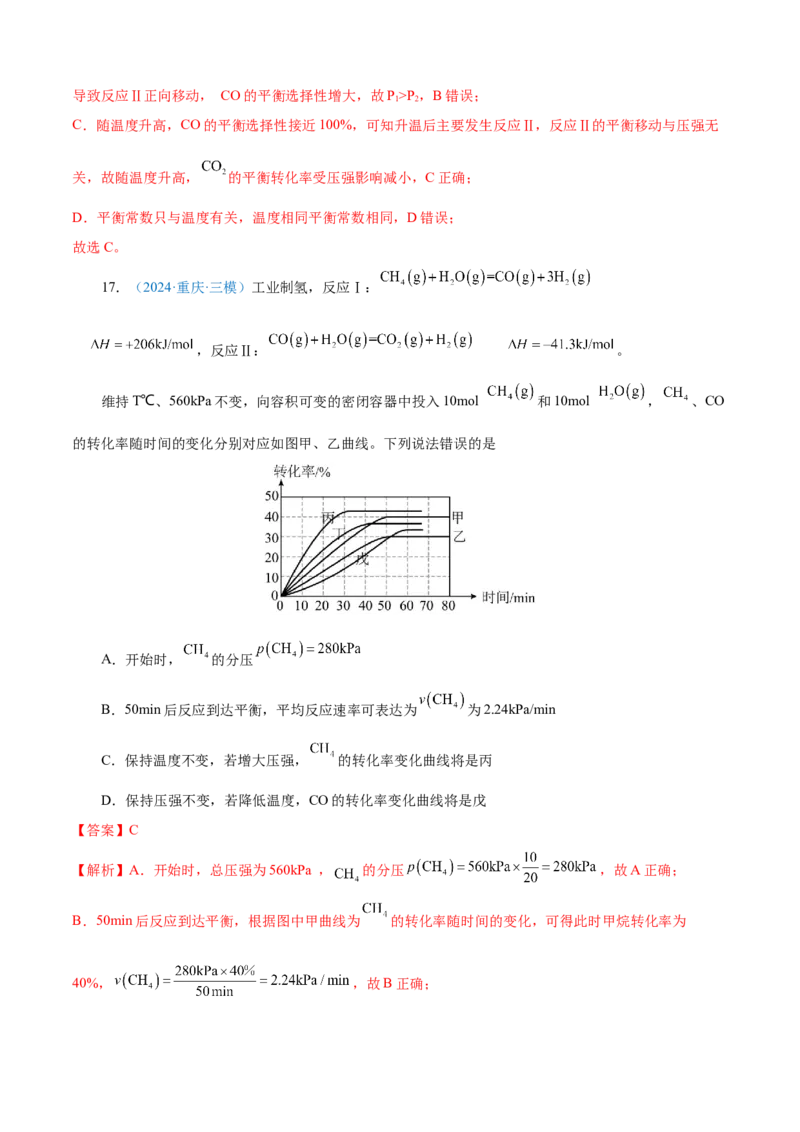
维持T℃、560kPa不变,向容积可变的密闭容器中投入10mol 和10mol , 、CO
的转化率随时间的变化分别对应如图甲、乙曲线。下列说法错误的是
A.开始时, 的分压
B.50min后反应到达平衡,平均反应速率可表达为 为2.24kPa/min
C.保持温度不变,若增大压强, 的转化率变化曲线将是丙
D.保持压强不变,若降低温度,CO的转化率变化曲线将是戊
【答案】C
【解析】A.开始时,总压强为560kPa , 的分压 ,故A正确;
B.50min后反应到达平衡,根据图中甲曲线为 的转化率随时间的变化,可得此时甲烷转化率为
40%, ,故B正确;C.保持温度不变, 为反应前后气体计量数不变的反应,因此若增大压强,平衡不移
动, 为反应气体计量数增大的反应,若增大压强,平衡逆向移动, 转化率降低,
且压强增大会导致反应速率加快,达到平衡的时间减少,因此 的转化率变化曲线将是丁,故C错误;
D.保持压强不变, 为放热反应,若降低温度,平衡正向移动,CO的转化率增大,
为吸热反应,若降低温度,平衡逆向移动,CO的转化率增大,降低温度会导致速率
减慢,达到平衡的时间增加,因此CO的转化率变化曲线将是戊,故D正确;
故答案选C。
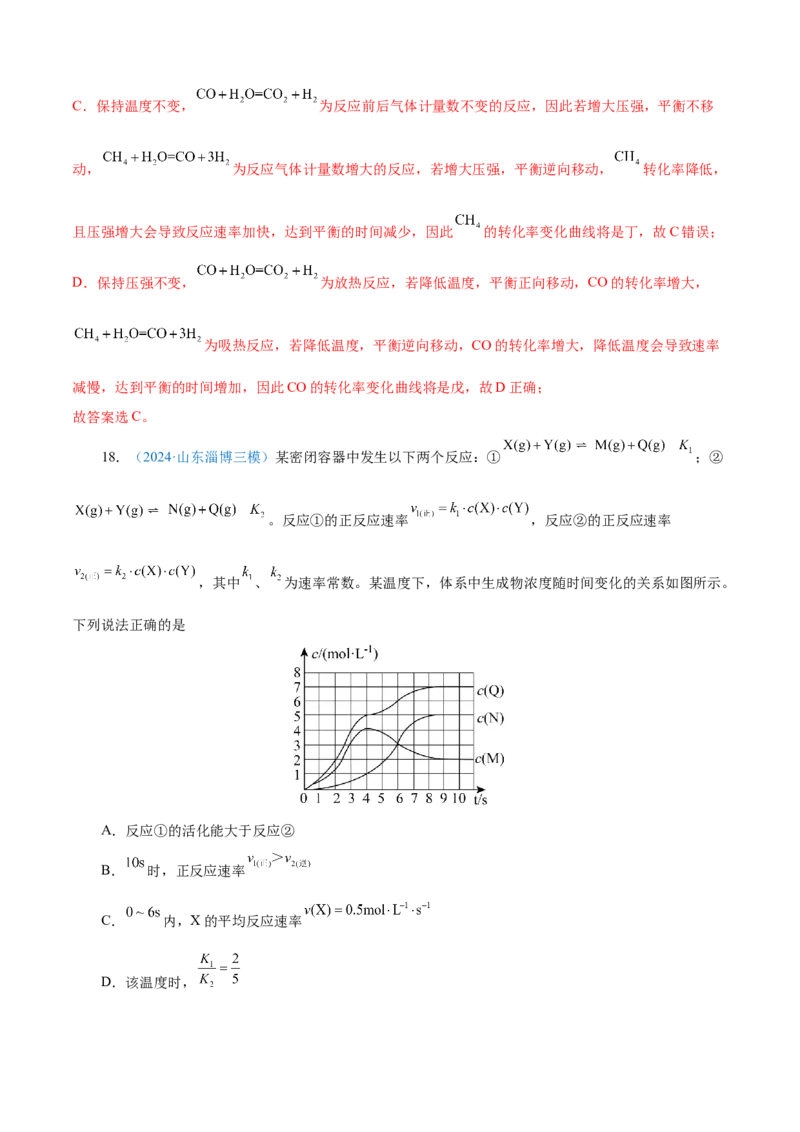
18.(2024·山东淄博三模)某密闭容器中发生以下两个反应:① ;②
。反应①的正反应速率 ,反应②的正反应速率
,其中 、 为速率常数。某温度下,体系中生成物浓度随时间变化的关系如图所示。
下列说法正确的是
A.反应①的活化能大于反应②
B. 时,正反应速率
C. 内,X的平均反应速率
D.该温度时,【答案】BD
【解析】A.由图可知,初始生成M的速率大于N,则反应①的话化能小于反应②,A错误;
B.由图可知,初始生成M的速率大于N,则 > ,10s时两个反应均达到平衡状态,由于
、 ,则正反应速率 ,B正确;
C.①②反应中XQ的系数均为1,则 内,X的平均反应速率为
,C错误;
D. 、 ,则 ,由图可知,平衡时刻M、N的浓度分别为2mol/L、
5mol/L,则 ,D错误;
故选A。