文档内容
热点强化练 9 催化剂、活化能与化学反应历程
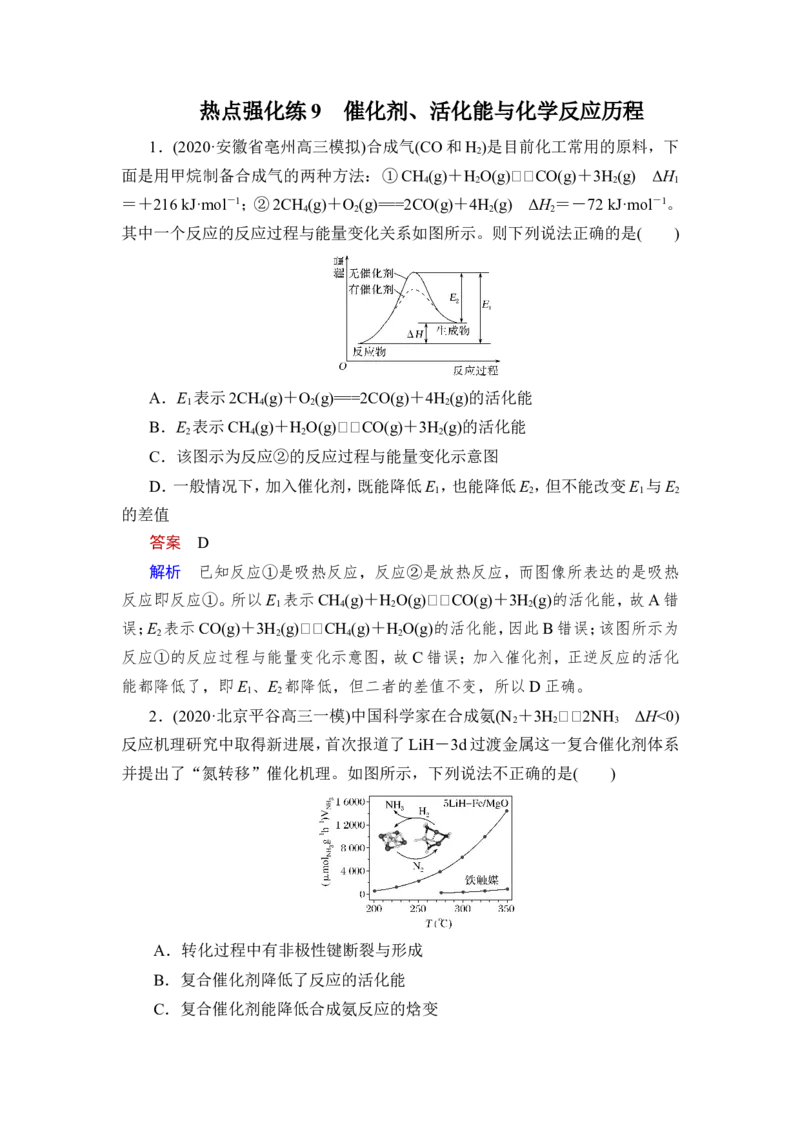
1.(2020·安徽省亳州高三模拟)合成气(CO和H )是目前化工常用的原料,下
2
面是用甲烷制备合成气的两种方法:①CH (g)+H O(g)CO(g)+3H (g) ΔH
4 2 2 1
=+216 kJ·mol-1;②2CH (g)+O (g)===2CO(g)+4H (g) ΔH =-72 kJ·mol-1。
4 2 2 2
其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是( )
A.E 表示2CH (g)+O (g)===2CO(g)+4H (g)的活化能
1 4 2 2
B.E 表示CH (g)+H O(g)CO(g)+3H (g)的活化能
2 4 2 2
C.该图示为反应②的反应过程与能量变化示意图
D.一般情况下,加入催化剂,既能降低E ,也能降低E ,但不能改变E 与E
1 2 1 2
的差值
答案 D
解析 已知反应①是吸热反应,反应②是放热反应,而图像所表达的是吸热
反应即反应①。所以E 表示CH (g)+H O(g)CO(g)+3H (g)的活化能,故A错
1 4 2 2
误;E 表示CO(g)+3H (g)CH (g)+H O(g)的活化能,因此B错误;该图所示为
2 2 4 2
反应①的反应过程与能量变化示意图,故C错误;加入催化剂,正逆反应的活化
能都降低了,即E 、E 都降低,但二者的差值不变,所以D正确。
1 2
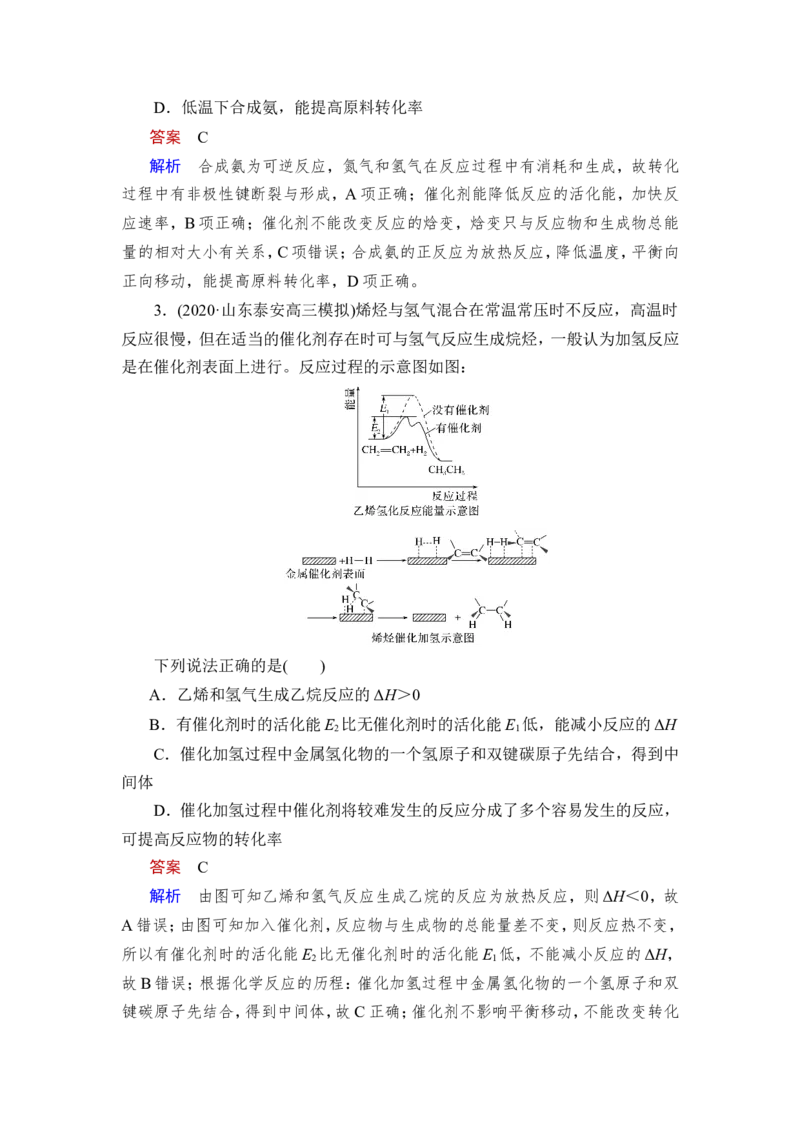
2.(2020·北京平谷高三一模)中国科学家在合成氨(N +3H 2NH ΔH<0)
2 2 3
反应机理研究中取得新进展,首次报道了LiH-3d过渡金属这一复合催化剂体系
并提出了“氮转移”催化机理。如图所示,下列说法不正确的是( )
A.转化过程中有非极性键断裂与形成
B.复合催化剂降低了反应的活化能
C.复合催化剂能降低合成氨反应的焓变D.低温下合成氨,能提高原料转化率
答案 C
解析 合成氨为可逆反应,氮气和氢气在反应过程中有消耗和生成,故转化
过程中有非极性键断裂与形成,A项正确;催化剂能降低反应的活化能,加快反
应速率,B项正确;催化剂不能改变反应的焓变,焓变只与反应物和生成物总能
量的相对大小有关系,C项错误;合成氨的正反应为放热反应,降低温度,平衡向
正向移动,能提高原料转化率,D项正确。
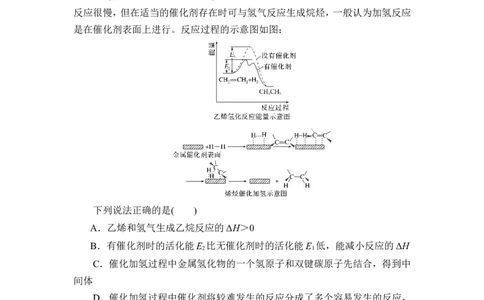
3.(2020·山东泰安高三模拟)烯烃与氢气混合在常温常压时不反应,高温时
反应很慢,但在适当的催化剂存在时可与氢气反应生成烷烃,一般认为加氢反应
是在催化剂表面上进行。反应过程的示意图如图:
下列说法正确的是( )
A.乙烯和氢气生成乙烷反应的ΔH>0
B.有催化剂时的活化能E 比无催化剂时的活化能E 低,能减小反应的ΔH
2 1
C.催化加氢过程中金属氢化物的一个氢原子和双键碳原子先结合,得到中
间体
D.催化加氢过程中催化剂将较难发生的反应分成了多个容易发生的反应,
可提高反应物的转化率
答案 C
解析 由图可知乙烯和氢气反应生成乙烷的反应为放热反应,则ΔH<0,故
A错误;由图可知加入催化剂,反应物与生成物的总能量差不变,则反应热不变,
所以有催化剂时的活化能E 比无催化剂时的活化能E 低,不能减小反应的ΔH,
2 1
故B错误;根据化学反应的历程:催化加氢过程中金属氢化物的一个氢原子和双
键碳原子先结合,得到中间体,故C正确;催化剂不影响平衡移动,不能改变转化率,故D错误。
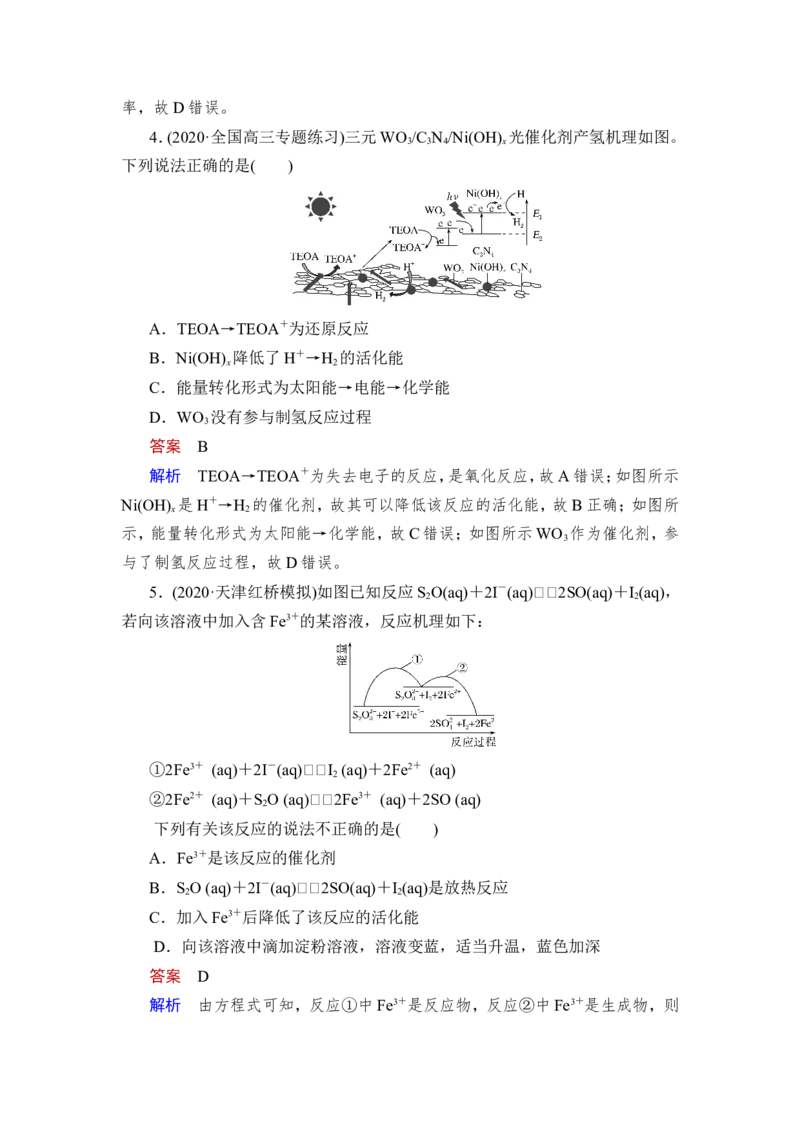
4.(2020·全国高三专题练习)三元WO /C N /Ni(OH) 光催化剂产氢机理如图。
3 3 4 x
下列说法正确的是( )
A.TEOA→TEOA+为还原反应
B.Ni(OH) 降低了H+→H 的活化能
x 2
C.能量转化形式为太阳能→电能→化学能
D.WO 没有参与制氢反应过程
3
答案 B
解析 TEOA→TEOA+为失去电子的反应,是氧化反应,故A错误;如图所示
Ni(OH) 是H+→H 的催化剂,故其可以降低该反应的活化能,故B正确;如图所
x 2
示,能量转化形式为太阳能→化学能,故C错误;如图所示WO 作为催化剂,参
3
与了制氢反应过程,故D错误。
5.(2020·天津红桥模拟)如图已知反应S O(aq)+2I-(aq)2SO(aq)+I (aq),
2 2
若向该溶液中加入含Fe3+的某溶液,反应机理如下:
①2Fe3+ (aq)+2I-(aq)I (aq)+2Fe2+ (aq)
2
②2Fe2+ (aq)+S O (aq)2Fe3+ (aq)+2SO (aq)
2
下列有关该反应的说法不正确的是( )
A.Fe3+是该反应的催化剂
B.S O (aq)+2I-(aq)2SO(aq)+I (aq)是放热反应
2 2
C.加入Fe3+后降低了该反应的活化能
D.向该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深
答案 D
解析 由方程式可知,反应①中Fe3+是反应物,反应②中Fe3+是生成物,则Fe3+是该反应的催化剂,故A正确;由图可知,反应物的总能量高于生成物的总
能量,该反应为放热反应,故B正确;催化剂能降低反应的活化能,Fe3+是该反应
的催化剂,则加入Fe3+后降低了该反应的活化能,故C正确;该反应为放热反应,
升高温度,平衡向逆反应方向移动,碘单质浓度减小,蓝色变浅,故D错误。
6.(2020·山东肥城高三模拟)最近,中国科学院大连化物所“CO 催化转化为
2
CO的研究”获得新进展。如图是使用不同催化剂(NiPc和CoPc)时转化过程中的
能量变化,下列说法不合理的是( )
A.·CO 经还原反应得到·COOH
2
B.该研究成果将有利于缓解温室效应,并解决能源转化问题
C.相同基团的物种分别吸附在NiPc和CoPc表面,其能量可能不同
D.催化剂可以改变CO 转化为CO反应的焓变
2
答案 D
解析 ·CO 转化为·COOH的过程中,碳元素的化合价降低,因此·CO 到
2 2
·COOH是还原反应,A正确;该过程中,CO 转化为CO,可减少空气中的CO 的
2 2
含量,缓解温室效应,同时反应生成CO具有可燃性,可解决能源转化危机,B正
确;由图可知,·COOHNiPc中的能量高于吸附在CoPc上的能量,因此吸附在相
同基团的物种分别吸附在NiPc和CoPc表面,其能量不同,C正确;催化剂只影响
反应速率,不改变反应焓变,D错误。
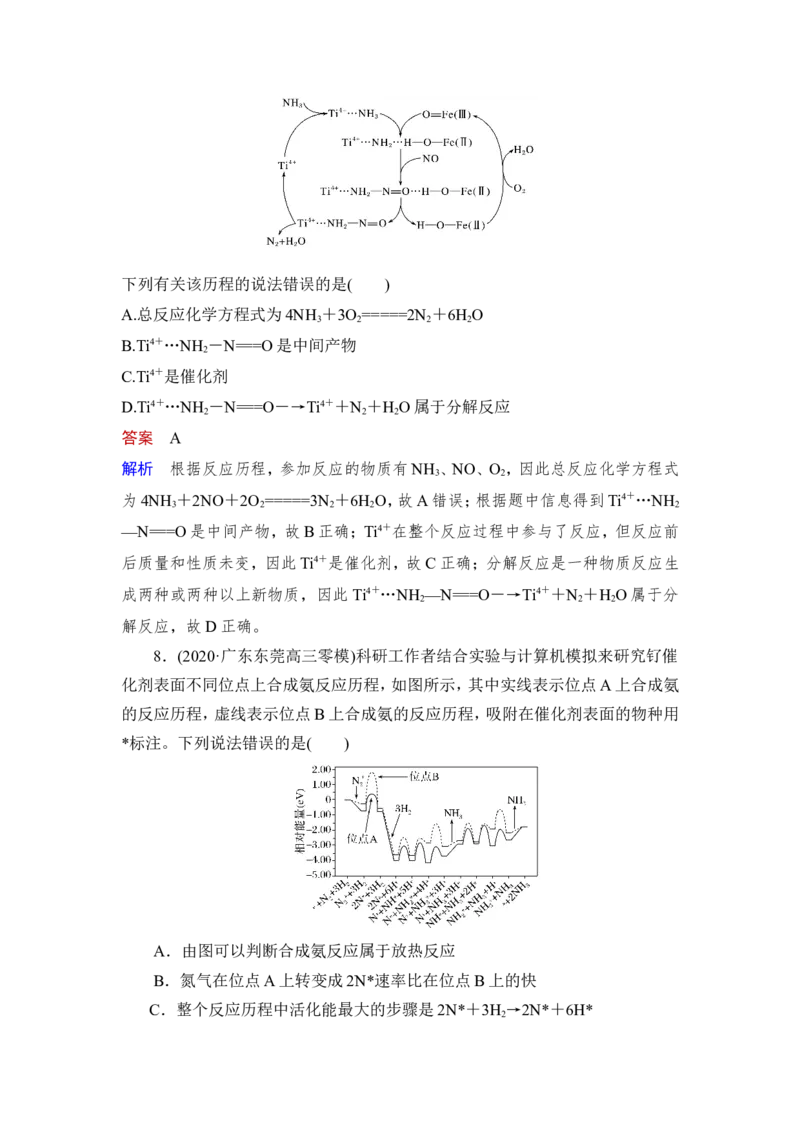
7.(2021·1月湖南普高校招生适应性考试,7)据文献报道,某反应的反应历程如图
所示:
INCLUDEPICTURE "G:\\2021课件\\X4.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\X4.TIF" \* MERGEFORMATINET下列有关该历程的说法错误的是( )
A.总反应化学方程式为4NH +3O =====2N +6H O
3 2 2 2
B.Ti4+…NH -N===O是中间产物
2
C.Ti4+是催化剂
D.Ti4+…NH -N===O―→Ti4++N +H O属于分解反应
2 2 2
答案 A
解析 根据反应历程,参加反应的物质有NH 、NO、O ,因此总反应化学方程式
3 2
为4NH +2NO+2O =====3N +6H O,故A错误;根据题中信息得到Ti4+…NH
3 2 2 2 2
—N===O是中间产物,故B正确;Ti4+在整个反应过程中参与了反应,但反应前
后质量和性质未变,因此Ti4+是催化剂,故C正确;分解反应是一种物质反应生
成两种或两种以上新物质,因此Ti4+…NH —N===O―→Ti4++N +H O属于分
2 2 2
解反应,故D正确。
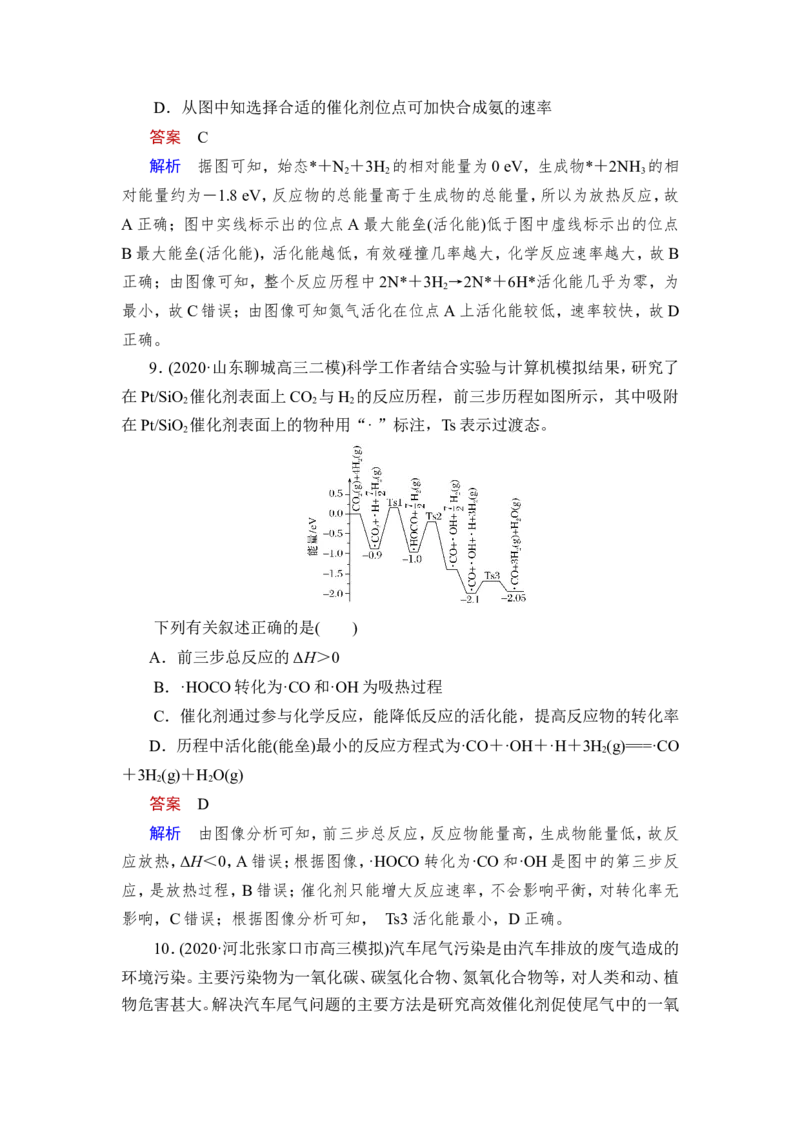
8.(2020·广东东莞高三零模)科研工作者结合实验与计算机模拟来研究钌催
化剂表面不同位点上合成氨反应历程,如图所示,其中实线表示位点A上合成氨
的反应历程,虚线表示位点B上合成氨的反应历程,吸附在催化剂表面的物种用
*标注。下列说法错误的是( )
A.由图可以判断合成氨反应属于放热反应
B.氮气在位点A上转变成2N*速率比在位点B上的快
C.整个反应历程中活化能最大的步骤是2N*+3H →2N*+6H*
2D.从图中知选择合适的催化剂位点可加快合成氨的速率
答案 C
解析 据图可知,始态*+N +3H 的相对能量为0 eV,生成物*+2NH 的相
2 2 3
对能量约为-1.8 eV,反应物的总能量高于生成物的总能量,所以为放热反应,故
A正确;图中实线标示出的位点A最大能垒(活化能)低于图中虚线标示出的位点
B最大能垒(活化能),活化能越低,有效碰撞几率越大,化学反应速率越大,故B
正确;由图像可知,整个反应历程中2N*+3H →2N*+6H*活化能几乎为零,为
2
最小,故C错误;由图像可知氮气活化在位点A上活化能较低,速率较快,故D
正确。
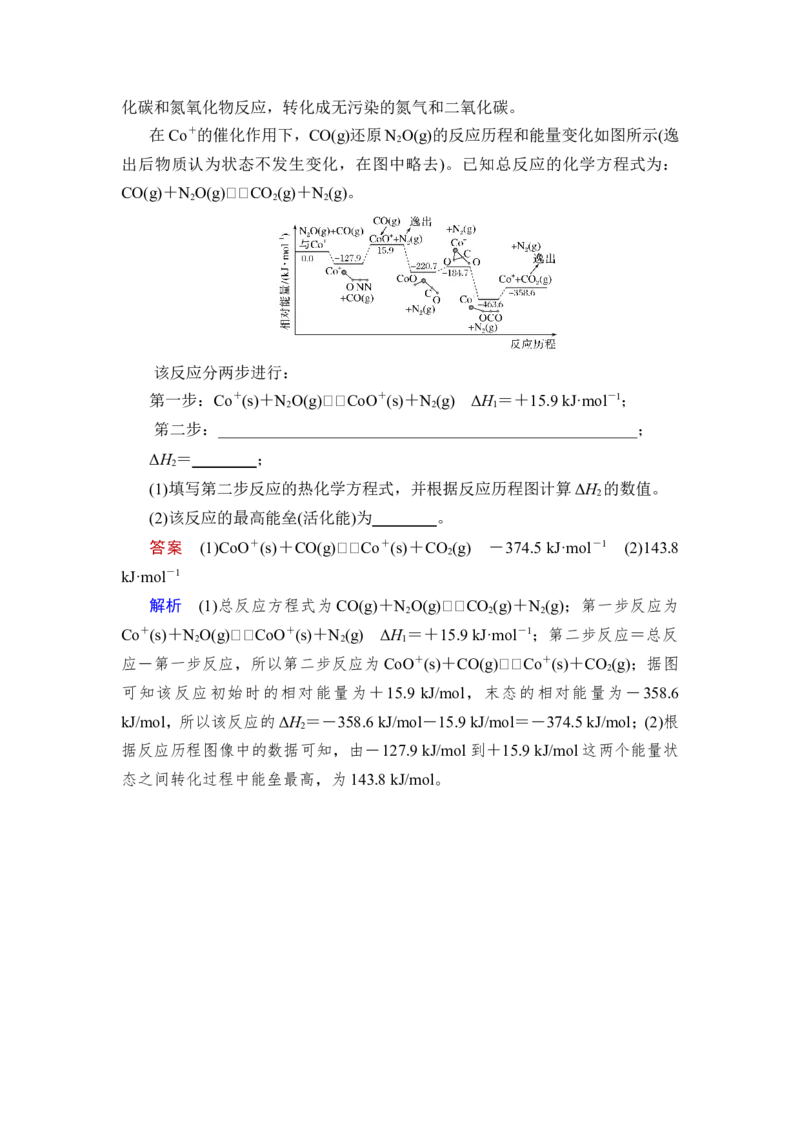
9.(2020·山东聊城高三二模)科学工作者结合实验与计算机模拟结果,研究了
在Pt/SiO 催化剂表面上CO 与H 的反应历程,前三步历程如图所示,其中吸附
2 2 2
在Pt/SiO 催化剂表面上的物种用“· ”标注,Ts表示过渡态。
2
下列有关叙述正确的是( )
A.前三步总反应的ΔH>0
B.·HOCO转化为·CO和·OH为吸热过程
C.催化剂通过参与化学反应,能降低反应的活化能,提高反应物的转化率
D.历程中活化能(能垒)最小的反应方程式为·CO+·OH+·H+3H (g)===·CO
2
+3H (g)+H O(g)
2 2
答案 D
解析 由图像分析可知,前三步总反应,反应物能量高,生成物能量低,故反
应放热,ΔH<0,A错误;根据图像,·HOCO转化为·CO和·OH是图中的第三步反
应,是放热过程,B错误;催化剂只能增大反应速率,不会影响平衡,对转化率无
影响,C错误;根据图像分析可知, Ts3活化能最小,D正确。
10.(2020·河北张家口市高三模拟)汽车尾气污染是由汽车排放的废气造成的
环境污染。主要污染物为一氧化碳、碳氢化合物、氮氧化合物等,对人类和动、植
物危害甚大。解决汽车尾气问题的主要方法是研究高效催化剂促使尾气中的一氧化碳和氮氧化物反应,转化成无污染的氮气和二氧化碳。
在Co+的催化作用下,CO(g)还原N O(g)的反应历程和能量变化如图所示(逸
2
出后物质认为状态不发生变化,在图中略去)。已知总反应的化学方程式为:
CO(g)+N O(g)CO (g)+N (g)。
2 2 2
该反应分两步进行:
第一步:Co+(s)+N O(g)CoO+(s)+N (g) ΔH =+15.9 kJ·mol-1;
2 2 1
笫二步:____________________________________________________;
ΔH =________;
2
(1)填写第二步反应的热化学方程式,并根据反应历程图计算ΔH 的数值。
2
(2)该反应的最高能垒(活化能)为________。
答案 (1)CoO+(s)+CO(g)Co+(s)+CO (g) -374.5 kJ·mol-1 (2)143.8
2
kJ·mol-1
解析 (1)总反应方程式为CO(g)+N O(g)CO (g)+N (g);第一步反应为
2 2 2
Co+(s)+N O(g)CoO+(s)+N (g) ΔH =+15.9 kJ·mol-1;第二步反应=总反
2 2 1
应-第一步反应,所以第二步反应为CoO+(s)+CO(g)Co+(s)+CO (g);据图
2
可知该反应初始时的相对能量为+15.9 kJ/mol,末态的相对能量为-358.6
kJ/mol,所以该反应的ΔH =-358.6 kJ/mol-15.9 kJ/mol=-374.5 kJ/mol;(2)根
2
据反应历程图像中的数据可知,由-127.9 kJ/mol到+15.9 kJ/mol这两个能量状
态之间转化过程中能垒最高,为143.8 kJ/mol。