文档内容
第 01 讲 化学实验的常用仪器和基本操作
目录
01 模拟基础练
【题型一】 仪器的识别与使用
【题型二】仪器的组合或组装
【题型三】化学实验安全
【题型四】试剂的保存
【题型五】装置型化学实验基本操作判断
【题型六】表格型简单实验设计与评价
02 重难创新练
03 真题实战练
题型一 仪器的识别与使用
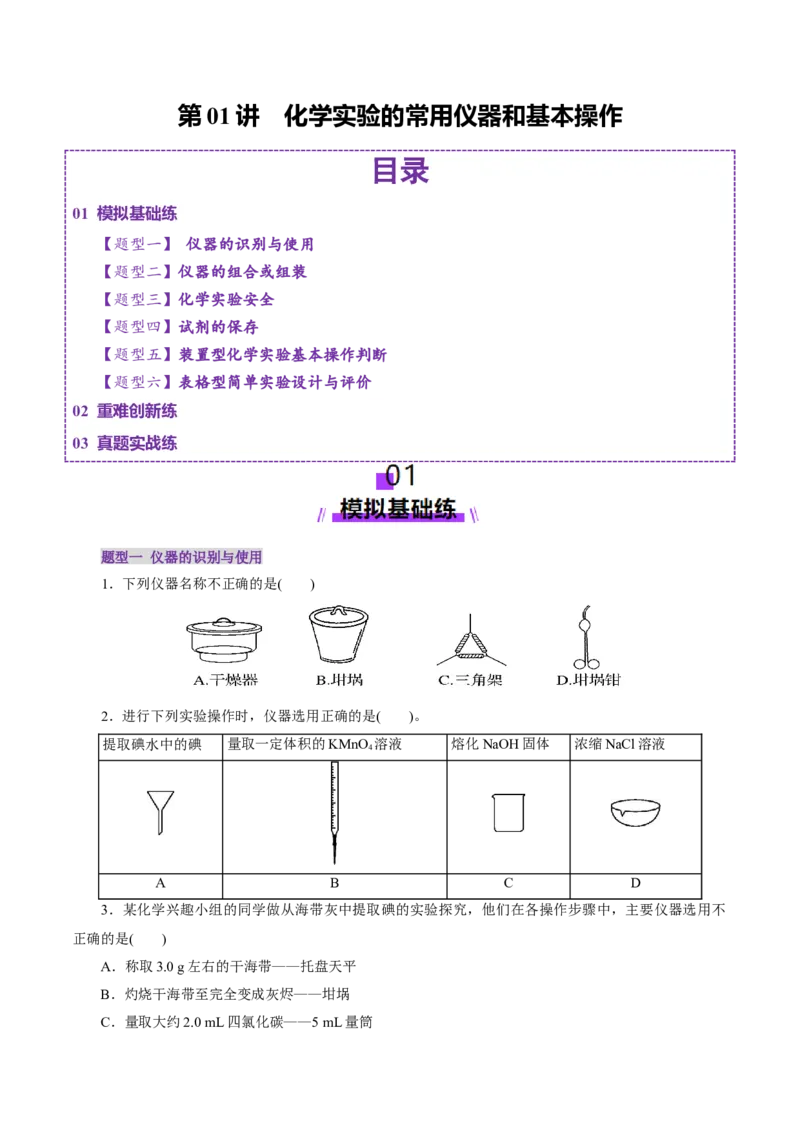
1.下列仪器名称不正确的是( )
2.进行下列实验操作时,仪器选用正确的是( )。
提取碘水中的碘 量取一定体积的KMnO 溶液 熔化NaOH固体 浓缩NaCl溶液
4
A B C D
3.某化学兴趣小组的同学做从海带灰中提取碘的实验探究,他们在各操作步骤中,主要仪器选用不
正确的是( )
A.称取3.0 g左右的干海带——托盘天平
B.灼烧干海带至完全变成灰烬——坩埚
C.量取大约2.0 mL四氯化碳——5 mL量筒D.用四氯化碳从氧化后的海带灰浸取液中提取碘——普通漏斗
4.(2024·山东省菏泽市二模)下列实验操作或实验仪器的使用错误的是( )
A.用酸式滴定管量取10.00mL高锰酸钾溶液
B.容量瓶和分液漏斗使用前均需检查是否漏水
C.保存氯化亚铁溶液时,加入少量稀盐酸和铁粉
D.皮肤溅上液溴,立即用苯洗涤,然后用水冲洗
题型二 仪器的组合或组装
5.(2024·湖南省邵阳市三模)关于下列仪器使用的说法错误的是( )
A.仪器①使用前,需要检查两处是否漏水
B.仪器②可用于测定硫酸铜晶体中的结晶水含量
C.仪器③和④可用于配制一定质量分数的CuSO 溶液
4
D.仪器⑤可用于移取0.1molL-1NaCr O 溶液
2 2 7
6.(2024·四川省成都市高三模⋅拟)为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考
虑存放试剂的容器和连接装置)( )
实验序号 实验目的 玻璃仪器 试剂
① 萃取碘水中的碘单质 长颈漏斗、烧杯 CCl 、碘水
4
启普发生器、试管、
② 制SO NaSO 固体、浓硫酸(70%)
2 导管 2 3
配制100mL一定物质 100mL容量瓶、烧
③ 蒸馏水、NaCl固体
的量浓度的NaCl溶液 杯、玻璃棒
葡萄糖的银镜反应实 试管、酒精灯、烧
④ 10%葡萄糖溶液、新制的银氨溶液
验 杯、量筒、胶头滴管
A.① B.② C.③ D.④
7.用下列实验器材(夹持仪器省略),能够完成相应实验的是( )
实验器材 相应实验
A 烧杯、玻璃棒、蒸发皿 硫酸铜溶液的浓缩结晶
B 烧杯、玻璃棒、滤纸 用盐酸除去硫酸钡中的少量碳酸钡
C 烧杯、胶头滴管、托盘天平 用固体氯化钠配制0.5mol·L-1的溶液D 烧杯、胶头滴管、分液漏斗 用溴水和CCl 除去NaBr溶液中的少量NaI
4
8.仅用下表提供的仪器(夹持仪器和试剂任选)不能达到相应实验目的的一组是( )
选项 实验目的 仪器
A 制取乙酸乙酯 试管、酒精灯
用浓硫酸配制250mL一定浓度的硫酸溶
B 250mL容量瓶、烧杯、玻璃棒、胶头滴管
液
C 从食盐水中获得NaCl晶体 酒精灯、玻璃棒、蒸发皿
D 用盐酸除去BaSO 中混有的少量BaCO 漏斗、烧杯、玻璃棒、胶头滴管、滤纸
4 3
9.为完成相应实验,实验器材(规格和数量不限)足够的一项是( )
相应实验 实验仪器和用品(夹持装置省略)
A 氯化钠溶液的蒸发结晶 烧杯、玻璃棒、酒精灯
B 用盐酸除去硫酸钡中的少量碳酸钡 烧杯、胶头滴管
C 配制0.5 mol·L-1的硫酸溶液 烧杯、玻璃棒、胶头滴管、容量瓶
D 用CCl 萃取溴水中的溴 分液漏斗、烧杯
4
题型三 化学实验安全
10.(2024·山东省济南市三模)下列实验室废弃物处理得当的是( )
A.废弃的钠屑分批加入乙醇中溶解,再加水稀释、用酸中和后方可排放
B.向铜和浓硫酸反应后的废液中加水稀释、用碱中和后方可排放
C.用适量浓氨水清洗银镜反应后的试管可得到能循环使用的银氨溶液
D.废弃的白磷固体用纸包裹后直接放入垃圾桶中
11.(2024·湖北省普通高中高考钾题预测)实验安全及操作规范至关重要。下列叙述不正确的是( )
A.磷化钙、磷化铝等金属磷化物应放在干燥器中保存,并贴上红色标签
B.启普发生器是简易制气装置,但实验室制备乙炔时不可使用启普发生器
C.在实验室做有机实验时若突发有机溶剂着火,则应迅速用大量水灭火
D.用滴定管量取20.00mL酸性高锰酸钾溶液时应选用酸式滴定管
12.(2024•高三下·河北省沧州市八县联考)下列实验室药品的保存或实验安全应急措施错误的是( )
A.漂白粉要避光、密封保存在阴凉处
B.浓溴水沾在皮肤上,先用大量水冲洗,再用酒精擦拭
C.AgNO 溶液应当保存在棕色细口瓶中
3
D.浓硫酸沾到皮肤上,先用大量水冲洗,然后涂抹稀NaOH溶液
13.(2024·重庆荣昌市高三模拟)实验室安全至关重要,下列做法正确的是( )
A.蒸发液体时液体体积不超过蒸发皿容积的 ,且要用玻璃棒搅拌B. 溶液不慎溅在皮肤上,先用大量水冲洗,再用 的碳酸氢钠溶液冲洗
C.H 还原Fe O 时,要先通一段时间氢气后再加热还原,最后还原铁粉在氢气气氛中冷却
2 3 4
D.蒸馏实验时忘记加碎瓷片,应停止加热,然后立即加入碎瓷片
14.(2024·江西省部分学校高三适应性考试大联考)实验室安全至关重要。下列做法正确的是( )
A.误食钡盐,可通过服用碳酸钠溶液解毒
B.中学实验室中未用完的钠、钾、白磷等不宜放回原试剂瓶
C.取用液溴时,需戴手套和护目镜,在通风橱中进行
D.苯酚不慎沾到皮肤上时,先用抹布擦拭,再用65℃以上的水冲洗
15.安全是顺利进行实验及避免伤害的保障。下列实验操作正确但不是从实验安全角度考虑的是(
)
A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.操作②:使用CCl 萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
4
C.操作③:吸收氨气或氯化氢气体并防止倒吸
D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
题型四 试剂的保存
16.下列试剂的保存方法正确的是( )。
A.溴化银通常保存在无色广口瓶中
B.钠常保存于无色广口瓶中,并可加适量CCl 液封
4
C.HF溶液通常密封于细口玻璃瓶中
D.NaCO 溶液通常密封于带橡胶塞的细口瓶中
2 3
17.下列盛放试剂的方法正确的是( )
A.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中
B.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中
C.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中
D.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中
18. 实验室保存下列试剂,其中保存方法和理由描述都正确的是( )
选项 试剂 保存方法 理由
防止与空气中水、氧气接触发生反
A 钠 保存在煤油中
应B 液溴 密封保存在细口瓶中 防止升华
C 浓硝酸 密封保存在铁质容器中 避免见光分解
D 烧碱 存放在带有磨口玻璃塞的广口瓶中 防止与空气中氧气接触被氧化
题型五 装置型化学实验基本操作判断
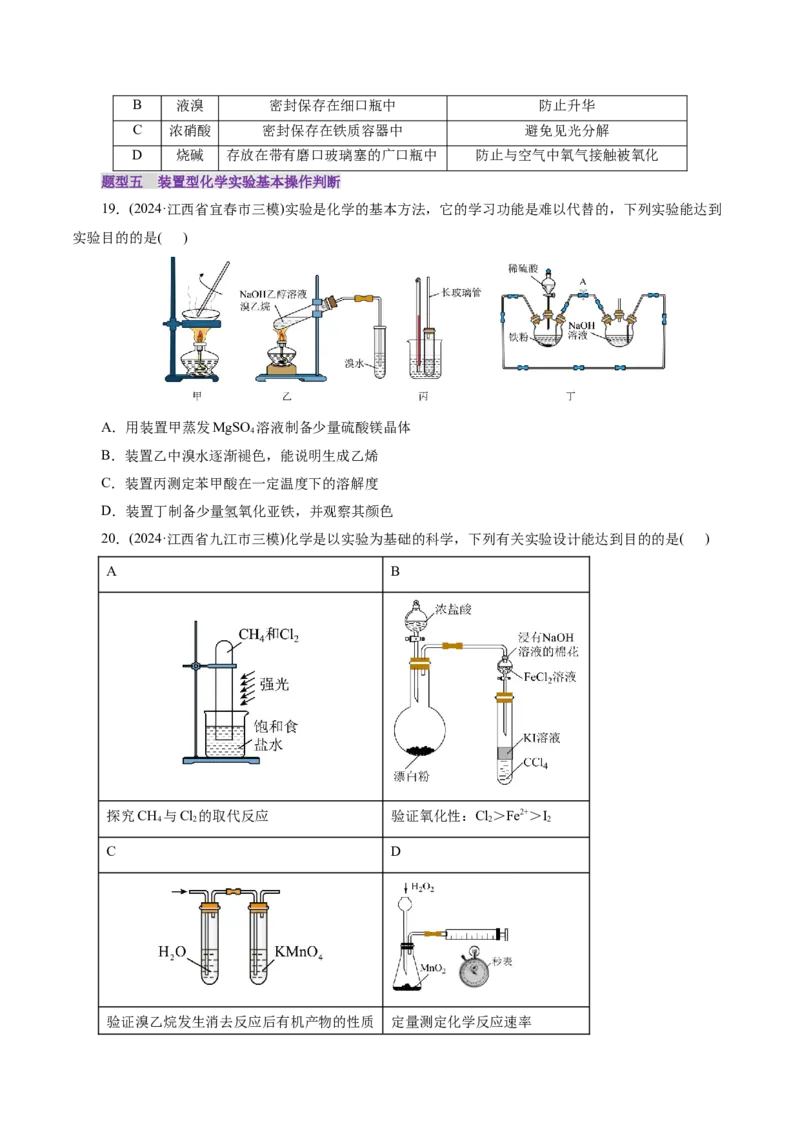
19.(2024·江西省宜春市三模)实验是化学的基本方法,它的学习功能是难以代替的,下列实验能达到
实验目的的是( )
A.用装置甲蒸发MgSO 溶液制备少量硫酸镁晶体
4
B.装置乙中溴水逐渐褪色,能说明生成乙烯
C.装置丙测定苯甲酸在一定温度下的溶解度
D.装置丁制备少量氢氧化亚铁,并观察其颜色
20.(2024·江西省九江市三模)化学是以实验为基础的科学,下列有关实验设计能达到目的的是( )
A B
探究CH 与Cl 的取代反应 验证氧化性:Cl>Fe2+>I
4 2 2 2
C D
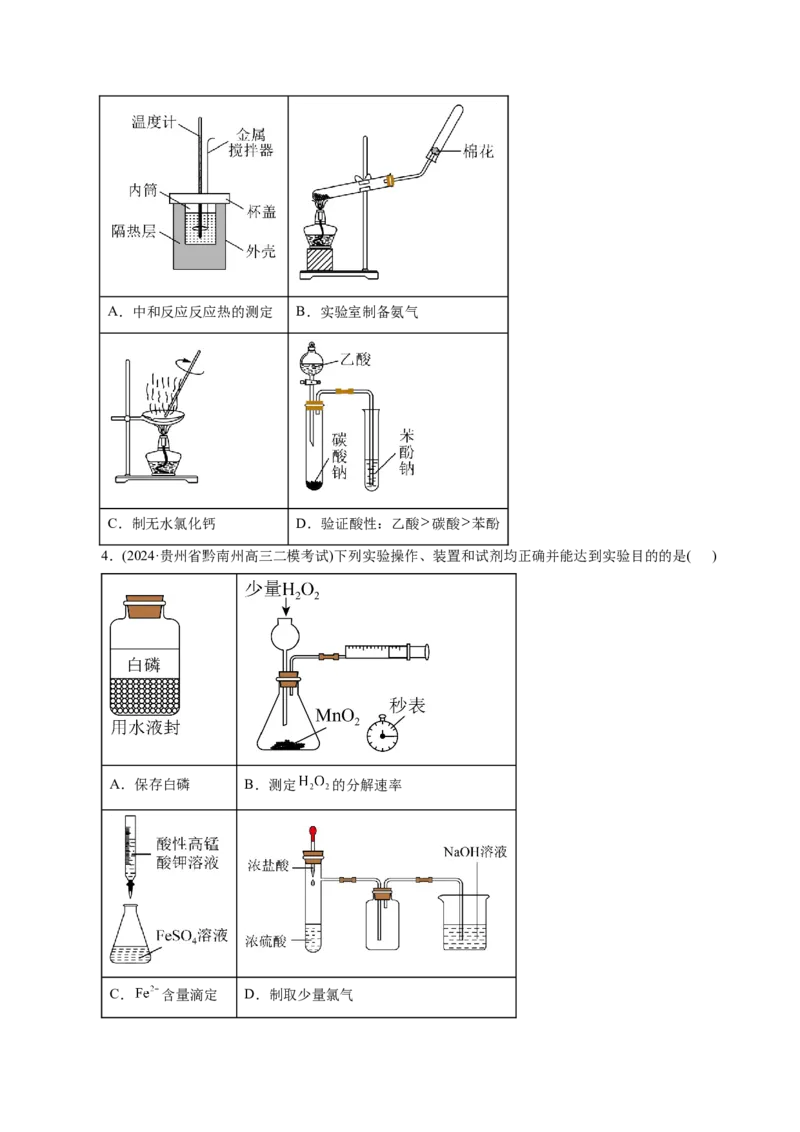
验证溴乙烷发生消去反应后有机产物的性质 定量测定化学反应速率21.(2024·辽宁省大连市二模)实验是探究化学过程的重要途径。下列装置能达到相应目的的是( )
A.制备Fe(OH) 胶体 B.测量NO 气体的体积 C.将剩余钠放回试剂瓶 D.分离碘和氯化铵固体
3 2
题型六 表格型简单实验设计与评价
22.(2024·浙江省北斗星盟高三联考)探究CHCOOH及相关化合物的性质,下列方案设计、现象、结
3
论都正确的是( )
实验方案 现象 结论
用 试纸分别测定 :
A ①NaNO 溶液; pH:① ② K(HNO)<K(CHCOOH)
2 a 2 a 3
②CHCOONa溶液
3
用 溶液分
别与等体积等浓度
反应热:ΔH< CHCOOH(aq) H+(aq)+
B CHCOOH溶液、盐酸反 1 3
3 ΔH CHCOO-(aq) ΔH>0
应,测得反应热依次为 2 3
ΔH、ΔH
1 2
常温下,分别测定浓度均为 常温下,1mol·L-1的
C 1mol·L-1的CH 3 COONH 4 溶 均等于7 CH 3 COONH 4 溶液和NaCl溶液
液和NaCl溶液的 中水的电离程度相等
混合过程中削弱了CHCOOH
3
常温下,将50 mL苯与50 所得混合溶液体 分子间的氢键,且苯与
D
mL CHCOOH混合 积为 CHCOOH分子间的作用弱于
3 3
氢键
23.(2024·浙江省宁波市镇海中学高三模拟)探究铜及其化合物的性质,下列方案设计、现象和结论都
正确的是( )
实验方案 现象 结论
向 浓度均为 的
K [Mg(OH) ]>
A MgCl、CuCl 混合溶液中加入 出现蓝色沉淀 sp 2
2 2 K [Cu(OH) ]
sp 2
溶液硫酸铜粉末溶解后
取适量硫酸铜粉末溶于水,再 显蓝色,加足浓氨 氨分子结合铜离子能力
B
向溶液中加入足量浓氨水 水后得到深蓝色溶 强于水分子
液
将铜和浓硫酸反应后的混合物
说明铜和浓硫酸反应后
C 倒入盛有稀盐酸、BaCl 混合溶 产生大量白色沉淀
2 有硫酸剩余
液的烧杯中
取一段未打磨的铝条,伸入稀 铝条表面出现紫红
D 铝活泼性比铜强
CuSO 溶液 色固体
4
24.(2024·浙江省绍兴市第一中学高三首考模拟)探究钠及其化合物的性质,下列方案设计、现象和结
论都正确的是( )
实验方案 现象 结论
将金属钠置于坩埚中燃烧,取燃烧后的少量固体粉末 有气体生
A 该固体粉末一定为NaO
于试管中,加入 蒸馏水 成 2 2
随温度升高,K 逐渐增大,
B 将25℃0.1mol·L-1 CH 3 COONa溶液加热到40℃,用 溶液的 CHCOONa溶液 W 中c(H+)增大,
传感器监测溶液 变化 逐渐减小 3
c(OH―)减小
有白色沉
C 向NaHCO 溶液中加入等体积等浓度的NaAlO 溶液 AlO-结合H+的能力强于CO2-
3 2 淀生成 2 3
测定中和热时,将稀 溶液缓慢倒入到盛有稀 温度差为 中和反应放热,将 代入公式
D
的内筒,搅拌使其充分混合,再盖上杯盖 算得中和热( )
25.(2024·浙江省温州市普通高中高三下学期第二次适应性考试)根据实验目的设计方案并进行实验,
观察到相关现象,其中设计和结论均合理的是( )
实验目的 实验方案设计 现象 结论
向Fe(NO ) 溶液中加入过量HI
探究Fe3+与I 的氧 3 3
A 2 溶液充分反应,再滴加淀粉溶 溶液变蓝色 氧化性:Fe3+>I
化性强弱 2
液
比较OH-与C HO-结 常温,测定0.1mol/LC HONa 结合H+能力:C HO-
B 2 5 2 5 pH=13 2 5
合H+ 的能力 溶液的pH >OH-
说明降低温度,
加热后溶液为
探究温度对化学平 将2mL0.5mol·L-1CuCl 溶液加 [Cu(H O) ]2++4Cl-
C 2 黄绿色,冷水 2 4
衡的影响 热后置于冷水中,观察现象 [CuCl ]2-+4H O
中变为蓝绿色 4 2
向正反应方向移动
向含有浓度均为0.001mol·L-1的
比较AgCl与 先生成白色
D Cl-、CrO2-溶液中,逐滴滴加 K :AgCl<Ag CrO
Ag CrO 的K 4 AgCl沉淀 sp 2 4
2 4 sp 0.001mol·L-1AgNO 溶液
326.(2024·浙江省金丽衢十二校高三下学期第二次联考)下列方案设计、现象和结论不正确的是( )
实验目的 实验方案 现象 结论
验证FeCl - (黄色) FeCl -在高浓度
4 向稀盐酸和FeCl 的混合溶液中, NaCl固体溶解,溶液 4
A 在高浓度Cl-的条 3 Cl-的条件下稳
加入NaCl固体 变为亮黄色
件下稳定 定
向2 mL0.1 mol/L KI溶液滴加2滴
比较AgI与Ag S 先产生淡黄色沉淀, K (AgI)>K
B 2 0.1 mol/L硝酸银,然后再滴加2 sp sp
的K 后转化为黑色沉淀 (Ag S)
sp 滴0.1 mol/L的KS溶液 2
2
检验乙酰水杨酸中 乙酰水杨酸中滴入稀硫酸,加
C 溶液呈紫色 存在酯基
存在酯基 热,冷却后滴加FeCl 溶液
3
前者产生白色沉淀;
比较Mg与Al的金 分别向MgCl >AlCl 溶液中滴加
D 2 3 后者先产生白色沉 Mg>Al
属性 足量的NaOH溶液
淀,沉淀后消失
1.(2024·湖南省北师联盟高三三模)下列有关实验室仪器和试剂的使用说法错误的是( )
A.进行钾与水反应的实验,可用培养皿代替小烧杯
B.实验室使用试管和烧瓶加热液体时,所盛液体体积应介于其容积的 之间
C.制备硝基苯时用到的混酸,可通过将浓硫酸缓缓注入浓硝酸中获得
D.用苯进行萃取溴水中的溴的实验时,振荡后打开分液漏斗的活塞及时放气
2.(2024·浙江省义乌中学选考模拟)下列有关实验基本操作不能达到目的的是( )
A.配制10% CuSO 溶液:称取5.0 g CuSO ·5H O,加入27.0 g水,搅拌溶解
4 4 2
B.在实验室中,采用加热氯酸钾和二氧化锰混合物的方法制取氧气,通过溶解、过滤、洗涤、干燥
的方法从反应产物中得到二氧化锰
C.可以用酒精灯、玻璃棒、坩埚、泥三角这些仪器从食盐水中获取NaCl晶体
D.配制100 mL 1 mol·L-1的NaCO 溶液可将固体放于天平左盘称其质量
2 3
3.(2024·河北省普通高中学业水平选择性考试冲刺卷)下列实验设计和操作均正确且能达到实验目的
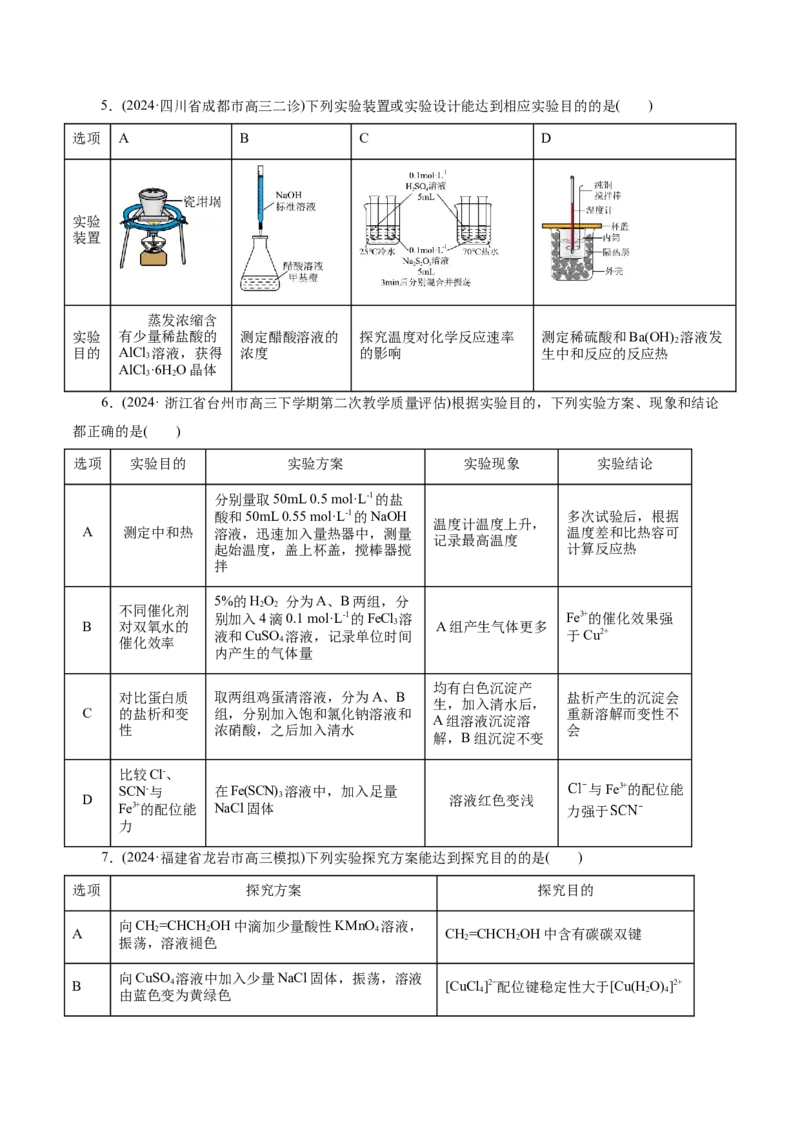
的是( )A.中和反应反应热的测定 B.实验室制备氨气
C.制无水氯化钙 D.验证酸性:乙酸 碳酸 苯酚
4.(2024·贵州省黔南州高三二模考试)下列实验操作、装置和试剂均正确并能达到实验目的的是( )
A.保存白磷 B.测定 的分解速率
C. 含量滴定 D.制取少量氯气5.(2024·四川省成都市高三二诊)下列实验装置或实验设计能达到相应实验目的的是( )
选项 A B C D
实验
装置
蒸发浓缩含
实验 有少量稀盐酸的 测定醋酸溶液的 探究温度对化学反应速率 测定稀硫酸和Ba(OH) 溶液发
2
目的 AlCl 溶液,获得 浓度 的影响 生中和反应的反应热
3
AlCl ·6H O晶体
3 2
6.(2024· 浙江省台州市高三下学期第二次教学质量评估)根据实验目的,下列实验方案、现象和结论
都正确的是( )
选项 实验目的 实验方案 实验现象 实验结论
分别量取50mL 0.5 mol·L-1的盐
酸和50mL 0.55 mol·L-1的NaOH 多次试验后,根据
温度计温度上升,
A 测定中和热 溶液,迅速加入量热器中,测量 温度差和比热容可
记录最高温度
起始温度,盖上杯盖,搅棒器搅 计算反应热
拌
5%的HO 分为A、B两组,分
不同催化剂 2 2
别加入4滴0.1 mol·L-1的FeCl 溶 Fe3+的催化效果强
B 对双氧水的 3 A组产生气体更多
液和CuSO 溶液,记录单位时间 于Cu2+
催化效率 4
内产生的气体量
均有白色沉淀产
对比蛋白质 取两组鸡蛋清溶液,分为A、B 盐析产生的沉淀会
生,加入清水后,
C 的盐析和变 组,分别加入饱和氯化钠溶液和 重新溶解而变性不
A组溶液沉淀溶
性 浓硝酸,之后加入清水 会
解,B组沉淀不变
比较Cl-、
SCN-与 在Fe(SCN) 溶液中,加入足量 与Fe3+的配位能
D 3 溶液红色变浅
Fe3+的配位能 NaCl固体 力强于
力
7.(2024·福建省龙岩市高三模拟)下列实验探究方案能达到探究目的的是( )
选项 探究方案 探究目的
向CH=CHCHOH中滴加少量酸性KMnO 溶液,
A 2 2 4 CH=CHCHOH中含有碳碳双键
振荡,溶液褪色 2 2
向CuSO 溶液中加入少量NaCl固体,振荡,溶液
B 4 [CuCl ]2−配位键稳定性大于[Cu(H O) ]2+
由蓝色变为黄绿色 4 2 4向酸性KCr O 溶液中加入相同体积不同浓度的
C 2 2 7 pH越大,化学反应速率越快
NaOH溶液,浓度越大,溶液黄色越深
向碳酸钠溶液中滴加浓盐酸,将产生的气体通入
D 碳酸的酸性大于苯酚
苯酚钠溶液中,溶液变浑浊
8.(2024·浙江省宁波市十校高三二模联考)根据实验目的设计方案并进行实验,观察到相关现象,下
列方案设计、结论均正确的是( )
实验目的 方案设计 现象 结论
金属Na与
探究金属Na、Ca的 将金属Na、Ca分别切成体积相等的 Na的金属性强于
A 水反应更加
金属性强弱 颗粒,投入蒸馏水中 Ca
剧烈
判断AlCl 的化学键 将AlCl 固体溶于水,进行导电性实 AlCl 溶液可 AlCl 中含有离子
B 3 3 3 3
类型 验 导电 键
炭与浓硝酸在加热
探究浓硝酸与炭在加 产生红棕色
C 将红热的木炭投入浓硝酸中 条件下反应生成
热条件下能否反应 气体
NO
2
分别向丙烯酸乙酯
前者无明显 氰基活化双键,使
探究有机物中官能团 (CH=CHCOOCH CH)和α-氰基丙
D 2 2 3 现象,后者 其更易发生加聚反
之间的影响 烯酸乙酯[CH=C(CN)COOCH CH]
2 2 3 快速固化 应
中滴入水
9.(2024·浙江省杭州市高三下学期二模)根据实验目的设计方案并进行实验,观察到相关现象,方案
设计或结论不正确的是( )
选项 实验目的 方案设计 现象 结论
探究NH F与 分别测定0.1mol·L-1的
4 F-水解程度小于
A CHCOONH 水 NH F和CHCOONH 溶液 前者 小
3 4 4 3 4 CHCOO-
解程度的大小 pH 3
探究Fe2+、 向FeCl 溶液依次滴加足量
2 加入KSCN后无明显变 结合 能力:
B Fe3+结合SCN-的 KSCN溶液、几滴HO 溶
2 2 化,加入HO 溶液变红 Fe3+>Fe2+
能力 液 2 2
用HSO 调节相同浓度
探究c(H+)对 2 4
KCl、KBr和KI溶液的 最低c(H+)顺序:KCl> c(H+)浓度越大,
C MnO 氧化性的
影响 2 ,测量氧化反应所需最低 KBr>KI MnO 2 氧化性越强
c(H+)
比较AlO-与
2 将等浓度等体积的NaAlO 结合 能力:CO2-
D CO2-结合H+能 2 产生白色沉淀 3
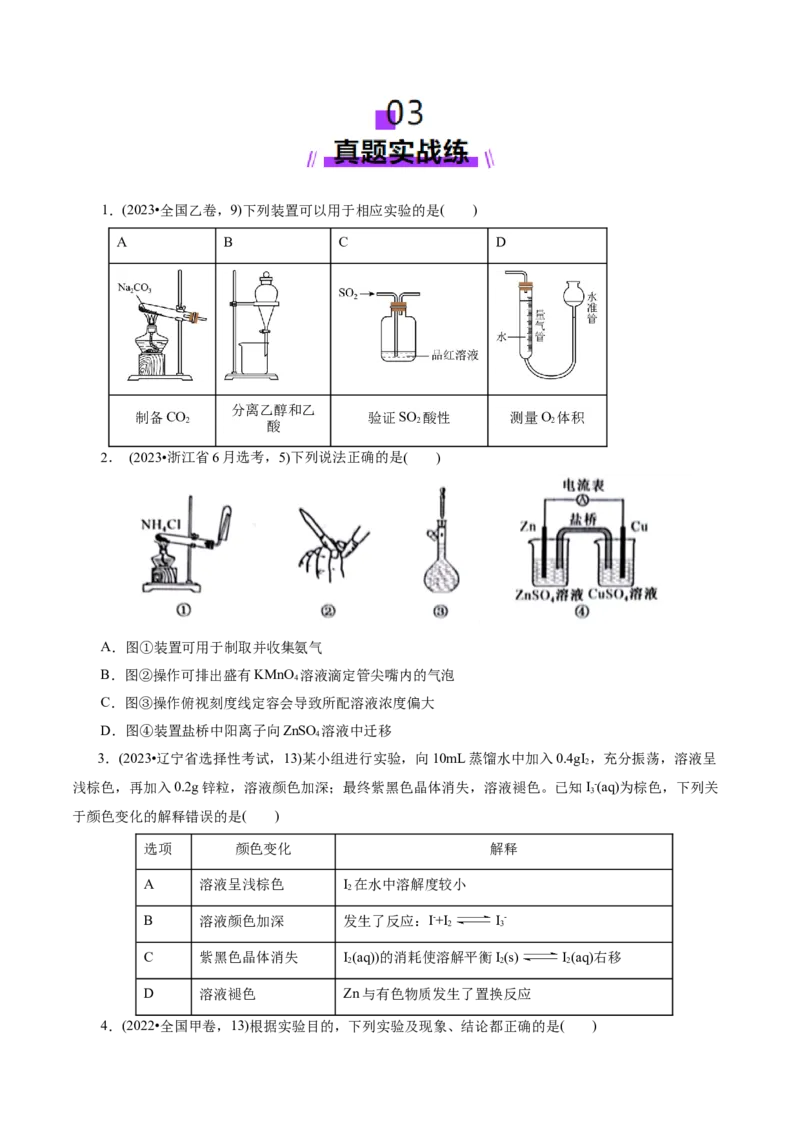
力 3 溶液和NaHCO 3 溶液混合 <AlO 2 -1.(2023•全国乙卷,9)下列装置可以用于相应实验的是( )
A B C D
分离乙醇和乙
制备CO 验证SO 酸性 测量O 体积
2 酸 2 2
2. (2023•浙江省6月选考,5)下列说法正确的是( )
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有KMnO 溶液滴定管尖嘴内的气泡
4
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向ZnSO 溶液中迁移
4
3.(2023•辽宁省选择性考试,13)某小组进行实验,向10mL蒸馏水中加入0.4gI,充分振荡,溶液呈
2
浅棕色,再加入0.2g锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知I-(aq)为棕色,下列关
3
于颜色变化的解释错误的是( )
选项 颜色变化 解释
A 溶液呈浅棕色 I 在水中溶解度较小
2
B 溶液颜色加深 发生了反应:I-+I I-
2 3
C 紫黑色晶体消失 I(aq))的消耗使溶解平衡I(s) I(aq)右移
2 2 2
D 溶液褪色 Zn与有色物质发生了置换反应
4.(2022•全国甲卷,13)根据实验目的,下列实验及现象、结论都正确的是( )选项 实验目的 实验及现象 结论
分别测浓度均为0.1 mol·L-1的
比较CHCOO-和HCO - K(CHCOO-)<
A 3 3 CHCOONH 和NaHCO 溶液的 h 3
的水解常数 3 4 3 K(HCO -)
pH,后者大于前者 h 3
检验铁锈中是否含有二 将铁锈溶于浓盐酸,滴入
B 铁锈中含有二价铁
价铁 KMnO 溶液,紫色褪去
4
探究氢离子浓度对 增大氢离子浓度,转化
向KCrO 溶液中缓慢滴加硫
C CrO2-、Cr O2-相互转化 2 4 平衡向生成Cr O2-的方
4 2 7 酸,黄色变为橙红色 2 7
的影响 向移动
向乙醇中加入一小粒金属钠,
D 检验乙醇中是否含有水 乙醇中含有水
产生无色气体
5.(2022•江苏卷,11)室温下,下列实验探究方案不能达到探究目的的是( )
选项 探究方案 探究目的
向盛有FeSO 溶液的试管中滴加几滴KSCN溶液,振
A 4 Fe2+具有还原性
荡,再滴加几滴新制氯水,观察溶液颜色变化
向盛有SO 水溶液的试管中滴加几滴品红溶液,振荡,
B 2 SO 具有漂白性
加热试管,观察溶液颜色变化 2
向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观
C Br 的氧化性比I 的强
察溶液颜色变化 2 2
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 CHCOOH是弱电解质
3
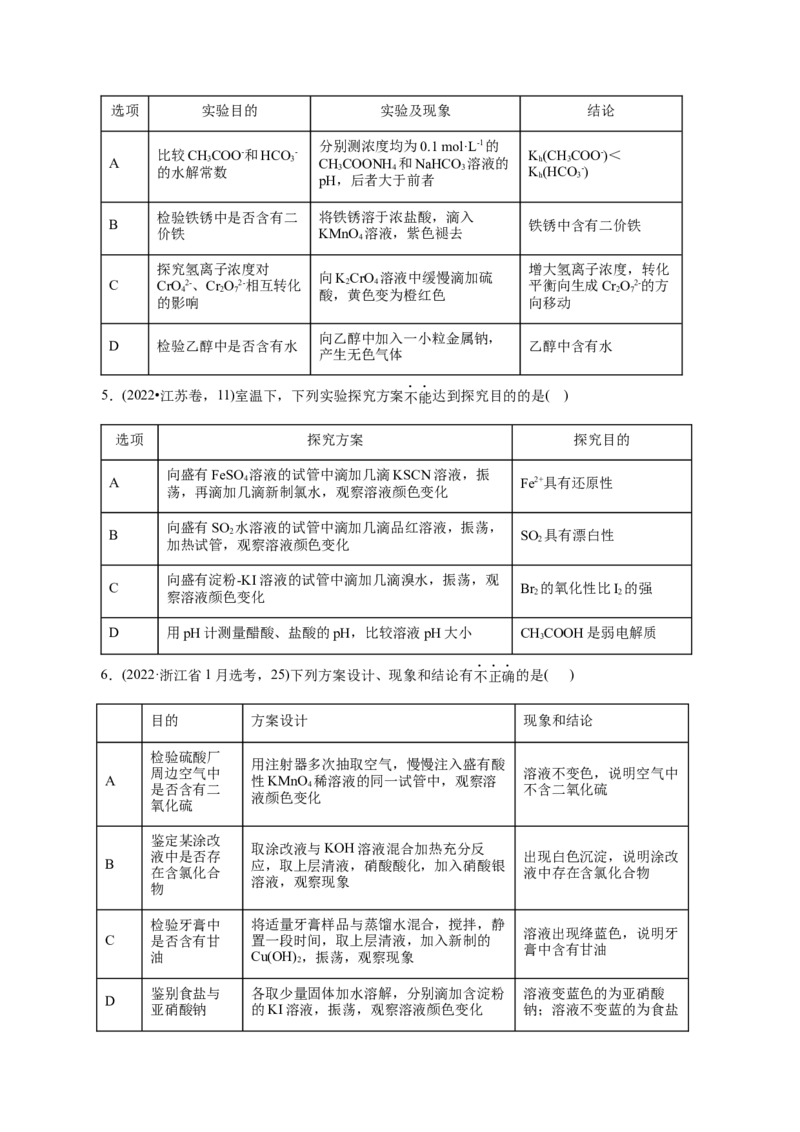
6.(2022·浙江省1月选考,25)下列方案设计、现象和结论有不正确的是( )
目的 方案设计 现象和结论
检验硫酸厂
用注射器多次抽取空气,慢慢注入盛有酸
周边空气中 溶液不变色,说明空气中
A 性KMnO 稀溶液的同一试管中,观察溶
是否含有二 4 不含二氧化硫
液颜色变化
氧化硫
鉴定某涂改
取涂改液与KOH溶液混合加热充分反
液中是否存 出现白色沉淀,说明涂改
B 应,取上层清液,硝酸酸化,加入硝酸银
在含氯化合 液中存在含氯化合物
溶液,观察现象
物
检验牙膏中 将适量牙膏样品与蒸馏水混合,搅拌,静
溶液出现绛蓝色,说明牙
C 是否含有甘 置一段时间,取上层清液,加入新制的
膏中含有甘油
油 Cu(OH) ,振荡,观察现象
2
鉴别食盐与 各取少量固体加水溶解,分别滴加含淀粉 溶液变蓝色的为亚硝酸
D
亚硝酸钠 的KI溶液,振荡,观察溶液颜色变化 钠;溶液不变蓝的为食盐7.(2021•浙江6月选考,25)下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
取4 mL乙醇,加入12 mL浓硫酸、少
若溴水褪色,则乙醇消
A 探究乙醇消去反应的产物 量沸石,迅速升温至140℃,将产生
去反应的产物为乙烯
的气体通入2 mL溴水中
探究乙酰水杨酸样品中是否 取少量样品,加入 蒸馏水和少量 若有紫色沉淀生成,则
B
含有水杨酸 乙醇,振荡,再加入1-2滴FeCl 溶液 该产品中含有水杨酸
3
若无气体生成,则固体
探究金属钠在氧气中燃烧所 取少量固体粉末,加入2~3 mL蒸馏 粉末为NaO;若有气体
C 2
得固体粉末的成分 水 生成,则固体粉末为
NaO
2 2
探究NaSO 固体样品是否变 取少量待测样品溶于蒸馏水,加入足 若有白色沉淀产生,则
D 2 3
质 量稀盐酸,再加入足量BaCl 溶液 样品已经变质
2
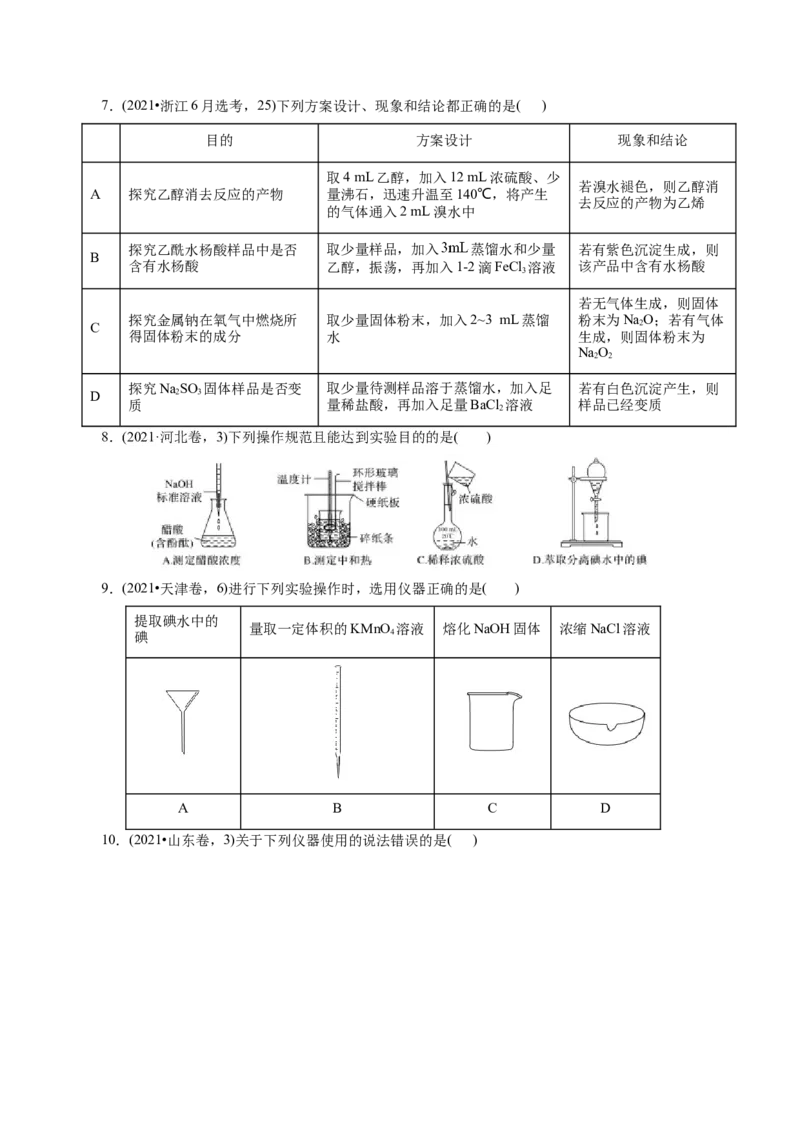
8.(2021·河北卷,3)下列操作规范且能达到实验目的的是( )
9.(2021•天津卷,6)进行下列实验操作时,选用仪器正确的是( )
提取碘水中的
量取一定体积的KMnO 溶液 熔化NaOH固体 浓缩NaCl溶液
碘 4
A B C D
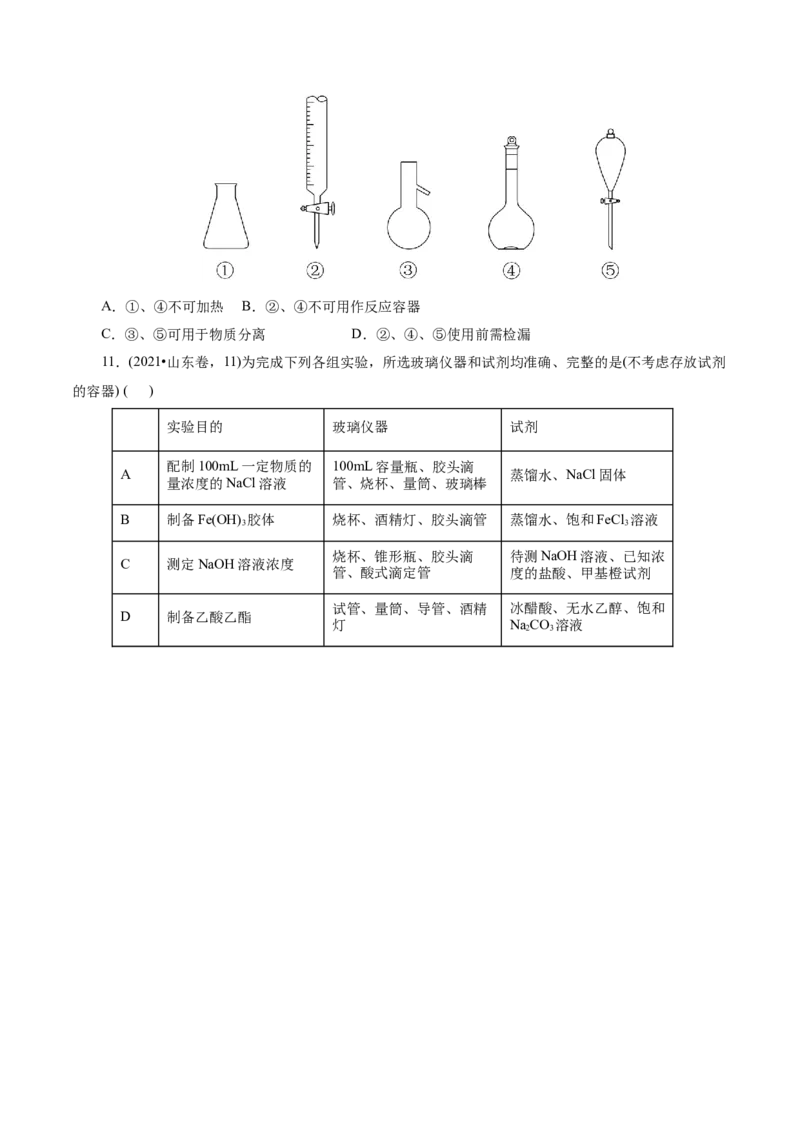
10.(2021•山东卷,3)关于下列仪器使用的说法错误的是( )A.①、④不可加热 B.②、④不可用作反应容器
C.③、⑤可用于物质分离 D.②、④、⑤使用前需检漏
11.(2021•山东卷,11)为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂
的容器) ( )
实验目的 玻璃仪器 试剂
配制100mL一定物质的 100mL容量瓶、胶头滴
A 蒸馏水、NaCl固体
量浓度的NaCl溶液 管、烧杯、量筒、玻璃棒
B 制备Fe(OH) 胶体 烧杯、酒精灯、胶头滴管 蒸馏水、饱和FeCl 溶液
3 3
烧杯、锥形瓶、胶头滴 待测NaOH溶液、已知浓
C 测定NaOH溶液浓度
管、酸式滴定管 度的盐酸、甲基橙试剂
试管、量筒、导管、酒精 冰醋酸、无水乙醇、饱和
D 制备乙酸乙酯
灯 NaCO 溶液
2 3