文档内容
第 09 讲 铁及其重要化合物
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查铁及其化合物的性质与应用
高频考点2 考查Fe2+、Fe3+ 的性质及其检验
高频考点3 考查“铁三角”的转化及应用
高频考点4 考查氢氧化亚铁的制备
高频考点5 考查有关铁及其化合物的计算
高频考点6、考查铁及其化合物性质的实验探究
正文
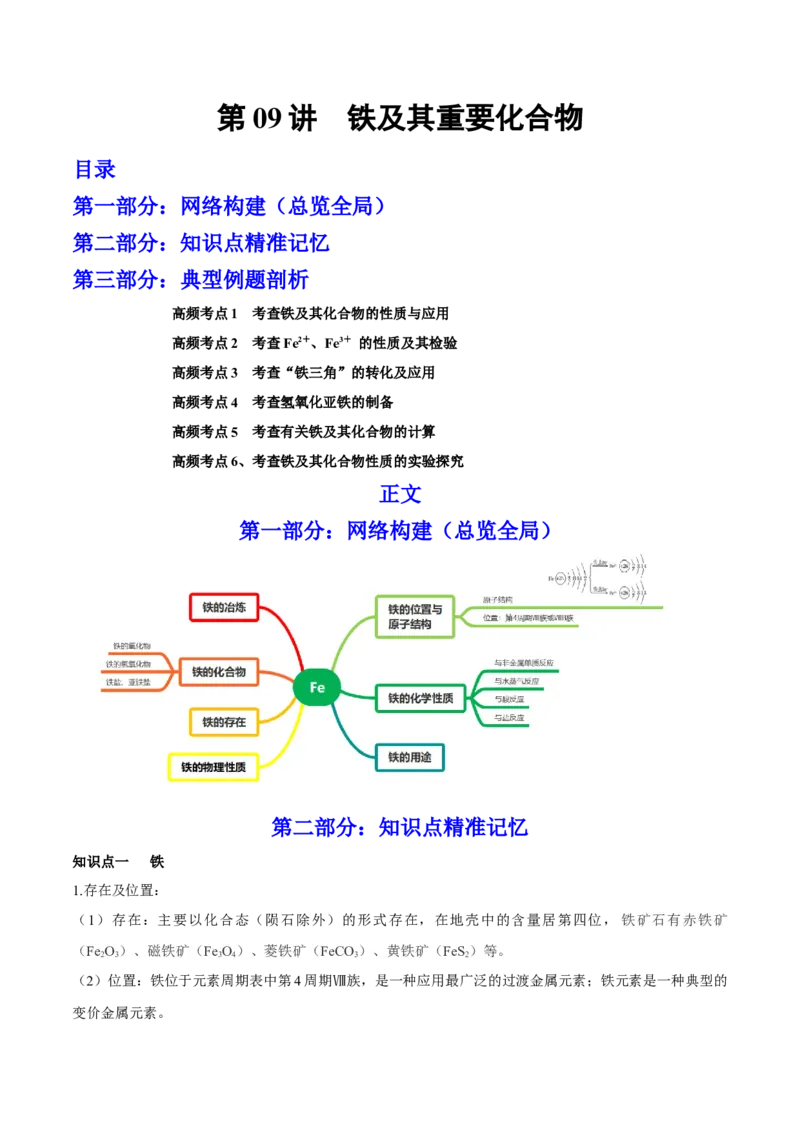
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 铁
1.存在及位置:
(1)存在:主要以化合态(陨石除外)的形式存在,在地壳中的含量居第四位,铁矿石有赤铁矿
(Fe O)、磁铁矿(Fe O)、菱铁矿(FeCO)、黄铁矿(FeS)等。
2 3 3 4 3 2
(2)位置:铁位于元素周期表中第4周期Ⅷ族,是一种应用最广泛的过渡金属元素;铁元素是一种典型的
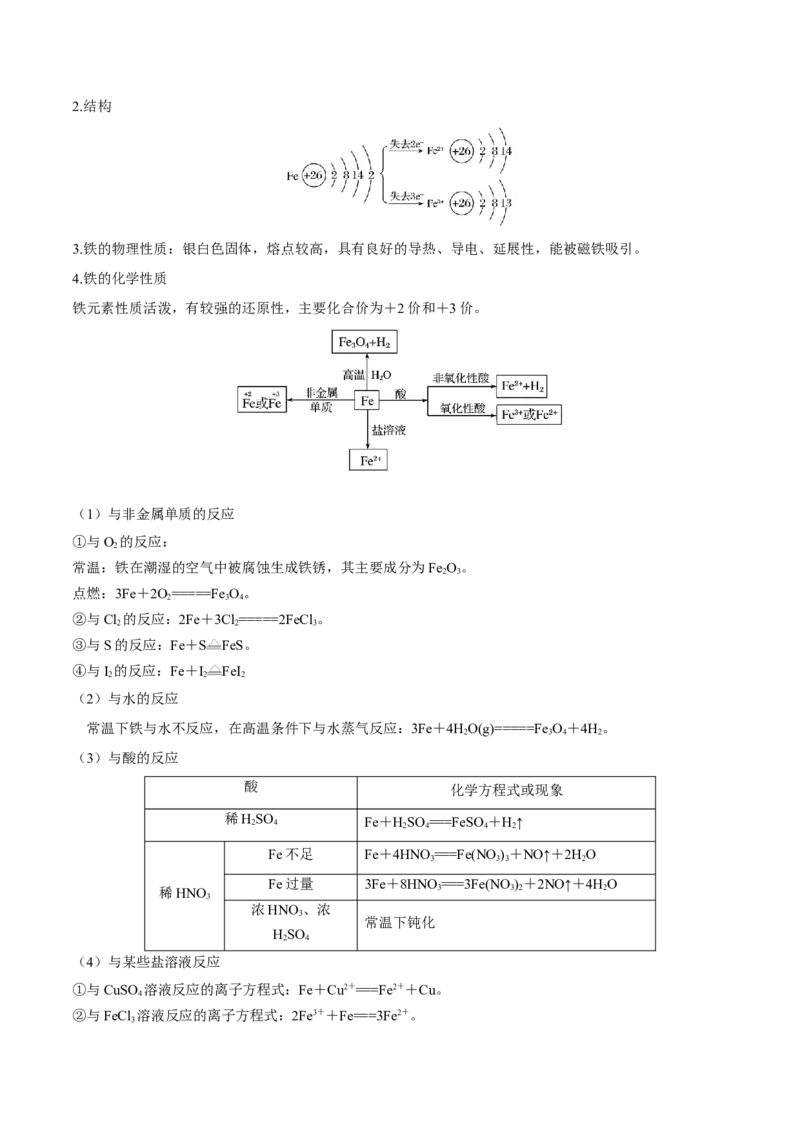
变价金属元素。2.结构
3.铁的物理性质:银白色固体,熔点较高,具有良好的导热、导电、延展性,能被磁铁吸引。
4.铁的化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
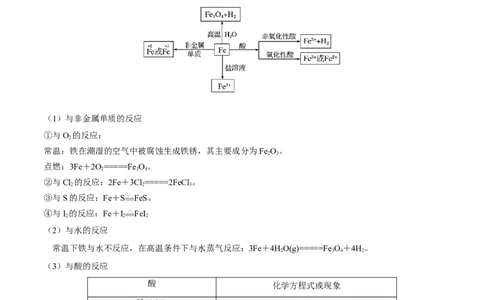
(1)与非金属单质的反应
①与O 的反应:
2
常温:铁在潮湿的空气中被腐蚀生成铁锈,其主要成分为Fe O。
2 3
点燃:3Fe+2O=====Fe O。
2 3 4
②与Cl 的反应:2Fe+3Cl=====2FeCl 。
2 2 3
③与S的反应:Fe+S FeS。
④与I 的反应:Fe+I FeI
2 2 2
(2)与水的反应
常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+4HO(g)=====Fe O+4H。
2 3 4 2
(3)与酸的反应
酸 化学方程式或现象
稀H 2 SO 4 Fe+H 2 SO 4 ===FeSO 4 +H 2 ↑
Fe不足 Fe+4HNO===Fe(NO)+NO↑+2HO
3 3 3 2
Fe过量 3Fe+8HNO===3Fe(NO)+2NO↑+4HO
稀HNO 3 3 2 2
3
浓HNO、浓
3
常温下钝化
HSO
2 4
(4)与某些盐溶液反应
①与CuSO 溶液反应的离子方程式:Fe+Cu2+===Fe2++Cu。
4
②与FeCl 溶液反应的离子方程式:2Fe3++Fe===3Fe2+。
3【易错提醒】①Fe与Cl 反应无论用量多少都生成FeCl ,而Fe与盐酸反应生成FeCl 。
2 3 2
②铁在潮湿的空气中生成的铁锈的主要成分是Fe O,而铁在纯氧中燃烧的产物是Fe O。
2 3 3 4
③铁与一般氧化剂(如S、HCl、FeCl 、CuSO 、I 等)反应时被氧化为Fe2+,铁与强氧化剂(如Cl 、Br 、
3 4 2 2 2
HNO、浓HSO 等)反应时被氧化为Fe3+。
3 2 4
④在电化学中铁作负极时电极反应式为Fe-2e-=Fe2+。
5.铁的冶炼
(1)原料:铁矿石、焦炭、空气、石灰石。
(2)设备:高炉。
(3)主要反应:
①还原剂的生成:C+O=====CO,CO+C=====2CO;
2 2 2
②铁的生成:Fe O+3CO=====2Fe+3CO。
2 3 2
知识点二 铁的重要化合物
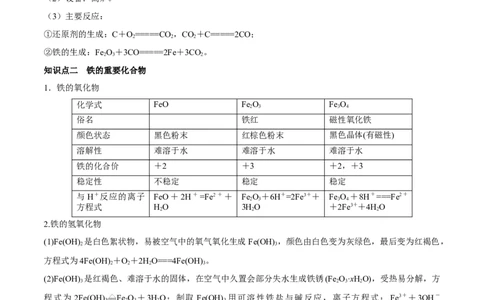
1.铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4
俗名 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 +2 +3 +2,+3
稳定性 不稳定 稳定 稳定
与H+反应的离子 FeO+2H+=Fe2++ Fe O +6H+=2Fe3++ Fe O +8H+===Fe2+
2 3 3 4
方程式 HO 3HO +2Fe3++4HO
2 2 2
2.铁的氢氧化物
(1)Fe(OH) 是白色絮状物,易被空气中的氧气氧化生成Fe(OH) ,颜色由白色变为灰绿色,最后变为红褐色,
2 3
方程式为4Fe(OH) +O+2HO===4Fe(OH) 。
2 2 2 3
(2)Fe(OH) 是红褐色、难溶于水的固体,在空气中久置会部分失水生成铁锈(Fe O·xHO),受热易分解,方
3 2 3 2
程式为 2Fe(OH) Fe O +3HO;制取 Fe(OH) 用可溶性铁盐与碱反应,离子方程式:Fe3++3OH-
3 2 3 2 3
===Fe(OH) ↓。
3
(3)二者之间的关系:在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是白色絮状沉淀迅速
2 3
变成灰绿色,最后变成红褐色,化学方程式为4Fe(OH) +O+2HO===4Fe(OH) 。
2 2 2 3
【易错提醒】①Fe(OH) 与硝酸反应不是发生中和反应生成盐和水,而是发生氧化还原反应3Fe(OH) +
2 2
10HNO=3Fe(NO)+NO↑+8HO。
3 3 3 2
②Fe(OH) 与氢碘酸(HI)反应不是发生中和反应生成盐和水,而是发生氧化还原反应2Fe(OH) +6HI=2FeI
3 3 2
+I+6HO。
2 2(2)制法
①可溶性亚铁盐与强碱或氨水反应:Fe2++2OH-===Fe(OH) ↓或Fe2++2NH ·HO===Fe(OH) ↓+2NH+。
2 3 2 2 4
注意:空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,防止Fe(OH) 氧化的方法:
2 3 2
A.将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
B.将盛有NaOH溶液的胶头滴管尖端插入盛有亚铁盐溶液的试管底部,并慢慢挤出NaOH溶液。
C.在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2
D.在亚铁盐溶液上面加保护层,如苯、植物油等。
E.常见的制备Fe(OH) 的装置:
2
说明:①②原理一样,都是先用氢气将装置中的空气排尽,并使生成的 Fe(OH) 处在氢气的保护中;③中
2
液面加苯阻止了空气进入;④中阳极为铁,阴极为石墨,利用电解实验可以制得纯净的Fe(OH) 白色沉淀。
2
②可溶性铁盐与强碱或氨水反应:Fe3++3OH-===Fe(OH) ↓或Fe3++3NH ·HO===Fe(OH) ↓+3NH+。
3 3 2 3 4
3.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,如:
遇Br 、Cl、HO、NO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++HO+2H+===2Fe3++2HO。
2 2 2 2 2
(2)可水解
Fe(OH) 是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。配制硫酸亚铁溶液时常加少量硫酸抑制Fe2+的水解,
2
加少量铁屑防止Fe2+被氧化。
4.铁盐的性质及应用
(1)氧化性:含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS、SO等均表现为氧化
2
性。
①Fe3+与S2-、I-、HS-、SO等具有较强还原性的离子不能大量共存。
②Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为2Fe3++Cu===Cu2++2Fe2+。
(2)易水解:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强的溶液中。
3
①利用Fe3+易水解的性质,实验室可用FeCl 滴入沸水中制取氢氧化铁胶体,反应的化学方程式:FeCl +
3 33HO Fe(OH) (胶体)+3HCl。
2 3
②利用Fe3+易水解的性质,工业上常用调节pH方法除去溶液中的铁离子。
③利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释
至所需浓度。
④Fe3+与HCO、[Al(OH) ]-、CO、ClO-等水解呈碱性的离子不能大量共存。
4
知识点三 Fe2+和Fe3+的检验
1.亚铁盐
(1)Fe2+的氧化性和还原性
①含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,如
遇Br 、Cl、HO、NO(H+)、MnO(H+)等均表现为还原性。
2 2 2 2
②Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++2H++HO===2Fe3++2HO
2 2 2 2 2
③向FeSO 溶液中滴加酸性KMnO 溶液,溶液褪色。反应的离子方程式:MnO+5Fe2++8H+===5Fe3++
4 4
Mn2++4HO。
2
(2)可水解
Fe2+的盐(如硫酸亚铁)溶液因水解呈酸性。
2.铁盐
(1)氧化性:含有Fe3+的溶液呈黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化性。
2
①Fe3+与Cu反应的离子方程式:2Fe3++Cu===Cu2++2Fe2+。
②Fe3+与I-反应的离子方程式:2Fe3++2I-===2Fe2++I。
2
(2)特性:含有Fe3+的盐溶液遇到KSCN时变成血红色。
(3)易水解:Fe3+极易水解,只能存在于酸性较强的溶液中。
3.Fe2+、Fe3+的检验方法
(1)Fe2+的检验
方法1 ―――――――→无现象―――――――→溶液变红色,证明含有Fe2+
――――――――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证明含
方法2
有Fe2+
方法3 ―――――――――→生成蓝色沉淀,证明含有Fe2+
(2)Fe3+的检验
方法1 ――――――――→溶液变红色,证明含有Fe3+
方法2 ―――――――→产生红褐色沉淀,证明含有Fe3+
方法3 ―――――――――→生成蓝色沉淀,证明含有Fe3+
(3)混合溶液中Fe3+、Fe2+的检验
①Fe3+的检验a.――→溶液变血红色,说明含有Fe3+
b.――→试纸变蓝色,说明含有Fe3+
②Fe2+的检验
a.――→KMnO 溶液褪色,说明含有Fe2+
4
b.――→溴水褪色,说明含有Fe2+
c.――→生成蓝色沉淀,说明含有Fe2+
【易错提醒】检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入足量的新制氯水中(新
制氯水能氧化SCN-),检验Fe2+最好用K[Fe(CN) ]溶液。
3 6
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,有干扰)。
4 4
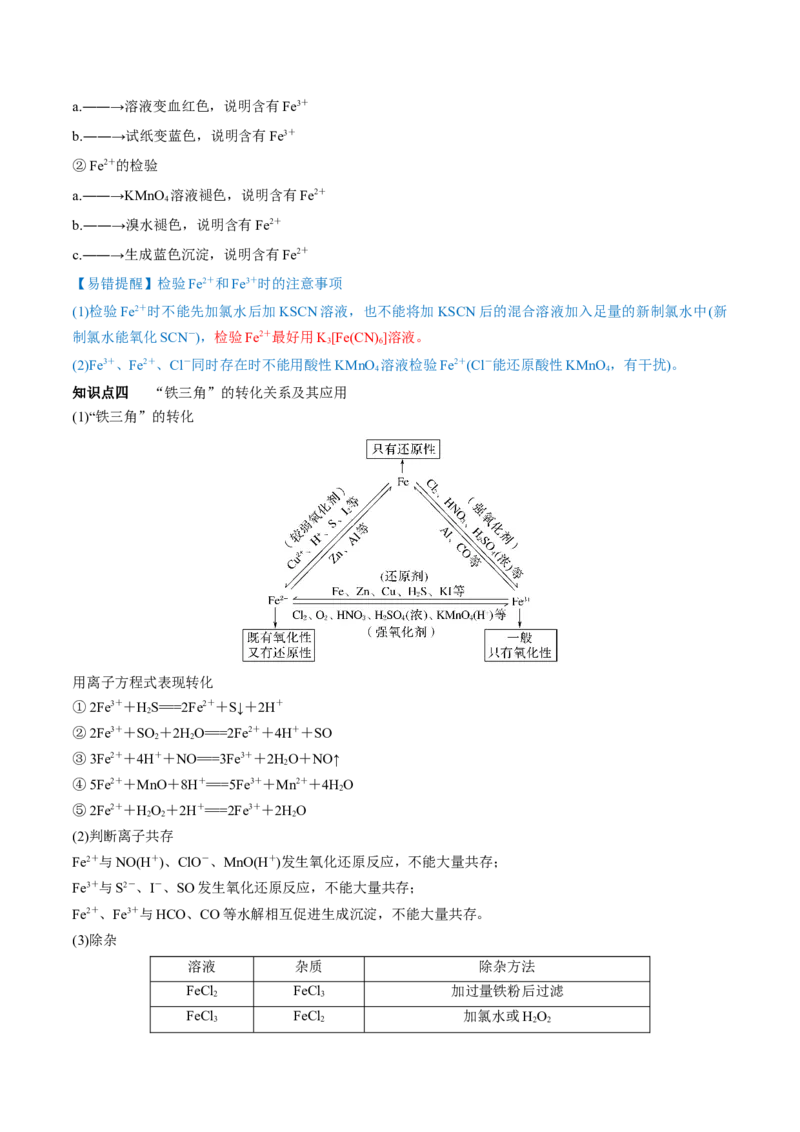
知识点四 “铁三角”的转化关系及其应用
(1)“铁三角”的转化
用离子方程式表现转化
①2Fe3++HS===2Fe2++S↓+2H+
2
②2Fe3++SO +2HO===2Fe2++4H++SO
2 2
③3Fe2++4H++NO===3Fe3++2HO+NO↑
2
④5Fe2++MnO+8H+===5Fe3++Mn2++4HO
2
⑤2Fe2++HO+2H+===2Fe3++2HO
2 2 2
(2)判断离子共存
Fe2+与NO(H+)、ClO-、MnO(H+)发生氧化还原反应,不能大量共存;
Fe3+与S2-、I-、SO发生氧化还原反应,不能大量共存;
Fe2+、Fe3+与HCO、CO等水解相互促进生成沉淀,不能大量共存。
(3)除杂
溶液 杂质 除杂方法
FeCl FeCl 加过量铁粉后过滤
2 3
FeCl FeCl 加氯水或HO
3 2 2 2FeCl CuCl 加过量铁粉后过滤
2 2
(4)盐溶液的配制与保存
(5)物质的制备
(6)铁及其化合物的转化关系——铁的价类二维图
说明:1)横向变化体现了同价态不同物质类别(氧化物、盐、碱)之间的转化;①碱性氧化物(Fe O 、FeO)都
2 3
能溶于酸(H+)转化为盐;②Fe2+、Fe3+与碱(OH-)反应生成对应的碱;③难溶性的碱易分解生成对应的氧
化物,但难溶性的碱性氧化物一般不与水反应生成对应的碱。
2)纵向变化体现不同价态同物质类别之间的转化,主要体现物质的氧化性或还原性。
3)斜向变化体现不同价态、不同物质类别之间的转化,主要体现物质的氧化性和还原性。
第三部分:典型例题剖析
高频考点1 考查铁及其化合物的性质与应用
例1.(2022·江苏省平潮高级中学模拟预测)下列有关铁及其化合物的性质与用途具有对应关系的是
A.铁粉具有还原性,可用作食品保存的抗氧化剂
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C.FeCl 溶液呈酸性,可用于腐蚀印刷电路板上的Cu
3
D.聚合硫酸铁能水解并形成胶体,可用于自来水的消毒
【解析】A.铁粉具有还原性,能消耗食品包装袋内的氧气,可用作食品保存的抗氧化剂,故选A;B.
Fe O 具有磁性,所以纳米Fe O 可用作铁磁性材料,与Fe O 能与酸反应无关,故不选B;C.FeCl 溶液
3 4 3 4 3 4 3
可用于腐蚀印刷电路板上的Cu,是因为Fe3+能把Cu氧化为Cu2+,故不选C;D.聚合硫酸铁能水解并形成
胶体,可用于净水,不能消毒,故不选D;选A。
【答案】A【名师点睛】本题考查氧化还原反应以及铁的单质化合物的性质,题目难度不大,本题关键是把握物质的
氧化性、还原性强弱判断反应的先后顺序。
【变式训练】(2022·江苏·模拟预测)下列关于铁及其化合物的性质与用途,不具有对应关系的是
A.Fe具有还原性,可用作食品抗氧化剂
B. 属于碱性氧化物,可用作粉刷墙壁的红色涂料
C. 具有磁性,可用作激光打印机墨粉的添加剂
D. 胶体具有吸附性,可用作自来水厂的净水剂
【解析】A.Fe具有还原性,能消耗氧气,可用作食品抗氧化剂,A不符合题意;B.Fe O 固体为红棕色,
2 3
可用作粉刷墙的红色涂料,其为碱性氧化物与作红色涂料无关,B符合题意;C.Fe O 具有磁性,可用作
3 4
激光打印机墨粉的添加剂,使墨粉具有磁性,C不符合题意;D.Fe(OH) 胶体具有吸附性,可吸附水中
3
的悬浮杂质,可用作自来水厂的净水剂 ,D不符合题意;故选B。
【答案】B
高频考点2 考查Fe2+、Fe3+ 的性质及其检验
例2.(2021·上海静安区·高三一模)欲证明某稀溶液中含有Fe2+而无Fe3+,必要的实验操作及最佳顺序为
①滴加少量氯水②滴加足量碘水③滴加少量硫氰化钾溶液
A.①→③ B.③→② C.③→① D.①→②→③
【解析】Fe3+遇硫氰化钾溶液会变红色,欲证明某稀溶液中含有Fe2+而无Fe3+,可先滴加少量硫氰化钾溶液,
同时,Fe2+易被氧化为Fe3+,氧化剂可以为:氯水,而碘水不能氧化Fe2+,故最佳顺序为③→①,答案选
C。
【答案】C
【易错警示】检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液;也不能将加KSCN后的混合溶液加入足量的新制氯水中(新
制氯水可能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,有干扰)。
4 4
【变式训练】(2021·上海奉贤区·高三二模)要证明某久置的 溶液中是否还含有 ,以下最适合
的试剂是
A.KSCN溶液 B. 溶液 C.酸性 溶液D. 溶液
【解析】A.三价铁离子遇到溶液或是KSCN溶液显红色,常用溶液或是KSCN溶液来检验三价铁离子,无法检验Fe2+,故A错误;B.加入氯化钡,都生成白色沉淀,不能证明含有亚铁离子,故B错误;C.加
入酸性溶液,可氧化亚铁离子,能证明含有亚铁离子,故C正确;D.加入KI,Fe3+与I-反应,Fe2+与I-不
反应,不能证明含有亚铁离子,故D错误;故选C。
【答案】C
高频考点3 考查“铁三角”的转化及应用
例3.(2022·江苏·模拟预测)铁元素是重要的金属元素,含有铁元素的物质,在人类的生产生活中有着重
要的应用。 是炼铁工业中的主反应。在指定条件下,下
列选项所示的物质间转化能实现的是
A.
B. (胶体)
C.
D.
【解析】A.KClO具有强氧化性,能将氢氧化铁氧化为高铁酸根,A正确;B.饱和氯化铁溶液滴入沸水
中制备氢氧化铁胶体,B错误;C.铜的还原性比铁弱,不能将亚铁离子还原为铁单质,C错误;D.氧化
铁与稀硫酸反应生成硫酸铁,铁的化合价为+3价,D错误;故选A。
【答案】A
【题后归纳】价类二维图在铁及其化合物转化中的应用
(1)横向变化体现了同价态不同类别(氧化物、碱、盐)之间的转化;
(2)纵向变化体现不同价态同类别物质之间的转化,主要体现物质的氧化性或还原性。
(3)斜向变化体现不同价态、不同类别之间物质的转化,主要体现物质的氧化物和还原性。
【变式训练】 (2020·青铜峡市高级中学月考)下列有关铁及其化合物的说法中不正确的是( )A.为了防止氯化亚铁溶液久置变质,常在其溶液中加入少许铁钉
B.将饱和FeCl 溶液滴入沸水中,能形成胶体
3
C.新制的氢氧化亚铁沉淀露置在空气中最终会变为红褐色
D.除去FeCl 溶液中的FeCl 杂质可以向溶液中加铁粉,然后过滤
3 2
【解析】亚铁离子在空气中易被氧化为铁离子,加铁钉可以防止氯化亚铁溶液的变质,故 A正确;制备氢
氧化铁胶体的方法是将饱和FeCl 溶液滴入沸水中,产生红褐色即可,故B正确;新制的氢氧化亚铁沉淀
3
露置在空气中迅速变成灰绿色,最终会变为红褐色的氢氧化铁,故C正确;除去FeCl 溶液中的FeCl 杂质
3 2
可以向溶液中滴加氯水,将氯化亚铁氧化为氯化铁,故D错误。
【答案】D
高频考点4 考查氢氧化亚铁的制备
例4.(2021·山东·高三专题练习)Fe(OH) 的制备实验是实验研究的热点,某化学学习小组设计了下列方法
2
制备氢氧化亚铁。
方法:用铁和石墨作电极材料,通过电解法制备氢氧化亚铁,装置如图所示。
(1)铁与电源的___________(填“正”或“负”)极相连。
(2)阴极发生的电极反应方程式___________。
(3)在标准状况下,当阴极产生 11.2L 气体时,理论上生成___________g Fe(OH)
2
【解析】(1)根据电解原理,活动性金属作阳极,活动性金属先失电子,即铁作阳极,与电源的正极相连;
故答案为:正;
(2)阴极上得电子,化合价降低,根据阳离子放电顺序水电离出H+先放电,即电极反应式为2HO+2e-
2
=H ↑+2OH-;故答案为2HO+2e-=H ↑+2OH-;
2 2 2
(3)根据转移电子守恒,建立关系式为H~2e-~Fe2+~Fe(OH) ,因此m[Fe(OH) ]=
2 2 2
45g;故答案为:45g。
【答案】(1)正极 (2)2H O+2e-=H ↑+2OH- (3)45
2 2
【反思归纳】防止Fe(OH) 氧化的方法
2
(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
(2)将盛有NaOH溶液的胶头滴管尖端插入盛有亚铁盐溶液的试管底部,并慢慢挤出NaOH溶液。
(3)在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2(4)在亚铁盐溶液上面加保护层,如苯、植物油等。
【变式训练】下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2
A.①②③④ B.①②③⑤ C.①③④⑤ D.②③④⑤
【解析】①铁与稀硫酸反应产生H ,排出了装置中的空气,烧杯中的水,隔绝空气中的氧气进入试管中,
2
然后滴加NaOH溶液,生成的Fe(OH) 能长时间存在,故①符合题意;②首先打开止水夹a,铁粉与稀硫酸
2
反应生成H ,排出装置中的空气,以及NaOH溶液中的氧气,让装置处于H 氛围中,关闭止水夹,利用
2 2
压强,将FeSO 压入NaOH溶液中,生成氢氧化亚铁,Fe(OH) 能长时间观察,故②符合题意;③该装置为
4 2
电解装置,铁作阳极,电极反应式为Fe-2e-===Fe2+,C为阴极,电极反应式为O +4e-+2HO===4OH-
2 2
汽油隔绝空气中氧气的进入,能长时间观察到氢氧化亚铁,故③符合题意;④该装置,没有隔绝空气的进
入,生成氢氧化亚铁迅速转化成氢氧化铁,不能长时间观察到氢氧化亚铁,故④不符合题意;⑤苯能隔绝
空气的进入,能够长时间观察到氢氧化亚铁白色沉淀,故⑤符合题意;综上所述,选项B正确。
【答案】B
高频考点5 考查有关铁及其化合物的计算
例5.(2022·湖南·长沙一中一模)将铁、氧化铁、氧化铜组成的混合物粉末mg放入盛 盐
酸的烧杯中,充分反应后产生2.24L H (标准状况),残留固体2.56g。过滤,滤液中无Cu2+。将滤液加水稀
2
释到500mL,测得其中c(H+)为 。下列说法正确的是
A.m=15.36
B.烧杯中转移电子的物质的量共为0.28mol
C.若将反应后的溶液倒入蒸发皿中直接蒸干可得到0.2mol FeCl
2
D.过滤时需要用到的玻璃仪器有烧杯、玻璃棒、漏斗、锥形瓶
【解析】既然还有较多H+离子剩余,且滤液中没有Cu2+可知残留物没有Fe,只有Cu,则反应后溶质为
HCl和FeCl ,根据Cl元素守恒可知:n(HCl)=2n(FeCl )+n剩余(H+),即5.00mol/
2 2
L×0.1L=2n(FeCl )+0.200mol/L×0.5L解得:n(FeCl )=0.2mol;2.56g Cu的物质的量为0.04mol,则与Cu2+参加
2 2反应的Fe的物质的量为0.04mol;标况下2.24L H 的物质的量为0.1mol,则H+参加反应的Fe的物质的量
2
为0.1mol;根据Fe2+守恒,可有与Fe3+反应的Fe的物质的量为0.2-0.1-0.04=0.06mol;因此原混合物中
n(Fe)=0.04+0.02+0.1=0.16mol,n(Fe O)=0.02mol,n(CuO)=0.04mol;据此分析解题。
2 3
A.据分析可知混合物的质量为:0.16mol×56g/mol+0.02mol×160g/mol+0.04mol×80g/mol=15.36g,A正确;
B.根据原混合物组成的各组分的物质的量可知,烧杯中转移电子的物质的量共为
(0.1mol+0.04mol+0.02mol)×2=0.32mol,B错误;C.由于氯化亚铁易水解易氧化,将反应后的溶液蒸干后
得到氢氧化铁,C错误;D.过滤时需要用到的玻璃仪器有烧杯、玻璃棒、漏斗,不需要锥形瓶,D错误;
答案选A。
【答案】A
【变式训练】铁的常见化合价有+2价和+3价。据研究,铁在浓HNO 中发生钝化时,可生成一种化学式
3
为Fe O 的化合物,它可以看作由FeO和Fe O 组成的复杂氧化物。该化合物可以表示为( )
8 11 2 3
A.FeO·3Fe O B.FeO·2Fe O
2 3 2 3
C.2FeO·3Fe O D.2FeO·Fe O
2 3 2 3
【解析】一般拆写成氧化物时,低价在前,高价在后,同时符合原子守恒; FeO·3Fe O 中铁原子和氧原
2 3
子个数比为7∶10,不符合8∶11,故A不符合题意; FeO·2Fe O 中铁原子和氧原子个数比为5∶7,不符
2 3
合8∶11,故B不符合题意; 2FeO·3Fe O 中铁原子和氧原子个数比为8∶11,符合8∶11,故C符合题意;
2 3
2FeO·Fe O 中铁原子和氧原子个数比为4∶5,不符合8∶11,故D不符合题意。
2 3
【答案】C
【方法归纳】确定铁的氧化物组成的基本方法
设铁的氧化物中铁元素与氧元素的质量比为m∶n,
则氧化物中n(Fe)∶n(O)=∶=a∶b,
若a∶b=1∶1,则铁的氧化物为FeO;
若a∶b=2∶3,则铁的氧化物为Fe O;
2 3
若a∶b=3∶4,则铁的氧化物是Fe O 或FeO与Fe O 按物质的量之比为1∶1的混合物或FeO、Fe O 、
3 4 2 3 2 3
Fe O 的混合物(其中FeO、Fe O 物质的量之比为1∶1,Fe O 为任意值)。
3 4 2 3 3 4
高频考点6、考查铁及其化合物性质的实验探究
例6.(2022·北京·和平街第一中学三模)某同学利用下列电池装置进行实验,探究 的氧化性和还原性。根据实验现象,下列分析不正确的是
A.电流表显示电子由铁电极流向石墨电极,可知盐桥中的阳离子进入石墨电极溶液中
B.一段时间后石墨电极上未见 析出且铁电极溶液中 增大,可知石墨电极溶液中 也增大
C.由A、B中的现象可知, 还原性小于 、氧化性小于
D.一段时间后两极溶液中的 浓度若相等,说明反应已达到平衡状态
【解析】该反应为Fe+2Fe3+=3Fe2+,负极为铁单质失电子生成亚铁离子,正极为铁离子得电子生成亚铁离
子。A.铁电极失电子为负极,石墨电极为正极,阳离子从负极向正极移动,故盐桥中阳离子进入石墨电
极溶液中,A正确;B.石墨电极上发生的反应为Fe3++e-=Fe2+,反应生成亚铁离子,负极的亚铁离子也会
向正极移动,故石墨电极溶液中亚铁离子浓度增大,B正确;C.负极反应为Fe-2e-=Fe2+,正极反应为
2Fe3++2e-=2Fe2+,总反应为Fe+2Fe3+=3Fe2+,反应中氧化剂为Fe3+,还原剂为Fe,Fe2+既是氧化产物也是还
原产物,故Fe2+还原性小于Fe,氧化性小于Fe3+,C正确;D.一段时间后两极溶液中亚铁离子浓度相等,
无法说明反应达到平衡状态,D错误;故答案选D。
【答案】D
【名师点睛】性质探究性实验方案的设计:主要是从物质的结构特点或从所属类型的典型代表物去推测物
质可能具有的一系列性质,而后据此设计出合理的实验方案,去探索它所可能具有的性质。设计的基本流
程为:根据物质的组成、结构和类型→提出性质猜想→设计实验逐个验证→记录现象和数据→归纳分析→
合理推断得出结论。
【变式训练】(2022·山东·模拟预测)手持技术(Hand-held Technology)是由计算机和微电子技术相结合的
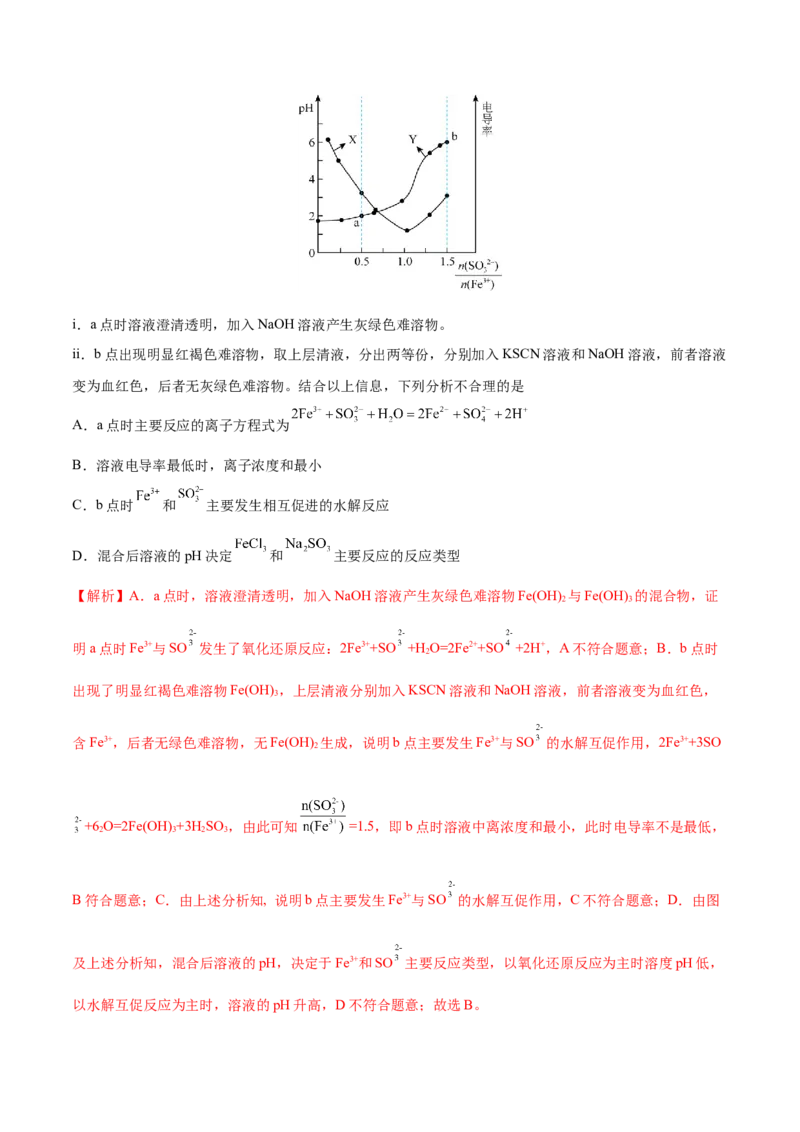
新型数字化实验手段。向 溶液中加入 溶液,控制不同 时,利用手持技术测量其与溶
液pH和电导率的关系如图所示:i.a点时溶液澄清透明,加入NaOH溶液产生灰绿色难溶物。
ii.b点出现明显红褐色难溶物,取上层清液,分出两等份,分别加入KSCN溶液和NaOH溶液,前者溶液
变为血红色,后者无灰绿色难溶物。结合以上信息,下列分析不合理的是
A.a点时主要反应的离子方程式为
B.溶液电导率最低时,离子浓度和最小
C.b点时 和 主要发生相互促进的水解反应
D.混合后溶液的pH决定 和 主要反应的反应类型
【解析】A.a点时,溶液澄清透明,加入NaOH溶液产生灰绿色难溶物Fe(OH) 与Fe(OH) 的混合物,证
2 3
明a点时Fe3+与SO 发生了氧化还原反应:2Fe3++SO +H O=2Fe2++SO +2H+,A不符合题意;B.b点时
2
出现了明显红褐色难溶物Fe(OH) ,上层清液分别加入KSCN溶液和NaOH溶液,前者溶液变为血红色,
3
含Fe3+,后者无绿色难溶物,无Fe(OH) 生成,说明b点主要发生Fe3+与SO 的水解互促作用,2Fe3++3SO
2
+6O=2Fe(OH) +3H SO ,由此可知 =1.5,即b点时溶液中离浓度和最小,此时电导率不是最低,
2 3 2 3
B符合题意;C.由上述分析知, 说明b点主要发生Fe3+与SO 的水解互促作用,C不符合题意;D.由图
及上述分析知,混合后溶液的pH,决定于Fe3+和SO 主要反应类型,以氧化还原反应为主时溶度pH低,
以水解互促反应为主时,溶液的pH升高,D不符合题意;故选B。【答案】B