文档内容
第 11 讲 铜 金属矿物的开发利用
目录
考情分析 考向2 考查铜及其化合物的制备
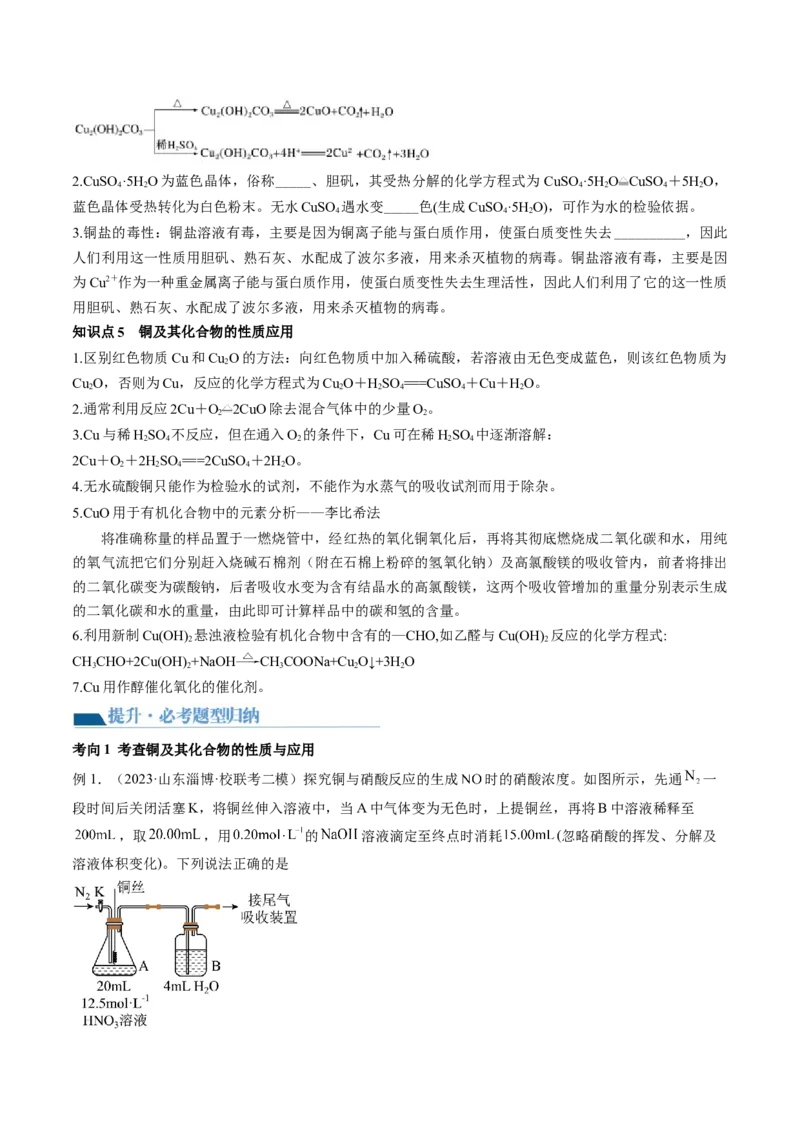
网络构建
考点二 金属矿物的开发利用
考点一 铜及其化合物
【夯基·必备基础知识梳理】
【夯基·必备基础知识梳理】
知识点1 金属材料
知识点1 铜的性质
知识点2 金属冶炼
知识点2 氧化铜和氧化亚铜
【提升·必考题型归纳】
知识点3 氢氧化铜
考向1 合金性质与金属材料的应用
知识点4 铜盐
考向2 金属矿物的开发利用
知识点5 铜及其化合物的性质应用
【提升·必考题型归纳】
真题感悟
考向1 考查铜及其化合物的性质与应用
考点要求 考题统计 考情分析
从近三年高考试题来看,铜及其化合物的性质与应用
2023湖北卷18题,14分 和合金的组成、性质和应用仍是高考的命题点;只有
铜及其化合物的性
2022山东卷12题,4分 浙江卷考查了金属矿物的开发利用。考查内容以金属
质与应用
及其化合物的性质、合金的性质、金属的冶炼、提纯
2021湖北卷2题,3分
以及在日常生活、生产中的应用为主。题型以选择题
和化工流程题为主。预测新的一年高考可能会可能会
金属矿物的开发利
2023湖南卷1题,3分 在选择题中考查合金的性质和应用及金属矿物的开发
用 2022广东卷1题,2分 利用,题目难度较小;在工艺流程图题中考查铜及其
2021河北卷1题,3分
化合物的转化与应用,题目综合性较强,难度较大。考点一 铜及其化合物
知识点1 铜的性质
1.存在及位置:
(1)存在:在自然界中铜大多数主要以硫化铜存在,主要是辉铜矿(Cu S)、黄铜矿(CuFeS )和斑铜
2 2
矿(Cu FeS)。铜还以游离态的形式存在自然铜是一种含铜矿石,成分是铜单质。
5 4
(2)位置:铜位于元素周期表中第_____周期_____族,是人类最早使用的金属之一;铜元素是一种的变
价金属元素(+1、+2)。
2.结构
铜(Cuprum)是一种金属元素,也是一种过渡元素,化学符号Cu,英文copper,原子序数29,原子结构
示意图为:
3.物理性质:_____色固体,具有良好的延展性、导热性和导电性。
4.化学性质
①生成铜绿的化学方程式:2Cu+O+CO+HO===Cu (OH) CO(_____色固体)。
2 2 2 2 2 3
②Cu和S反应的化学方程式:2Cu+S=====Cu S。
2
③与浓硫酸共热的化学方程式:Cu+2HSO (浓)=====CuSO +SO ↑+2HO。
2 4 4 2 2
④与稀硝酸反应的离子方程式:3Cu+8H++2NO===3Cu2++2NO↑+4HO。
2
⑤与浓硝酸反应的离子方程式:Cu+4H++2NO===Cu2++2NO ↑+2HO。
2 2
⑥与FeCl 溶液反应的离子方程式:Cu+2Fe3+===2Fe2++Cu2+。
3
5.铜的冶炼
(1)湿法炼铜:Fe+CuSO ===FeSO+Cu。
4 4(2)高温炼铜:工业上用高温冶炼黄铜矿的方法获得铜(粗铜):
2CuFeS+4O=====Cu S+3SO +2FeO(炉渣)
2 2 2 2
2Cu S+3O======2Cu O+2SO
2 2 2 2
2Cu O+Cu S======6Cu+SO ↑
2 2 2
(3)电解精炼铜:
粗铜中铜的含量为99.5%~99.7%,主要含有Ag、Zn、Fe、Au等杂质,粗铜通过电解精炼可得到纯
度达99.95%~99.98%的铜。电解精炼铜的原理是用_____作阳极,铜在阳极上失电子变为_____+,用
_____作阴极,Cu2+在阴极上得电子生成_____。
知识点2 氧化铜和氧化亚铜
1.氧化铜
(1)物理性质:_____色_____溶于水的固体。
(2)化学性质:与酸反应, 可以用H、CO、Al还原出Cu。
2
①与酸反应(H+):CuO+2H+===Cu2++HO
2
②与H 反应:H+CuO __________;
2 2
③与CO反应:CO+CuO __________
2.氧化亚铜
(1)物理性质:_____色_____溶于水的固体。
(2)化学性质:
①与酸反应(H+)为Cu O+2H+===Cu+Cu2++HO 。
2 2
②Cu O遇到HNO 发生氧化反应生成Cu2+。
2 3
③与H 反应: Cu O+H=====2Cu+HO。
2 2 2 2
④CuO加强热的反应:4CuO=====2Cu O+O↑。
2 2
知识点3 氢氧化铜
1.物理性质:蓝色不溶于水的固体。
2.化学性质及应用:
反应①的化学方程式:Cu(OH) CuO+HO;
2 2
反应②的离子方程式:Cu(OH) +2H+===Cu2++2HO。
2 2
反应③的化学方程式:RCHO + 2Cu(OH) +NaOH RCOONa + Cu O↓ + 3HO
2 2 2
知识点4 铜盐
1.Cu (OH) CO 的名称为碱式碳酸铜,是铜绿的成分,是铜在潮湿的空气中被_____的结果,其受热分解的
2 2 3
化学方程式为Cu (OH) CO 2CuO+HO+CO↑。
2 2 3 2 22.CuSO ·5H O为蓝色晶体,俗称_____、胆矾,其受热分解的化学方程式为 CuSO ·5H O CuSO +5HO,
4 2 4 2 4 2
蓝色晶体受热转化为白色粉末。无水CuSO 遇水变_____色(生成CuSO ·5H O),可作为水的检验依据。
4 4 2
3.铜盐的毒性:铜盐溶液有毒,主要是因为铜离子能与蛋白质作用,使蛋白质变性失去__________,因此
人们利用这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。铜盐溶液有毒,主要是因
为Cu2+作为一种重金属离子能与蛋白质作用,使蛋白质变性失去生理活性,因此人们利用了它的这一性质
用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。
知识点5 铜及其化合物的性质应用
1.区别红色物质Cu和Cu O的方法:向红色物质中加入稀硫酸,若溶液由无色变成蓝色,则该红色物质为
2
Cu O,否则为Cu,反应的化学方程式为Cu O+HSO ===CuSO+Cu+HO。
2 2 2 4 4 2
2.通常利用反应2Cu+O 2CuO除去混合气体中的少量O。
2 2
3.Cu与稀HSO 不反应,但在通入O 的条件下,Cu可在稀HSO 中逐渐溶解:
2 4 2 2 4
2Cu+O+2HSO ===2CuSO+2HO。
2 2 4 4 2
4.无水硫酸铜只能作为检验水的试剂,不能作为水蒸气的吸收试剂而用于除杂。
5.CuO用于有机化合物中的元素分析——李比希法
将准确称量的样品置于一燃烧管中,经红热的氧化铜氧化后,再将其彻底燃烧成二氧化碳和水,用纯
的氧气流把它们分别赶入烧碱石棉剂(附在石棉上粉碎的氢氧化钠)及高氯酸镁的吸收管内,前者将排出
的二氧化碳变为碳酸钠,后者吸收水变为含有结晶水的高氯酸镁,这两个吸收管增加的重量分别表示生成
的二氧化碳和水的重量,由此即可计算样品中的碳和氢的含量。
6.利用新制Cu(OH) 悬浊液检验有机化合物中含有的—CHO,如乙醛与Cu(OH) 反应的化学方程式:
2 2
CHCHO+2Cu(OH) +NaOH CHCOONa+Cu O↓+3HO
3 2 3 2 2
7.Cu用作醇催化氧化的催化剂。
考向1 考查铜及其化合物的性质与应用
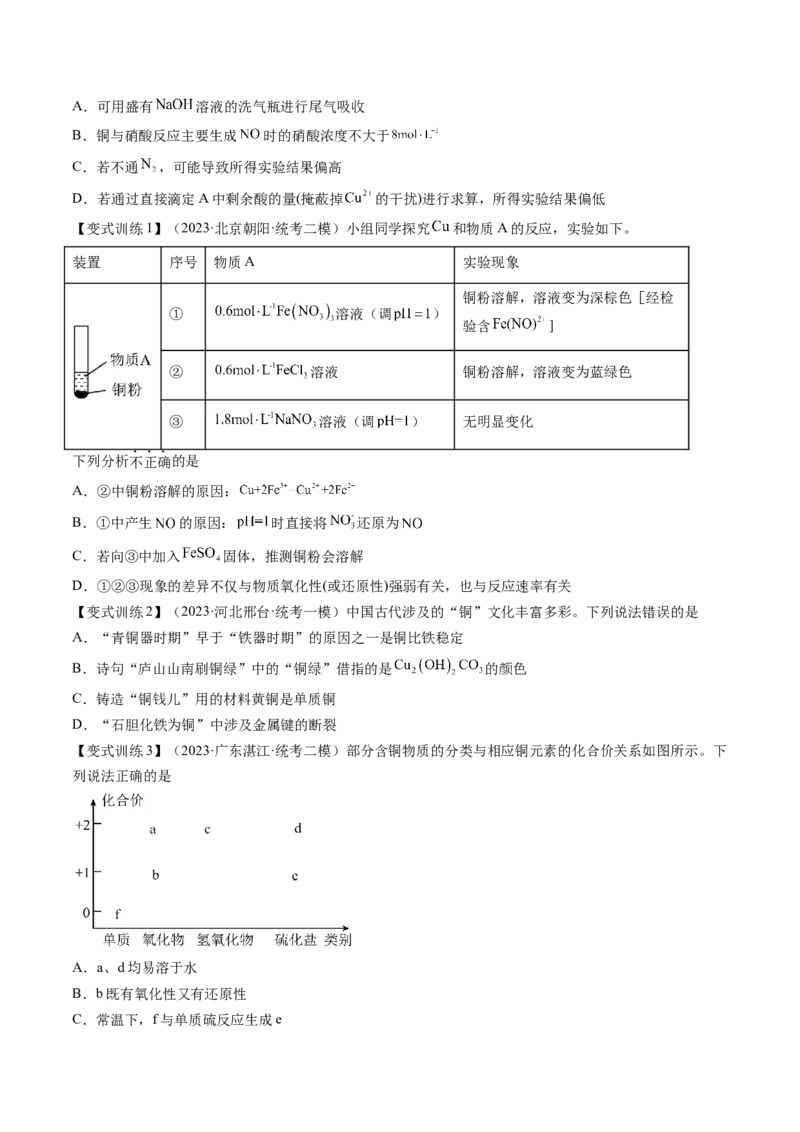
例1.(2023·山东淄博·校联考二模)探究铜与硝酸反应的生成 时的硝酸浓度。如图所示,先通 一
段时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至
,取 ,用 的 溶液滴定至终点时消耗 (忽略硝酸的挥发、分解及
溶液体积变化)。下列说法正确的是A.可用盛有 溶液的洗气瓶进行尾气吸收
B.铜与硝酸反应主要生成 时的硝酸浓度不大于
C.若不通 ,可能导致所得实验结果偏高
D.若通过直接滴定A中剩余酸的量(掩蔽掉 的干扰)进行求算,所得实验结果偏低
【变式训练1】(2023·北京朝阳·统考二模)小组同学探究 和物质A的反应,实验如下。
装置 序号 物质A 实验现象
铜粉溶解,溶液变为深棕色[经检
① 溶液(调 )
验含 ]
② 溶液 铜粉溶解,溶液变为蓝绿色
③ 溶液(调 ) 无明显变化
下列分析不正确的是
A.②中铜粉溶解的原因:
B.①中产生 的原因: 时直接将 还原为
C.若向③中加入 固体,推测铜粉会溶解
D.①②③现象的差异不仅与物质氧化性(或还原性)强弱有关,也与反应速率有关
【变式训练2】(2023·河北邢台·统考一模)中国古代涉及的“铜”文化丰富多彩。下列说法错误的是
A.“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
B.诗句“庐山山南刷铜绿”中的“铜绿”借指的是 的颜色
C.铸造“铜钱儿”用的材料黄铜是单质铜
D.“石胆化铁为铜”中涉及金属键的断裂
【变式训练3】(2023·广东湛江·统考二模)部分含铜物质的分类与相应铜元素的化合价关系如图所示。下
列说法正确的是
A.a、d均易溶于水
B.b既有氧化性又有还原性
C.常温下,f与单质硫反应生成eD.向固体c中通入HS气体生成e
2
考向2 考查铜及其化合物的制备
例2.(2023·山东济宁·统考一模)碱式碳酸铜[Cu (OH) CO]是一种用途广泛的化工原料,实验室中以废
2 2 3
铜屑为原料,制取碱式碳酸铜的流程如下。下列说法错误的是
A.“加热”步骤可选用水浴加热
B.“酸浸”产生的气体可用NaOH溶液吸收
C.“滤液”中溶质的主要成分为
D.可用盐酸和 溶液检验“滤液”中是否有
【变式训练】(2023·福建三明·统考模拟预测)实验室制取NO和 固体,下列装置能达到实验目
的的是
A.用装置甲制取NO气体
B.用装置乙除去NO中少量的
C.用装置丙收集NO气体
D.用装置丁灼烧 得到
考点二 金属矿物的开发利用
知识点1 金属材料
1.合金
(1)概念:合金是指两种或两种以上的__________ (或_______________)熔合而成的具有金属特性的物质。
(2)成分:一种金属为主,另一种或几种是金属或非金属。即合金中一定含金属元素,可能 含非金属元素(如
钢中含碳) 。
(3)性能:合金具有不同于各成分金属的物理、化学性能或机械性能。
①熔点:一般比它的各成分金属的_____;②硬度和强度:一般比它的各成分金属的_____。
【特别提醒】①构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含
金属元素。合金一定是混合物。
②常温下,多数合金是固,但钾、钠合金呈液态。
③合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面不同
于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
(4)新型合金及重要应用
①“蛟龙”号载人潜水器的耐压球壳用钛合金制造,利用了钛合金的硬度大、机械强度高、耐腐蚀等性质。
②喷气式飞机的发动机叶片由镍钴合金制造,利用了其熔点高、耐高温的性质。
2.常见金属材料及应用
(1)金属材料的工业分类
黑色金属材料 有色金属材料
铁、铬、锰以及它们的合金 除黑色金属以外的其他金属及其合金
(2)黑色金属材料——钢铁
①_____是用量最大、用途最广的合金。
②钢
(3)有色金属材料——铜和铝
①铝及铝合金
②铜及铜合金
【特别提醒】合金的组成与性质
(1)构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含金属元素。合
金一定是混合物。
(2)常温下,多数合金是固态,但钾、钠合金呈液态。
(3)合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面不同
于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
知识点2 金属冶炼
1.金属在自然界中的存在
2.金属冶炼的实质
金属的冶炼过程就是把金属从_____态还原为_____态的过程。即:Mn++ne-===M(写反应通式,用M表示
金属)。
3.金属冶炼的一般步骤4.金属冶炼的方法——金属活动顺序与金属冶炼的关系
①电解法:适合冶炼金属活动性很强的金属(一般指在金属活动性顺序中排在锌前面的金属)。
工业上用电解法冶炼Na、Mg、Al的化学方程式分别为
a.2NaCl(熔融)=====2Na+Cl↑、
2
b.MgCl (熔融)=====Mg+Cl↑、
2 2
c.2Al O=====4Al+3O↑。
2 3 2
②热还原法:用还原剂(C、CO、H、Al等)还原金属氧化物,适合较活泼的金属。
2
a.CO还原Fe O:Fe O+4CO=====3Fe+4CO;
3 4 3 4 2
b.C还原ZnO:ZnO+C=====Zn+CO↑;
c.H 还原WO:WO+3H=====W+3HO。
2 3 3 2 2
【注意】在高炉炼铁中,加入的还原剂是焦炭,但反应中真正作还原剂的是CO。
③热分解法:适用于不活泼的金属,如Hg和Ag。由HgO冶炼Hg的化学方程式:2HgO=====2Hg+
O↑;由Ag O冶炼Ag的化学方程式:2Ag O=====4Ag+O↑。
2 2 2 2
5.铝热反应
Al和某些金属氧化物在高温下进行,反应迅速并放出大量的热,新生成的金属
实验原理
单质呈熔融态且易与Al O 分离
2 3
实验
装置
实验 ①镁带剧烈燃烧,放出一定的热,并发出耀眼的白光,氧化铁和铝粉在较高
现象 温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
实验 高温下,铝与氧化铁发生反应,放出大量的热,反应的化学方程式为2Al+
结论 Fe O=====2Fe+Al O
2 3 2 3
原理 ①制取熔点较高、活泼性弱于Al的金属铬、锰、钨等;②金属焊接,如野
应用 外焊接钢轨等
【特别提醒】铝热反应的三个注意事项
①铝热反应是在高温干态下进行的置换反应,铝只能与金属活动性顺序中排在铝之后的金属的氧化物反应。②铝热反应会放出大量的热(这一特性常出现在推断题中)。Mg条、KClO 的作用是产生高温,引发铝热反
3
应。
③铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
6.特殊金属的冶炼方法:
有些很活泼的金属也可以用还原法来冶炼,如
Na+KCl=====K↑+NaCl
2RbCl+Mg=====MgCl +2Rb↑等,
2
主要运用了化学平衡移动原理,利用K、Rb沸点低,汽化离开反应体系,使化学反应得以向正反应方向进
行。
考向1 合金性质与金属材料的应用
例1.(2023·上海宝山·统考二模)关于生铁和钢的区别正确的是
A.生铁属于纯净物,钢属于混合物 B.生铁比钢的含碳量更高
C.生铁比钢弹性更好 D.生铁属于铁-碳合金,钢也是合金但不含碳
【变式训练】(2021·辽宁·模拟预测)《考工记》:金(青铜)有六齐,六分其金而锡居一,谓之钟鼎之齐;
五分其金而锡居一,谓之斧斤之齐;四分其金而锡居一,谓之戈戟之齐;三分其金而锡居一,谓之大刃之
齐;五分其金而锡居二,谓之削杀矢之齐;金锡半,谓之鉴燧之齐。下列有关说法错误的是
A.六齐是铜锡合金6种配比 B.大刃硬度大于斧斤
C.六齐之金,日久也会有铜绿生成 D.依据铜锡不同比例可以配成黄铜
考向2 金属矿物的开发利用
例1.(2023·河北邯郸·统考一模)“太空金属”钛广泛应用于新型功能材料等方面,工业上用钛铁矿(主
要成分是TiO,含少量FeO和Fe O)冶炼金属钛的工艺流程如图所示,下列说法正确的是
2 2 3
A.基态钛原子核外有4个未成对电子
B.金属Mg与TiCl 可在氮气气氛条件下进行反应
4
C.步骤II加热可促进TiO2+的水解
D.步骤III中可能发生的反应为TiO+2Cl+C TiCl +CO
2 2 4
【变式训练1】(2023·上海嘉定·统考一模)下列金属冶炼的反应原理,不恰当的是
A.2NaCl(熔融)B.
C.
D.
【变式训练2】(2023·山东烟台·统考二模)一种锰矿的主要成分为 ,杂质为 、 、
MnS、FeS、CuS、NiS等。研究人员设计了如下流程制备金属锰,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.5 7.6
沉淀完全pH 3.2 6.7 8.5 9.8
下列说法正确的是
A.“脱硫”过程中FeS发生反应:
B.物质X为 ,滤渣Y为
C.上述流程表明: ,
D.“电解”所得阳极产物均可循环利用
1.(2023·湖南·统考高考真题)中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.青铜器“四羊方尊”的主要材质为合金
B.长沙走马楼出土的竹木简牍主要成分是纤维素
C.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
D.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
2.(2023·山东·统考高考真题)利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,
甲、乙两室均预加相同的 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
3.(2022·浙江·统考高考真题)下列说法不正确的是
A.用标准液润洗滴定管后,应将润洗液从滴定管上口倒出
B.铝热反应非常剧烈,操作时要戴上石棉手套和护目镜
C.利用红外光谱法可以初步判断有机物中具有哪些基团
D.蒸发浓缩硫酸铵和硫酸亚铁(等物质的量)的混合溶液至出现晶膜,静置冷却,析出硫酸亚铁铵晶体
4.(2023·湖北·统考高考真题)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______,装置B的作用为_______。
(2)铜与过量 反应的探究如下:
实验②中Cu溶解的离子方程式为_______;产生的气体为_______。比较实验①和②,从氧化还原角度说
明 的作用是_______。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰
性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为_______。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示
剂,用 标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
, )标志滴定终点的现象是_______,粗品中X的相对含量为_______。