文档内容
第 13 讲 硫及其化合物
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查硫及其化合物的性质与应用
高频考点2 考查二氧化硫的检验
高频考点3 考查浓硫酸的性质及应用
高频考点4 考查硫酸根离子的检验
高频考点5 考查含硫化合物的转化关系及应用
高频考点6 考查硫及其化合物性质的实验探究
正文
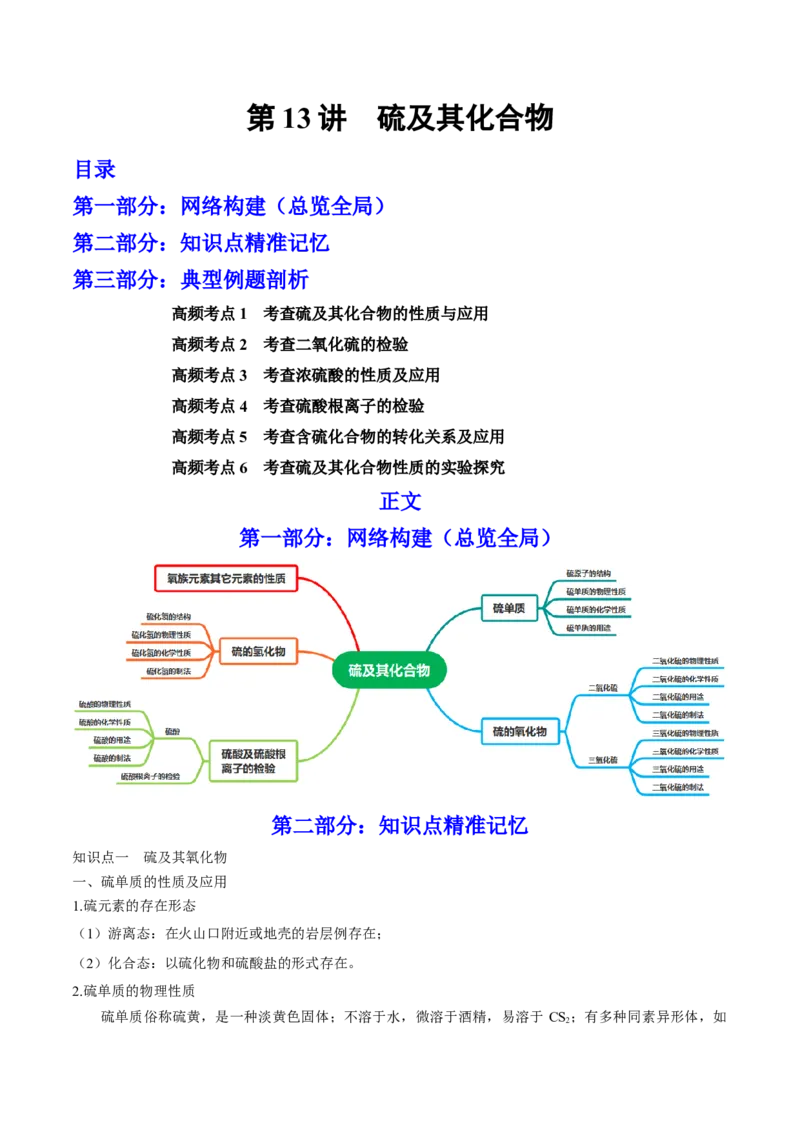
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 硫及其氧化物
一、硫单质的性质及应用
1.硫元素的存在形态
(1)游离态:在火山口附近或地壳的岩层例存在;
(2)化合态:以硫化物和硫酸盐的形式存在。
2.硫单质的物理性质
硫单质俗称硫黄,是一种淡黄色固体;不溶于水,微溶于酒精,易溶于 CS ;有多种同素异形体,如
2单斜硫、斜方硫等。
3.从化合价的角度认识硫单质的化学性质
HS ←――――――→SO
2 2
(1)S的氧化性
①S与Fe、Cu、Hg反应的化学方程式依次为Fe+S FeS、2Cu+S Cu S、S+Hg===HgS(此反应适
2
用于除去室内洒落的Hg)。
②S与H 反应的化学方程式为S+H HS
2 2 2
(2)S的还原性
①S与O 反应的化学方程式为S+O=====SO ,在空气中燃烧火焰为淡蓝色。
2 2 2
②与强氧化剂反应(如浓硫酸)的化学方程式为S+2HSO (浓) 3SO ↑+2HO。
2 4 2 2
(3)S与NaOH溶液反应的化学方程式为3S+6NaOH 2NaS+NaSO +3HO,该反应中硫既是氧化剂,
2 2 3 2
又是还原剂,此反应可用于除去试管内黏附的S。
【特别提醒】
①硫与变价金属反应时,生成低价态金属硫化物(如Cu S、FeS)。
2
②汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
二、硫的氢化物——硫化氢及氢硫酸
1.硫化氢
1)物理性质
(1)无色,有臭鸡蛋气味的有毒气体。
(2)密度比空气大(HS:34>空气:29)
2
(3)微溶于水(1:2.6),水溶液叫氢硫酸,显弱酸性。
2)化学性质
(1)不稳定性:HS S+H
2 2
(2)还原性
氧化性:KMnO >Cl>O >Br >I >S>H S
4 2 2 2 2 2
A.与O 反应(可燃性:淡蓝色火焰), 产物:S或S,SO 或SO
2 2 2
O 不足:2HS+O=====2S+HO
2 2 2 2
O 足量:2HS+3O=====2SO+HO
2 2 2 2 2
B.与卤素单质的反应: HS+X=S↓+2HX(X=Cl、Br、I)
2 2
现象:溴水/碘水褪色且生成淡黄色沉淀。
C.与酸性KMnO 反应:2KMnO +5H S+3HSO=5S↓+KSO+2MnSO+8HO
4 4 2 2 4 2 4 4 2
KMnO 的强氧化性体现:+7价Mn
4现象:酸性KMnO 溶液的颜色变浅(MnO -:紫红色)
4 4
2.氢硫酸的化学性质
1)还原性:同HS气体。HS还原性的体现:-2价S;HS氧化性的体现:+1价H
2 2 2
2)弱酸性
(1)与碱反应
(2)与活泼金属反应(氧化性)
3.与某些盐反应(复分解反应)
HS+CuSO=CuS(黑色)↓+HSO,CuS不溶于水,不溶于酸
2 4 2 4
HS+Pb(Ac) =PbS(黑色)↓+2HAc,PbS不溶于水,不溶于酸
2 2
检验HS气体:上述溶液或湿润的Pb(Ac) 试纸。
2 2
3.实验室制HS
2
1)原理:强酸制弱酸
FeS+HSO=HS↑+FeSO
2 4 2 4
2)发生装置:固+液,不加热
3)干燥装置:无水CaCl 或PO,不能用浓硫酸(强氧化性)。
2 2 5
4)收集装置:向上排空气法
5)尾气吸收装置:NaOH溶液
三、硫的氧化物(SO 、SO )的性质及应用
2 3
1.二氧化硫(SO )
2
(1)物理性质
二氧化硫是无色、有刺激性气味的有毒气体,是大气污染物之一;易溶于水,通常状况下,1体积水
溶解约40体积SO 。
2
(2)化学性质
①酸性氧化物的通性,与水反应:SO +H O HSO ;与NaOH(足量)反应:2NaOH+SO ===Na SO +
2 2 2 3 2 2 3
HO。
2
②氧化性(如与HS溶液反应):SO +2HS===3S↓+2HO
2 2 2 2
③还原性
a.与O 反应:2SO +O 2SO ;
2 2 2 3
b.与卤素单质的水溶液反应:X+SO +2HO=2HX+HSO (X=Cl、Br、I);
2 2 2 2 4c.与铁盐溶液反应:2Fe3++SO +2HO=2Fe3++2H++SO 2-;
2 2 4
d.与CuX 溶液反应生成CuX白色沉淀:2CuX+SO +2HO=2CuX↓+HSO +2HX(X=Cl、Br、I);
2 2 2 2 2 4
④漂白性:可使品红溶液等有机色质褪色,生成不稳定的化合物。
(3)实验室制法
①固体NaSO 与较浓HSO 反应
2 3 2 4
NaSO +HSO ===Na SO +SO ↑+HO;
2 3 2 4 2 4 2 2
②铜与浓HSO 混合加热
2 4
Cu+2HSO (浓) CuSO +SO ↑+2HO。
2 4 4 2 2
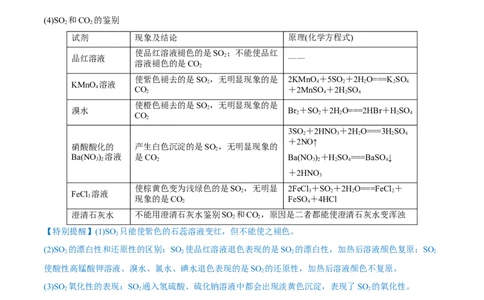
(4)SO 和CO 的鉴别
2 2
试剂 现象及结论 原理(化学方程式)
使品红溶液褪色的是SO ;不能使品红
品红溶液 2 ——
溶液褪色的是CO
2
使紫色褪去的是SO ,无明显现象的是 2KMnO +5SO +2HO===K SO
KMnO 溶液 2 4 2 2 2 4
4 CO +2MnSO +2HSO
2 4 2 4
使橙色褪去的是SO ,无明显现象的是
溴水 2 Br +SO +2HO===2HBr+HSO
CO 2 2 2 2 4
2
3SO +2HNO+2HO===3H SO
2 3 2 2 4
+2NO↑
硝酸酸化的 产生白色沉淀的是SO ,无明显现象的
2
Ba(NO ) 溶液 是CO Ba(NO )+HSO ===BaSO ↓
3 2 2 3 2 2 4 4
+2HNO
3
使棕黄色变为浅绿色的是SO ,无明显 2FeCl +SO +2HO===FeCl +
FeCl 溶液 2 3 2 2 2
3 现象的是CO FeSO +4HCl
2 4
澄清石灰水 不能用澄清石灰水鉴别SO 和CO,原因是二者都能使澄清石灰水变浑浊
2 2
【特别提醒】(1)SO 只能使紫色的石蕊溶液变红,但不能使之褪色。
2
(2)SO 的漂白性和还原性的区别:SO 使品红溶液退色表现的是SO 的漂白性,加热后溶液颜色复原;SO
2 2 2 2
使酸性高锰酸钾溶液、溴水、氯水、碘水退色表现的是SO 的还原性,加热后溶液颜色不复原。
2
(3)SO 氧化性的表现:SO 通入氢硫酸、硫化钠溶液中都会出现淡黄色沉淀,表现了SO 的氧化性。
2 2 2
(4)三类漂白剂的区别
类型 原理 举例 特点 备注
HClO、NaClO、
将有机色质内部“生色团”破 不可逆、持 无选
氧化型 Ca(ClO) 、NaO、
坏掉 2 2 2 久 择性
HO、O 等
2 2 3
与有机色质内部“生色团” 可逆、不持 有选
加合型 SO
“化合”成无色物质 2 久 择性
吸附
吸附型 将有色物质吸附而退色 活性炭 物理变化
色素
2.三氧化硫(SO )
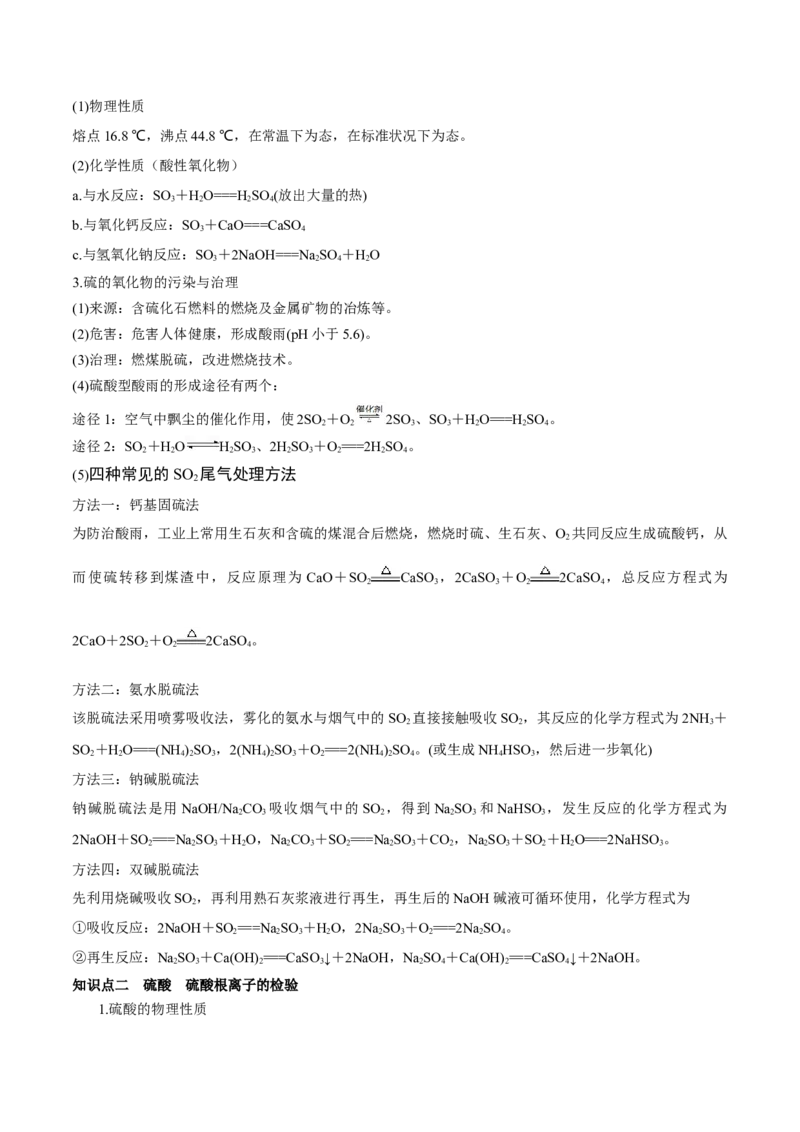
3(1)物理性质
熔点16.8 ℃,沸点44.8 ℃,在常温下为态,在标准状况下为态。
(2)化学性质(酸性氧化物)
a.与水反应:SO +HO===H SO (放出大量的热)
3 2 2 4
b.与氧化钙反应:SO +CaO===CaSO
3 4
c.与氢氧化钠反应:SO +2NaOH===Na SO +HO
3 2 4 2
3.硫的氧化物的污染与治理
(1)来源:含硫化石燃料的燃烧及金属矿物的冶炼等。
(2)危害:危害人体健康,形成酸雨(pH小于5.6)。
(3)治理:燃煤脱硫,改进燃烧技术。
(4)硫酸型酸雨的形成途径有两个:
途径1:空气中飘尘的催化作用,使2SO +O 2SO 、SO +HO===H SO 。
2 2 3 3 2 2 4
途径2:SO +HO HSO 、2HSO +O===2H SO 。
2 2 2 3 2 3 2 2 4
(5)四种常见的SO 尾气处理方法
2
方法一:钙基固硫法
为防治酸雨,工业上常用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、O 共同反应生成硫酸钙,从
2
而使硫转移到煤渣中,反应原理为 CaO+SO CaSO ,2CaSO +O 2CaSO ,总反应方程式为
2 3 3 2 4
2CaO+2SO +O 2CaSO。
2 2 4
方法二:氨水脱硫法
该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的 SO 直接接触吸收SO ,其反应的化学方程式为2NH +
2 2 3
SO +HO===(NH)SO ,2(NH )SO +O===2(NH)SO 。(或生成NH HSO ,然后进一步氧化)
2 2 4 2 3 4 2 3 2 4 2 4 4 3
方法三:钠碱脱硫法
钠碱脱硫法是用 NaOH/Na CO 吸收烟气中的 SO ,得到NaSO 和NaHSO ,发生反应的化学方程式为
2 3 2 2 3 3
2NaOH+SO ===Na SO +HO,NaCO+SO ===Na SO +CO,NaSO +SO +HO===2NaHSO 。
2 2 3 2 2 3 2 2 3 2 2 3 2 2 3
方法四:双碱脱硫法
先利用烧碱吸收SO ,再利用熟石灰浆液进行再生,再生后的NaOH碱液可循环使用,化学方程式为
2
①吸收反应:2NaOH+SO ===Na SO +HO,2NaSO +O===2Na SO 。
2 2 3 2 2 3 2 2 4
②再生反应:NaSO +Ca(OH) ===CaSO ↓+2NaOH,NaSO +Ca(OH) ===CaSO ↓+2NaOH。
2 3 2 3 2 4 2 4
知识点二 硫酸 硫酸根离子的检验
1.硫酸的物理性质(1)纯硫酸是一种无色油状液体,沸点高(沸点338℃,高沸点酸能用于制备低沸点酸),难挥发;98%的
浓硫酸的密度为1.84g/cm3。
(2)溶解性:浓硫酸与水以任意比混溶,溶解时可放出大量热。
(3)稀释方法:将浓硫酸沿器壁慢慢注入水中并不断搅拌。
2.硫酸的化学性质
(1)稀硫酸具有酸的通性
硫酸是强电解质,在水溶液中的电离方程式为HSO ===2H++SO,具有酸的通性。
2 4
①指示剂变色:石蕊变红;酚酞不变色。
②与金属反应:Fe+H SO ==FeSO +H ↑ ;2Al + 3H SO ==Al (SO ) + 3H ↑
2 4 4 2 2 4 2 4 3 2
③与碱的反应:2NaOH+H SO ==Na SO +2H O;Ba2++2OH-+2H++SO===BaSO ↓+2HO;
2 4 2 4 2 4 2
④与碱性氧化物反应:CuO +H SO == CuSO +H O;MgO+2H+===Mg2++HO;
2 4 4 2 2
⑤与某些盐的反应:BaCl +H SO ==BaSO ↓+ 2HCl;SO+2H+===H O+SO ↑;
2 2 4 4 2 2
3.浓HSO 的特性
2 4
1)吸水性与脱水性的区别
浓硫酸吸水是把物质本身中含有的自由HO分子或结晶水吸收。浓硫酸脱水是把本身不含水的有机物
2
中的氢元素和氧元素按原子个数比2∶1的形式脱去,C H O 12C+11H O。所以,二者的本质区别
12 22 11 2
是物质中有没有现成的水分子。注意:在浓硫酸作用下,结晶水合物失去结晶水属于浓硫酸的吸水性。
利用浓硫酸的吸水性,常用浓硫酸作干燥剂,浓硫酸可以干燥 H 、Cl 、O 、SO 、N 、CO 、CO、
2 2 2 2 2 2
CH 等气体,但是它不能用来干燥碱性气体(如NH )和强还原性气体(如HBr、HI、HS)。
4 3 2
2)强氧化性:在浓硫酸中主要是以硫酸分子的形式存在,体现的是硫酸分子的性质。在硫酸分子中,存
在+6价硫,很容易得电子被还原,所以具有很强的氧化性。浓硫酸能将大多数金属(如 Cu)或非金属
(如C)氧化:
(1)Fe、Al的钝化
常温下,当Fe、Al等金属遇到浓硫酸时,会与浓硫酸发生反应,表面生成一层致密的氧化物薄膜而出
现“钝化”现象。
(2)与不活泼金属和非金属的反应
由于浓硫酸具有强氧化性,故存在与稀硫酸不同的化学性质,能够与不活泼金属或非金属发生反应,
反应过程中有如下规律:
①反应要加热,否则不反应;
②还原产物一般是SO 。一般金属被氧化为高价态的硫酸盐,非金属被氧化为高价态氧化物或含氧酸。
2
③浓硫酸与金属反应时,既表现酸性又表现强氧化性,而与非金属反应时,只表现强氧化性。如:Cu+2H SO (浓) CuSO + 2H O +SO ↑
2 4 4 2 2
2Ag+2HSO (浓) Ag SO +SO↑+2H O
2 4 2 4 2 2
C+2H SO (浓) CO↑+2H O+2SO ↑
2 4 2 2 2
S+2HSO (浓) 3SO ↑+2H O
2 4 2 2
④浓硫酸氧化含低价非金属元素的化合物
HS+HSO (浓)==S↓+SO ↑+2H O或HS+3HSO (浓) 4SO ↑+4H O
2 2 4 2 2 2 2 4 2 2
2HI+HSO (浓)==I +SO↑+2H O
2 4 2 2 2
2HBr+HSO (浓)==Br +SO↑+2H O
2 4 2 2 2
⑤随着反应的进行,浓硫酸浓度变小,一旦变为稀硫酸,反应就停止。
【特别提醒】①HSO 是高沸点、难挥发性的强酸,利用这一性质可以制取HCl和HF:HSO (浓)+
2 4 2 4
NaCl=====NaHSO+HCl↑,CaF +HSO ===CaSO +2HF↑。
4 2 2 4 4
②由“量变”引起的“质变”:金属(如Cu、Zn等)与浓HSO 反应时,要注意HSO 浓度对反应产物的影
2 4 2 4
响。开始阶段产生SO 气体,随着反应的进行,HSO 的浓度变小,最后变为稀HSO ,Cu与稀HSO 不
2 2 4 2 4 2 4
反应,Zn与稀HSO 反应生成H 而不是SO 。
2 4 2 2
4.硫酸的用途
(1)制取化肥、硫酸盐、挥发性酸。
(2)消除金属表面的氧化物。
(3)用于精炼石油,制造炸药、农药、染料等,是实验室里常用的试剂。
5.硫酸的工业制备
三步骤 三反应
黄铁矿煅烧 4FeS+11O=====2Fe O+8SO
2 2 2 3 2
SO 2 的催化氧化 2SO 2 +O 2 2SO 3
SO 吸收 SO +HO===H SO
3 3 2 2 4
6.SO、SO的检验
(1)SO的检验
①向溶液中加入盐酸,将产生的气体通入品红溶液中,红色褪去,发生的离子反应为SO+2H+===HO+
2
SO ↑。
2
②加入氯化钡溶液生成白色沉淀,然后向沉淀中加入盐酸,沉淀溶解并产生具有刺激性气味的气体,发生
反应的离子方程式为SO+Ba2+===BaSO ↓,BaSO+2H+===Ba2++SO ↑+HO。
3 3 2 2(2)检验SO的正确操作方法:被检液――――――→取清液――――――→有无白色沉淀产生(判断有无
SO)。
先加稀盐酸的目的是防止CO、SO、Ag+干扰,再加BaCl 溶液,有白色沉淀产生。整个过程中可能发
2
生反应的离子方程式:CO+2H+===CO ↑+HO、SO+2H+===SO↑+HO、Ag++Cl-===AgCl↓、Ba2++
2 2 2 2
SO===BaSO ↓。
4
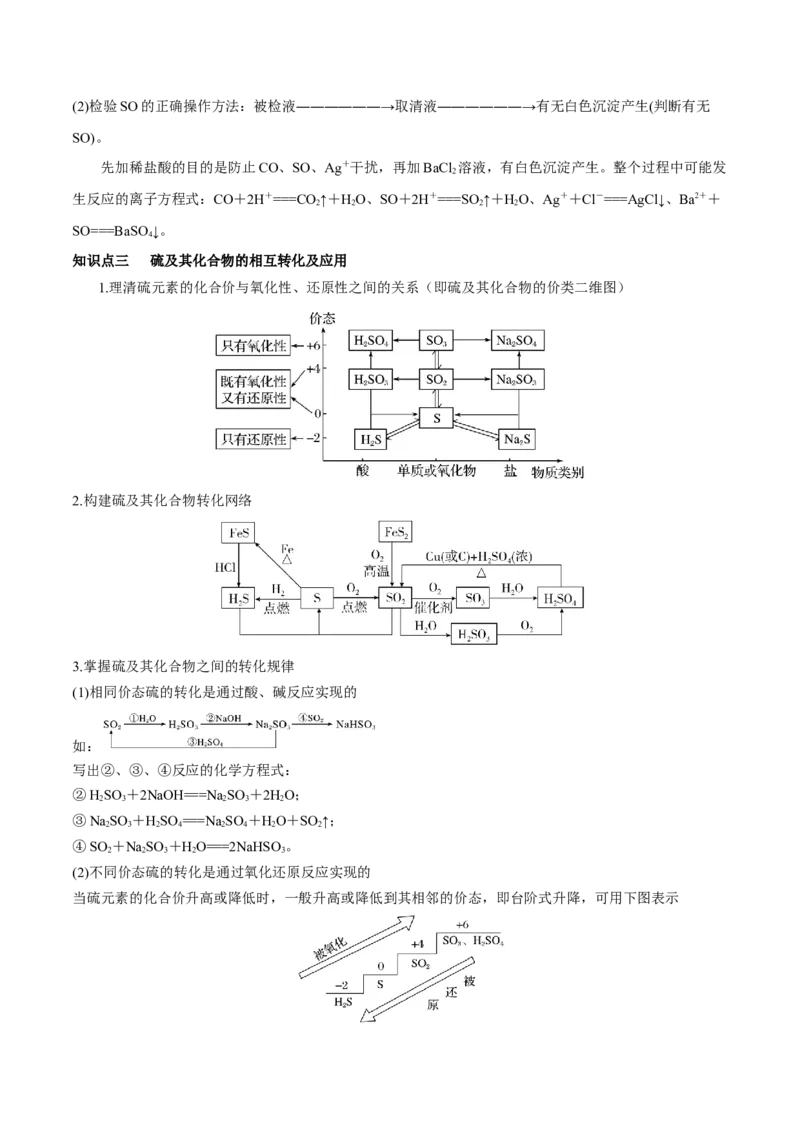
知识点三 硫及其化合物的相互转化及应用
1.理清硫元素的化合价与氧化性、还原性之间的关系(即硫及其化合物的价类二维图)
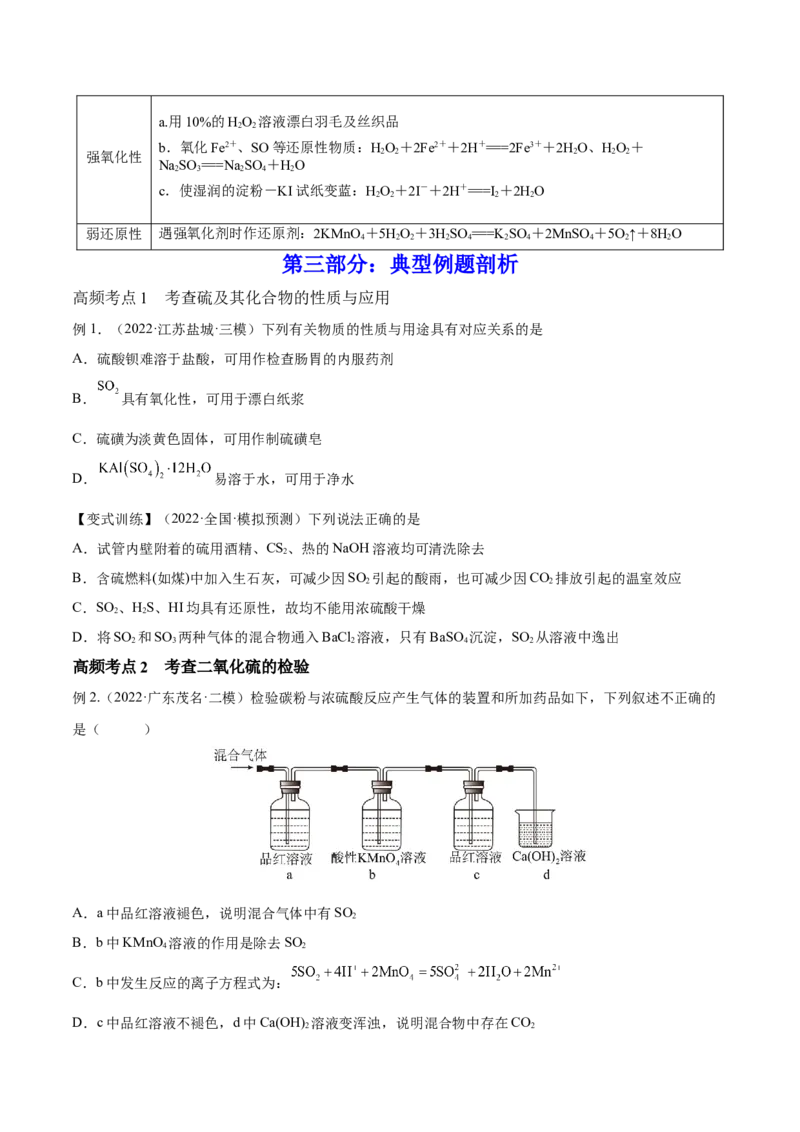
2.构建硫及其化合物转化网络
3.掌握硫及其化合物之间的转化规律
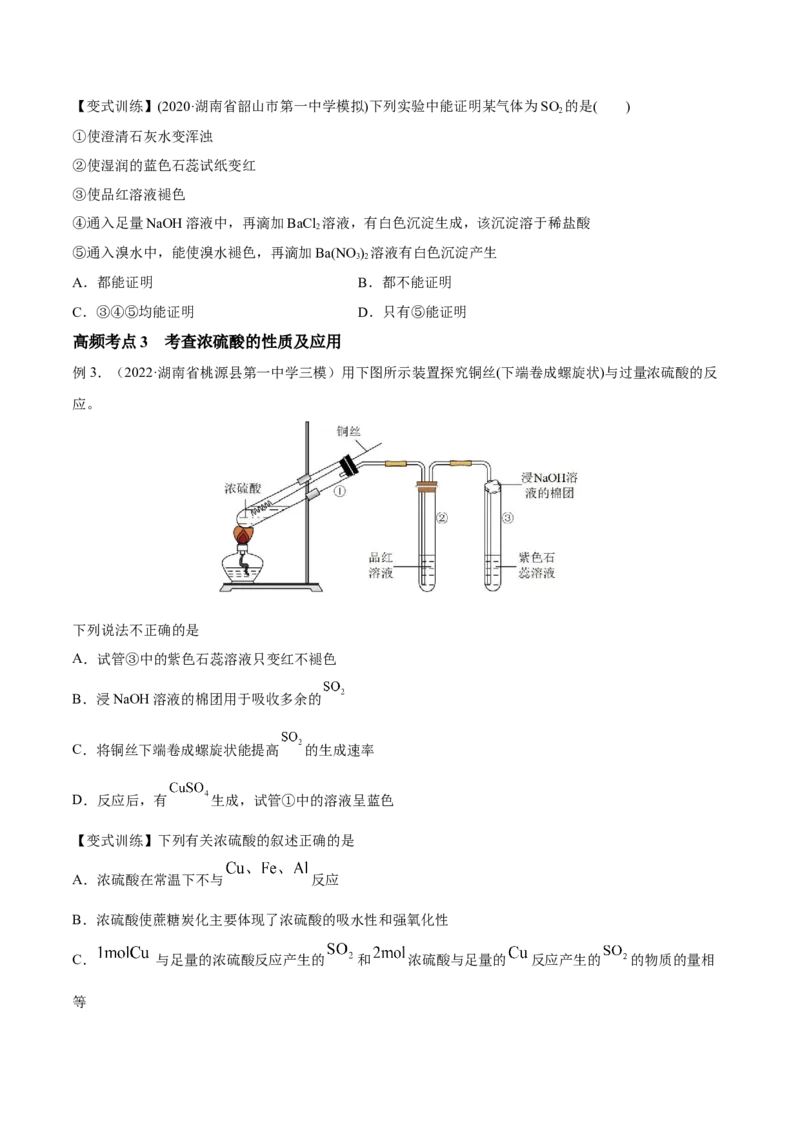
(1)相同价态硫的转化是通过酸、碱反应实现的
如:
写出②、③、④反应的化学方程式:
②HSO +2NaOH===Na SO +2HO;
2 3 2 3 2
③NaSO +HSO ===Na SO +HO+SO ↑;
2 3 2 4 2 4 2 2
④SO +NaSO +HO===2NaHSO 。
2 2 3 2 3
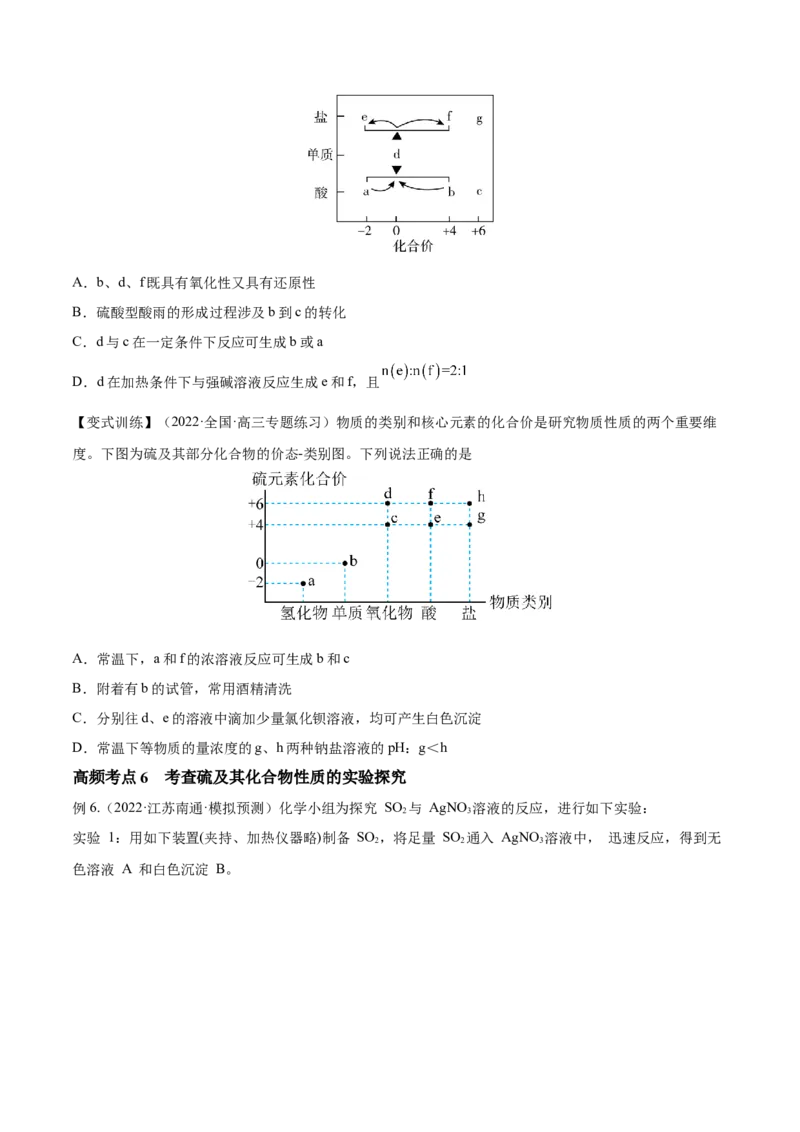
(2)不同价态硫的转化是通过氧化还原反应实现的
当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,可用下图表示注意:(1)同种元素相邻价态的粒子间不发生氧化还原反应,如 S和HS、S和SO 、SO 和浓硫酸之间不发
2 2 2
生氧化还原反应。
(2)当硫元素的高价态粒子与低价态粒子反应时,一般生成中间价态,如 2NaS+NaSO +
2 2 3
3HSO ===3Na SO +3S↓+3HO。
2 4 2 4 2
知识点四 第六主族的其它知识归纳
1.硫代硫酸钠(Na SO)
2 2 3
(1)制备
①硫化碱法,即将NaS和NaCO 以物质的量之比为2∶1配成溶液,然后通入SO ,发生的反应为2NaS
2 2 3 2 2
+NaCO+4SO ===3Na SO+CO。
2 3 2 2 2 3 2
②亚硫酸钠法,使沸腾的NaSO 溶液同硫粉反应,其反应的方程式为NaSO +S NaSO。
2 3 2 3 2 2 3
(2)性质
①中等强度还原剂,可被碘氧化成连四硫酸钠(Na SO),该反应常用来定量测定碘的含量,反应的离子方
2 4 6
程式为I+2SO===2I-+SO(用于直接碘量法和间接碘量法测定物质的浓度或含量)。
2 2 4
②可被氯、溴等氧化为SO,如NaSO +4Cl +5HO=== Na SO +HSO +8HCl(用作纺织工业上的脱氯
2 2 3 2 2 2 4 2 4
剂)。
③可与酸反应,离子方程式为2H++SO===S↓+SO ↑+HO(用于探究速率与浓度、温度的关系)。
2 2 2
2.焦亚硫酸钠(Na SO)
2 2 5
(1)制备:NaHSO 过饱和溶液结晶脱水而成,2NaHSO===Na SO+HO。
3 3 2 2 5 2
(2)性质
①与酸反应放出二氧化硫,如NaSO+2HCl===2NaCl+2SO ↑+HO。
2 2 5 2 2
②强还原性,如NaSO+2I+3HO===2NaHSO +4HI。
2 2 5 2 2 4
3.过二硫酸钠(Na SO)、连二亚硫酸钠(Na SO)
2 2 8 2 2 4
(1)过二硫酸钠中S为+6价,含有1个过氧键(—O—O—),性质与过氧化氢相似,具有氧化性。作为氧化
剂参与反应时,过氧键断裂,过氧键中的氧原子由-1价变为-2价,硫原子化合价不变。如 SO+2I-
2
=====2SO+I ,5SO+2Mn2++8HO===10SO+2MnO+16H+。过二硫酸钠不稳定,受热分解生成
2 2 2
NaSO 、SO 和O。
2 4 3 2
(2)连二亚硫酸钠中S为+3价,是强还原剂,能将I 、Cu2+、Ag+还原,能被空气中的氧气氧化。在无氧
2
条件下,用锌粉还原亚硫酸氢钠可制得连二亚硫酸钠。
4.硒及其化合物的性质
(1)单质硒及其氢化物在空气中燃烧可得到SeO。
2(2)SeO 的氧化性比 SO 强,属于中等强度的氧化剂,可氧化 HS、NH 等:SeO +2HS===Se+2S+
2 2 2 3 2 2
2HO;3SeO+4NH ===3Se+2N+6HO。
2 2 3 2 2
(3)亚硒酸可作氧化剂,能氧化SO ,HSeO+2SO +HO===2H SO +Se,但遇到强氧化剂时表现还原性,
2 2 3 2 2 2 4
可被氧化成硒酸,HSeO+Cl+HO===H SeO+2HCl。
2 3 2 2 2 4
5.碲及其化合物的性质
(1)碲在空气或纯氧中燃烧生成TeO 。
2
(2)TeO 是不挥发的白色固体,微溶于水,易溶于强酸、强碱,如TeO +2NaOH===Na TeO +HO。
2 2 2 3 2
(3)TeO (H TeO )具有氧化性和还原性:
2 2 3
HTeO +2SO +HO===2H SO +Te;
2 3 2 2 2 4
HTeO +Cl+HO===H TeO +2HCl。
2 3 2 2 2 4
(4)硒和碲的一切化合物均有毒。
6.O 和HO 的性质及应用
3 2 2
1)臭氧(O )
3
(1)组成:臭氧的分子式为O,与O 互为同素异形体。
3 2
(2)化学性质
O 不稳定,容易分解,分解的化学方程式为2O===3O ;在放电条件下空气中的
不稳定性 3 3 2
O 可以转化为O,反应的化学方程式为3O=====2O
2 3 2 3
O 容易使淀粉-KI溶液变蓝色,反应的化学方程式为2KI+O+HO===I +
强氧化性 3 3 2 2
2KOH+O
2
漂白性 O 具有强氧化性,能使有色物质褪色,可用作杀菌消毒剂
3
(3)臭氧层可以吸收来自太阳的紫外线,是人类和其他生物的“保护伞”。
2)过氧化氢(H O)
2 2
(1)结构
电子式: ,结构式:H—O—O—H。
(2)化学性质
不稳定性 易分解,加热、加催化剂都能使分解速率加快:2HO=====2HO+O↑
2 2 2 2
弱酸性 相当于二元弱酸,HOH++HO,HOH++O
2 2a.用10%的HO 溶液漂白羽毛及丝织品
2 2
b.氧化Fe2+、SO等还原性物质:HO+2Fe2++2H+===2Fe3++2HO、HO+
强氧化性 2 2 2 2 2
NaSO ===Na SO +HO
2 3 2 4 2
c.使湿润的淀粉-KI试纸变蓝:HO+2I-+2H+===I +2HO
2 2 2 2
弱还原性 遇强氧化剂时作还原剂:2KMnO +5HO+3HSO ===K SO +2MnSO +5O↑+8HO
4 2 2 2 4 2 4 4 2 2
第三部分:典型例题剖析
高频考点1 考查硫及其化合物的性质与应用
例1.(2022·江苏盐城·三模)下列有关物质的性质与用途具有对应关系的是
A.硫酸钡难溶于盐酸,可用作检查肠胃的内服药剂
B. 具有氧化性,可用于漂白纸浆
C.硫磺为淡黄色固体,可用作制硫磺皂
D. 易溶于水,可用于净水
【变式训练】(2022·全国·模拟预测)下列说法正确的是
A.试管内壁附着的硫用酒精、CS、热的NaOH溶液均可清洗除去
2
B.含硫燃料(如煤)中加入生石灰,可减少因SO 引起的酸雨,也可减少因CO 排放引起的温室效应
2 2
C.SO 、HS、HI均具有还原性,故均不能用浓硫酸干燥
2 2
D.将SO 和SO 两种气体的混合物通入BaCl 溶液,只有BaSO 沉淀,SO 从溶液中逸出
2 3 2 4 2
高频考点2 考查二氧化硫的检验
例2.(2022·广东茂名·二模)检验碳粉与浓硫酸反应产生气体的装置和所加药品如下,下列叙述不正确的
是( )
A.a中品红溶液褪色,说明混合气体中有SO
2
B.b中KMnO 溶液的作用是除去SO
4 2
C.b中发生反应的离子方程式为:
D.c中品红溶液不褪色,d中Ca(OH) 溶液变浑浊,说明混合物中存在CO
2 2【变式训练】(2020·湖南省韶山市第一中学模拟)下列实验中能证明某气体为SO 的是( )
2
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaCl 溶液,有白色沉淀生成,该沉淀溶于稀盐酸
2
⑤通入溴水中,能使溴水褪色,再滴加Ba(NO ) 溶液有白色沉淀产生
3 2
A.都能证明 B.都不能证明
C.③④⑤均能证明 D.只有⑤能证明
高频考点3 考查浓硫酸的性质及应用
例3.(2022·湖南省桃源县第一中学三模)用下图所示装置探究铜丝(下端卷成螺旋状)与过量浓硫酸的反
应。
下列说法不正确的是
A.试管③中的紫色石蕊溶液只变红不褪色
B.浸NaOH溶液的棉团用于吸收多余的
C.将铜丝下端卷成螺旋状能提高 的生成速率
D.反应后,有 生成,试管①中的溶液呈蓝色
【变式训练】下列有关浓硫酸的叙述正确的是
A.浓硫酸在常温下不与 反应
B.浓硫酸使蔗糖炭化主要体现了浓硫酸的吸水性和强氧化性
C. 与足量的浓硫酸反应产生的 和 浓硫酸与足量的 反应产生的 的物质的量相
等D.浓硫酸有吸水性,可以干燥 等气体
高频考点4 考查硫酸离子的检验
例4.(2021·全国·模拟预测)下列过程中,最终的白色沉淀物不一定是BaSO 的是( )
4
A.Fe(NO ) 溶液――→白色沉淀
3 2
B.Ba(NO ) 溶液――→白色沉淀
3 2
C.无色溶液――→白色沉淀
D.无色溶液――→无色溶液――→白色沉淀
【变式训练】甲、乙、丙三位同学各设计了一个实验,结果各自都认为自己的试样中含有SO 2-离子。
4
甲的实验为:
(1)乙认为甲的实验不严谨,因为试样A中若含有________离子(仅填一种)也会有此现象。
乙的实验为:
(2)丙认为乙的实验也不严谨,因为试样B中若含有________离子(仅填一种)也会有此现象。
丙的实验为:
若丙方案合理,回答:
(3)若丙实验合理,则其中试剂Ⅰ是___________,现象Ⅰ是__________;试剂Ⅱ是___________,现象
Ⅱ是__________。(若你认为丙方案不合理,以上四空可以不填)
高频考点5 考查含硫化合物的转化关系及应用
例5.(2022·山东淄博·三模)在“价一类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定
量关系。图中的字母分别代表硫及其常见化合物,相关推断不合理的是A.b、d、f既具有氧化性又具有还原性
B.硫酸型酸雨的形成过程涉及b到c的转化
C.d与c在一定条件下反应可生成b或a
D.d在加热条件下与强碱溶液反应生成e和f,且
【变式训练】(2022·全国·高三专题练习)物质的类别和核心元素的化合价是研究物质性质的两个重要维
度。下图为硫及其部分化合物的价态-类别图。下列说法正确的是
A.常温下,a和f的浓溶液反应可生成b和c
B.附着有b的试管,常用酒精清洗
C.分别往d、e的溶液中滴加少量氯化钡溶液,均可产生白色沉淀
D.常温下等物质的量浓度的g、h两种钠盐溶液的pH:g<h
高频考点6 考查硫及其化合物性质的实验探究
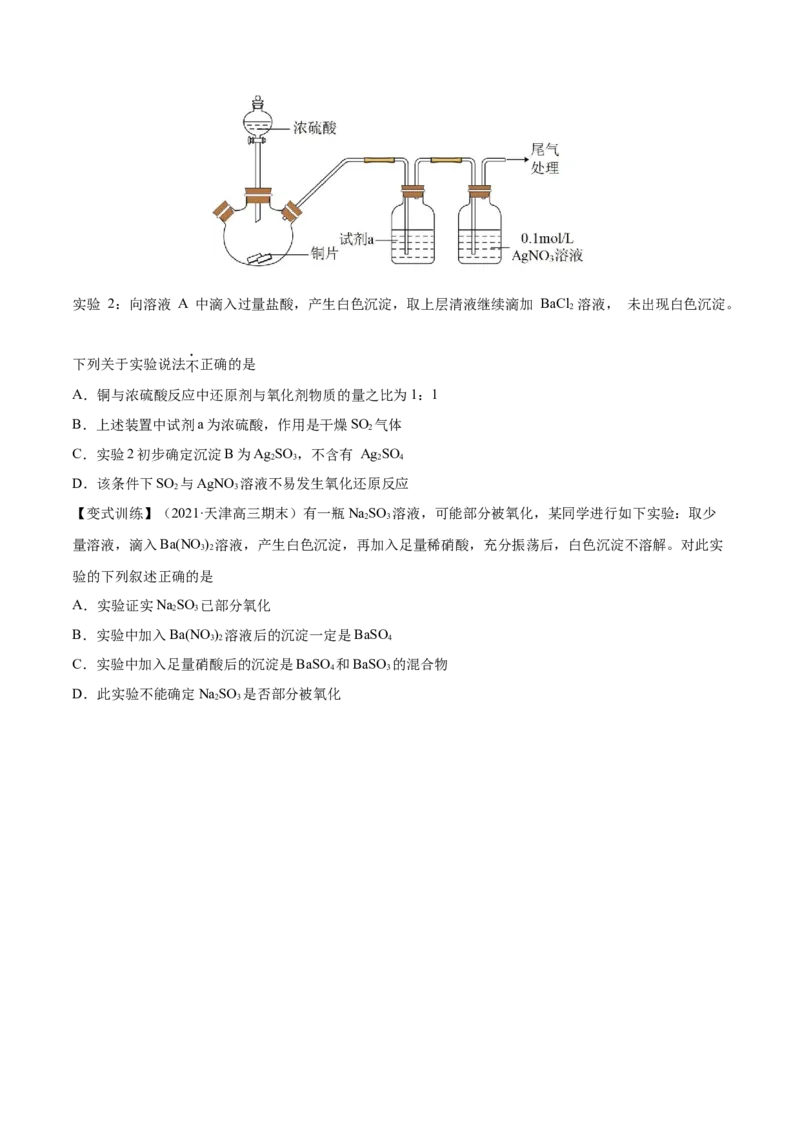
例6.(2022·江苏南通·模拟预测)化学小组为探究 SO 与 AgNO 溶液的反应,进行如下实验:
2 3
实验 1:用如下装置(夹持、加热仪器略)制备 SO ,将足量 SO 通入 AgNO 溶液中, 迅速反应,得到无
2 2 3
色溶液 A 和白色沉淀 B。实验 2:向溶液 A 中滴入过量盐酸,产生白色沉淀,取上层清液继续滴加 BaCl 溶液, 未出现白色沉淀。
2
下列关于实验说法不正确的是
A.铜与浓硫酸反应中还原剂与氧化剂物质的量之比为1:1
B.上述装置中试剂a为浓硫酸,作用是干燥SO 气体
2
C.实验2初步确定沉淀B为Ag SO ,不含有 Ag SO
2 3 2 4
D.该条件下SO 与AgNO 溶液不易发生氧化还原反应
2 3
【变式训练】(2021·天津高三期末)有一瓶NaSO 溶液,可能部分被氧化,某同学进行如下实验:取少
2 3
量溶液,滴入Ba(NO ) 溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,白色沉淀不溶解。对此实
3 2
验的下列叙述正确的是
A.实验证实NaSO 已部分氧化
2 3
B.实验中加入Ba(NO ) 溶液后的沉淀一定是BaSO
3 2 4
C.实验中加入足量硝酸后的沉淀是BaSO 和BaSO 的混合物
4 3
D.此实验不能确定NaSO 是否部分被氧化
2 3