文档内容
训练(四十七) 化学实验常用仪器及基本操作
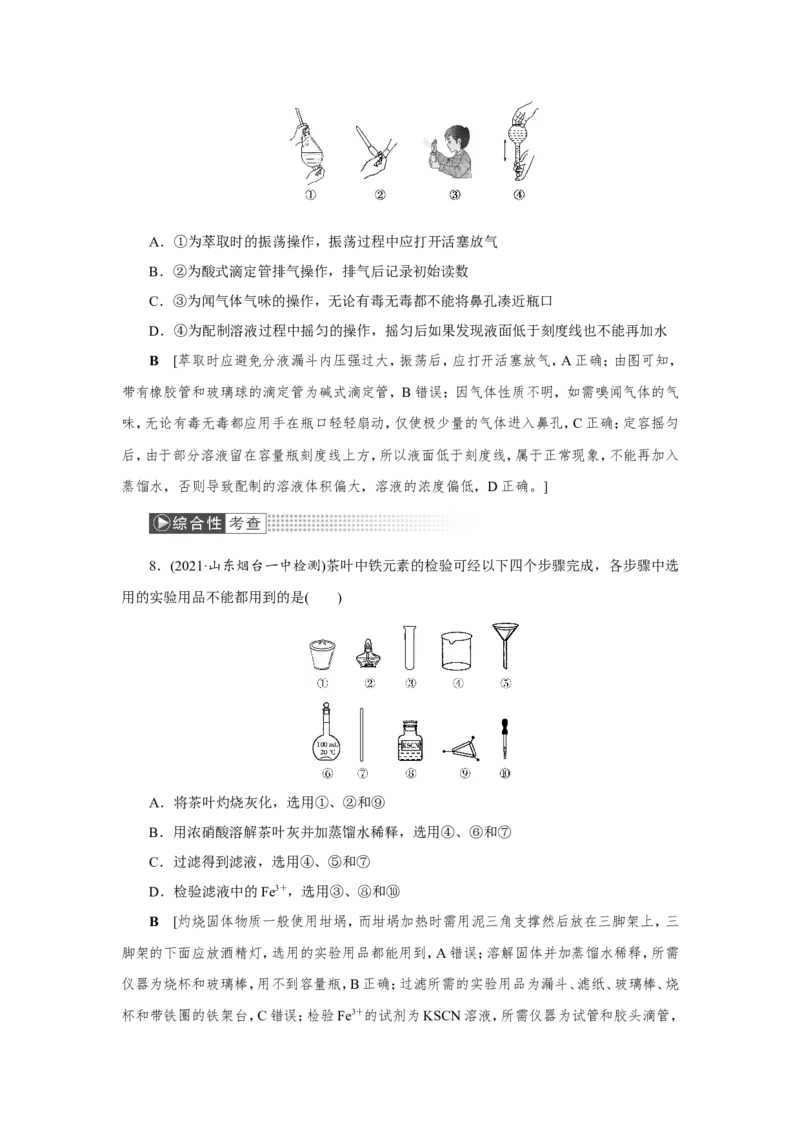
1.(2019·海南卷)某试剂瓶标签上安全标志如下图,该试剂是( )
A.氨水 B.乙酸
C.氢氧化钠 D.硝酸
D [氨水、乙酸和NaOH都属于腐蚀品,但都不是氧化剂;硝酸具有强氧化性,且具有
较强的腐蚀性,D项正确。]
2.(2021·重庆第一中学检测)安全是顺利进行实验及避免伤害的保障。如图实验操作正
确但不是从实验安全角度考虑的是( )
A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.操作②:移动蒸发皿
C.操作③:吸收氨或氯化氢气体并防止倒吸
D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
D [A项,漏斗中有空气,操作不正确;B项,不能用手直接拿加热的蒸发皿;D项,操作
正确,容量瓶漏水没有安全隐患。]
3.(2018·全国卷Ⅲ)下列实验操作不当的是( )
A.用稀硫酸和锌粒制取H 时,加几滴CuSO 溶液以加快反应速率
2 4
B.用标准HCl溶液滴定NaHCO 溶液来测定其浓度,选择酚酞为指示剂
3
C.用铂丝蘸取某碱金属的盐溶液燃烧,火焰呈黄色,证明其中含有Na+
D.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二
B [用标准盐酸滴定NaHCO 溶液,滴定至终点时溶液呈弱酸性,应选用甲基橙作指示
3
剂,B项错误;加几滴CuSO 溶液发生反应:Zn+Cu2+===Zn2++Cu,Zn与置换出来的Cu及
4
稀HSO 构成Cu—Zn原电池,加快了放出H 的速率,A项正确;黄色是钠元素的焰色,C项
2 4 2正确;常压蒸馏时,加入液体的体积既不能太少,也不能超过圆底烧瓶容积的三分之二,D项
正确。]
4.(2020·山东等级模拟考)实验室提供的玻璃仪器有试管、导管、容量瓶、烧杯、酒精灯、
表面皿、玻璃棒(非玻璃仪器任选),选用上述仪器能完成的实验是( )
A.粗盐的提纯
B.制备乙酸乙酯
C.用四氯化碳萃取碘水中的碘
D.配制0.1 mol·L-1的盐酸溶液
B [A选项缺漏斗、蒸发皿;C选项缺分液漏斗;D选项缺量筒。]
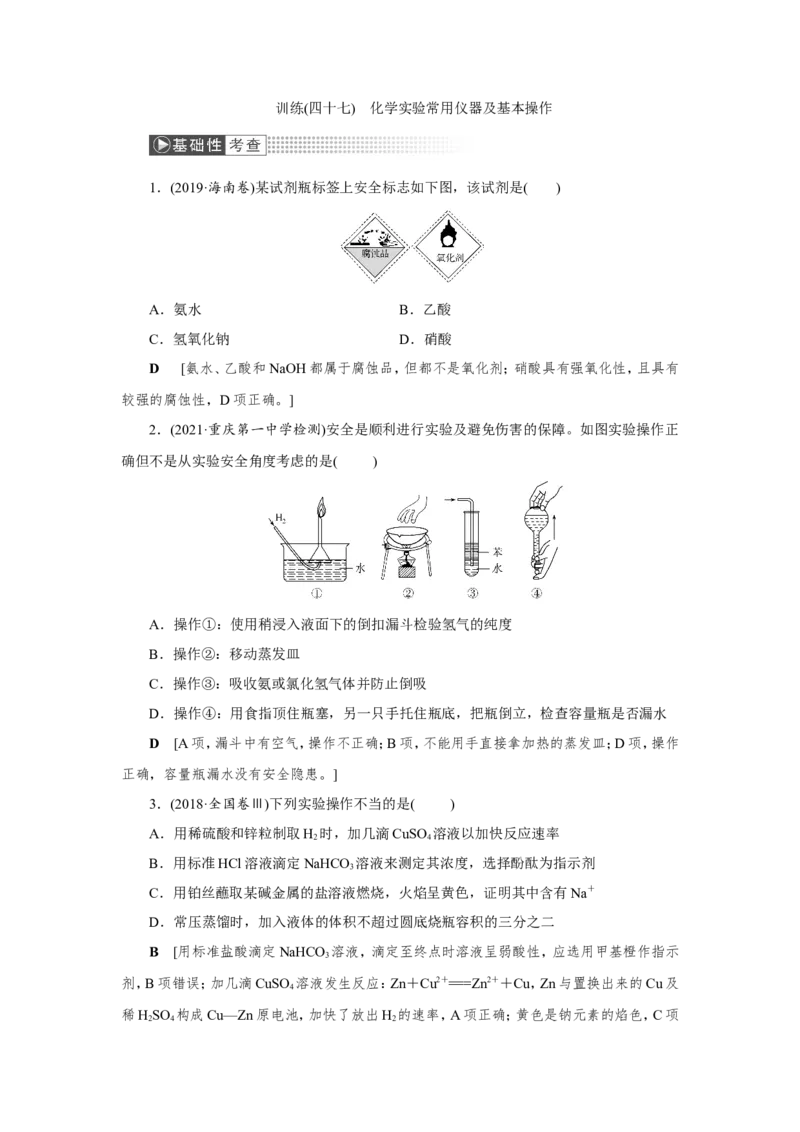
5.(2021·湖北武汉联考)实验室保存下列试剂,其中保存方法和理由描述都正确的是(
)
选项 试剂 保存方法 理由
防止与空气中水、氧气接触发生
A 钠 保存在煤油中
反应
B 液溴 液封保存在细口瓶中 防止升华
C 浓硝酸 密封保存在铁质容器中 避免见光分解
D 烧碱 存放在带有磨口玻璃塞的广口瓶中 防止与空气中氧气接触被氧化
A [B项防止液溴的挥发;C项中浓硝酸使铁制品钝化;D项,固体NaOH易潮解,能吸
收空气中的CO 变质,且不能存放在磨口塞的广口瓶中。]
2
6.(2021·山东实验中学检测)仅用下表提供的玻璃仪器(非玻璃仪器任选)就能达到相应
目的的是( )
选项 实验目的 实验仪器
A 除去KCl中的少量二氧化锰 烧杯、玻璃棒、分液漏斗
用 10 mol·L-1盐酸配制 100 mL 0.5
B 100 mL容量瓶、玻璃棒、烧杯、胶头滴管
mol·L-1盐酸
C 用碳酸钠溶液制备碳酸钠晶体 蒸发皿、酒精灯、玻璃棒
D 分离乙醇汽油中的乙醇和汽油 分液漏斗、烧杯
C [A项缺少漏斗,用不到分液漏斗;B项缺少量筒;D项汽油和乙醇互溶,必须用蒸馏
操作及相关仪器。]
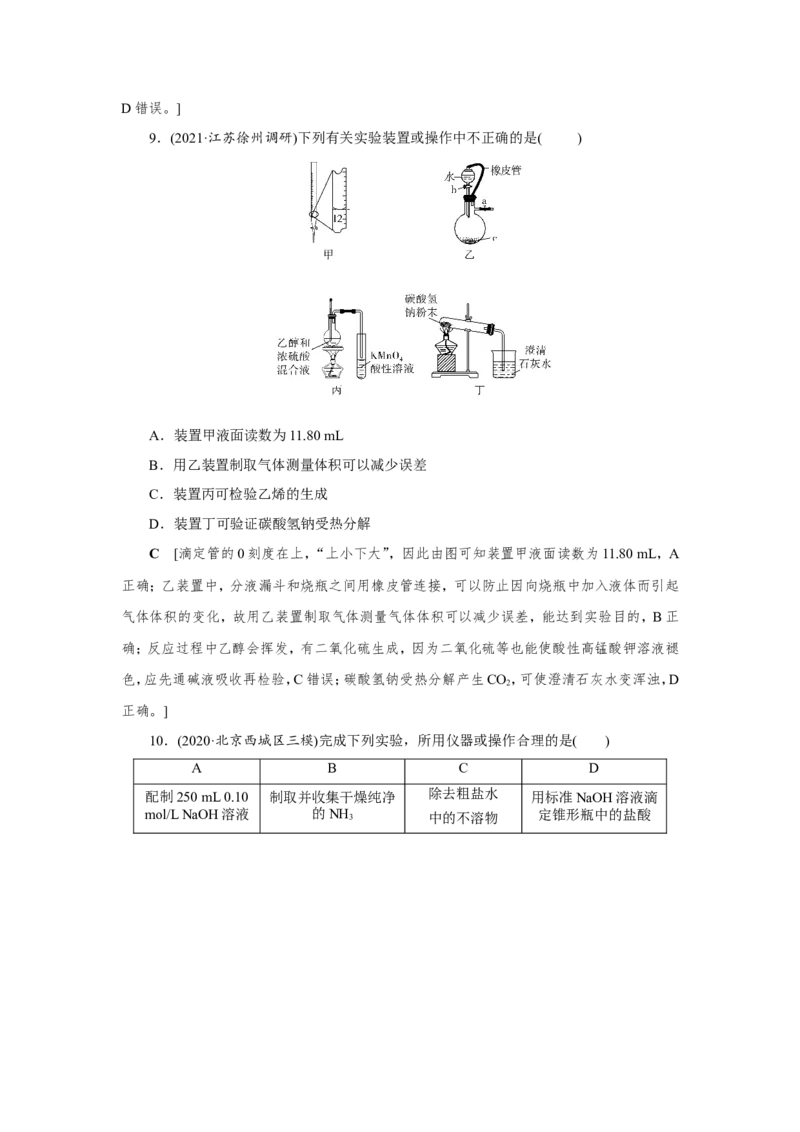
7.(2021·天津滨海新区四校联考)下列操作及其描述错误的是( )A.①为萃取时的振荡操作,振荡过程中应打开活塞放气
B.②为酸式滴定管排气操作,排气后记录初始读数
C.③为闻气体气味的操作,无论有毒无毒都不能将鼻孔凑近瓶口
D.④为配制溶液过程中摇匀的操作,摇匀后如果发现液面低于刻度线也不能再加水
B [萃取时应避免分液漏斗内压强过大,振荡后,应打开活塞放气,A正确;由图可知,
带有橡胶管和玻璃球的滴定管为碱式滴定管,B错误;因气体性质不明,如需嗅闻气体的气
味,无论有毒无毒都应用手在瓶口轻轻扇动,仅使极少量的气体进入鼻孔,C正确;定容摇匀
后,由于部分溶液留在容量瓶刻度线上方,所以液面低于刻度线,属于正常现象,不能再加入
蒸馏水,否则导致配制的溶液体积偏大,溶液的浓度偏低,D正确。]
8.(2021·山东烟台一中检测)茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选
用的实验用品不能都用到的是( )
A.将茶叶灼烧灰化,选用①、②和⑨
B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验滤液中的Fe3+,选用③、⑧和⑩
B [灼烧固体物质一般使用坩埚,而坩埚加热时需用泥三角支撑然后放在三脚架上,三
脚架的下面应放酒精灯,选用的实验用品都能用到,A错误;溶解固体并加蒸馏水稀释,所需
仪器为烧杯和玻璃棒,用不到容量瓶,B正确;过滤所需的实验用品为漏斗、滤纸、玻璃棒、烧
杯和带铁圈的铁架台,C错误;检验Fe3+的试剂为KSCN溶液,所需仪器为试管和胶头滴管,D错误。]
9.(2021·江苏徐州调研)下列有关实验装置或操作中不正确的是( )
A.装置甲液面读数为11.80 mL
B.用乙装置制取气体测量体积可以减少误差
C.装置丙可检验乙烯的生成
D.装置丁可验证碳酸氢钠受热分解
C [滴定管的0刻度在上,“上小下大”,因此由图可知装置甲液面读数为11.80 mL,A
正确;乙装置中,分液漏斗和烧瓶之间用橡皮管连接,可以防止因向烧瓶中加入液体而引起
气体体积的变化,故用乙装置制取气体测量气体体积可以减少误差,能达到实验目的,B正
确;反应过程中乙醇会挥发,有二氧化硫生成,因为二氧化硫等也能使酸性高锰酸钾溶液褪
色,应先通碱液吸收再检验,C错误;碳酸氢钠受热分解产生CO,可使澄清石灰水变浑浊,D
2
正确。]
10.(2020·北京西城区三模)完成下列实验,所用仪器或操作合理的是( )
A B C D
配制250 mL 0.10 制取并收集干燥纯净 除去粗盐水 用标准NaOH溶液滴
mol/L NaOH溶液 的NH 3 中的不溶物 定锥形瓶中的盐酸C [配制 0.10 mol/L NaOH溶液时,NaOH固体要在烧杯中溶解,不能直接在容量瓶中
溶解,A错误;NH 的密度小于空气的密度,要采用向下排空气法收集,要将集气瓶倒立,且
3
导管插入集气瓶底部,B错误;采用过滤法除去粗盐水中的不溶物,C正确;中和滴定时,眼
睛要注视锥形瓶中溶液颜色的变化,不能注视滴定管中液面,D错误。]
11.(2019·全国卷Ⅲ,27题节选)乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通
过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
水杨酸 醋酸酐 乙酰水杨酸
熔点/℃ 157~159 -72~-74 135~138
相对密度/(g·cm-3) 1.44 1.10 1.35
相对分子质量 138 102 180
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全
溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如
下操作。
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
回答下列问题:
(1)该合成反应中应采用________加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的有_______________________(填名称)。
解析 (1)由题给信息“维持瓶内温度在70 ℃左右”可知,该反应中应采用热水浴加热。
(2)①中涉及过滤操作,需要用到题给玻璃仪器中的烧杯、漏斗,不需要使用题给玻璃仪器中
的分液漏斗和容量瓶。
答案 (1)A (2)BD 分液漏斗、容量瓶
12.(2018·全国卷Ⅰ,26节选)醋酸亚铬[(CHCOO)Cr·2H O]为砖红色晶体,难溶于冷水,
3 2 2
易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还
原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如
图所示。回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是___________________。仪器a的
名称是_________________________________________________________________。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,
关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为________________________。
②同时c中有气体产生,该气体的作用是__________________________________。
答案 (1)去除水中溶解氧 分液(或滴液)漏斗
(2)①Zn+2Cr3+===Zn2++2Cr2+
②排除c中空气
13.(2021·安徽蚌埠质检)实验室制备无水二氯化锡的主要步骤如下:
步骤1:在圆底烧瓶中加入1.20 g碎锡箔和5 mL浓盐酸、1滴硝酸,实验装置如图所示。
组装好后在95 ℃时回流0.5 h,待圆底烧瓶中只剩余少量锡箔为止;步骤2:将上述反应的上清液迅速转移到仪器X中,在二氧化碳气氛保护下,蒸发浓缩,
冷却结晶,过滤得到二氯化锡晶体;
步骤3:在二氯化锡晶体中加入10 mL醋酸酐,即可得无水二氯化锡,过滤;
步骤4:用少量乙醚冲洗三次,置于通风橱内,待乙醚全部挥发后得到无水二氯化锡。
回答下列问题:
(1)步骤1中,圆底烧瓶中发生反应的化学方程式为____________________________;
(2)冷却水从接口_____(填“a”或“b”)进入。实验采取的加热方式是______________;球
形冷凝管上连接装有碱石灰的干燥管的目的是_______________________________。
(3) 步 骤 2 中 , 仪 器 X 的 名 称 为 __________ ; 二 氧 化 碳 气 氛 的 作 用 是
________________________________________________________________________。
(4)步骤3中,醋酸酐的作用是________;二氯化锡晶体在进行步骤3操作前应采取的加
工措施是________,该加工措施需要仪器的名称是________。
解析 (1)Sn 和浓盐酸反应生成 SnCl 和 H ,反应的化学方程式为 Sn+
2 2
2HCl(浓)=====SnCl +H↑,为了充分冷却蒸气且防止温度过高的蒸气急剧冷却而炸裂冷凝
2 2
管,则冷凝管中的水是逆流的,所以a是进水口、b是出水口;温度小于100 ℃时采用水浴加
热的方法,所以该实验的条件是95 ℃水浴加热;浓盐酸易挥发,挥发出的HCl会污染空气,
所以尾气要处理。(2)蒸发浓缩溶液的仪器是蒸发皿;Sn2+不稳定,易被空气氧化,故需要在二
氧化碳气氛中进行。(3)醋酸酐能和水反应生成醋酸,则醋酸酐有吸水作用;二氯化锡的晶体
表面积越大时,除去晶体中的水分越充分,所以在操作3之前必须将其研碎;研碎晶体的仪
器是研钵。
答案 (1)Sn+2HCl(浓)=====SnCl +H↑
2 2
(2)a 95 ℃水浴加热 吸收HCl,防止HCl气体进入空气
(3)蒸发皿 防止空气中的氧气氧化Sn2+
(4)吸水 研碎 研钵