文档内容
第 29 讲 原子结构与性质
1.下列叙述错误的是( )
A.所有的非金属元素都在p区
B.磷的价电子排布式为3s23p3
C.碱金属元素具有较小的电负性
D.当各原子轨道处于全充满、半充满、全空时原子较稳定
2.下列有关电子排布图的表述正确的是( )
A. 可表示单核10电子粒子基态时电子排布
B. 此图错误,违背了泡利原理
C. 表示基态N原子的价电子排布
D. 表示处于激发态的B的电子排布图
3.下列说法正确的是( )
A.Fe3+的最外层电子排布式为3s23p63d5
B.高温时CuO比Cu O稳定
2
C.基态碳原子价电子的轨道表示式:
D.元素周期表每一周期元素原子的最外层电子排布均是从ns1过渡到ns2np6
4.人们通常将在同一原子轨道上运动、自旋状态相反的2个电子,称为“电子对”,将在某一原子轨道上
运动的单个电子,称为“未成对电子”。下列基态原子的电子排布式中,未成对电子数最多的是( )
A.1s22s22p63s23p6
B.1s22s22p63s23p63d54s2
C.1s22s22p63s23p63d54s1
D.1s22s22p63s23p63d104s1
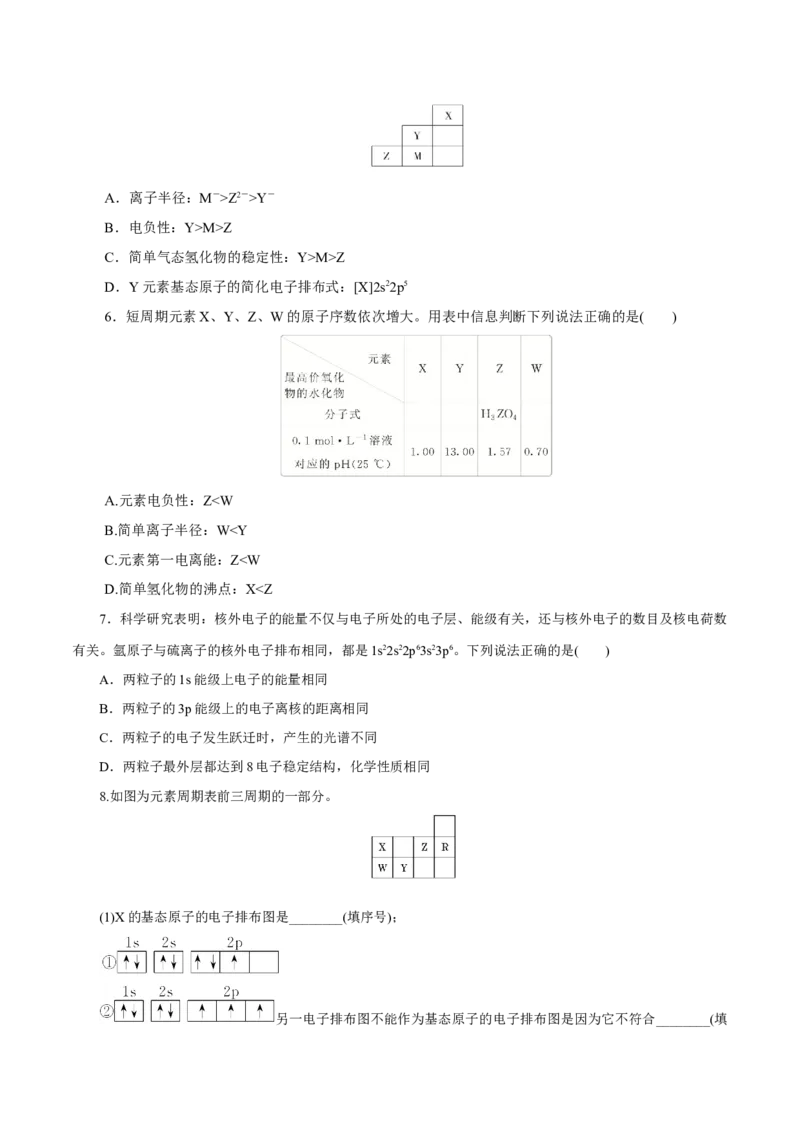
5.如图为元素周期表中短周期的一部分,下列说法不正确的是( )A.离子半径:M->Z2->Y-
B.电负性:Y>M>Z
C.简单气态氢化物的稳定性:Y>M>Z
D.Y元素基态原子的简化电子排布式:[X]2s22p5
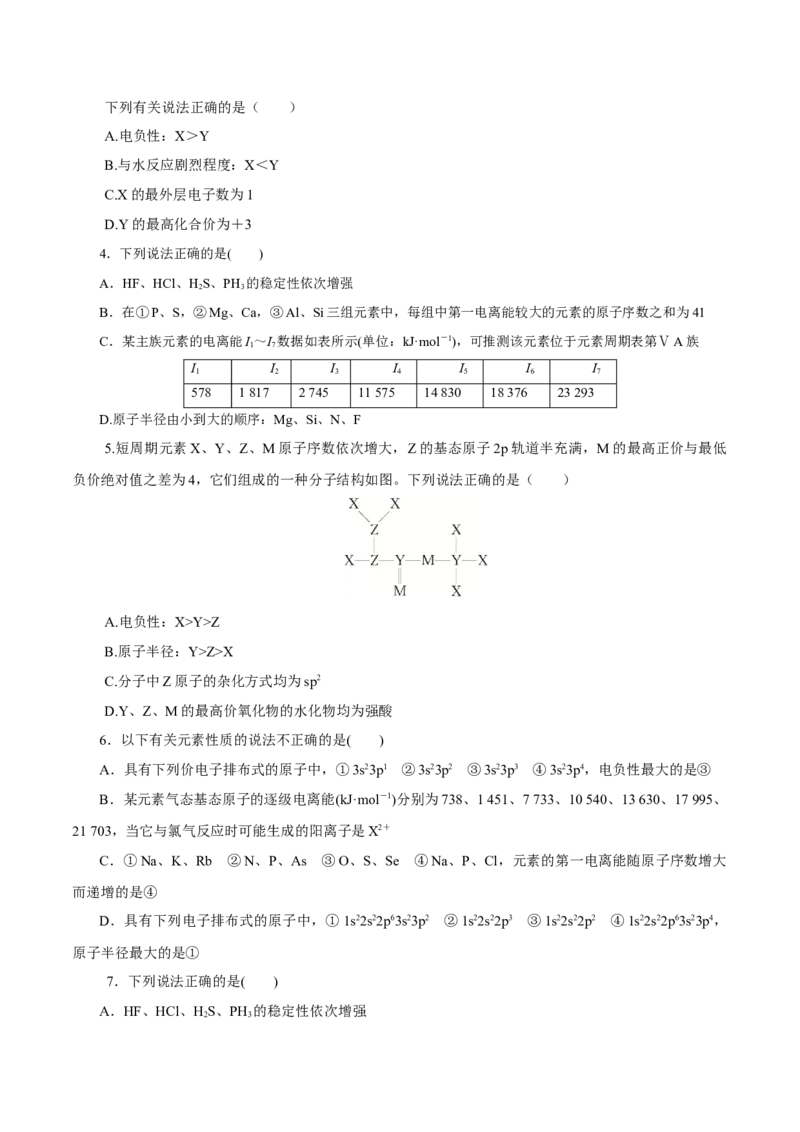
6.短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是( )
A.元素电负性:Z③>②>①
B.原子半径:②>①>④>③
C.电负性:④>③>②>①
D.最高正化合价:④>③=②>①
3.X、Y是同周期的两种主族元素,它们的逐级电离能(I)数据如下表所示:
电离能
I I I I I ……
1 2 3 4 5
(kJ/mol)
X 496 4562 6912 9543 13353 ……
Y 738 1451 7733 10540 13630 ……下列有关说法正确的是( )
A.电负性:X>Y
B.与水反应剧烈程度:X<Y
C.X的最外层电子数为1
D.Y的最高化合价为+3
4.下列说法正确的是( )
A.HF、HCl、HS、PH 的稳定性依次增强
2 3
B.在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为41
C.某主族元素的电离能I~I 数据如表所示(单位:kJ·mol-1),可推测该元素位于元素周期表第ⅤA族
1 7
I I I I I I I
1 2 3 4 5 6 7
578 1 817 2 745 11 575 14 830 18 376 23 293
D.原子半径由小到大的顺序:Mg、Si、N、F
5.短周期元素X、Y、Z、M原子序数依次增大,Z的基态原子2p轨道半充满,M的最高正价与最低
负价绝对值之差为4,它们组成的一种分子结构如图。下列说法正确的是( )
A.电负性:X>Y>Z
B.原子半径:Y>Z>X
C.分子中Z原子的杂化方式均为sp2
D.Y、Z、M的最高价氧化物的水化物均为强酸
6.以下有关元素性质的说法不正确的是( )
A.具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,电负性最大的是③
B.某元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、
21 703,当它与氯气反应时可能生成的阳离子是X2+
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的第一电离能随原子序数增大
而递增的是④
D.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,
原子半径最大的是①
7.下列说法正确的是( )
A.HF、HCl、HS、PH 的稳定性依次增强
2 3B.在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为
41
C.某主族元素的电离能I ~I 数据如表所示(单位:kJ·mol-1),可推测该元素位于元素周期表第ⅤA
1 7
族
I I I I I I I
1 2 3 4 5 6 7
578 1 817 2 745 11 575 14 830 18 376 23 293
D.原子半径由小到大的顺序:Mg、Si、N、F
8.(1)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性小的元素
是 ;26号元素价层电子排布式为 ;L原子核外电子占有9个轨道,而且有一个未成对电
子,L是 元素。
(2)硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
①基态硒原子的价层电子排布式为 。
②锗、砷、硒三种元素的第一电离能大小排序为 。
③下列说法正确的是 (填字母)。
A.第一电离能:As>Ga
B.电负性:As>Ga
C.原子半径:As>Ga
④锗(Ge)是用途很广的半导体材料,基态锗原子的价层电子排布式为 。在第二周期中,第
一电离能位于硼元素与氮元素之间的元素有 种。
⑤硼(B)及其化合物在化学中有重要的地位。Ga与B同主族,Ga的基态原子的核外电子排布式为
,B、C、O三种元素的第一电离能由大到小的顺序是 。
(3)已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y
元素原子的最外层2p轨道上有2个未成对电子。X与Y可形成化合物XY,Z元素可以形成负一价离子。
2 3
①X元素基态原子的电子排布式为 ,该元素的化学符号是 。
②Y元素原子的价层电子排布图为 ,该元素的名称是 。
③已知化合物XY 在稀硫酸中可被金属锌还原为XZ ,产物还有ZnSO 和HO,该反应的化学方程式
2 3 3 4 2
是 。
1.[2019·高考全国卷Ⅲ,35(1)]在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基
态原子核外M层电子的自旋状态________(填“相同”或“相反”)。2.[2019·高考全国卷Ⅱ,35(2)]Fe成为阳离子时首先失去________轨道电子,Sm的价层电子排布式为
4f66s2,Sm3+价层电子排布式为________。
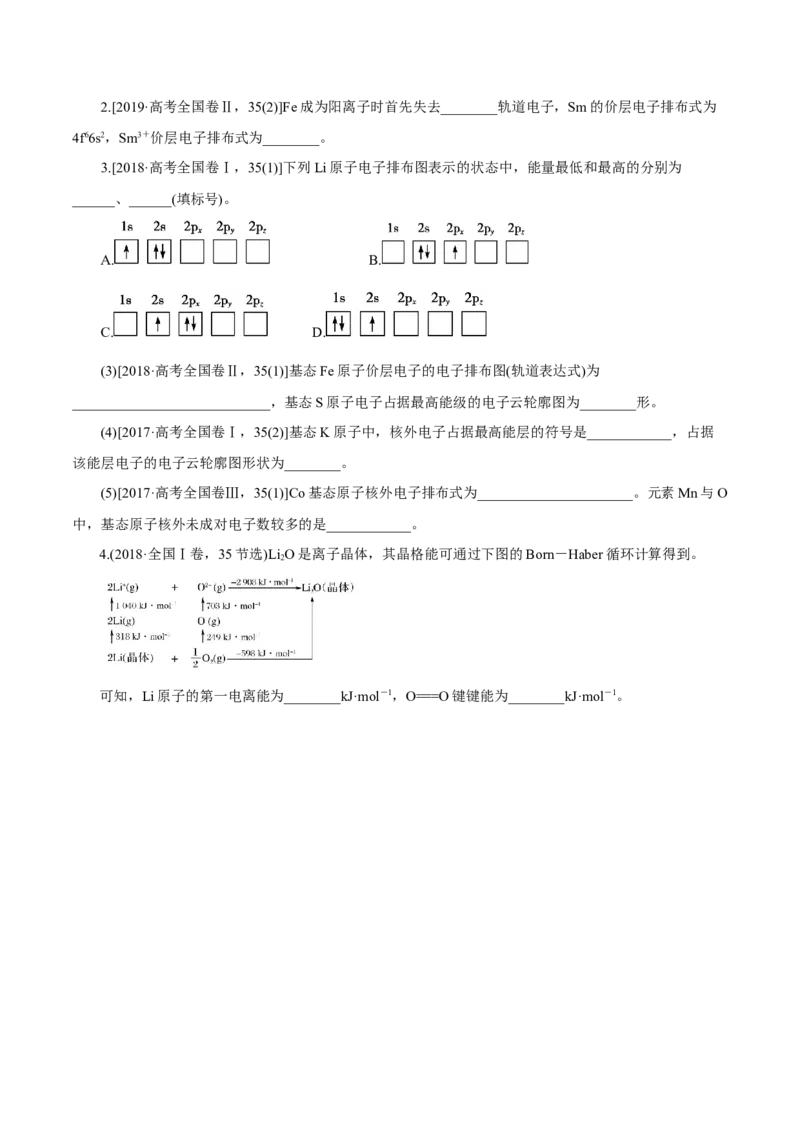
3.[2018·高考全国卷Ⅰ,35(1)]下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
______、______(填标号)。
A. B.
C. D.
(3)[2018·高考全国卷Ⅱ,35(1)]基态Fe原子价层电子的电子排布图(轨道表达式)为
____________________________,基态S原子电子占据最高能级的电子云轮廓图为________形。
(4)[2017·高考全国卷Ⅰ,35(2)]基态K原子中,核外电子占据最高能层的符号是____________,占据
该能层电子的电子云轮廓图形状为________。
(5)[2017·高考全国卷Ⅲ,35(1)]Co基态原子核外电子排布式为______________________。元素Mn与O
中,基态原子核外未成对电子数较多的是____________。
4.(2018·全国Ⅰ卷,35节选)Li O是离子晶体,其晶格能可通过下图的Born-Haber循环计算得到。
2
可知,Li原子的第一电离能为________kJ·mol-1,O===O键键能为________kJ·mol-1。