文档内容
专题 12 化学反应与电能
第 34 练 原电池
1.下列装置中能构成原电池的是( )
A. B. C. D.
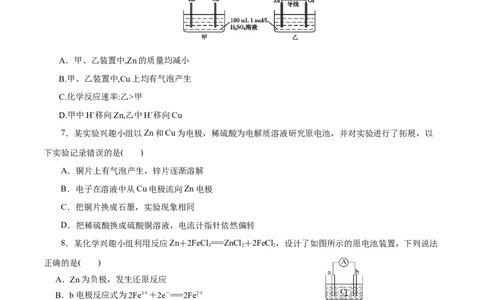
2.某原电池的总反应为Zn+Cu2+=Zn2++Cu,该原电池的正确构成是( )
A. B. C. D.
3.铜锌原电池如图所示,电解质溶液为硫酸铜。下列说法错误的是( )
A.锌电极将逐渐被腐蚀
B.铜电极为正极,发生氧化反应
C.铜电极上的反应为:Cu2++2e-=Cu
D.电子从锌电极经过导线流向铜电极
4.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验
装置
部分实 电流从a极流向d
a极质量减小; b极有气体产生; d极溶解;
验现象 极b极质量增加 c极无变化 c极有气体产生
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
5.在盛有稀硫酸的烧杯中放入用导线连接的铁片和铜片,下列说法正确的是( )
A.铁片上有气泡逸出 B.电子通过导线由铜流向铁
C.溶液中H+向铜片移动 D.铁片上发生氧化反应:Fe-3e-=Fe3+
6.有甲、乙两个装置,下列说法错误的是( )
A.甲、乙装置中,Zn的质量均减小
B.甲、乙装置中,Cu上均有气泡产生
C.化学反应速率:乙>甲
D.甲中H+移向Zn,乙中H+移向Cu
7.某实验兴趣小组以Zn和Cu为电极,稀硫酸为电解质溶液研究原电池,并对实验进行了拓展,以
下实验记录错误的是( )
A.铜片上有气泡产生,锌片逐渐溶解
B.电子在溶液中从Cu电极流向Zn电极
C.把铜片换成石墨,实验现象相同
D.把稀硫酸换成硫酸铜溶液,电流计指针依然偏转
8.某化学兴趣小组利用反应Zn+2FeCl ===ZnCl+2FeCl ,设计了如图所示的原电池装置,下列说法
3 2 2
正确的是( )
A.Zn为负极,发生还原反应
B.b电极反应式为2Fe3++2e-===2Fe2+
C.电子流动方向是a电极→FeCl 溶液→b电极
3
D.电池的正极材料可以选用石墨、铂电极,也可以用铜
9.如图所示装置中,电流表G指针发生偏转,同时Y极逐渐变粗,X极逐渐变细。下列判断正确的
是( )A.X是Zn,Y是Cu,Z为HSO 溶液
2 4
B.X是Cu,Y是Zn,Z为HSO 溶液
2 4
C.X是Zn,Y是Cu,Z为酒精溶液
D.X是Zn,Y是Cu,Z为CuSO 溶液
4
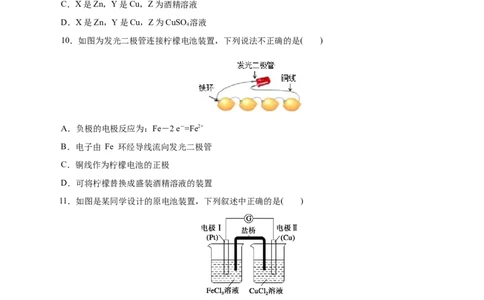
10.如图为发光二极管连接柠檬电池装置,下列说法不正确的是( )
A.负极的电极反应为:Fe-2 e-=Fe2+
B.电子由 Fe 环经导线流向发光二极管
C.铜线作为柠檬电池的正极
D.可将柠檬替换成盛装酒精溶液的装置
11.如图是某同学设计的原电池装置,下列叙述中正确的是( )
A.电极Ⅰ上发生还原反应,作原电池的负极
B.该原电池的总反应为2Fe3++Cu=Cu2++2Fe2+
C.电极Ⅱ的电极反应为Cu2++2e-=Cu
D.盐桥中装有含琼胶的氯化钾饱和溶液,其作用是传递电子
12.某原电池装置示意图如图所示,下列有关该原电池的说法正确的是( )A.锌片是正极,铁片是负极
B.锌片上发生的电极反应:2H++2e-=H ↑
2
C.电子由铁电极经导线流向锌电极
D.如果将锌片换成铜片,电路中的电流方向改变
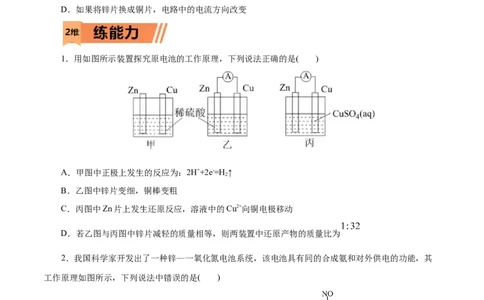
1.用如图所示装置探究原电池的工作原理,下列说法正确的是( )
A.甲图中正极上发生的反应为:2H++2e-=H ↑
2
B.乙图中锌片变细,铜棒变粗
C.丙图中Zn片上发生还原反应,溶液中的Cu2+向铜电极移动
D.若乙图与丙图中锌片减轻的质量相等,则两装置中还原产物的质量比为
2.我国科学家开发出了一种锌—一氧化氮电池系统,该电池具有同的合成氨和对外供电的功能,其
工作原理如图所示,下列说法中错误的是( )
A.电极电势:Zn /ZnO电极<M S 电极
O 2B.Zn /ZnO电极的反应式为Zn+2OH--2e- =ZnO+HO
2
C.电池工作一段时间后,正极区溶液的 减小
D.电子流向:Zn /ZnO电极→负载→M S 电极
O 2
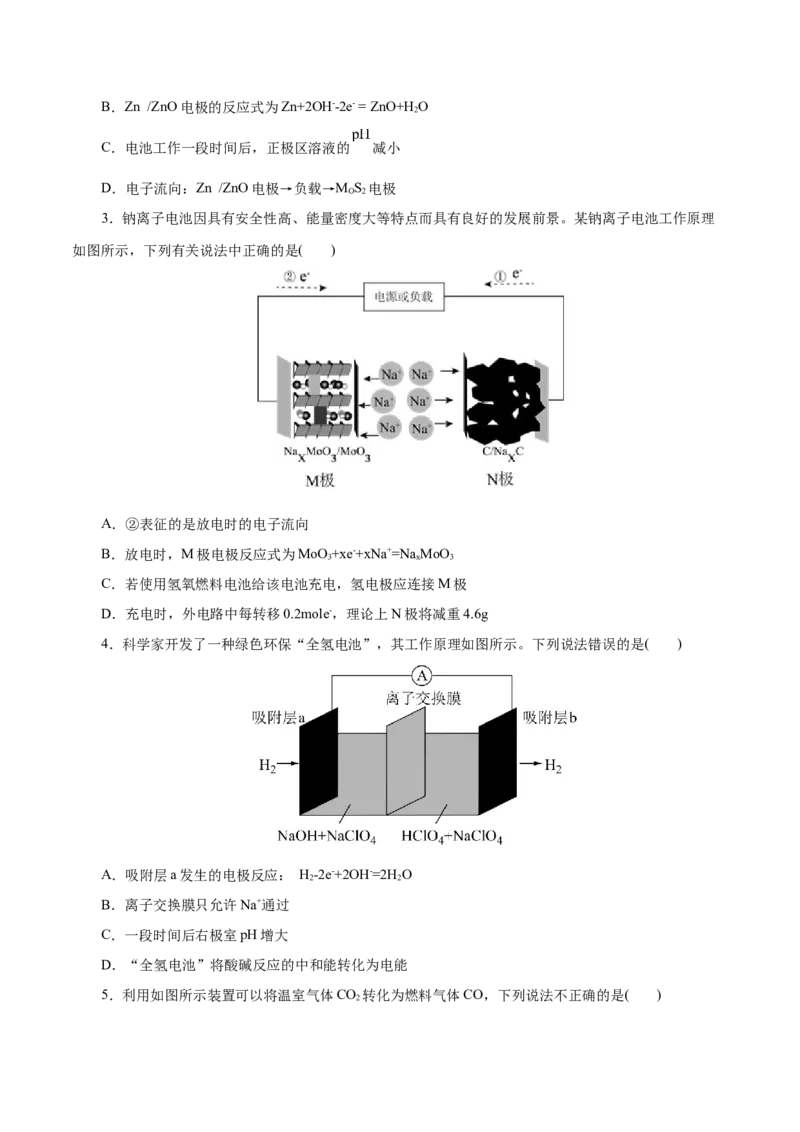
3.钠离子电池因具有安全性高、能量密度大等特点而具有良好的发展前景。某钠离子电池工作原理
如图所示,下列有关说法中正确的是( )
A.②表征的是放电时的电子流向
B.放电时,M极电极反应式为MoO +xe-+xNa+=Na MoO
3 x 3
C.若使用氢氧燃料电池给该电池充电,氢电极应连接M极
D.充电时,外电路中每转移0.2mole-,理论上N极将减重4.6g
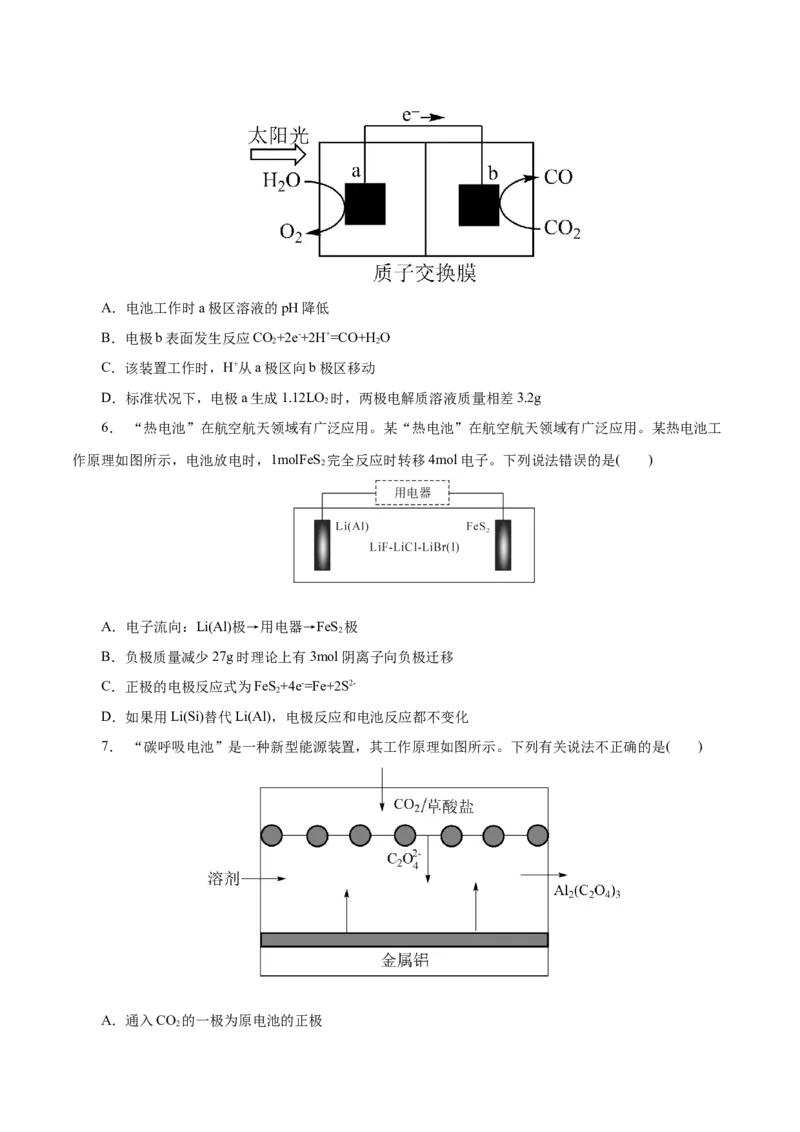
4.科学家开发了一种绿色环保“全氢电池”,其工作原理如图所示。下列说法错误的是( )
A.吸附层a发生的电极反应: H-2e-+2OH-=2H O
2 2
B.离子交换膜只允许Na+通过
C.一段时间后右极室pH增大
D.“全氢电池”将酸碱反应的中和能转化为电能
5.利用如图所示装置可以将温室气体CO 转化为燃料气体CO,下列说法不正确的是( )
2A.电池工作时a极区溶液的pH降低
B.电极b表面发生反应CO+2e-+2H+=CO+H O
2 2
C.该装置工作时,H+从a极区向b极区移动
D.标准状况下,电极a生成1.12LO 时,两极电解质溶液质量相差3.2g
2
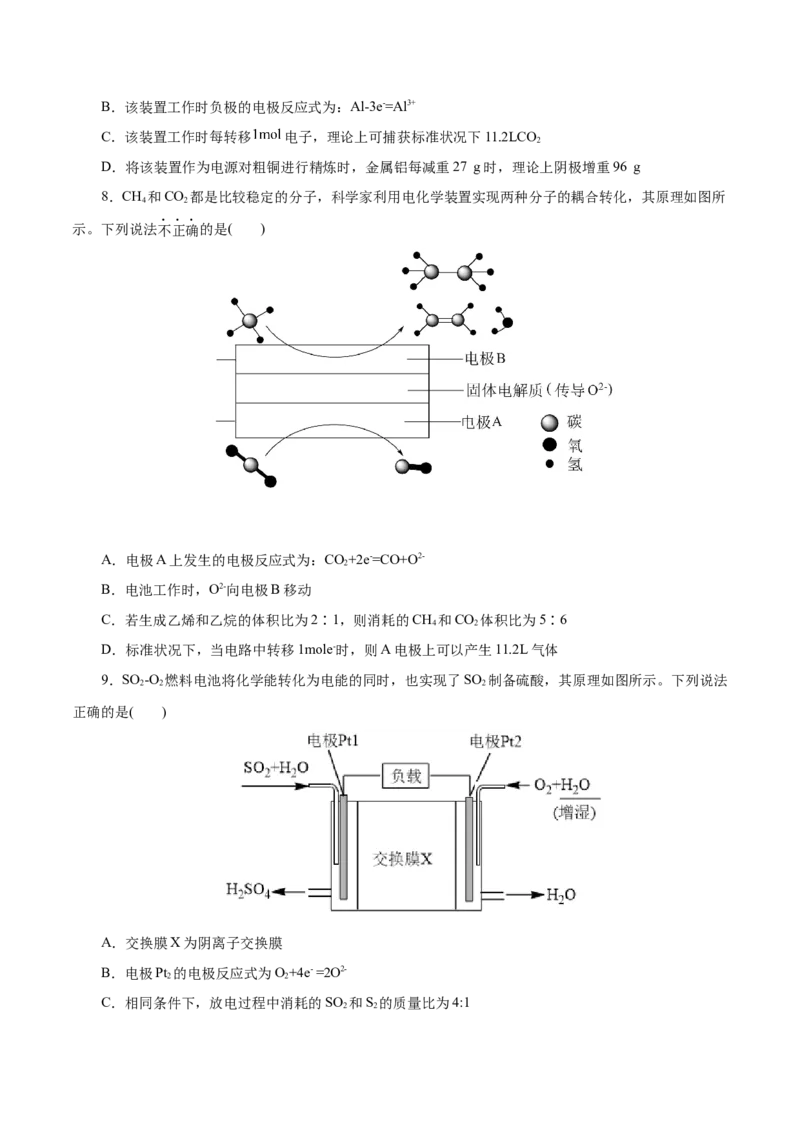
6. “热电池”在航空航天领域有广泛应用。某“热电池”在航空航天领域有广泛应用。某热电池工
作原理如图所示,电池放电时,1molFeS 完全反应时转移4mol电子。下列说法错误的是( )
2
A.电子流向:Li(Al)极→用电器→FeS 极
2
B.负极质量减少27g时理论上有3mol阴离子向负极迁移
C.正极的电极反应式为FeS+4e-=Fe+2S2-
2
D.如果用Li(Si)替代Li(Al),电极反应和电池反应都不变化
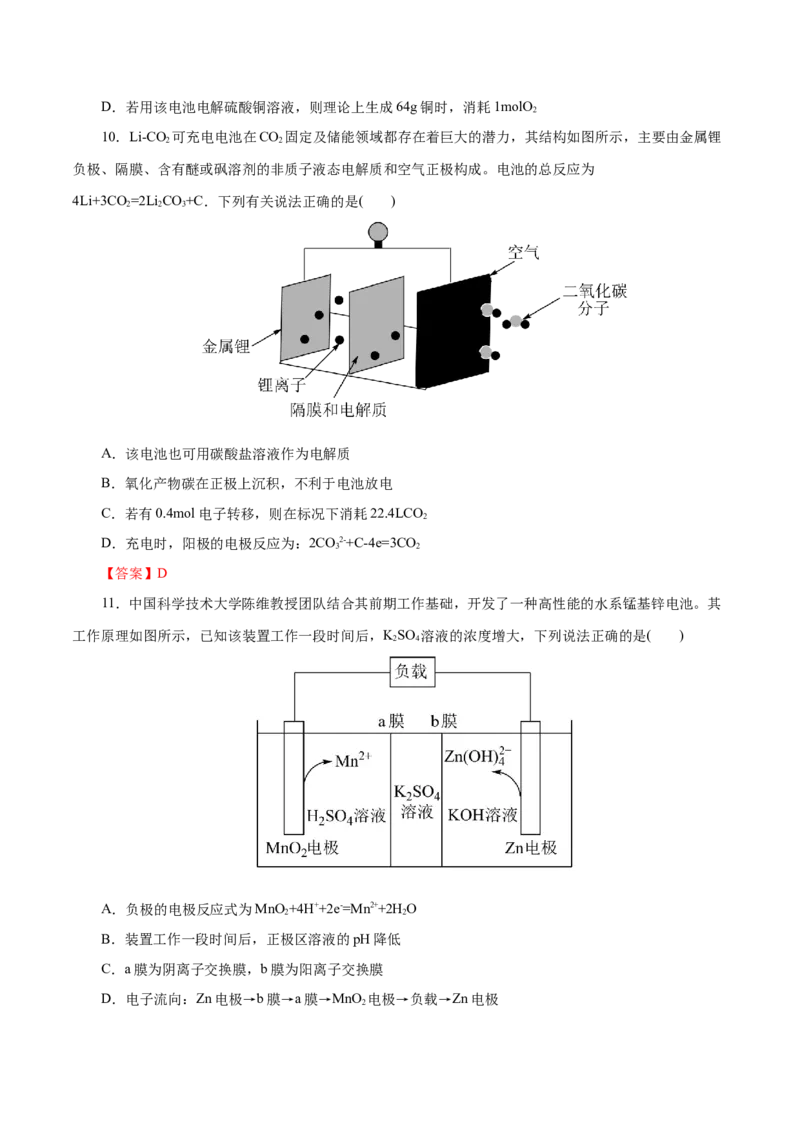
7. “碳呼吸电池”是一种新型能源装置,其工作原理如图所示。下列有关说法不正确的是( )
A.通入CO 的一极为原电池的正极
2B.该装置工作时负极的电极反应式为:Al-3e-=Al3+
C.该装置工作时每转移 电子,理论上可捕获标准状况下11.2LCO
2
D.将该装置作为电源对粗铜进行精炼时,金属铝每减重27 g时,理论上阴极增重96 g
8.CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所
4 2
示。下列说法不正确的是( )
A.电极A上发生的电极反应式为:CO+2e-=CO+O2-
2
B.电池工作时,O2-向电极B移动
C.若生成乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为5∶6
4 2
D.标准状况下,当电路中转移1mole-时,则A电极上可以产生11.2L气体
9.SO -O 燃料电池将化学能转化为电能的同时,也实现了SO 制备硫酸,其原理如图所示。下列说法
2 2 2
正确的是( )
A.交换膜X为阴离子交换膜
B.电极Pt 的电极反应式为O+4e- =2O2-
2 2
C.相同条件下,放电过程中消耗的SO 和S 的质量比为4:1
2 2D.若用该电池电解硫酸铜溶液,则理论上生成64g铜时,消耗1molO
2
10.Li-CO 可充电电池在CO 固定及储能领域都存在着巨大的潜力,其结构如图所示,主要由金属锂
2 2
负极、隔膜、含有醚或砜溶剂的非质子液态电解质和空气正极构成。电池的总反应为
4Li+3CO=2Li CO+C.下列有关说法正确的是( )
2 2 3
A.该电池也可用碳酸盐溶液作为电解质
B.氧化产物碳在正极上沉积,不利于电池放电
C.若有0.4mol电子转移,则在标况下消耗22.4LCO
2
D.充电时,阳极的电极反应为:2CO2-+C-4e=3CO
3 2
【答案】D
11.中国科学技术大学陈维教授团队结合其前期工作基础,开发了一种高性能的水系锰基锌电池。其
工作原理如图所示,已知该装置工作一段时间后,KSO 溶液的浓度增大,下列说法正确的是( )
2 4
A.负极的电极反应式为MnO+4H++2e-=Mn2++2H O
2 2
B.装置工作一段时间后,正极区溶液的pH降低
C.a膜为阴离子交换膜,b膜为阳离子交换膜
D.电子流向:Zn电极→b膜→a膜→MnO 电极→负载→Zn电极
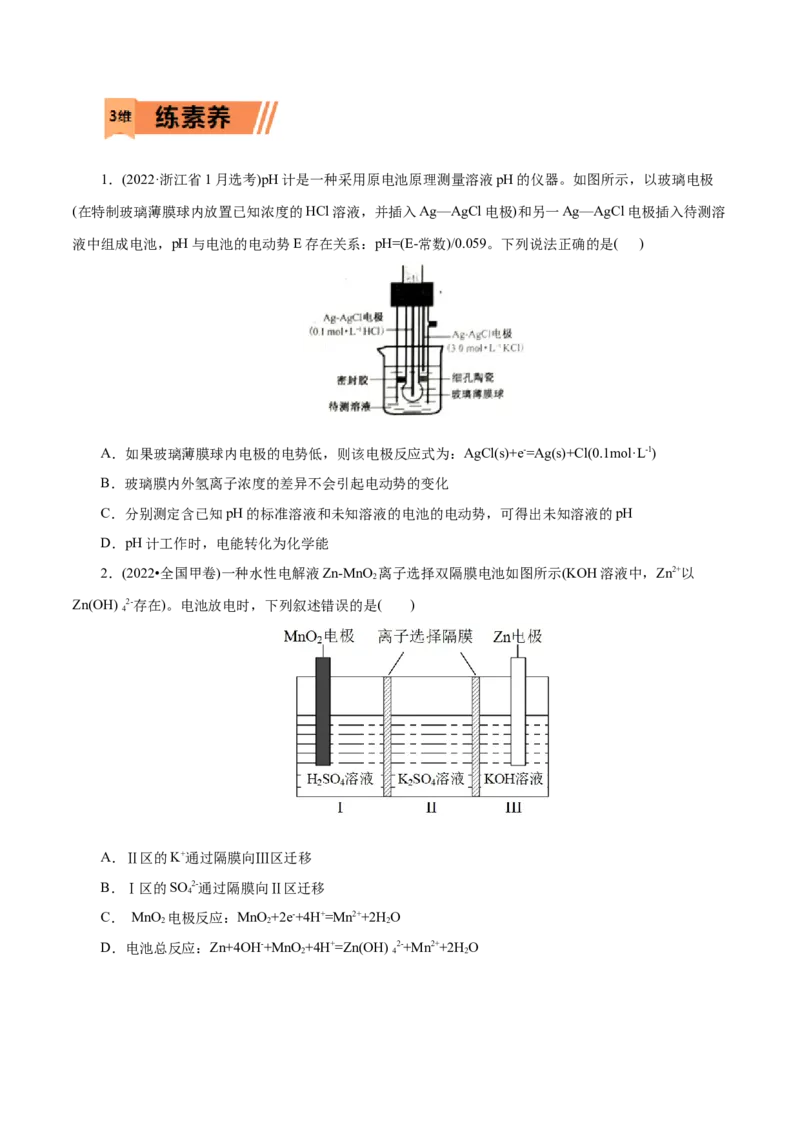
21.(2022·浙江省1月选考)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电极
(在特制玻璃薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测溶
液中组成电池,pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是( )
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
2.(2022•全国甲卷)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 2-存在)。电池放电时,下列叙述错误的是( )
4
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 2-通过隔膜向Ⅱ区迁移
4
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O
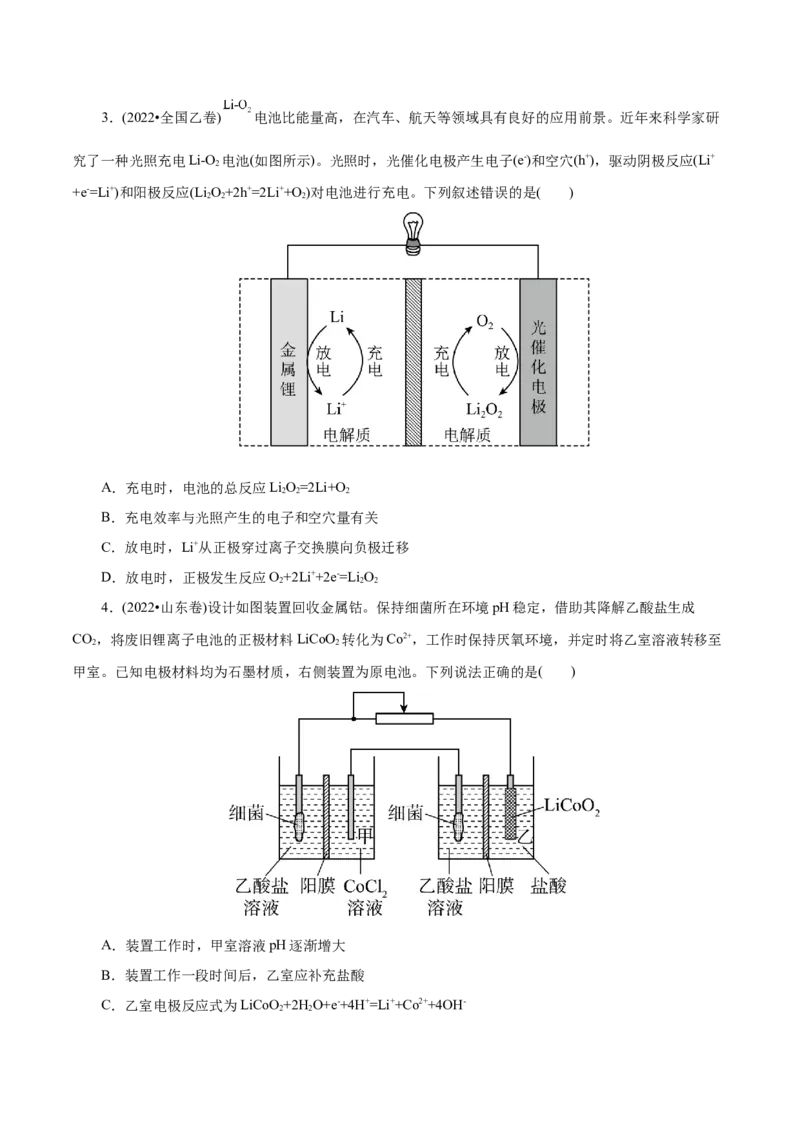
2 4 23.(2022•全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研
究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动阴极反应(Li+
2
+e-=Li+)和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是( )
2 2 2
A.充电时,电池的总反应LiO=2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应O+2Li++2e-=Li O
2 2 2
4.(2022•山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成
CO,将废旧锂离子电池的正极材料LiCoO 转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液转移至
2 2
甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是( )
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为LiCoO +2H O+e-+4H+=Li++Co2++4OH-
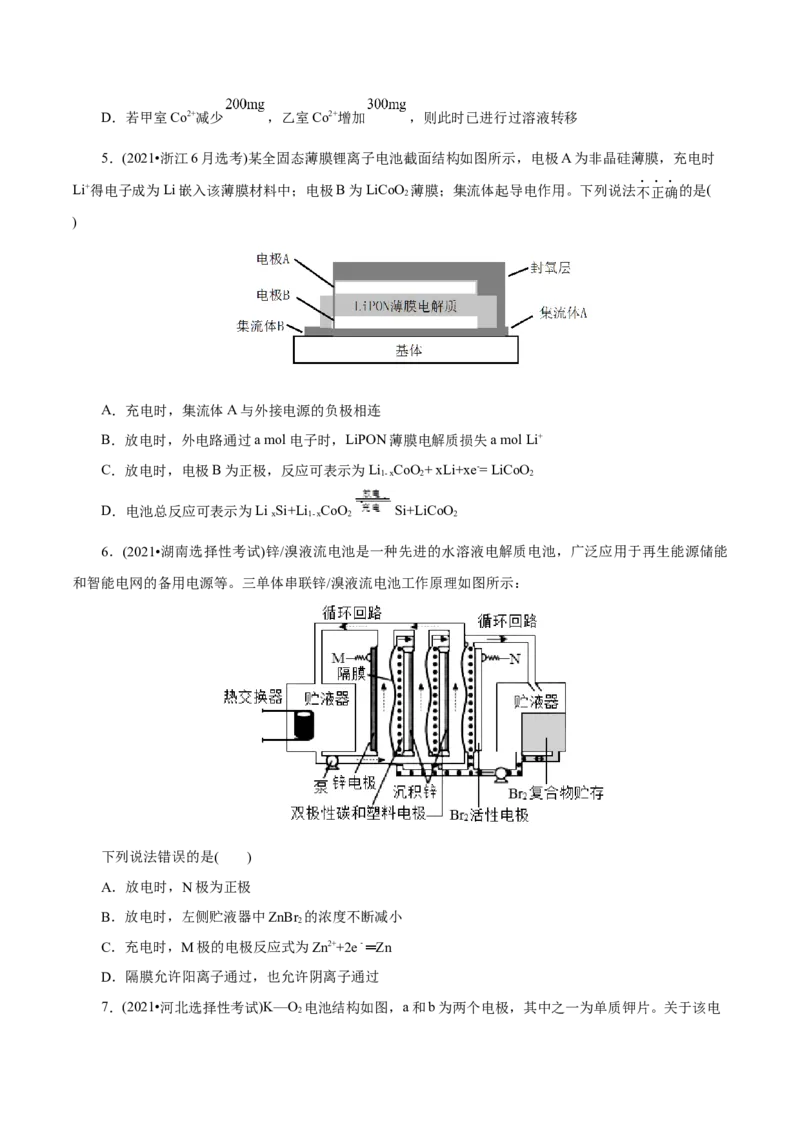
2 2D.若甲室Co2+减少 ,乙室Co2+增加 ,则此时已进行过溶液转移
5.(2021•浙江6月选考)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时
Li+得电子成为Li嵌入该薄膜材料中;电极B为LiCoO 薄膜;集流体起导电作用。下列说法不正确的是(
2
)
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过a mol电子时,LiPON薄膜电解质损失a mol Li+
C.放电时,电极B为正极,反应可表示为Li CoO+ xLi+xe-= LiCoO
1- x 2 2
D.电池总反应可表示为Li Si+Li CoO Si+LiCoO
x 1- x 2 2
6.(2021•湖南选择性考试)锌/溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能
和智能电网的备用电源等。三单体串联锌/溴液流电池工作原理如图所示:
下列说法错误的是( )
A.放电时,N极为正极
B.放电时,左侧贮液器中ZnBr 的浓度不断减小
2
C.充电时,M极的电极反应式为Zn2++2e﹣═Zn
D.隔膜允许阳离子通过,也允许阴离子通过
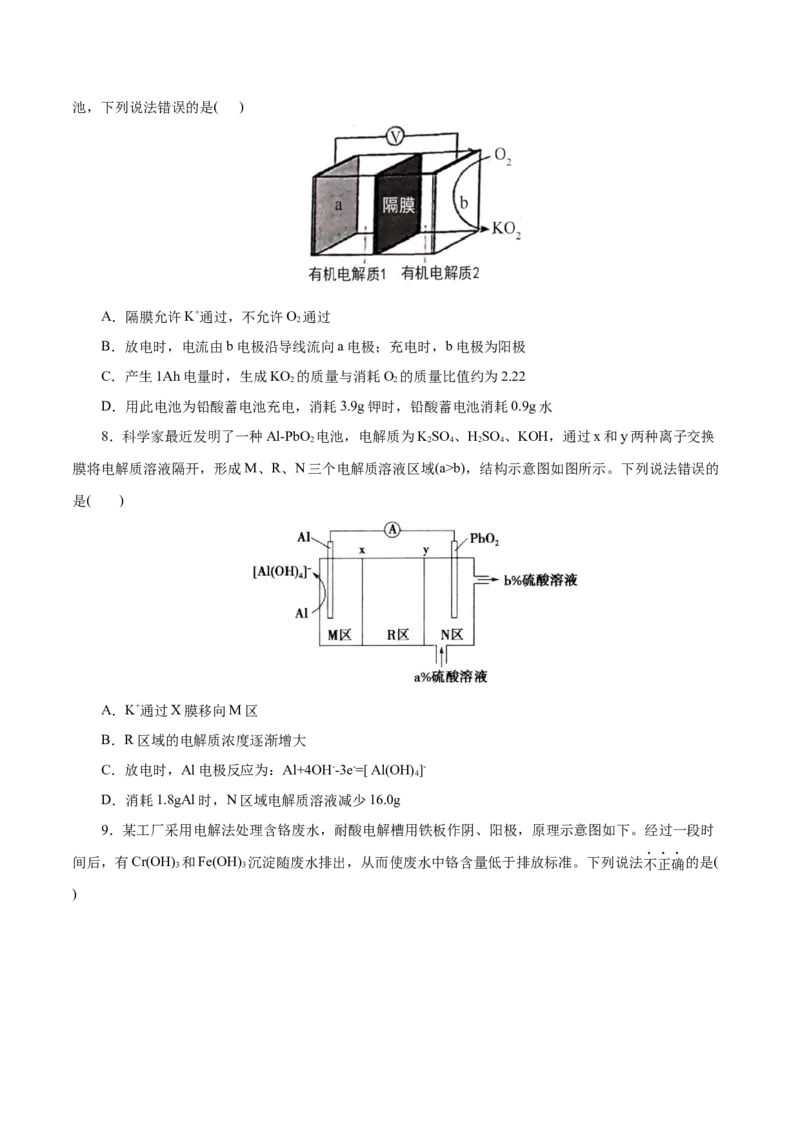
7.(2021•河北选择性考试)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电
2池,下列说法错误的是( )
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
8.科学家最近发明了一种Al-PbO 电池,电解质为KSO 、HSO 、KOH,通过x和y两种离子交换
2 2 4 2 4
膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域(a>b),结构示意图如图所示。下列说法错误的
是( )
A.K+通过X膜移向M区
B.R区域的电解质浓度逐渐增大
C.放电时,Al电极反应为:Al+4OH--3e-=[ Al(OH) ]-
4
D.消耗1.8gAl时,N区域电解质溶液减少16.0g
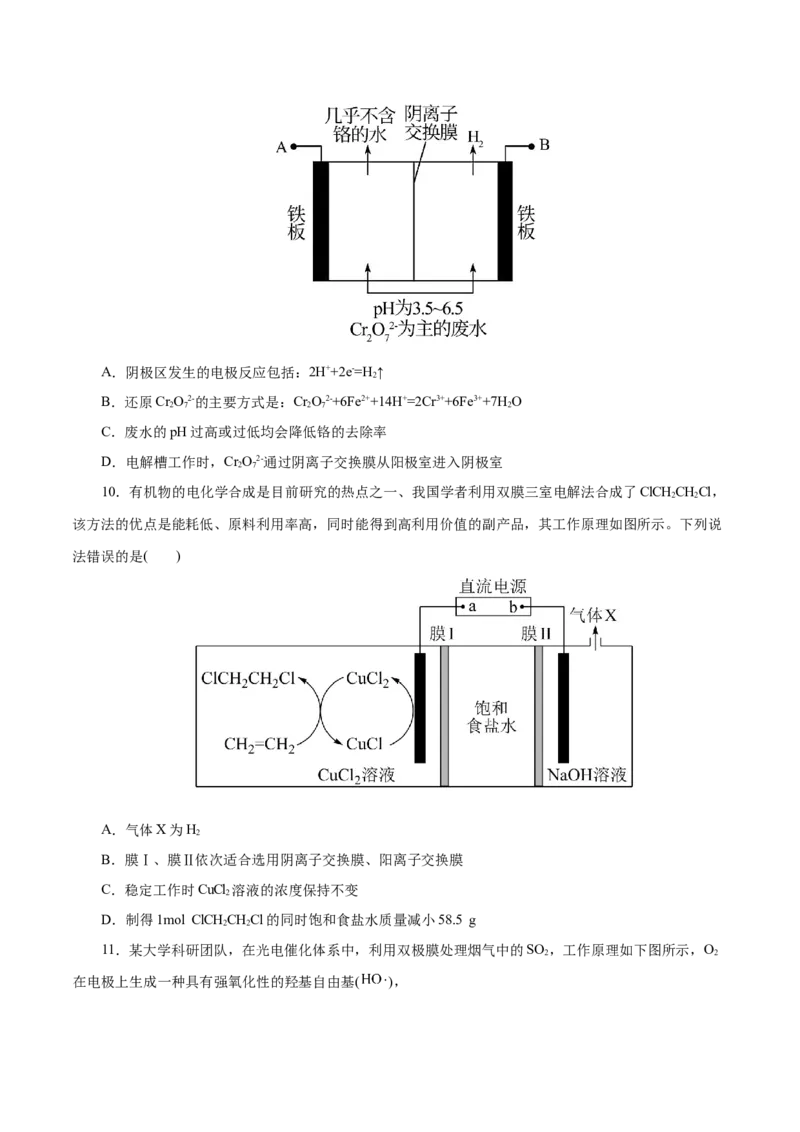
9.某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,原理示意图如下。经过一段时
间后,有Cr(OH) 和Fe(OH) 沉淀随废水排出,从而使废水中铬含量低于排放标准。下列说法不正确的是(
3 3
)A.阴极区发生的电极反应包括:2H++2e-=H ↑
2
B.还原CrO2-的主要方式是:CrO2-+6Fe2++14H+=2Cr3++6Fe3++7H O
2 7 2 7 2
C.废水的pH过高或过低均会降低铬的去除率
D.电解槽工作时,CrO2-通过阴离子交换膜从阳极室进入阴极室
2 7
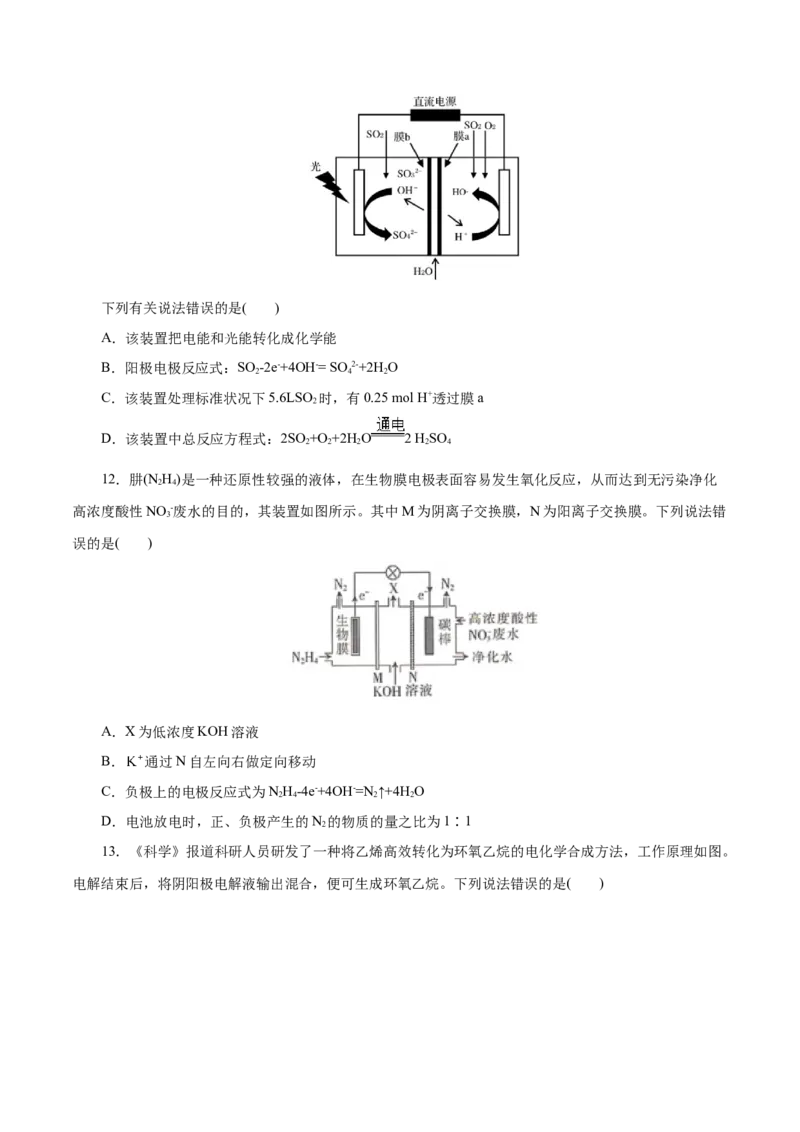
10.有机物的电化学合成是目前研究的热点之一、我国学者利用双膜三室电解法合成了ClCH CHCl,
2 2
该方法的优点是能耗低、原料利用率高,同时能得到高利用价值的副产品,其工作原理如图所示。下列说
法错误的是( )
A.气体X为H
2
B.膜Ⅰ、膜Ⅱ依次适合选用阴离子交换膜、阳离子交换膜
C.稳定工作时CuCl 溶液的浓度保持不变
2
D.制得1mol ClCH CHCl的同时饱和食盐水质量减小58.5 g
2 2
11.某大学科研团队,在光电催化体系中,利用双极膜处理烟气中的SO ,工作原理如下图所示,O
2 2
在电极上生成一种具有强氧化性的羟基自由基( ),下列有关说法错误的是( )
A.该装置把电能和光能转化成化学能
B.阳极电极反应式:SO -2e-+4OH-= SO 2-+2H O
2 4 2
C.该装置处理标准状况下5.6LSO 时,有0.25 mol H+透过膜a
2
D.该装置中总反应方程式:2SO +O +2H O 2 H SO
2 2 2 2 4
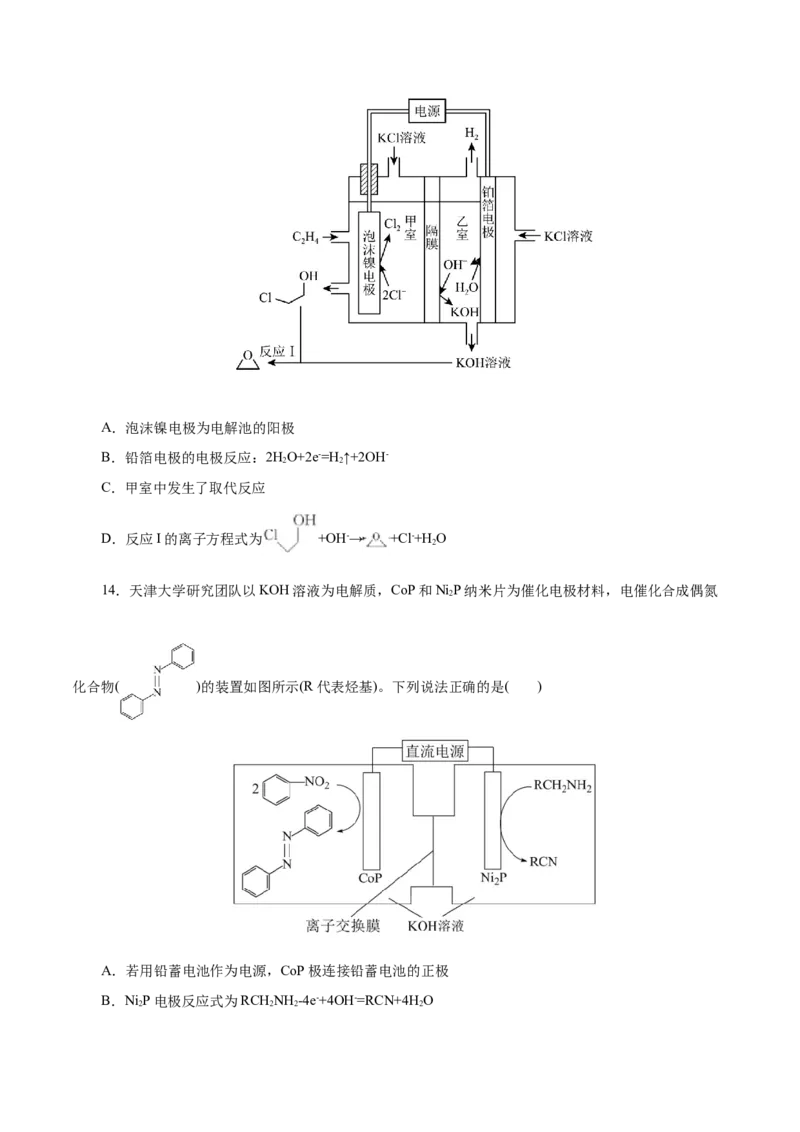
12.肼(N H)是一种还原性较强的液体,在生物膜电极表面容易发生氧化反应,从而达到无污染净化
2 4
高浓度酸性NO -废水的目的,其装置如图所示。其中M为阴离子交换膜,N为阳离子交换膜。下列说法错
3
误的是( )
A.X为低浓度KOH溶液
B. 通过N自左向右做定向移动
C.负极上的电极反应式为NH-4e-+4OH-=N ↑+4H O
2 4 2 2
D.电池放电时,正、负极产生的N 的物质的量之比为1∶1
2
13.《科学》报道科研人员研发了一种将乙烯高效转化为环氧乙烷的电化学合成方法,工作原理如图。
电解结束后,将阴阳极电解液输出混合,便可生成环氧乙烷。下列说法错误的是( )A.泡沫镍电极为电解池的阳极
B.铅箔电极的电极反应:2HO+2e-=H ↑+2OH-
2 2
C.甲室中发生了取代反应
D.反应I的离子方程式为 +OH-→ +Cl-+H O
2
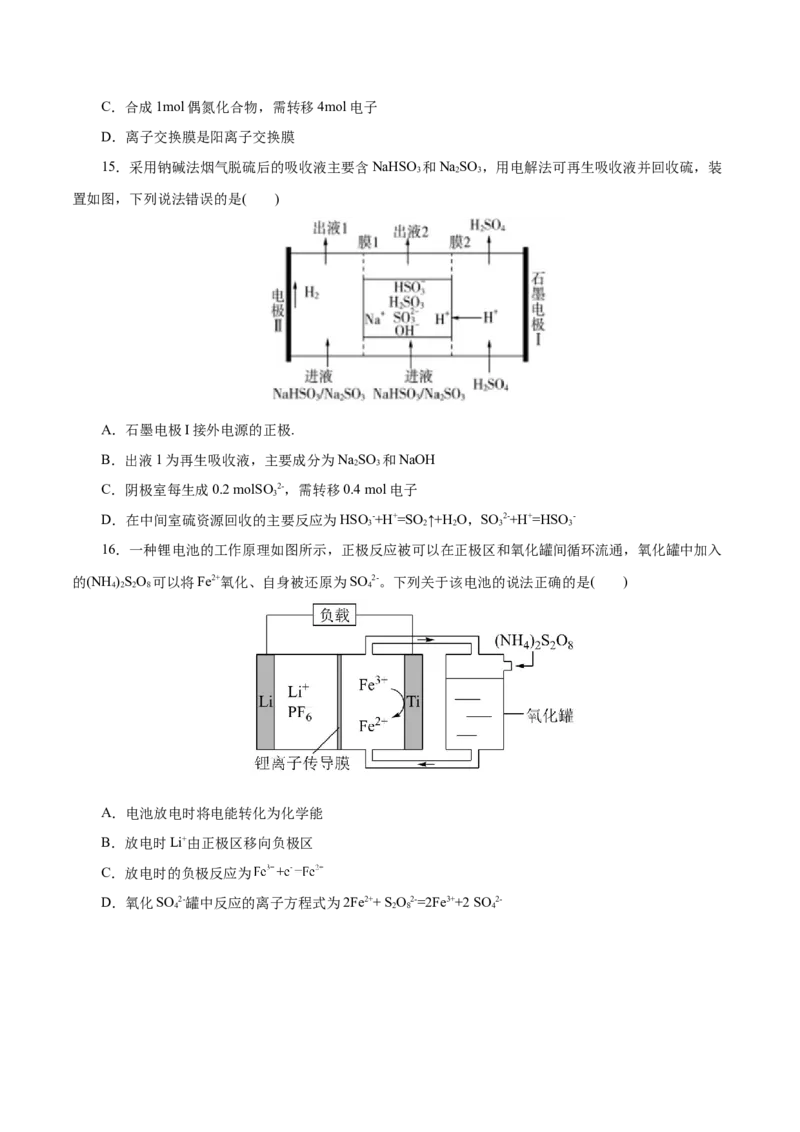
14.天津大学研究团队以KOH溶液为电解质,CoP和Ni P纳米片为催化电极材料,电催化合成偶氮
2
化合物( )的装置如图所示(R代表烃基)。下列说法正确的是( )
A.若用铅蓄电池作为电源,CoP极连接铅蓄电池的正极
B.Ni P电极反应式为RCHNH -4e-+4OH-=RCN+4H O
2 2 2 2C.合成1mol偶氮化合物,需转移4mol电子
D.离子交换膜是阳离子交换膜
15.采用钠碱法烟气脱硫后的吸收液主要含NaHSO 和NaSO ,用电解法可再生吸收液并回收硫,装
3 2 3
置如图,下列说法错误的是( )
A.石墨电极I接外电源的正极.
B.出液1为再生吸收液,主要成分为NaSO 和NaOH
2 3
C.阴极室每生成0.2 molSO 2-,需转移0.4 mol电子
3
D.在中间室硫资源回收的主要反应为HSO -+H+=SO↑+H O,SO 2-+H+=HSO -
3 2 2 3 3
16.一种锂电池的工作原理如图所示,正极反应被可以在正极区和氧化罐间循环流通,氧化罐中加入
的(NH )SO 可以将Fe2+氧化、自身被还原为SO 2-。下列关于该电池的说法正确的是( )
4 2 2 8 4
A.电池放电时将电能转化为化学能
B.放电时Li+由正极区移向负极区
C.放电时的负极反应为
D.氧化SO 2-罐中反应的离子方程式为2Fe2++ S O2-=2Fe3++2 SO 2-
4 2 8 4