文档内容
第 38 讲 晶体结构与性质
目录
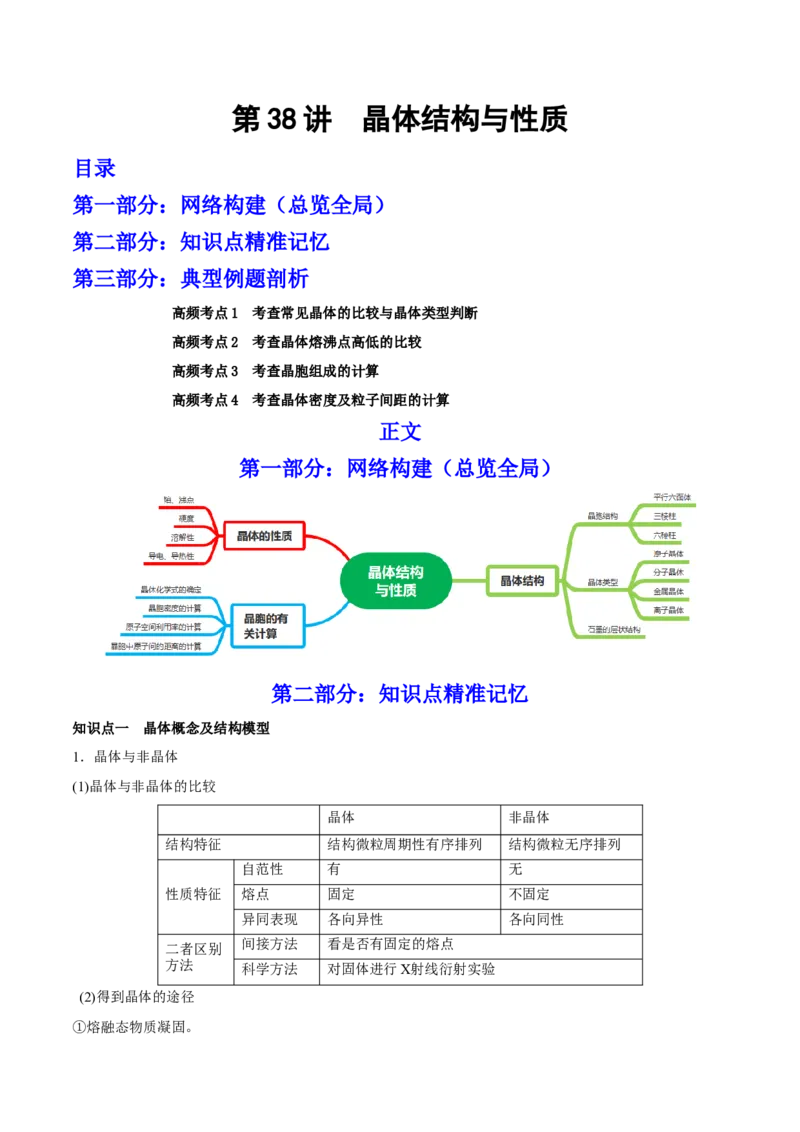
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查常见晶体的比较与晶体类型判断
高频考点2 考查晶体熔沸点高低的比较
高频考点3 考查晶胞组成的计算
高频考点4 考查晶体密度及粒子间距的计算
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 晶体概念及结构模型
1.晶体与非晶体
(1)晶体与非晶体的比较
晶体 非晶体
结构特征 结构微粒周期性有序排列 结构微粒无序排列
自范性 有 无
性质特征 熔点 固定 不固定
异同表现 各向异性 各向同性
间接方法 看是否有固定的熔点
二者区别
方法 科学方法 对固体进行X射线衍射实验
(2)得到晶体的途径
①熔融态物质凝固。②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
(3)晶胞
①概念:描述晶体结构的基本单元。
②晶体中晶胞的排列——无隙、并置
A.无隙:相邻晶胞之间没有任何间隙。
B.并置:所有晶胞平行排列、取向相同。
2.晶胞组成的计算——均摊法
(1)原则
晶胞任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份额就是。
(2)方法
①长方体(包括立方体)晶胞中不同位置的粒子数的计算。
②非长方体晶胞中粒子视具体情况而定,如石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)被三
个六边形共有,每个六边形占。
3.晶胞中粒子配位数的计算
一个粒子周围最邻近的粒子的数目称为配位数
(1)晶体中原子(或分子)的配位数:若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配位数
指的是该原子(或分子)最接近且等距离的原子(或分子)的数目。
(2)离子晶体的配位数:指一个离子周围最接近且等距离的异种电性离子的数目。
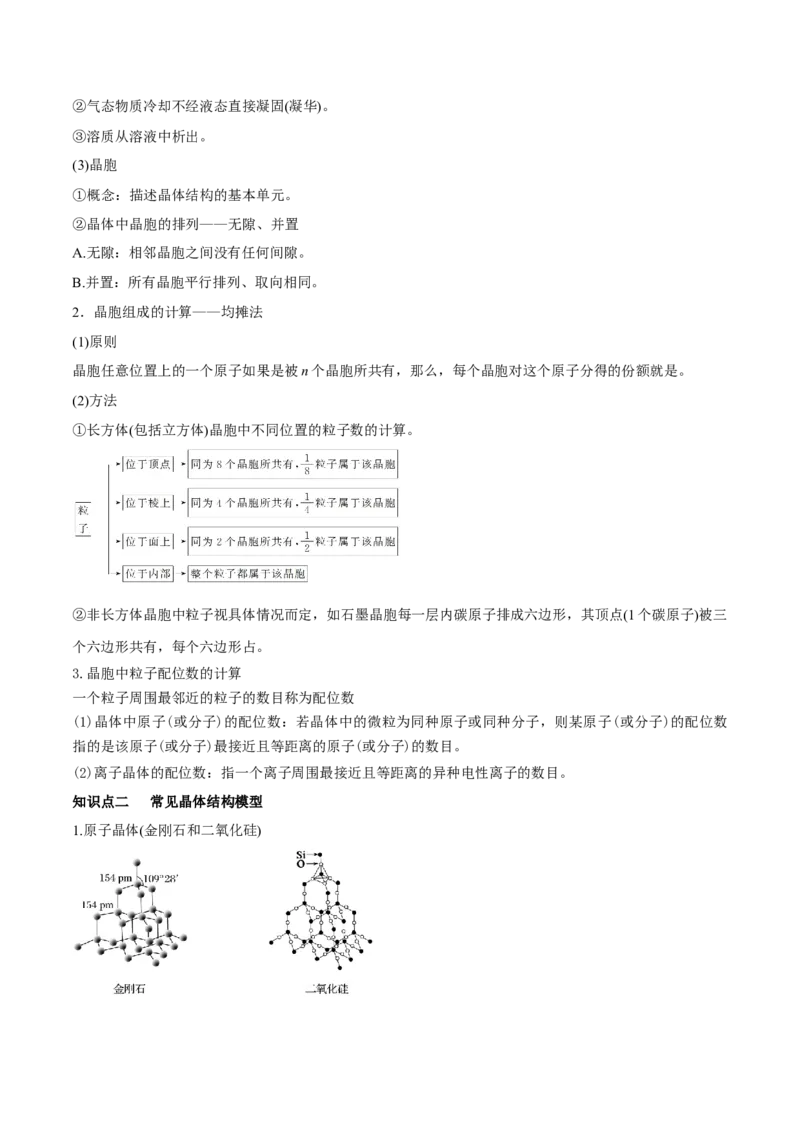
知识点二 常见晶体结构模型
1.原子晶体(金刚石和二氧化硅)①金刚石晶体中,每个C与另外4个C形成共价键,C—C 键之间的夹角是109°28′,最小的环是六元环。
含有1 mol C的金刚石中,形成的共价键有2 mol。
②SiO 晶体中,每个Si原子与4个O原子成键,每个O原子与2个硅原子成键,最小的环是十二元环,在
2
“硅氧”四面体中,处于中心的是Si原子,1 mol SiO 中含有4 mol Si—O键。
2
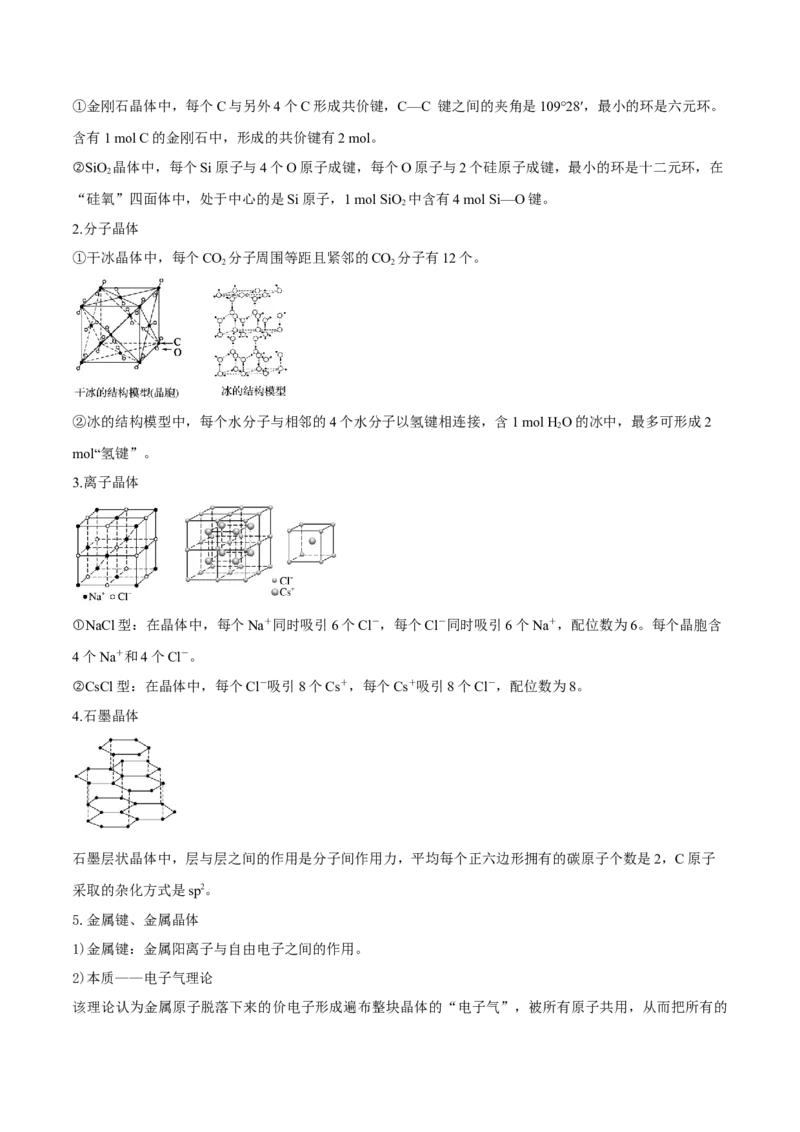
2.分子晶体
①干冰晶体中,每个CO 分子周围等距且紧邻的CO 分子有12个。
2 2
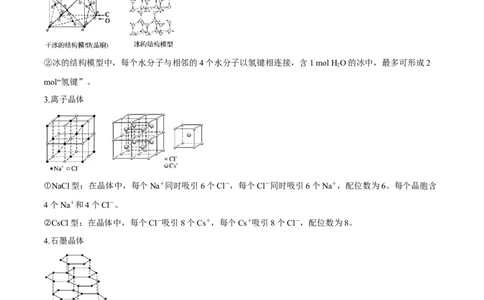
②冰的结构模型中,每个水分子与相邻的4个水分子以氢键相连接,含1 mol H O的冰中,最多可形成2
2
mol“氢键”。
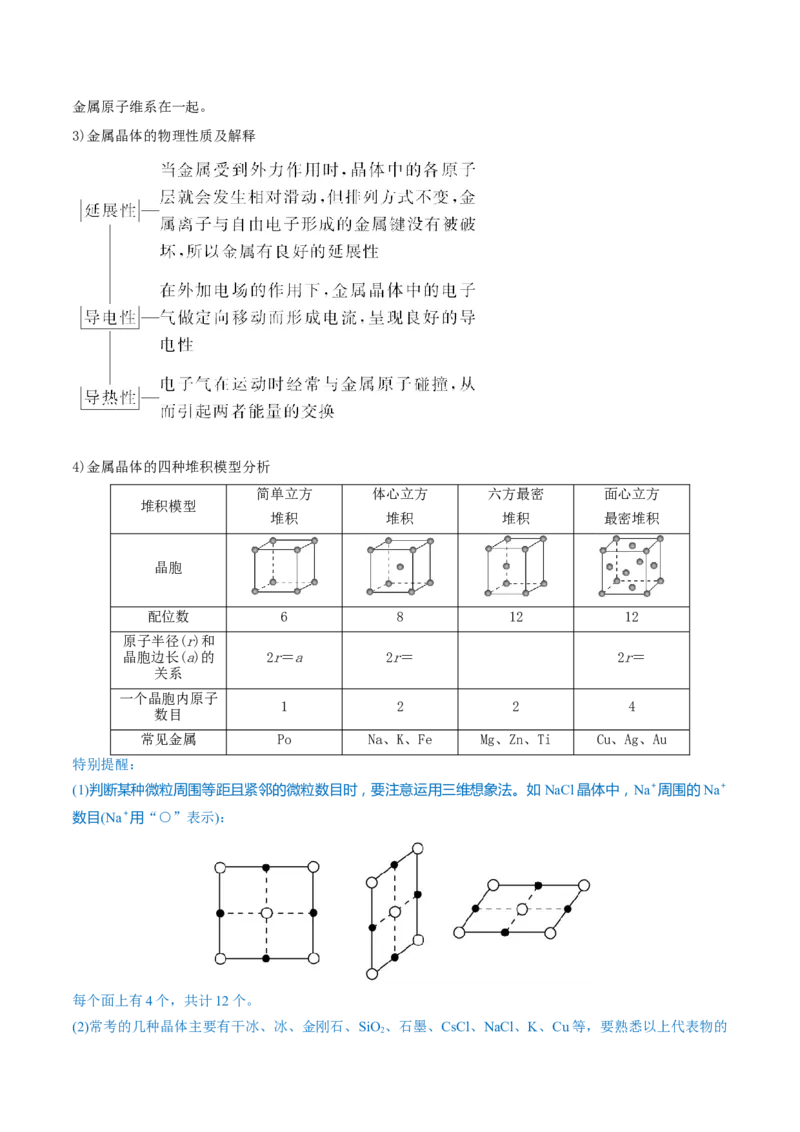
3.离子晶体
①NaCl型:在晶体中,每个Na+同时吸引6个Cl-,每个Cl-同时吸引6个Na+,配位数为6。每个晶胞含
4个Na+和4个Cl-。
②CsCl型:在晶体中,每个Cl-吸引8个Cs+,每个Cs+吸引8个Cl-,配位数为8。
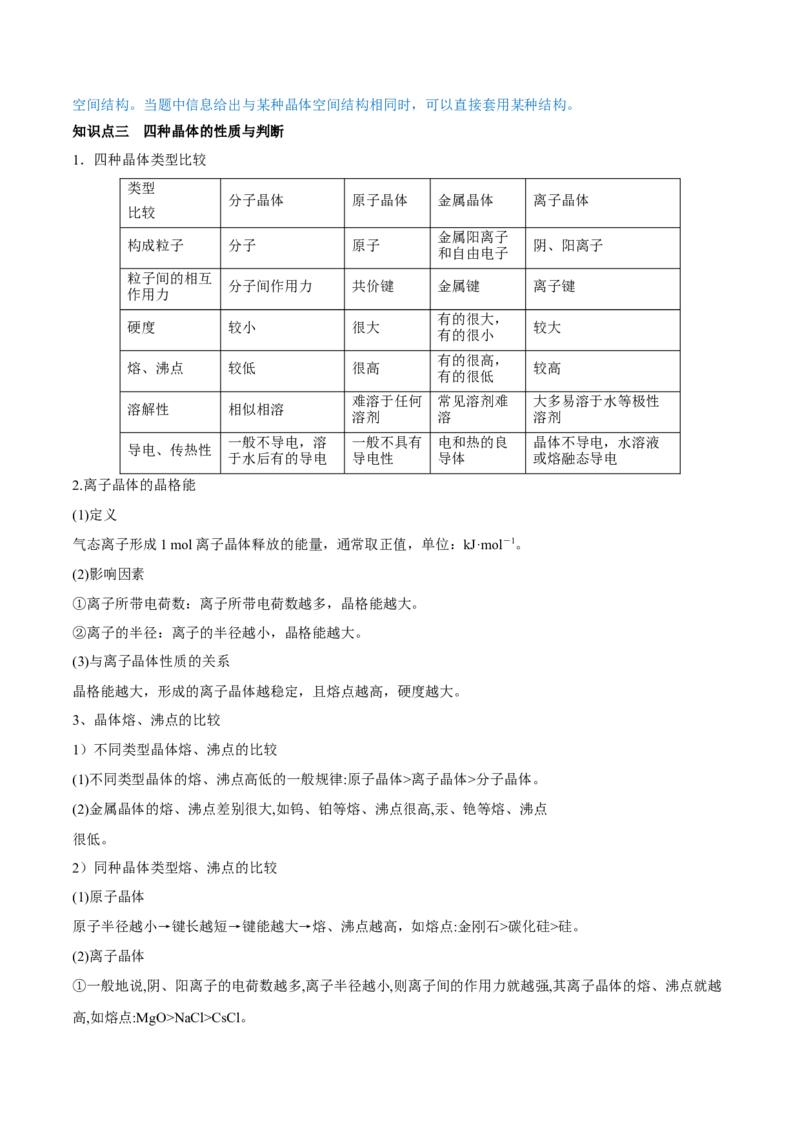
4.石墨晶体
石墨层状晶体中,层与层之间的作用是分子间作用力,平均每个正六边形拥有的碳原子个数是2,C原子
采取的杂化方式是sp2。
5.金属键、金属晶体
1)金属键:金属阳离子与自由电子之间的作用。
2)本质——电子气理论
该理论认为金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子共用,从而把所有的金属原子维系在一起。
3)金属晶体的物理性质及解释
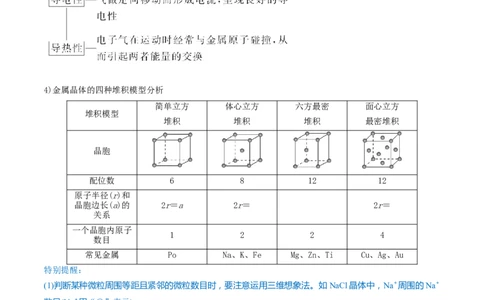
4)金属晶体的四种堆积模型分析
简单立方 体心立方 六方最密 面心立方
堆积模型
堆积 堆积 堆积 最密堆积
晶胞
配位数 6 8 12 12
原子半径(r)和
晶胞边长(a)的 2r=a 2r= 2r=
关系
一个晶胞内原子
1 2 2 4
数目
常见金属 Po Na、K、Fe Mg、Zn、Ti Cu、Ag、Au
特别提醒:
(1)判断某种微粒周围等距且紧邻的微粒数目时,要注意运用三维想象法。如NaCl晶体中,Na+周围的Na+
数目(Na+用“○”表示):
每个面上有4个,共计12个。
(2)常考的几种晶体主要有干冰、冰、金刚石、SiO 、石墨、CsCl、NaCl、K、Cu等,要熟悉以上代表物的
2空间结构。当题中信息给出与某种晶体空间结构相同时,可以直接套用某种结构。
知识点三 四种晶体的性质与判断
1.四种晶体类型比较
类型
分子晶体 原子晶体 金属晶体 离子晶体
比较
金属阳离子
构成粒子 分子 原子 阴、阳离子
和自由电子
粒子间的相互
分子间作用力 共价键 金属键 离子键
作用力
有的很大,
硬度 较小 很大 较大
有的很小
有的很高,
熔、沸点 较低 很高 较高
有的很低
难溶于任何 常见溶剂难 大多易溶于水等极性
溶解性 相似相溶
溶剂 溶 溶剂
一般不导电,溶 一般不具有 电和热的良 晶体不导电,水溶液
导电、传热性
于水后有的导电 导电性 导体 或熔融态导电
2.离子晶体的晶格能
(1)定义
气态离子形成1 mol离子晶体释放的能量,通常取正值,单位:kJ·mol-1。
(2)影响因素
①离子所带电荷数:离子所带电荷数越多,晶格能越大。
②离子的半径:离子的半径越小,晶格能越大。
(3)与离子晶体性质的关系
晶格能越大,形成的离子晶体越稳定,且熔点越高,硬度越大。
3、晶体熔、沸点的比较
1)不同类型晶体熔、沸点的比较
(1)不同类型晶体的熔、沸点高低的一般规律:原子晶体>离子晶体>分子晶体。
(2)金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点
很低。
2)同种晶体类型熔、沸点的比较
(1)原子晶体
原子半径越小→键长越短→键能越大→熔、沸点越高,如熔点:金刚石>碳化硅>硅。
(2)离子晶体
①一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,其离子晶体的熔、沸点就越
高,如熔点:MgO>NaCl>CsCl。②衡量离子晶体稳定性的物理量是晶格能。晶格能越大,形成的离子晶体越稳定,熔、沸点越高,硬度越大。
(3)分子晶体
①分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常得高,如HO>HTe>HSe>HS。
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如SnH>GeH>SiH>CH。
4 4 4 4
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高,如CO>N、
2
CHOH>CHCH。
3 3 3
④同分异构体支链越多,熔、沸点越低。如CHCHCHCHCH>CHCH(CH )CHCH>CHC(CH)CH。
3 2 2 2 3 3 3 2 3 3 3 2 3
(4)金属晶体
金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高,如熔、沸点:Na金刚石>碳化硅 D.
【解析】A.Al、Mg、Na都是金属晶体,Al、Mg、Na电荷数顺序:Al>Mg>Na;原子半径顺序:Al<Mg<
Na,金属晶体中原子半径越小,电荷越多,熔点越大,所以熔点顺序:Al>Mg>Na,故A错误;B.MgO、
NaCl、KCl都是离子晶体,镁离子半径小于钠离子、钾离子半径,氧负离子半径小于氯离子半径;离子晶
体中阴阳离子半径和越小,电荷越大,熔点越大;所以熔点高低顺序为:MgO>NaCl>KCl,故B正确;C.晶体硅、金刚石、碳化硅都是原子晶体,因键长C-C<C-Si<Si-Si,原子晶体中半径越小,共价键越强,
熔点越大,则熔点为金刚石>碳化硅>晶体硅,故C错误;D.AsH、PH、NH 都是分子晶体,分子晶体中
3 3 3
相对分子质量越大,熔点越大,NH 中含有氢键,则熔点最高,所以熔点顺序为:NH>AsH>PH,故D错
3 3 3 3
误;故选B。
【答案】B
【名师点睛】晶体熔、沸点的比较
(1)不同类型晶体的熔、沸点高低的一般规律:原子晶体>离子晶体>分子晶体。
(2)相同类型晶体
①金属晶体:金属原子的价电子数越多,原子半径越小,金属熔、沸点就越高。
②离子晶体:a.晶格能越大,形成的离子晶体越稳定,熔点越高,硬度越大。b.阴、阳离子的电荷数越多,
离子半径越小,熔、沸点就越高。
③原子晶体:原子半径越小,键长越短,熔沸点越高。
④分子晶体:组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高。
【变式训练】(2021·上海金山·二模)已知有钠、钾及钠钾合金,对于它们三者熔点高低比较正确的是
A.钠钾合金>钠>钾 B.钠>钾>钠钾合金
C.钠>钠钾合金>钾 D.钾>钠钾合金>钠
【解析】合金的熔点比各成分的熔点低,碱金属的熔点随原子序数的增大而减小,则熔点为钠>钾>钠和钾
的合金,故答案选B。
【答案】B
高频考点3 考查晶胞组成的计算
例3.(2021·湖北·模拟预测)最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性,因这三
种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如上图所示,则该晶体的化学式为
( )
A.MgCNi B.MgCNi C.MgCNi D.MgCNi
2 3 2 3 2
【解析】碳原子位于该晶胞的体心上,所以该晶胞中含有一个碳原子;镁原子个数=8× =1,所以该晶胞
含有1个镁原子;镍原子个数=6× =3,该晶胞中含有3个镍原子,所以该晶胞的化学式为:MgCNi,故
3答案为C。
【答案】C
【名师点睛】均摊法确定立方晶胞中粒子数目的方法是:①顶点:每个顶点的原子被8个晶胞共有,所以
晶胞对顶点原子只占 份额;②棱:每条棱的原子被4个晶胞共有,所以晶胞对顶点原子只占 份额;③
面上:每个面的原子被2个晶胞共有,所以晶胞对顶点原子只占 份额;④内部:内部原子不与其他晶胞
分享,完全属于该晶胞。
【变式训练】(2022·全国·高三专题练习)现有四种晶体的晶胞,原子的排列方式如图所示,化学式为
MN 的是
3
A. B.
C. D.
【解析】A.晶胞中M原子数目为 、N原子数目为1,化学式为MN,A错误;B.晶胞中M原子数目
为 、N原子数目为 ,化学式为MN,B正确;C.晶胞中M原子数目为 、N原子数目
3
为 ,化学式为MN,C错误;D.晶胞中M原子数目为 、N原子数目为 ,
化学式为MN,D错误;故选B。
【答案】B
高频考点4 考查晶体密度及粒子间距的计算
例4.(2021·广东·模拟预测节选)硫化锂LiS(摩尔质量Mg∙mol-1)的纳米晶体是开发先进锂电池的关键
2
材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个
S2-的距离是___nm。(用含a、M、N 的计算式表示)
A【解析】由晶胞结构可知,X原子个数为: ,Y原子个数为:8,所以X为S2-,Y为Li+, 设
晶胞的边长为bcm, , cm,距离最近的两个S2-的是面对角线的一般,面对
角线为 ,则距离最近的两个S2-的距离为 nm,故答案为: 。
【答案】
【方法总结】晶体密度及微粒间距离的计算
(1)计算晶体密度的方法
以一个晶胞为研究对象,根据m=ρ·V,其一般的计算规律和公式可表示为:×n=ρ×a3,其中M为晶体
的摩尔质量,n为晶胞所占有的粒子数,N为阿伏加德罗常数,ρ为晶体密度,a为晶胞参数。
A
(2)计算晶体中微粒间距离的方法
【变式训练】(2022·全国·高三专题练习)铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶
胞结构如图所示,则该晶体的化学式为_______,铜原子构成的空间构型为_______,铜原子距离最近的Ni
有_______个;已知该晶体的密度为ρg·cm-3,则晶胞中距离最近的Ni原子和Cu原子的核间距为
_______pm(用N 表示阿伏伽德罗常数的值,列出计算式即可)。
A【解析】其立方晶胞结构如图所示,Cu=6 ,Ni=8 ,则该晶体的化学式为CuNi,铜原子构成
3
的空间构型为正八面体,铜原子距离最近的Ni有4个;晶胞中距离最近的Ni原子和Cu原子的核间距为边
长的 ,设边长为apm,则有m= ,则有:1×(64×3+59)g=(a×10-10cm)3×ρg·cm-3×N,a=
A
pm,最近距离为: pm。
【答案】CuNi 正八面体 4
3