文档内容
专题 10 化学反应速率与平衡
第 39 练 共价键
1.下列物质只含共价键的是( )
A.NaO B.HO C.NH Cl D.NaOH
2 2 2 4
2.下列物质的分子中既含有极性键,又含有非极性键的是( )
A.CO B.HO C.HO D.H
2 2 2 2 2
3.下列分子中,只有σ键没有π键的是( )
A.CH B.N C.CH==CH D.CH≡CH
4 2 2 2
4.下列物质分子中一定含有π键的是( )
A.HCl B.HO C.C H D.CHCl
2 2 2 4 2 2
5.下列分子中键角最大的是( )
A.CH B.NH C.HO D.CO
4 3 2 2
6.下列说法正确的
A.含有共价键的化合物一定是共价化合物
B.分子中只有共价键的化合物一定是共价化合物
C.由共价键形成的一定是共价化合物分子
D.只有非金属原子间才能形成共价键
7.下列对化学键及化合物的分类完全正确的一组是
A.MgCl 与NaOH均既含离子键又含共价键,均属离子化合物
2
B.BaCO 与HSO 化学键类型不完全相同,均属电解质
3 2 4
C.乙醇与醋酸,均只含共价键,均属非电解质
D.氯气与氧气,均只含共价键,均只作氧化剂
8.下列物质中,既有离子键,又有极性共价键的是
A.KCl B.NH Cl C.HO D.NaO
4 2 2 2
9.下列实验事实可以证明氯化氢是共价化合物的是( )
A.氯化氢的水溶液显酸性 B.液态氯化氢不导电
C.氯化氢溶于水发生电离 D.氯化氢不易分解
10.下列常见分子中σ键、π键判断正确的是
A.C 2-与O2+互为等电子体,1mol O2+中含有的π键数目为2N
2 2 2 AB.CO与N 结构相似,CO分子中σ键与π键数目之比为2∶1
2
C.CN-与N 结构相似,CH=CHCN分子中σ键与π键数目之比为1∶1
2 2
D.已知反应NO(1)+ 2N H(1) = 3N(g) +4H O(1),若该反应中有4 molN-H键断裂,则形成的π键数
2 4 2 4 2 2
目为6 N
A
11.下列分子中,既含有σ键,又含有π键的是
A.CH B.HCl C.HO D.C H
4 2 2 4
12.下列各组物质中,所有化学键都是共价键的是( )
A.HS和NaO B.HO 和CaF C.NH 和N D.HNO 和NaCl
2 2 2 2 2 2 3 2 3
13.下列分子中的σ键是由两个原子的s轨道以“头碰头”方式重叠构建而成的是( )
A.H B.CCl C.Cl D.F
2 4 2 2
14.下列分了中既含σ键,又含π键的是
A B C D
水 乙醇 氨 乙醛
15.下列有关共价键的键参数的说法不正确的是( )
A.CH、C H、CO 分子中的键角依次增大
4 2 4 2
B.HF、HCl、HBr分子中的键长依次增长
C.HO、HS、HSe分子中的键能依次减小
2 2 2
D.分子中共价键的键能越大,分子的熔、沸点越高
16.下列事实不能用键能的大小来解释的是( )
A.N元素的电负性较大,但N 的化学性质很稳定
2
B.稀有气体一般难发生反应
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.F 比O 更容易与H 反应
2 2 2
17.关于键长、键能和键角,下列说法不正确的是( )
A.键角是确定多原子分子立体结构(分子形状)的重要参数
B.通过反应物和生成物分子中键能数据可以粗略预测反应的能量变化情况
C.键长越长,键能越小,共价化合物越稳定
D.同种原子间形成的共价键键长长短总是遵循;叁键<双键<单键1.下列反应中既有离子键、极性共价键、非极性共价键的断裂又有其形成的反应是
A.NH Cl NH ↑+HCl
4 3
B.2NaO+2H O = 4NaOH+O ↑
2 2 2 2
C.2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2
D.2NaOH+Cl =NaCl+NaClO+H O
2 2
2.下列关于共价键的说法不正确的是( )
A.HS分子中两个共价键的键角接近90°的原因是共价键有方向性
2
B.N 分子中有1个σ键、2个π键
2
C.两个原子形成共价键时至少有1个σ键,可能还有其他键
D.在双键中,σ键的键能小于π键的键能
3.对σ键的认识不正确的是( )
A.ss σ键与sp σ键的对称性相同
B.σ键不属于共价键,是另一种化学键
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
4.下列说法中不正确的是
A.σ键比π键的电子云重叠程度大,形成的共价键强
B.s—sσ键与s—pσ键的电子云形状对称性相同
C.丙烯(CH—CH=CH)分子有8个σ键1个π键
3 2
D.N 分子中有一个σ键,2个π键;CH 中4个C—H键的键能不相同
2 4
5.在乙烯分子中有5个σ键和1个π键,它们分别是
A.sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键,未杂化的2p轨道形成σ键
C.C—H之间是sp2杂化轨道形成σ键,C—C之间是未杂化的2p轨道形成π键
D.C—C之间是sp2杂化轨道形成σ键,C—H之间是未杂化的2p轨道形成π键
6.P元素的外围电子排布为3s23p3,P与Cl形成的化合物有PCl 、PCl ,对此判断正确的是( )
3 5
A.磷原子最外层有三个未成对电子,故只能结合三个氯原子形成PCl
3
B.PCl 分子中的P—Cl键含有π键
3
C.PCl 分子中的P—Cl键都是π键
5
D.磷原子最外层有三个未成对电子,但是能形成PCl ,说明传统的价键理论存在缺陷
5
7.等电子体是指原子总数相同、价电子总数也相同的微粒。下列各选项中的两种微粒不互为等电子体的是( )
A.NO和CO B.O 和NO - C.CH 和NH + D.CO 和NH -
2 2 3 2 4 4 2 2
8.关于键长、键能和键角,下列说法中错误的是( )
A.C=C键等于C-C键键能的2倍
B.键长的大小与成键原子的半径和成键数目有关
C.键角是描述分子立体结构的重要参数
D.因为O-H键的键能小于H-F键的键能,所以O、F 与H 反应的能力逐渐增强
2 2 2
9.下列有关化学键知识的比较肯定错误的是( )
A.键能:C—N<C===N<C≡N
B.键长:I—I>Br—Br>Cl—Cl
C.分子中的键角:HO>CO
2 2
D.相同元素原子间形成的共价键键能:σ键>π键
10.下列事实不能用键能的大小来解释的是( )
A.N元素的电负性较大,但N 的化学性质很稳定
2
B.稀有气体一般难发生反应
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.F 比O 更容易与H 反应
2 2 2
11.下列说法中能说明BF 分子中的4个原子位于同一平面的是( )
3
A.任意两个B—F键间的夹角相等
B.3个B—F键键能相等
C.3个B—F键键长相等
D.任意两个B—F键间的夹角为120°
12.根据下表中所列的键能数据,判断下列分子中最不稳定的是( )
化学键 H—H H—Cl H—Br Br—Br
键能/kJ·mol-1 436.0 431.8 366 193.7
A.HCl B.HBr
C.H D.Br
2 2
1.下列分子的结构式与共价键的饱和性不相符的是( )
A.HO(过氧化氢):H—O===O—H
2 2B.NH(肼):
2 4
C.C HSH(乙硫醇):
2 5
D.SiHCl (三氯氢硅):
3
2.以下说法正确的是( )
A.共价化合物内部可能有极性键和非极性键
B.原子或离子间相互的吸引力叫化学键
C.非金属元素间只能形成共价键
D.金属元素与非金属元素的原子间只形成离子键
3.从实验测得不同物质中氧—氧之间的键长和键能的数据如下表:
O—O键
O O O O
2
数据
键长/10-12m 149 128 121 112
键能/kJ·mol-1 x y z=494 w=628
其中x、y的键能数据尚未测定,但可根据规律性推导键能的大小顺序为w>z>y>x。该规律性是( )
A.成键时电子数越多,键能越大
B.键长越短,键能越大
C.成键所用的电子数越少,键能越小
D.成键时电子对越偏移,键能越大
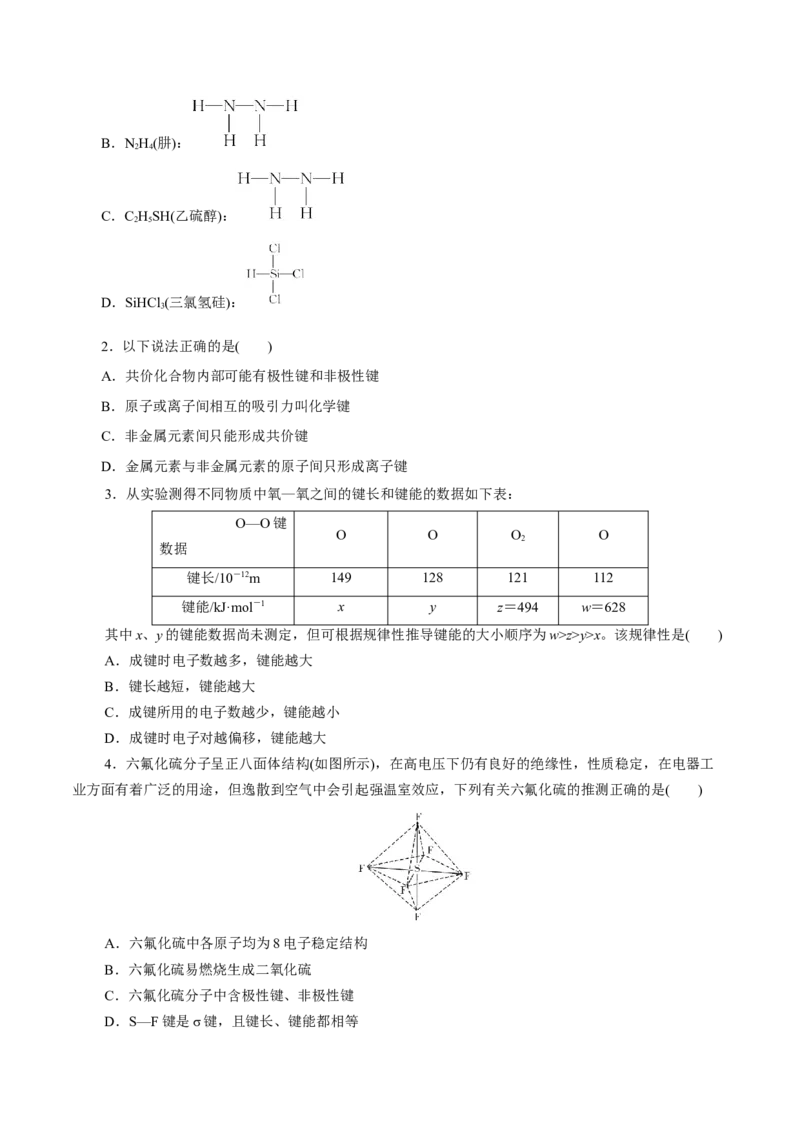
4.六氟化硫分子呈正八面体结构(如图所示),在高电压下仍有良好的绝缘性,性质稳定,在电器工
业方面有着广泛的用途,但逸散到空气中会引起强温室效应,下列有关六氟化硫的推测正确的是( )
A.六氟化硫中各原子均为8电子稳定结构
B.六氟化硫易燃烧生成二氧化硫
C.六氟化硫分子中含极性键、非极性键
D.S—F键是σ键,且键长、键能都相等5.N 的分子结构可以表示为 ,CO的分子结构可以表示为 ,其中椭圆框表示π键,下
2
列说法中不正确的是( )
A.N 分子与CO分子中都含有三键
2
B.N 分子与CO分子中的π键并不完全相同
2
C.N 与CO键能不同
2
D.N 与CO的化学性质相同
2
6.下表为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是(
)
A.W、R元素单质分子内都存在非极性键
B.X、Z元素都能形成双原子分子
C.键长W—HW—H
D.键长X—H