文档内容
专题 15 晶体结构与性质
第 45 练 配合物与超分子
1.下列不能形成配位键的组合是( )
A.Ag+、NH B.HO、H+ C.Co3+、CO D.Ag+、H+
3 2
2.下列有关配位键的分析正确的是( )
A.是离子键 B.是极性键 C.是非极性键 D.是π键
3.既有离子键又有共价键和配位键的化合物是( )
A.NH NO B.NaOH C.HSO D.HO
4 3 2 4 2
4.下列说法中,不正确的是( )
A.配位键也是一种静电作用
B.配位键实质上也是一种共价键
C.形成配位键的电子对由成键双方原子提供
D.配位键具有饱和性和方向性
5.下列物质不是配合物的是( )
A.NaCl B.[Fe(SCN) ]Cl
2
C.[Cu(NH )]Cl D.[Ag(NH)]OH
3 4 2 3 2
6.下列关于配位化合物的叙述中,不正确的是( )
A.配位化合物中必定存在配位键
B.配位化合物中只有配位键
C.[Cu(H O) ]2+中的Cu2+提供空轨道,HO中的氧原子提供孤电子对形成配位键
2 4 2
D.配位化合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有着广泛的应用
7.下列过程与配合物的形成无关的是( )
A.除去Fe粉中的SiO 可用强碱溶液
2
B.向一定量的AgNO 溶液中加入氨水至沉淀消失
3
C.向FeCl 溶液中加入KSCN溶液
3
D.向一定量的CuSO 溶液中加入氨水至沉淀消失
4
8.下列有关超分子的说法错误的是( )
A.超分子是由两种或多种分子形成的聚集体
B.分子形成超分子的作用可能是分子间作用力
C.超分子具有分子识别的特性
D.分子以共价键聚合形成超分子9.下列关于超分子的叙述中正确的是( )
A.超分子就是高分子 B.超分子都是无限伸展的
C.形成超分子的微粒都是分子 D.超分子具有分子识别和自组装的特征
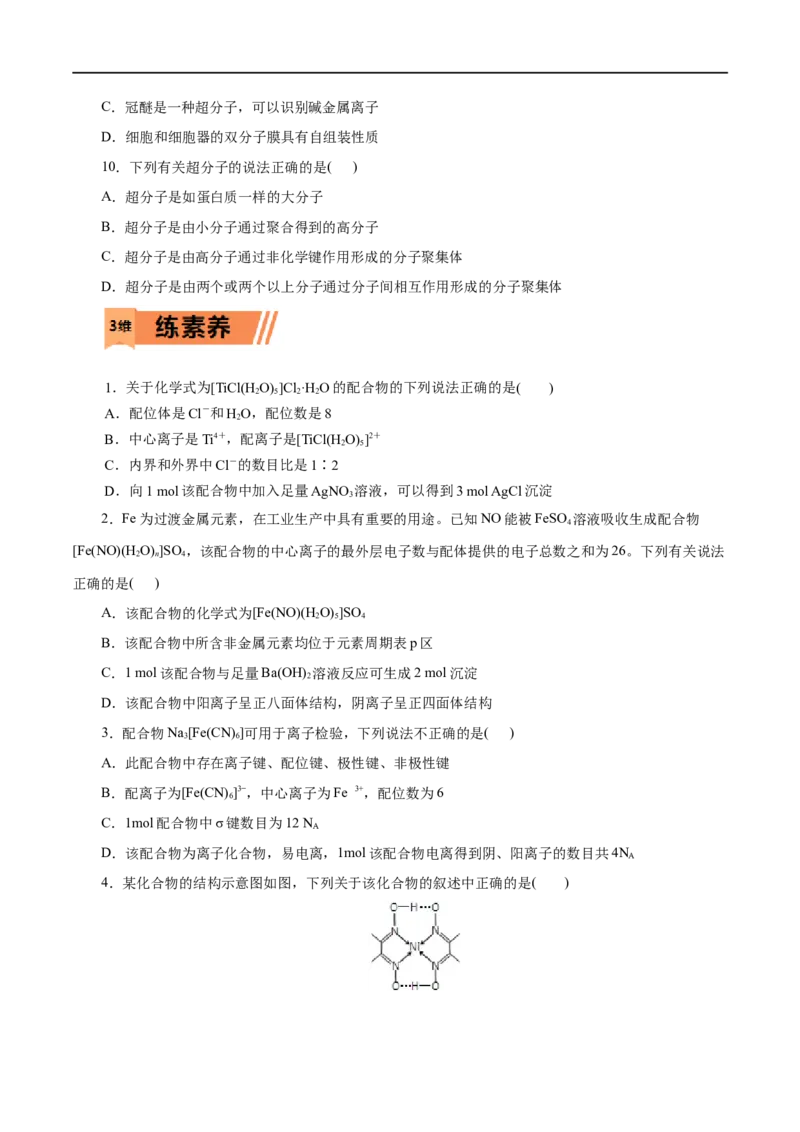
10.冠醚(皇冠状分子)因具有分子识别能力,成为超分子化学中重要一员。18-冠-6 是其中的一种,结
构如图。下列说法正确的是( )
A.该分子是CHOCH 的同系物
3 3
B.该分子中所有原子可能共平面
C.该分子含有σ键、极性键、非极性键
D.该有机物的最简式与甲醛的最简式相同
11.下列关于超分子和配合物的叙述不正确的是( )
A.利用超分子的分子识别特征,可以分离C 和C
60 70
B.配合物中只含配位键
C.[Cu(H O) ]2+中的Cu2+提供空轨道,HO中氧原子提供孤对电子,从而形成配位键
2 6 2
D.配合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有广泛应用
1.下列关于Cu(NH )]SO 的说法中,正确的有( )
3 4 4
A.Cu(NH )]SO 中所含的化学键有离子键、极性共价键和配位键
3 4 4
B.Cu(NH )]SO 含有NH 分子,其水溶液中也含有NH 分子
3 4 4 3 3
C.Cu(NH )]SO 的组成元素中第一电离能最大的是氧元素
3 4 4
D.Cu(NH )]SO 中SO的空间构型为平面三角形
3 4 4
2.关于[Ti(NH )Cl]Cl 的说法中正确的是( )
3 5 2
A.1 mol [Ti(NH )Cl]Cl 含有σ键的数目为15N
3 5 2 A
B.中心原子的化合价为+3价
C.中心原子的配位数是5
D.含1 mol [Ti(NH )Cl]Cl 的水溶液中加入足量AgNO 溶液,产生3 mol白色沉淀
3 5 2 3
3.关于[Cr(H O) Br ]Br·2H O的说法正确的是( )
2 4 2 2
A.配体为水分子,外界为Br-B.中心离子的配位数为6
C.中心离子Cr3+提供孤电子对
D.中心离子的化合价为+2
4.配合物Na[Fe(CN) (NO)]可用于离子检验,下列说法不正确的是( )
2 5
A.此配合物中存在离子键、配位键、极性键、非极性键
B.配离子为[Fe(CN) (NO)]2-,中心离子为Fe3+,配位数为6,配位原子有C和N
5
C.1mol配合物中σ键数目为12N
A
D.该配合物为离子化合物,易电离,1mol配合物电离共得到3N 阴阳离子
A
5.HCHO与[Zn(CN) ]2-在水溶液中发生反应:4HCHO+[Zn(CN) ]2-+4H++4H O=[Zn(HO) ] 2+
4 4 2 2 4
+4HOCH CN,下列说法错误的是( )
2
A.反应中HCHO发生了加成反应
B.HCHO和HO中心原子的价层电子对数不相同
2
C.CN-和HO与Zn2+的配位能力:CN->HO
2 2
D.Zn 2+与CN-生成的配离子[Zn(CN) ]2-中,σ键和π键的数目之比为1∶1
4
6.将灼热的铜丝伸入盛氯气的集气瓶中,剧烈燃烧产生棕黄色烟,向集气瓶中加入少量水,观察到
溶液呈黄绿色,主要原因是CuCl 溶液中存在黄绿色的CuCl ]2-。现向蓝色的硫酸铜溶液中,加入少量稀
2 4
氨水,得到蓝色絮状沉淀,继续加入氨水后,蓝色沉淀溶解,得到深蓝色溶液,再向其中加入少量浓盐酸,
得到绿色溶液,则该绿色溶液中主要存在的离子是( )
A.Cu2+、Cu(HO) ]2+、SO
2 4
B.CuCl ]2-、Cu(HO) ]2+、NH、SO
4 2 4
C.CuCl]、NH、SO
D.Cu(NH )]2+、Cu(HO) ]2+、SO
3 4 2 4
7.下列组合中,中心原子的电荷数和配位数均相同的是( )
A.K[Ag(CN) ]、[Cu(NH )]SO B.[Ni(NH )]Cl 、[Cu(NH )]SO
2 3 4 4 3 4 2 3 4 4
C.[Ag(NH)]Cl、K[Fe(SCN) ] D.[Ni(NH )]Cl 、[Ag(NH)]Cl
3 2 3 6 3 4 2 3 2
8.向盛有少量CuCl 溶液的试管中滴入少量NaOH溶液,再滴入适量浓氨水,下列叙述不正确的是(
2
)
A.开始生成蓝色沉淀,加入过量氨水时,形成无色溶液
B.开始生成Cu(OH) ,它不溶于水,但溶于浓氨水,生成深蓝色溶液
2
C.开始生成蓝色沉淀,加入氨水后,沉淀溶解生成深蓝色溶液
D.开始生成Cu(OH) ,之后生成更稳定的配合物
2
9.下列关于超分子的说法不正确的是( )
A.超分子是两种或两种以上的分子通过分子间相互作用形成的分子聚集体
B.超分子都是无限伸展的C.冠醚是一种超分子,可以识别碱金属离子
D.细胞和细胞器的双分子膜具有自组装性质
10.下列有关超分子的说法正确的是( )
A.超分子是如蛋白质一样的大分子
B.超分子是由小分子通过聚合得到的高分子
C.超分子是由高分子通过非化学键作用形成的分子聚集体
D.超分子是由两个或两个以上分子通过分子间相互作用形成的分子聚集体
1.关于化学式为[TiCl(H O) ]Cl ·H O的配合物的下列说法正确的是( )
2 5 2 2
A.配位体是Cl-和HO,配位数是8
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中Cl-的数目比是1∶2
D.向1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
2.Fe为过渡金属元素,在工业生产中具有重要的用途。已知NO能被FeSO 溶液吸收生成配合物
4
[Fe(NO)(H O) ]SO ,该配合物的中心离子的最外层电子数与配体提供的电子总数之和为26。下列有关说法
2 n 4
正确的是( )
A.该配合物的化学式为[Fe(NO)(H O) ]SO
2 5 4
B.该配合物中所含非金属元素均位于元素周期表p区
C.1 mol该配合物与足量Ba(OH) 溶液反应可生成2 mol沉淀
2
D.该配合物中阳离子呈正八面体结构,阴离子呈正四面体结构
3.配合物Na[Fe(CN) ]可用于离子检验,下列说法不正确的是( )
3 6
A.此配合物中存在离子键、配位键、极性键、非极性键
B.配离子为[Fe(CN) ]3−,中心离子为Fe 3+,配位数为6
6
C.1mol配合物中σ键数目为12 N
A
D.该配合物为离子化合物,易电离,1mol该配合物电离得到阴、阳离子的数目共4N
A
4.某化合物的结构示意图如图,下列关于该化合物的叙述中正确的是( )A.该化合物含有 H、O、N、Ni 四种元素
B.该化合物是配合物,中心离子的配位数是2,配体是氮元素
C.该化合物属于配合物,中心离子是 N
D.该化合物中含有σ键、π键、极性键、非极性键、配位键和氢键
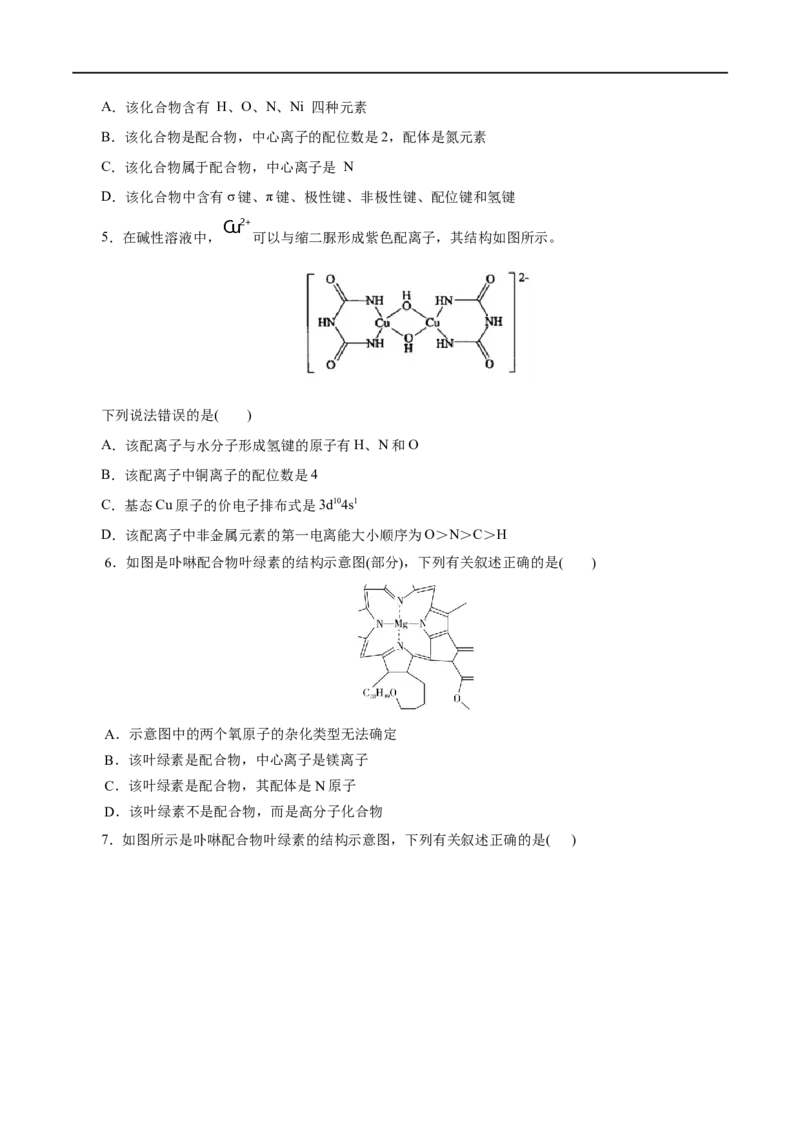
5.在碱性溶液中, 可以与缩二脲形成紫色配离子,其结构如图所示。
下列说法错误的是( )
A.该配离子与水分子形成氢键的原子有H、N和O
B.该配离子中铜离子的配位数是4
C.基态Cu原子的价电子排布式是3d104s1
D.该配离子中非金属元素的第一电离能大小顺序为O>N>C>H
6.如图是卟啉配合物叶绿素的结构示意图(部分),下列有关叙述正确的是( )
A.示意图中的两个氧原子的杂化类型无法确定
B.该叶绿素是配合物,中心离子是镁离子
C.该叶绿素是配合物,其配体是N原子
D.该叶绿素不是配合物,而是高分子化合物
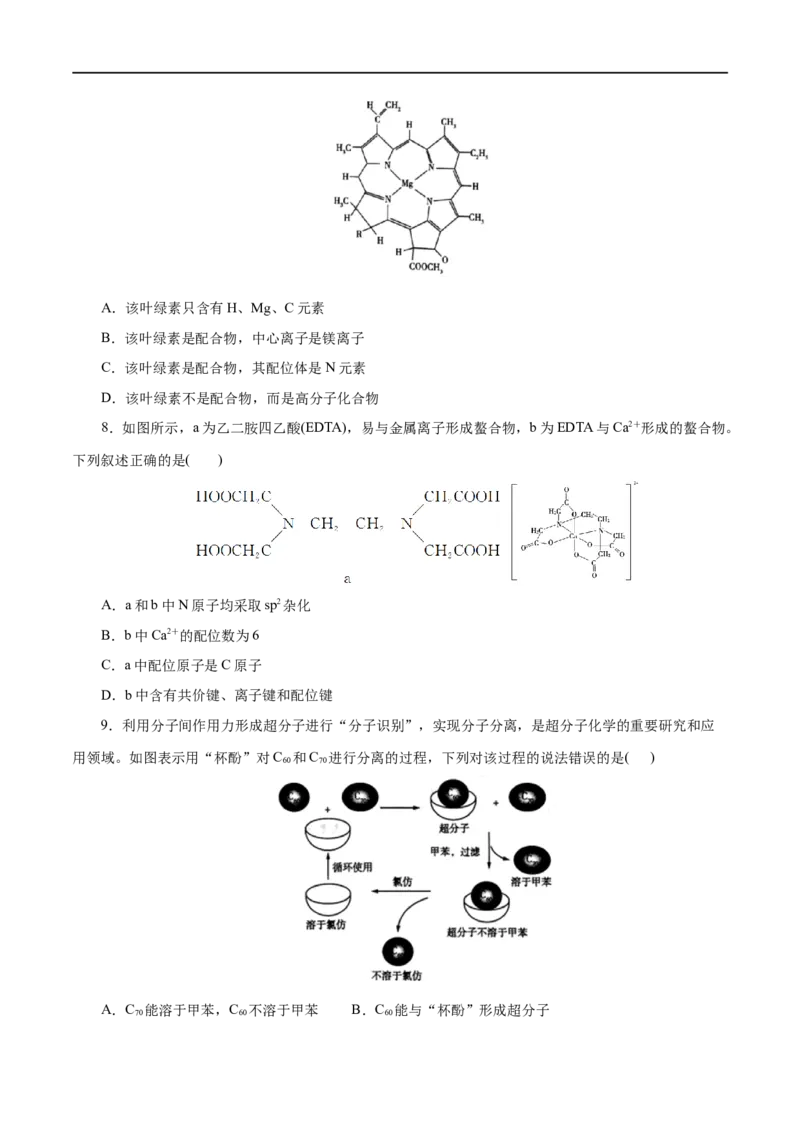
7.如图所示是卟啉配合物叶绿素的结构示意图,下列有关叙述正确的是( )A.该叶绿素只含有H、Mg、C元素
B.该叶绿素是配合物,中心离子是镁离子
C.该叶绿素是配合物,其配位体是N元素
D.该叶绿素不是配合物,而是高分子化合物
8.如图所示,a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物,b为EDTA与Ca2+形成的螯合物。
下列叙述正确的是( )
A.a和b中N原子均采取sp2杂化
B.b中Ca2+的配位数为6
C.a中配位原子是C原子
D.b中含有共价键、离子键和配位键
9.利用分子间作用力形成超分子进行“分子识别”,实现分子分离,是超分子化学的重要研究和应
用领域。如图表示用“杯酚”对C 和C 进行分离的过程,下列对该过程的说法错误的是( )
60 70
A.C 能溶于甲苯,C 不溶于甲苯 B.C 能与“杯酚”形成超分子
70 60 60C.C 不能与“杯酚”形成超分子 D.“杯酚”能够循环使用
70
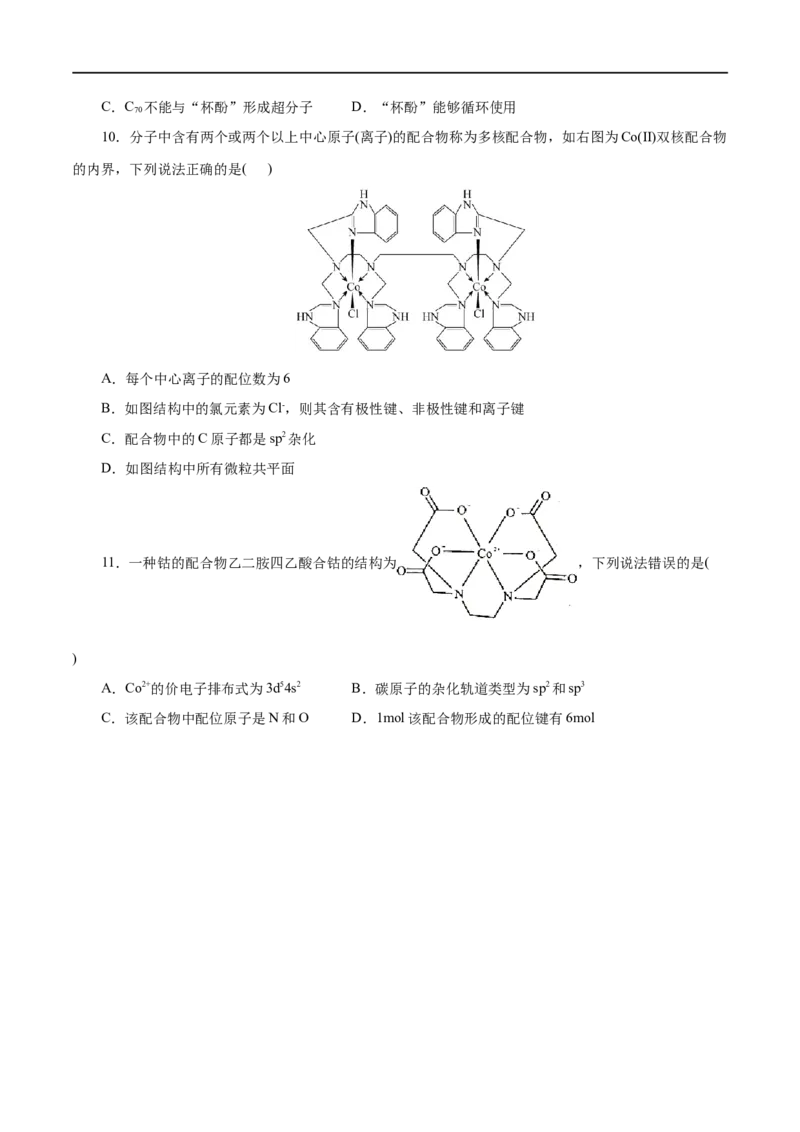
10.分子中含有两个或两个以上中心原子(离子)的配合物称为多核配合物,如右图为Co(II)双核配合物
的内界,下列说法正确的是( )
A.每个中心离子的配位数为6
B.如图结构中的氯元素为Cl-,则其含有极性键、非极性键和离子键
C.配合物中的C原子都是sp2杂化
D.如图结构中所有微粒共平面
11.一种钴的配合物乙二胺四乙酸合钴的结构为 ,下列说法错误的是(
)
A.Co2+的价电子排布式为3d54s2 B.碳原子的杂化轨道类型为sp2和sp3
C.该配合物中配位原子是N和O D.1mol该配合物形成的配位键有6mol