文档内容
第 7 讲 铁及其化合物
【练基础】
1.春秋初年,我国已掌握了冶铁技术。下列有关铁的化学反应的叙述正确的是
A.室温下,过量Fe与浓硫酸反应生成FeSO
4
B.加热时,过量Fe与氯气反应生成FeCl
2
C.高温下,铁与水蒸气反应有Fe O 生成
3 4
D.高温下,铁粉与氧化铝粉末反应生成单质铝
2.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起销,用刀
刮其销,……,所刮下之销末,名铁线粉”。这里的“铁线粉”是指( )
A.Fe B.FeCl
3
C.FeO D.Fe O
2 3
3.将铁钉投入热的浓硝酸中,一段时间后,下列说法错误的是
A.铁钉表面形成致密的氧化膜 B.溶液可能呈棕黄色
C.铁钉会溶解 D.产生红棕色的气体
4.下列物质的用途与氧化还原反应无关的是
A.浓盐酸用于实验室制备氯气 B.铁粉用作暖贴发热剂
C.干冰用作制冷剂 D.镁粉用于炼铁脱硫
5.下列铁及其化合物性质与用途具有对应关系的是
A.Fe粉具有还原性,可用作抗氧化剂 B.Fe O 粉末呈红棕色,可用于制取铁盐
2 3
C.Fe (SO ) 易溶于水,可用作净水剂 D.FeCl 溶液呈酸性,用于蚀刻铜电路板
2 4 3 3
6.将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A.硫酸 B.氯水
C.硫酸锌 D.氯化铜
7.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2
A.①② B.①③
C.②③ D.①②③
8.下列指定反应的离子方程式正确的是A.NaO 与H18O反应:2NaO+2H 18O=4Na++4OH- +18O↑
2 2 2 2 2 2 2
B.向次氯酸钠溶液中通入少量的CO:ClO—+CO +H O=HClO+HCO
2 2 2
C.FeCl 溶液中加过量NaS溶液:S2- + 2Fe3+ =S↓+2Fe2+
3 2
D.向Fe(OH) 胶体中加入HI溶液:Fe(OH) +3H+ =Fe3+ +3H O
3 3 2
【练提升】
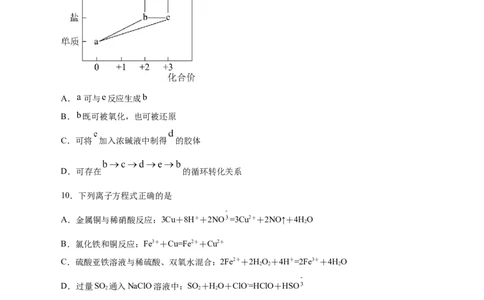
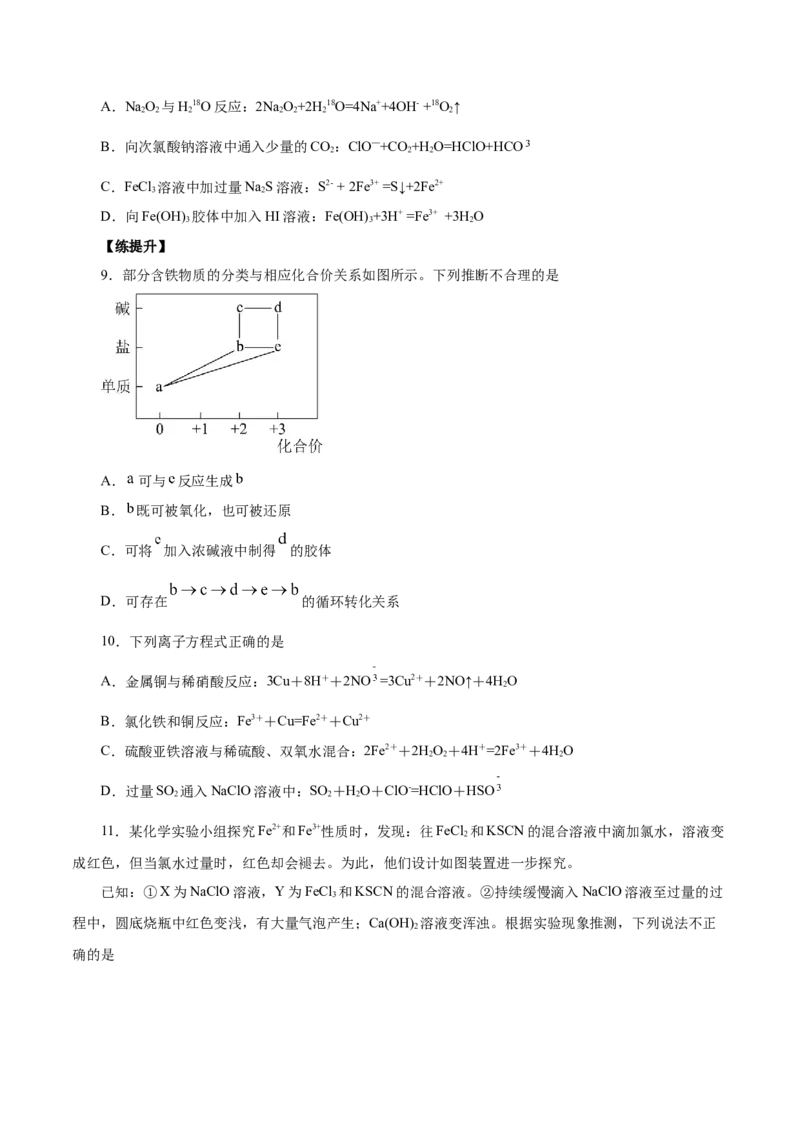
9.部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在 的循环转化关系
10.下列离子方程式正确的是
A.金属铜与稀硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4HO
2
B.氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++2HO+4H+=2Fe3++4HO
2 2 2
D.过量SO 通入NaClO溶液中:SO +HO+ClO-=HClO+HSO
2 2 2
11.某化学实验小组探究Fe2+和Fe3+性质时,发现:往FeCl 和KSCN的混合溶液中滴加氯水,溶液变
2
成红色,但当氯水过量时,红色却会褪去。为此,他们设计如图装置进一步探究。
已知:①X为NaClO溶液,Y为FeCl 和KSCN的混合溶液。②持续缓慢滴入NaClO溶液至过量的过
3
程中,圆底烧瓶中红色变浅,有大量气泡产生;Ca(OH) 溶液变浑浊。根据实验现象推测,下列说法不正
2
确的是A.烧瓶中还可能产生红褐色沉淀
B.烧瓶中产生的气体中一定含有SO
2
C.多孔陶瓷的作用是增大气体与溶液的接触面积
D.KSCN中硫元素、氮元素被氧化
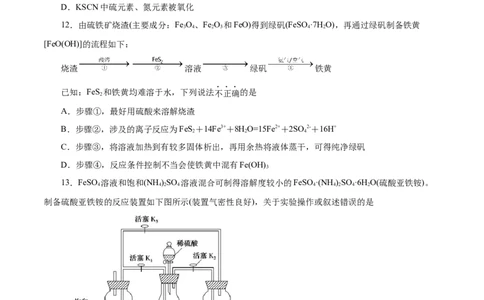
12.由硫铁矿烧渣(主要成分:Fe O、Fe O 和FeO)得到绿矾(FeSO ·7H O),再通过绿矾制备铁黄
3 4 2 3 4 2
[FeO(OH)]的流程如下:
烧渣 溶液 绿矾 铁黄
已知:FeS 和铁黄均难溶于水,下列说法不正确的是
2
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS+14Fe3++8HO=15Fe2++2SO 2-+16H+
2 2 4
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)
3
13.FeSO 溶液和饱和(NH )SO 溶液混合可制得溶解度较小的FeSO ·(NH )SO ·6H O(硫酸亚铁铵)。
4 4 2 4 4 4 2 4 2
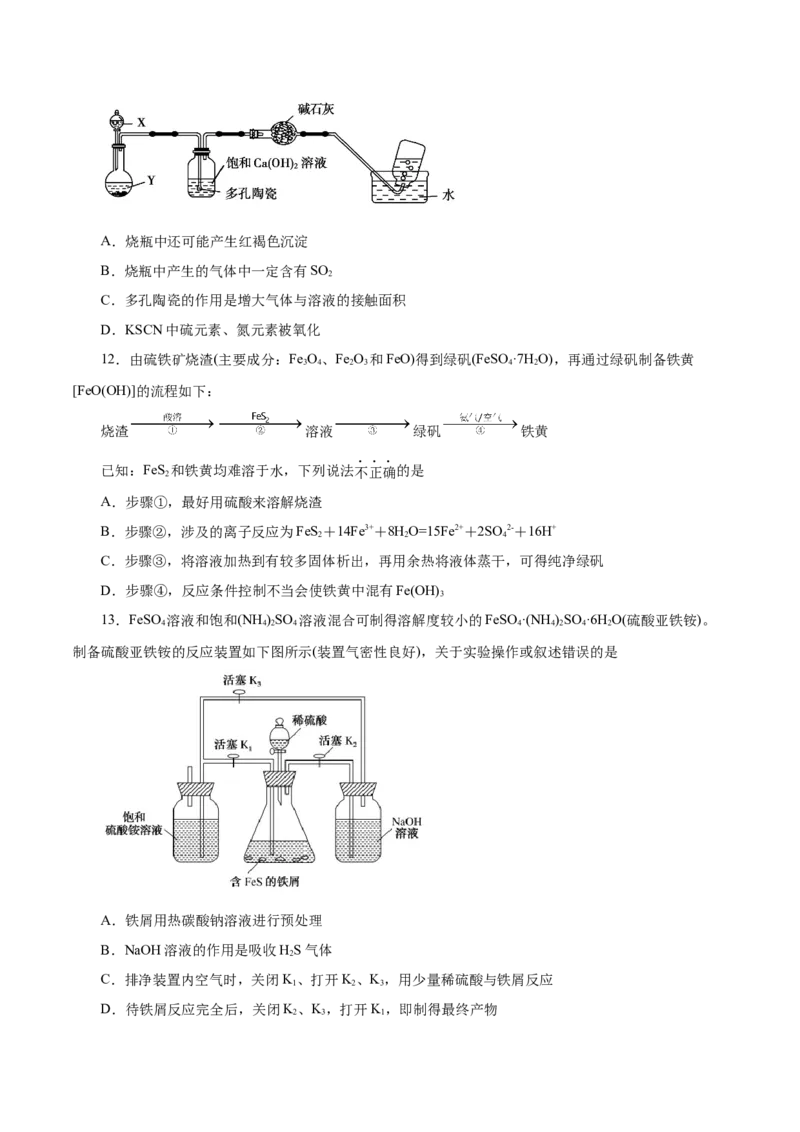
制备硫酸亚铁铵的反应装置如下图所示(装置气密性良好),关于实验操作或叙述错误的是
A.铁屑用热碳酸钠溶液进行预处理
B.NaOH溶液的作用是吸收HS气体
2
C.排净装置内空气时,关闭K、打开K、K,用少量稀硫酸与铁屑反应
1 2 3
D.待铁屑反应完全后,关闭K、K,打开K,即制得最终产物
2 3 114.用废铁屑制备磁性氧化铁(Fe O),制取过程如图:
3 4
下列说法不正确的是
A.浸泡过程中适当加热并搅拌效果更好
B.检验A中的Fe3+可以用KSCN溶液
C.加HO 时发生反应的离子方程式为:HO+2Fe2++2H+=2Fe3+ +2H O
2 2 2 2 2
D.制备Fe O 的反应Fe2++2Fe3++8OH- Fe O+4H O是氧化还原反应
3 4 3 4 2
15.在铁粉与水蒸气反应后的残留固体X中,加入足量的稀硫酸,充分反应后得到溶液Y。下列说法
正确的是
A.若X中含有铁,则反应时一定有气泡
B.若向Y中滴入KSCN溶液显红色,则X中无铁
C.Y一定能使高锰酸钾溶液褪色
D.Y中滴入NaOH溶液,一定有沉淀产生
16.将铁棒插入95%的浓硫酸中(如图所示),探究铁与浓硫酸的反应。观察到立即产生大量的细腻气
泡聚集在液体表面,犹如白色泡沫,由快变慢直至停止,酸液中出现白色不溶物,静置后分层。下列说法
错误的是
A.产生的气体可能是SO 和少量的H
2 2
B.取上层清液滴加少量饱和FeSO 溶液,有白色固体X析出,推测固体X可能是FeSO
4 4
C.反应过程中FeSO 的生成也可能使反应由快变慢
4
D.取反应后铁棒直接放入盛有KSCN溶液的烧杯中,可检验反应时是否有Fe3+生成
17.某混合物由Fe、Fe O 和FeCO 组成。现称取一定质量的该混合物,将其溶于100 mL 1.25 mol·L-
2 3 3
1硫酸中,生成0.56 L(标准状况)气体,并得到溶液X,测得溶液X中c(H+)为0.5 mol·L-1(溶液体积变化忽
略不计)。下列说法正确的是( )
A.混合物中Fe O 的物质的量为0.025 mol
2 3
B.混合物中FeCO 的物质的量为0.03 mol
3
C.若溶液X遇KSCN溶液显红色,则溶液X中n(Fe2+)+n(Fe3+)=0.1 molD.若溶液X中n(Fe2+)=n(Fe3+),则混合物中n(Fe)+n(Fe O)+n(FeCO)=0.08 mol
2 3 3
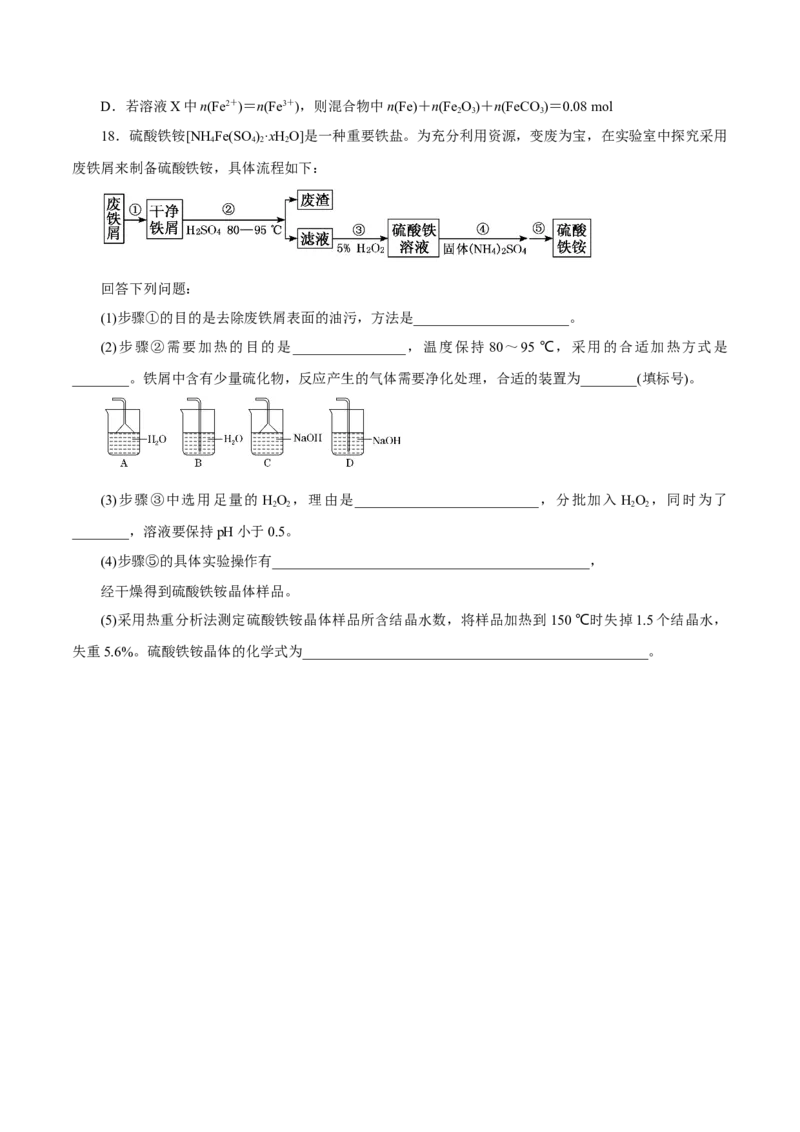
18.硫酸铁铵[NH Fe(SO )·xHO]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用
4 4 2 2
废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是______________________。
(2)步骤②需要加热的目的是________________,温度保持 80~95 ℃,采用的合适加热方式是
________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为________(填标号)。
(3)步骤③中选用足量的 HO ,理由是__________________________,分批加入 HO ,同时为了
2 2 2 2
________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有_____________________________________________,
经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到 150 ℃时失掉1.5个结晶水,
失重5.6%。硫酸铁铵晶体的化学式为_________________________________________________。