文档内容
第7课时 必备知识——金属的腐蚀与防护
[重要概念]①化学腐蚀;②电化学腐蚀;③析氢腐蚀;④吸氧腐蚀
知识清单
[基本规律]①金属腐蚀快慢的规律;②金属腐蚀的防护方法
知识点1 金属的腐蚀
1.金属腐蚀的概念
金属腐蚀是金属或合金与周围的气体或液体发生氧化还原反应而引起损耗的现象。
2.金属腐蚀的本质
金属原子失去电子变成金属阳离子,金属发生氧化反应。
3.金属腐蚀的类型
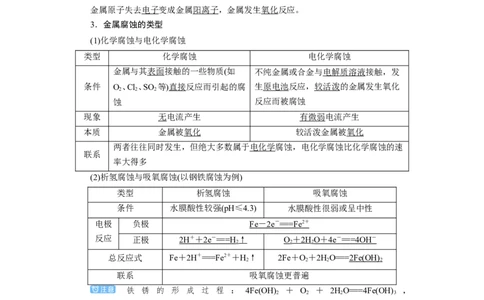
(1)化学腐蚀与电化学腐蚀
类型 化学腐蚀 电化学腐蚀
金属与其表面接触的一些物质(如 不纯金属或合金与电解质溶液接触,发
条件 O、Cl、SO 等)直接反应而引起的腐 生原电池反应,较活泼的金属发生氧化
2 2 2
蚀 反应而被腐蚀
现象 无电流产生 有微弱电流产生
本质 金属被氧化 较活泼金属被氧化
两者往往同时发生,但绝大多数属于电化学腐蚀,电化学腐蚀比化学腐蚀的速
联系
率大得多
(2)析氢腐蚀与吸氧腐蚀(以钢铁腐蚀为例)
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强(pH≤4.3) 水膜酸性很弱或呈中性
电极 负极 Fe - 2e - == =Fe 2 +
反应 正极 2H + + 2e - == =H ↑ O + 2H O + 4e - == =4OH -
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO=== 2Fe (OH)
2 2 2 2
联系 吸氧腐蚀更普遍
铁 锈 的 形 成 过 程 : 4Fe(OH) + O + 2HO===4Fe(OH) ,
2 2 2 3
2Fe(OH) ===Fe O·xHO(铁锈)+(3-x)HO。
3 2 3 2 2
[通关1] (易错排查)判断正误
(1)(2020.7·浙江选考)钢铁在潮湿空气中生锈主要是发生了电化学腐蚀(√)
(2)Al、Fe、Cu在潮湿的空气中腐蚀均生成氧化物(×)
(3)钢铁发生电化学腐蚀时,负极铁失去电子生成Fe3+(×)
(4)钢铁发生电化学腐蚀时,C是正极,O 在C表面上发生还原反应(×)
2
(5)Cu在潮湿的空气中能发生析氢腐蚀(×)(6)纯银器表面变黑和钢铁表面生锈腐蚀原理一样(×)
[通关2] (人教选修4·P88,6题改编)下列事实与电化学腐蚀无关的是( )
A.光亮的自行车钢圈不易生锈
B.黄铜(Cu、Zn合金)制的铜锣不易生锈
C.铜、铝电线一般不连接起来作导线
D.生铁比熟铁(几乎是纯铁)容易生锈
A [B、C、D项均与原电池有关,能用电化学知识来解释。]
[通关3] (2019·江苏卷)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装
置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是( )
A.铁被氧化的电极反应式为Fe-3e-===Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀,
C [A、D错:铁在中性环境中发生吸氧腐蚀,负极上铁失电子发生氧化反应,电极反应
式为Fe-2e-===Fe2+,正极上氧气得电子发生还原反应,电极反应式为2HO+O+4e-
2 2
===4OH-。B错:铁的电化学腐蚀过程中,化学能除转化为电能外还有部分转化为热能。]
[通关4] (人教选修4·P85,实验改编)实验探究(如图所示)
(1)若棉团浸有NH Cl溶液,铁钉发生__________腐蚀,正极反应式为
4
______________________________,右试管中现象是____________________。,(2)若棉团浸
有NaCl溶液,铁钉发生________腐蚀,正极反应式为_______________________________,
右试管中现象是__________________________。
答案 (1)析氢 2H++2e-===H ↑ 有气泡冒出,(2)吸氧 O+4e-+2HO===4OH-
2 2 2
导管内液面上升
知识点2 金属的防护1.金属的防护考虑的因素
金属的防护主要是从金属、与金属接触的物质及两者反应的条件等方面来考虑的。
2.金属的防护
(1)改变金属材料的组成,在金属中添加其他金属或非金属可以制成性能优异的合金,如
钛合金等。
(2)在金属表面覆盖保护层,在金属表面覆盖致密的保护层,将金属制品与周围物质隔开
是一种普遍采用的防护方法,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
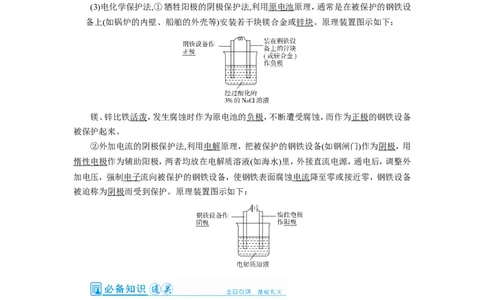
(3)电化学保护法,①牺牲阳极的阴极保护法,利用原电池原理,通常是在被保护的钢铁设
备上(如锅炉的内壁、船舶的外壳等)安装若干块镁合金或锌块。原理装置图示如下:
镁、锌比铁活泼,发生腐蚀时作为原电池的负极,不断遭受腐蚀,而作为正极的钢铁设备
被保护起来。
②外加电流的阴极保护法,利用电解原理,把被保护的钢铁设备(如钢闸门)作为阴极,用
惰性电极作为辅助阳极,两者均放在电解质溶液(如海水)里,外接直流电源,通电后,调整外
加电压,强制电子流向被保护的钢铁设备,使钢铁表面腐蚀电流降至零或接近零,钢铁设备
被迫称为阴极而受到保护。原理装置图示如下:
[通关1] (易错排查)判断正误
(1)在金属表面覆盖保护层,若保护层破损后,就完全失去了对金属的保护作用(×)
(2)若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀(×)
(3)铁表面镀锌可增强其抗腐蚀性(√)
(4)用锡焊接的铁质器件,焊接处易生锈(√)
(5)镀层破损后,镀锌钢板比镀锡钢板耐腐蚀(√)
[通关2] (2020·江苏卷)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。
在如图所示的情境中,下列有关说法正确的是( )A.阴极的电极反应式为Fe-2e-===Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
C [阴极得电子,A错误;金属M失电子,其活动性应强于铁,B错误;M失去的电子流
入钢铁设施表面,钢铁设施表面因积累大量电子而被保护,C正确;海水中所含电解质的浓
度远大于河水中的,因此钢铁设施在海水中被腐蚀的速率快,D错误。]
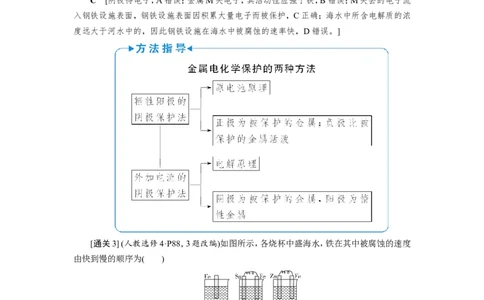
[通关3] (人教选修4·P88,3题改编)如图所示,各烧杯中盛海水,铁在其中被腐蚀的速度
由快到慢的顺序为( )
A.②①③④⑤⑥ B.⑤④③①②⑥
C.⑤④②①③⑥ D.⑤③②④①⑥
C [①是Fe为负极,杂质碳为正极的原电池腐蚀,是铁的吸氧腐蚀,腐蚀较慢,其电极
反应式:负极Fe-2e-===Fe2+,正极2HO+O+4e-===4OH-。②、③、④均为原电池,③中
2 2Fe为正极,被保护;②、④中Fe为负极,均加快了Fe的腐蚀,但Fe和Cu的金属活动性差别
大于Fe和Sn的,故FeCu原电池中Fe腐蚀的较快。⑤是Fe接电源正极作阳极,Cu接电源负
极作阴极,加快了Fe的腐蚀。⑥是Fe接电源负极作阴极,Cu接电源正极作阳极,防止了Fe
的腐蚀。根据以上分析可知铁在其中被腐蚀由快到慢的顺序为⑤>④>②>①>③>⑥。]
[通关4] (深度思考)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:
(1)A中反应的离子方程式是_______________________________。
(2)B中Sn极的电极反应式为____________________________________________,
Sn极附近溶液的pH______(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是________,总反应离子方程式是_________________________,
比较A、B、C中铁被腐蚀的速率由快到慢的顺序是____________________________。
解析 (1)A中发生Fe与稀硫酸间的置换反应。
(2)B中Sn为正极,H+放电生成H:2H++2e-===H ↑,导致Sn附近溶液中c(H+)减小,
2 2
pH增大。
(3)C中Zn为负极被腐蚀。
答案 (1)Fe+2H+===Fe2++H↑ (2)2H++2e-===H ↑ 增大 (3)Zn Zn+2H+
2 2
===Zn2++H↑ B>A>C
2
训练(三十三) 金属的腐蚀与防护
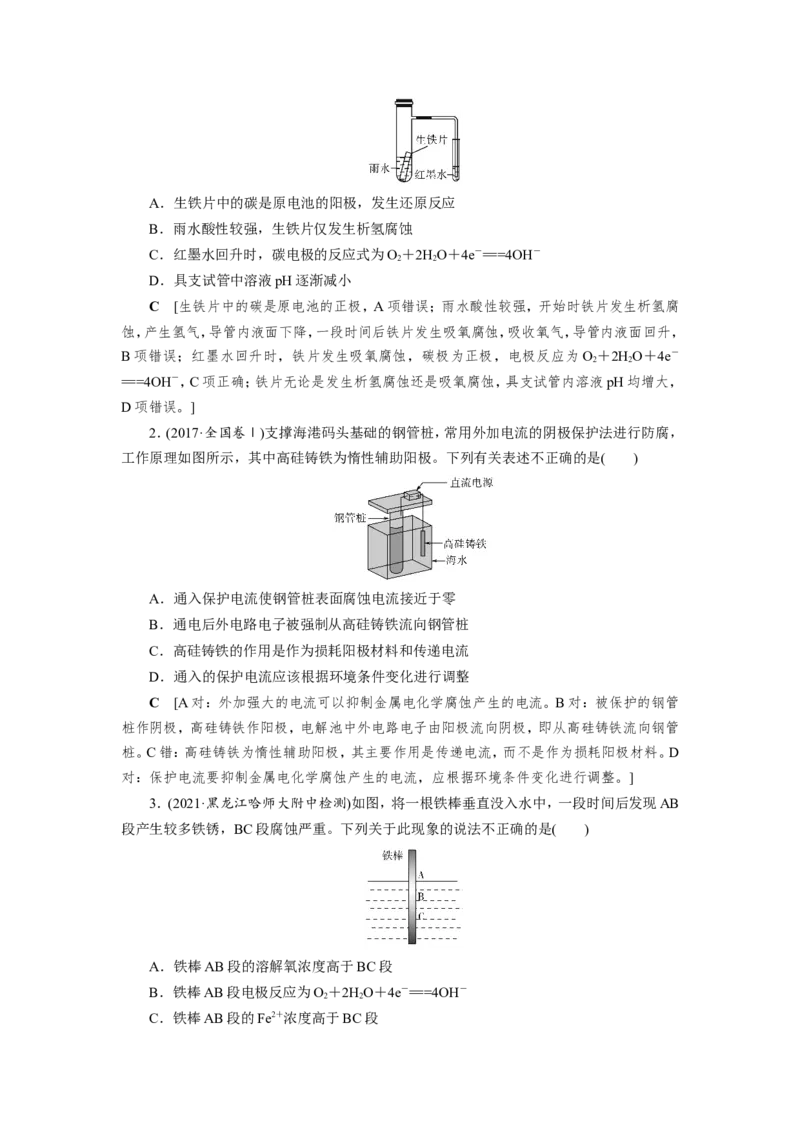
1.(2021·湖南郴州检测)如图装置中,小试管内为红墨水,具支试管内盛有pH=4久置的
雨水和生铁片。实验时观察到:开始时导管内液面下降,一段时间后导管内液面回升,略高于
小试管内液面。下列说法正确的是( )A.生铁片中的碳是原电池的阳极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.红墨水回升时,碳电极的反应式为O+2HO+4e-===4OH-
2 2
D.具支试管中溶液pH逐渐减小
C [生铁片中的碳是原电池的正极,A项错误;雨水酸性较强,开始时铁片发生析氢腐
蚀,产生氢气,导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面回升,
B项错误;红墨水回升时,铁片发生吸氧腐蚀,碳极为正极,电极反应为O +2HO+4e-
2 2
===4OH-,C项正确;铁片无论是发生析氢腐蚀还是吸氧腐蚀,具支试管内溶液pH均增大,
D项错误。]
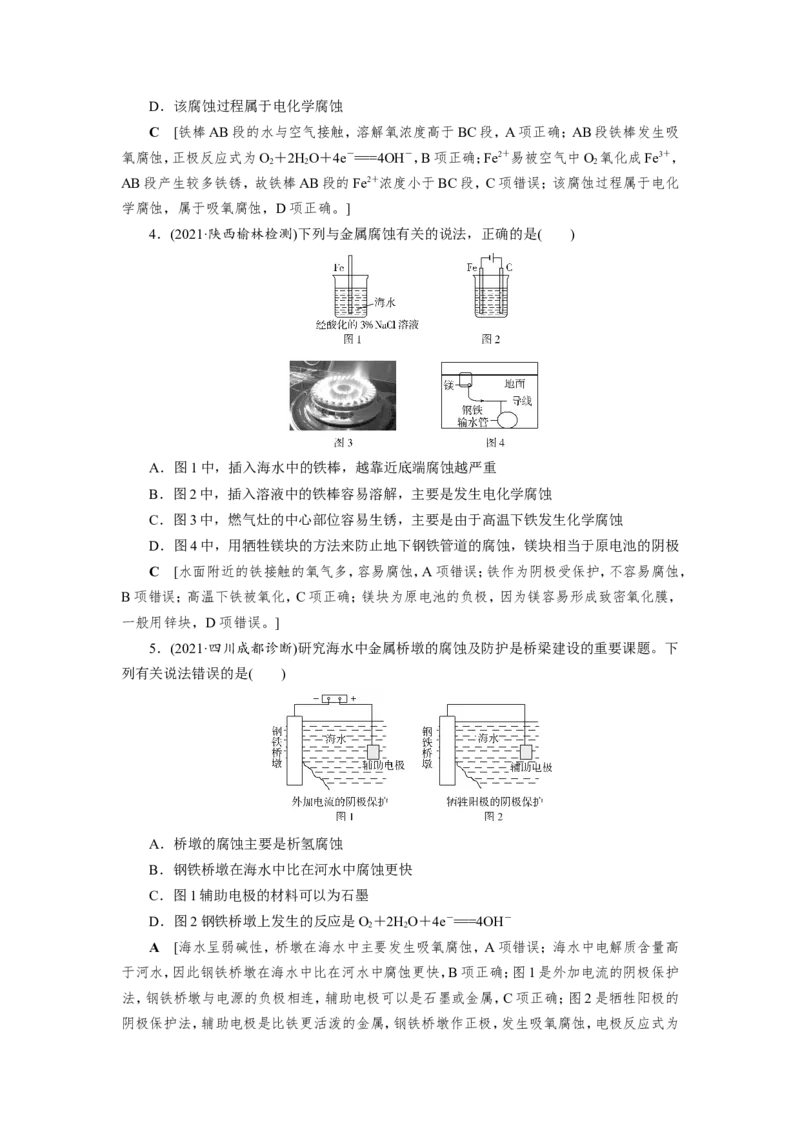
2.(2017·全国卷Ⅰ)支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,
工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
C [A对:外加强大的电流可以抑制金属电化学腐蚀产生的电流。B对:被保护的钢管
桩作阴极,高硅铸铁作阳极,电解池中外电路电子由阳极流向阴极,即从高硅铸铁流向钢管
桩。C错:高硅铸铁为惰性辅助阳极,其主要作用是传递电流,而不是作为损耗阳极材料。D
对:保护电流要抑制金属电化学腐蚀产生的电流,应根据环境条件变化进行调整。]
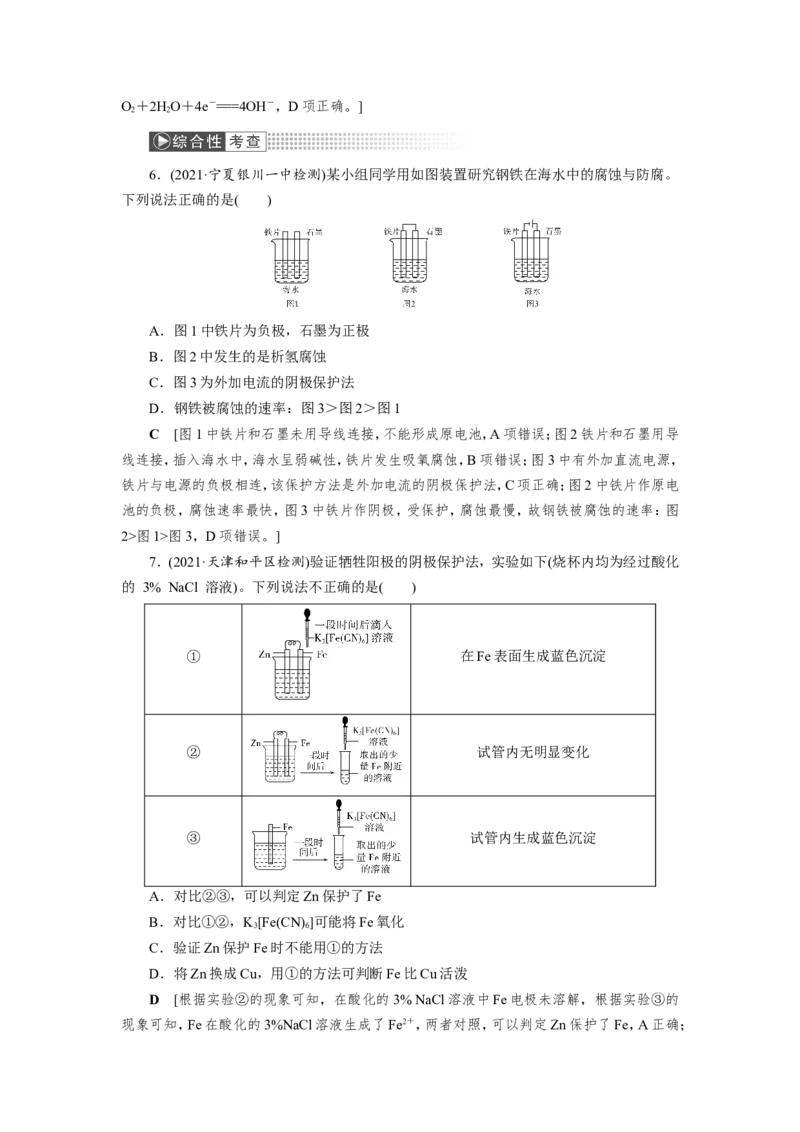
3.(2021·黑龙江哈师大附中检测)如图,将一根铁棒垂直没入水中,一段时间后发现AB
段产生较多铁锈,BC段腐蚀严重。下列关于此现象的说法不正确的是( )
A.铁棒AB段的溶解氧浓度高于BC段
B.铁棒AB段电极反应为O+2HO+4e-===4OH-
2 2
C.铁棒AB段的Fe2+浓度高于BC段D.该腐蚀过程属于电化学腐蚀
C [铁棒AB段的水与空气接触,溶解氧浓度高于BC段,A项正确;AB段铁棒发生吸
氧腐蚀,正极反应式为O+2HO+4e-===4OH-,B项正确;Fe2+易被空气中O 氧化成Fe3+,
2 2 2
AB段产生较多铁锈,故铁棒AB段的Fe2+浓度小于BC段,C项错误;该腐蚀过程属于电化
学腐蚀,属于吸氧腐蚀,D项正确。]
4.(2021·陕西榆林检测)下列与金属腐蚀有关的说法,正确的是( )
A.图1中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图2中,插入溶液中的铁棒容易溶解,主要是发生电化学腐蚀
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的阴极
C [水面附近的铁接触的氧气多,容易腐蚀,A项错误;铁作为阴极受保护,不容易腐蚀,
B项错误;高温下铁被氧化,C项正确;镁块为原电池的负极,因为镁容易形成致密氧化膜,
一般用锌块,D项错误。]
5.(2021·四川成都诊断)研究海水中金属桥墩的腐蚀及防护是桥梁建设的重要课题。下
列有关说法错误的是( )
A.桥墩的腐蚀主要是析氢腐蚀
B.钢铁桥墩在海水中比在河水中腐蚀更快
C.图1辅助电极的材料可以为石墨
D.图2钢铁桥墩上发生的反应是O+2HO+4e-===4OH-
2 2
A [海水呈弱碱性,桥墩在海水中主要发生吸氧腐蚀,A项错误;海水中电解质含量高
于河水,因此钢铁桥墩在海水中比在河水中腐蚀更快,B项正确;图1是外加电流的阴极保护
法,钢铁桥墩与电源的负极相连,辅助电极可以是石墨或金属,C项正确;图2是牺牲阳极的
阴极保护法,辅助电极是比铁更活泼的金属,钢铁桥墩作正极,发生吸氧腐蚀,电极反应式为O+2HO+4e-===4OH-,D项正确。]
2 2
6.(2021·宁夏银川一中检测)某小组同学用如图装置研究钢铁在海水中的腐蚀与防腐。
下列说法正确的是( )
A.图1中铁片为负极,石墨为正极
B.图2中发生的是析氢腐蚀
C.图3为外加电流的阴极保护法
D.钢铁被腐蚀的速率:图3>图2>图1
C [图1中铁片和石墨未用导线连接,不能形成原电池,A项错误;图2铁片和石墨用导
线连接,插入海水中,海水呈弱碱性,铁片发生吸氧腐蚀,B项错误;图3中有外加直流电源,
铁片与电源的负极相连,该保护方法是外加电流的阴极保护法,C项正确;图2中铁片作原电
池的负极,腐蚀速率最快,图3中铁片作阴极,受保护,腐蚀最慢,故钢铁被腐蚀的速率:图
2>图1>图3,D项错误。]
7.(2021·天津和平区检测)验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化
的 3% NaCl 溶液)。下列说法不正确的是( )
① 在Fe表面生成蓝色沉淀
② 试管内无明显变化
③ 试管内生成蓝色沉淀
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K[Fe(CN) ]可能将Fe氧化
3 6
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
D [根据实验②的现象可知,在酸化的3% NaCl溶液中Fe电极未溶解,根据实验③的
现象可知,Fe在酸化的3%NaCl溶液生成了Fe2+,两者对照,可以判定Zn保护了Fe,A正确;根据实验②取出Fe附近的溶液,滴加K[Fe(CN) ]溶液,无明显变化,可知Fe电极附近未生
3 6
成Fe2+,而实验①中Fe表面变蓝,说明K[Fe(CN) ]可能将Fe氧化,B、C正确;将Zn换成
3 6
Cu,用①的方法K[Fe(CN) ]可将Fe氧化,Fe表面也会生成蓝色沉淀,不能根据电化学原理
3 6
判断Fe比Cu活泼,D错误。]