文档内容
第五章 物质结构 元素周期律
能力提升检测卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 N 14 O16 Mg 24 Al 27 S 32 Cl 35.5 Cu 64 Ba 137
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2022·湖南省新化县第一中学模拟预测)我国自主研制的核电技术成果“华电一号”其主要核燃料铀
238得到一个中子后经过2次β衰变成为钚239: U+ n→ U, U→ e+ Np, Np→ Pu+ e。
下列有关说法错误的是
A. U和 U互为同位素 B. Np和 Pu化学性质不相同
C. U的中子数为145 D. U经过三步化学反应得到 Pu
2.(2022·北京市回民学校模拟预测)下列有关化学用语表述正确的是
A.还原性:Na Mg(OH) B.氧化性:FeCl > CuCl
2 3 2
C.酸性:HI > HF D.热稳定性:NaCO > NaHCO
2 3 3
6.(2022·上海徐汇·三模)金属表面的电子在光线照射下逸出产生电流的现象称为光电效应。以下碱金属
中最容易发生光电效应的是
A.Na B.K C.Rb D.Cs
7.(2022·贵州遵义·三模)a、b、c、d是原子序数依次增大的短周期元素,甲、乙、丙、丁、戊、己是由
这四种元素组成的单质或化合物。它们之间有如下反应:①甲+乙→戊+己;②甲+丙→丁+己。已知己是由
c元素形成的常见单质,常温时,0.01mol/L戊溶液的pH=12。下列说法中不正确的是
A.b是第二周期元素
B.甲中有非极性共价键,且lmol甲中含有4mol离子
C.己在自然界中有同素异形体
D.c、d形成的简单离子,它们的电子层结构相同
8.(2022·河南·模拟预测)W、X、Y、Z为原子序数依次增大的短周期主族元素,其中X、Z同主族且两
者的单质在常温下均为气体,Y的最外层电子数等于其电子层数,W与Y的族序数之和等于X的族序数。
下列有关说法错误的是
A.熔融态下YZ 不导电,其属于非电解质
3
B.原子半径;Y>Z> W> X
C.简单氢化物的沸点和热稳定性均存在:X> Z
D.W与X组成的二元化合物中可能同时含有极性共价键和非极性共价键
9.(2022·安徽师范大学附属中学模拟预测)已知X、Y、Z、W是原子序数依次增大的短周期主族元素,
位于三个不同的周期。由X、Y、Z组成的某有机物常用于合成高分子化合物,其结构如图所示。W原子
的最外层电子数比Z多。下列说法正确的是
A.原子半径W>Z>Y>X
B.Y、Z、W不可以组成各原子均满足8电子稳定结构的某种微粒
C.Z的简单氢化物熔点高于Y的简单氢化物.
D.氧化物对应水化物的酸性:W一定比Z强10.(2022·上海虹口·模拟预测)已知非金属元素X、Y的单质能发生如下反应 ,
下列说法正确的是
A.氧化产物: B.氧化性:
C.非金属性: D.每生成 ,转移 电子
11.(2022·湖南·模拟预测)已知X、Y、W、Z、Q为原子序数依次增大的短周期主族元素,相关信息如
下表。
元
相关信息
素
X 某种同位素的原子中没有中子
Y 地壳中含量最高的元素
W 在同周期中原子半径最大
Z 单质是一种常见的半导体材料
Q 该元素的氧化物能形成酸雨
下列说法不正确的是A.原子半径:W> Z>Q> Y> X
B.气态氢化物的稳定性:Y> Q> Z
C.Y元素与其他四种元素均可以形成两种常见的化合物
D.X、Y、W形成的化合物中既含共价键又含离子键
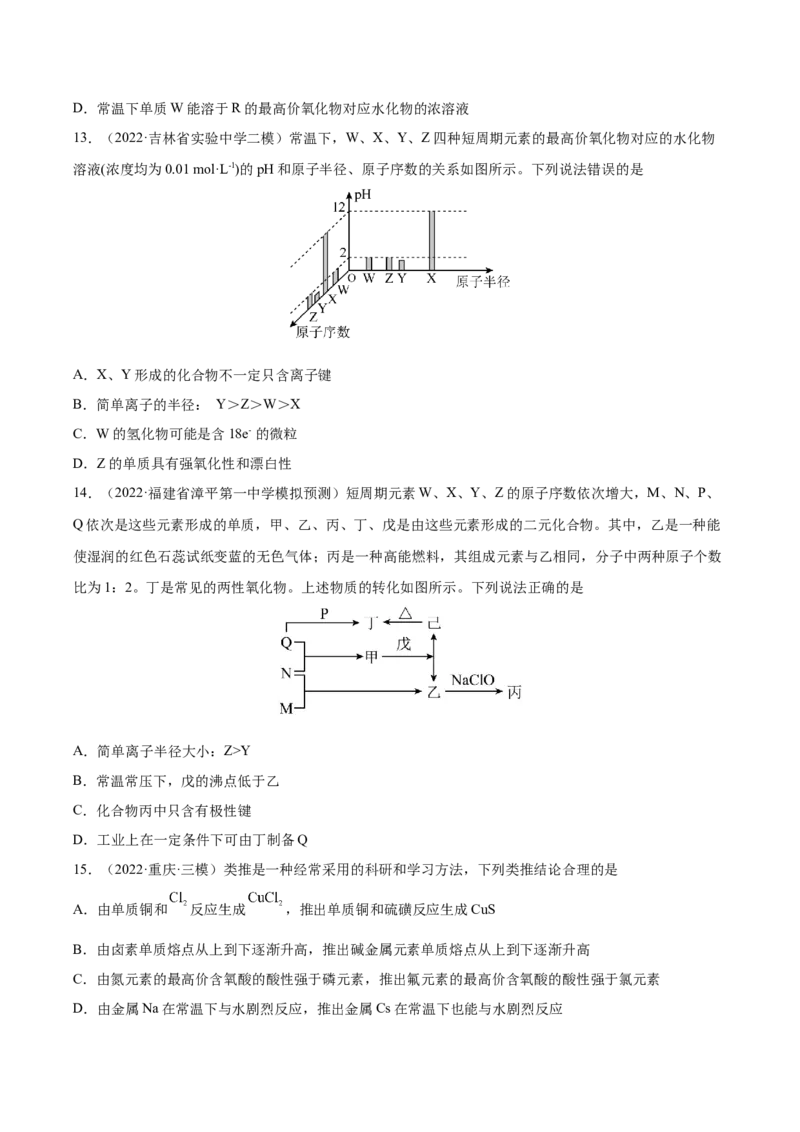
12.(2022·贵州贵阳·模拟预测)短周期元素X、Y、Z、W、R的化合价与原子序数的关系如图所示,下
列说法正确的是
A.离子半径:R>W>Z>Y
B.气态氢化物稳定性:YY
B.常温常压下,戊的沸点低于乙
C.化合物丙中只含有极性键
D.工业上在一定条件下可由丁制备Q
15.(2022·重庆·三模)类推是一种经常采用的科研和学习方法,下列类推结论合理的是
A.由单质铜和 反应生成 ,推出单质铜和硫磺反应生成CuS
B.由卤素单质熔点从上到下逐渐升高,推出碱金属元素单质熔点从上到下逐渐升高
C.由氮元素的最高价含氧酸的酸性强于磷元素,推出氟元素的最高价含氧酸的酸性强于氯元素
D.由金属Na在常温下与水剧烈反应,推出金属Cs在常温下也能与水剧烈反应16.(2022·河南洛阳·二模)短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素可以组成一种
分子簇,其分子结构如图所示(球大小表示原子半径的相对大小),W、X位于不同周期,X原子的最外层
电子数是次外层电子数的3倍,Z的族序数等于其周期数,下列说法中一定正确的是
A.X可以分别与W、Y可形成化合物WX、YX
2 2 2 2
B.工业上获得Y、Z单质均可采用电解它们的熔融氯化物
C.简单离子半径: Z>Y>X>W
D.相同条件下,Y单质的沸点比Z单质的低
二、主观题(共5小题,共52分)
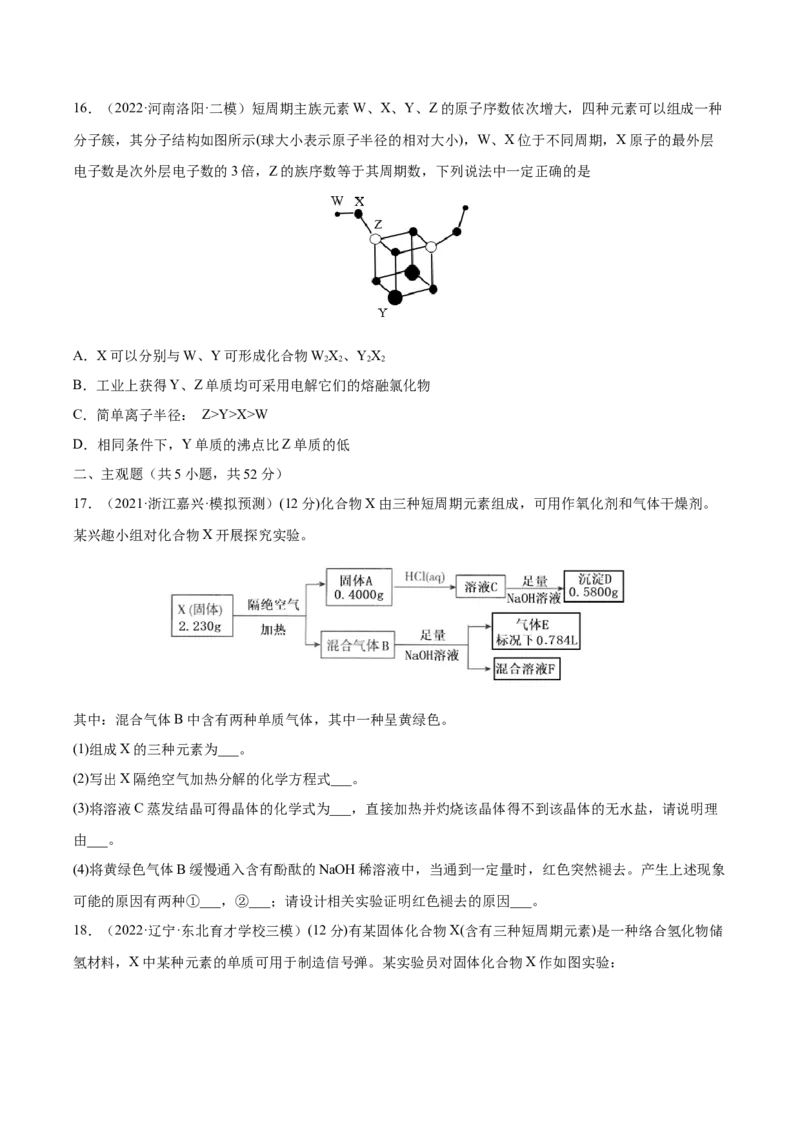
17.(2021·浙江嘉兴·模拟预测)(12分)化合物X由三种短周期元素组成,可用作氧化剂和气体干燥剂。
某兴趣小组对化合物X开展探究实验。
其中:混合气体B中含有两种单质气体,其中一种呈黄绿色。
(1)组成X的三种元素为___。
(2)写出X隔绝空气加热分解的化学方程式___。
(3)将溶液C蒸发结晶可得晶体的化学式为___,直接加热并灼烧该晶体得不到该晶体的无水盐,请说明理
由___。
(4)将黄绿色气体B缓慢通入含有酚酞的NaOH稀溶液中,当通到一定量时,红色突然褪去。产生上述现象
可能的原因有两种①___,②___;请设计相关实验证明红色褪去的原因___。
18.(2022·辽宁·东北育才学校三模)(12分)有某固体化合物X(含有三种短周期元素)是一种络合氢化物储
氢材料,X中某种元素的单质可用于制造信号弹。某实验员对固体化合物X作如图实验:其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化
合物。请回答:
(1)化合物X的组成元素_______,写出H的电子式_______。
(2)X在400℃分解的化学方程式_______。
(3)溶液E和过量CO 发生反应的离子方程式为_______。
2
(4)金属互化物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为_______。
(5)气体A与单质D制备化合物H的过程中,通常产物中会夹杂单质D,请设计实验方案,检验产品中是
否含有单质D:_______。
19.(2020·湖南·模拟预测)(8分)自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元
素周期表中的成员数目不断增加。回答下列问题:
(1)2010年和2012年,俄罗斯的杜布纳联合核研究所两次成功合成了超重元素 ,中文名为“石田”。元
素 可由反应 得到,该反应________(填“是”或“不是”)化学反应。 的
质子数为________。
(2) 的同族元素F的一种化合物为 ,若该化合物分子中的每个原子都达到8电子稳定结构,则
的电子式为________,该分子内存在的共价键类型有________。
20.(2021·上海金山·一模)(10分)全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚
硫酸氢钠制取,相关反应如下:
___________NaIO +___________NaHSO →3NaHSO+___________Na SO +___________I +___________H O(
3 3 4 2 4 2 2
未配平)
完成下列填空:
(1)该反应实质是两步反应:①IO +3HSO →3SO +I-+3H+,则第二步反应的离子方程式为②___________;
若要使碘酸钠的利用率最高,碘酸钠在第一步和第二步反应中的用量之比是___________。
(2)过滤反应析出的碘沉淀得到粗碘,再用升华法即可得到99%左右的碘产品,碘升华克服的微粒间作用力
为___________。(3)能说明氯、碘两种元素非金属性相对强弱的依据是___________。(选填编号)
a.原子的最外层都有7个电子
b.ICl中碘元素为+1价
c.酸性:HClO>HIO
3 3
d.氯化钠、碘化钠与浓硫酸共热,分别生成氯化氢、单质碘
(4)检验亚硫酸钠固体是否氧化变质的方法是___________。
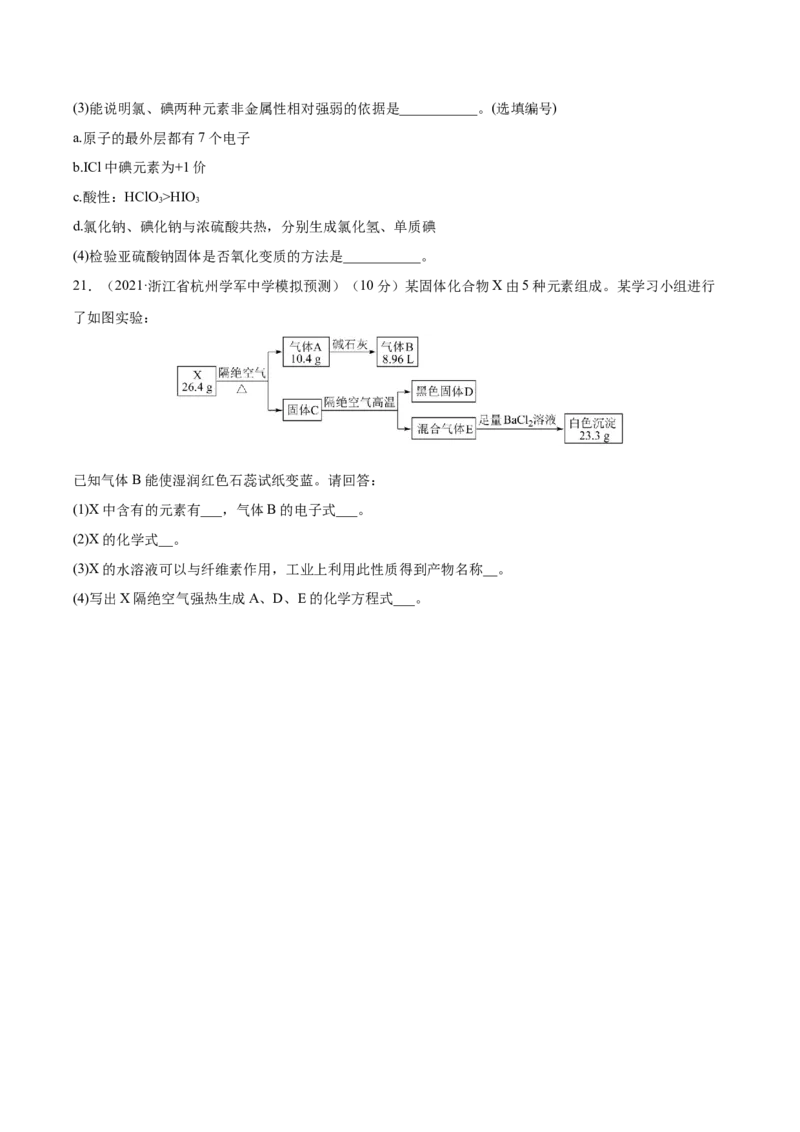
21.(2021·浙江省杭州学军中学模拟预测)(10分)某固体化合物X由5种元素组成。某学习小组进行
了如图实验:
已知气体B能使湿润红色石蕊试纸变蓝。请回答:
(1)X中含有的元素有___,气体B的电子式___。
(2)X的化学式__。
(3)X的水溶液可以与纤维素作用,工业上利用此性质得到产物名称__。
(4)写出X隔绝空气强热生成A、D、E的化学方程式___。