文档内容
解密 10 水溶液中离子反应
一、选择题
1.(2021·安徽池州市高三月考)已知:常温下,CN-的水解常数K=1.6×10-5。该温度下,将浓度均为
h
0.1 mol·L-1的HCN溶液和NaCN溶液等体积混合。下列说法正确的是( )
A.混合溶液的pH<7
B.混合液中水的电离程度小于纯水的
C.混合溶液中存在c(CN-)>c(Na+)>c(HCN)>c(OH-)>c(H+)
D.若c mol·L-1盐酸与0.6 mol·L-1 NaCN溶液等体积混合后溶液呈中性,则c=
【答案】D
【解析】A项,CN-的水解常数K =1.6×10-5,则HCN的电离平衡常数为K= =6.2510-
h a
10,K > K,所以水解程度更大,溶液显碱性,pH>7,故A错误;B项,CN-的水解促进水的电离,HCN
h a
电离抑制水的电离,而水解程度更大,所以水的电离受到促进,混合液中水的电离程度大于纯水的,故B
错误;C项,CN-的水解程度大于HCN的电离程度,所以c(HCN)>c(Na+)>c(CN-),故C错误;D项,c
mol·L-1盐酸与0.6 mol·L-1 NaCN溶液等体积混合后溶液中存在电荷守恒c(H+)+c(Na+)= c(OH-)+c(CN-)
+c(Cl-),溶液显中性,所以c(CN-)=c(Na+)- c(Cl-)= mol/L,溶液中还存在物料守恒c(HCN)
+c(CN-)=c(Na+),所以c(HCN)=c(Na+)-c(CN-)= mol/L,所以有K= =6.2510-
a
10,解得c= ,故D正确;故选D。
2.(2021·吉林长春市东北师大附中期末)根据下表提供的数据,下列说法正确的是( )
化学式 CHCOOH HClO HCO
3 2 3
电离常数 K=1.8×10-5 K=3.0×10-8 K=4.0×10-7 K=4.0×10-44
1 2
A.向NaClO溶液中通入少量CO 发生反应:ClO-+CO +H O=HClO+ HCO -
2 2 2 3
B.等浓度的NaClO和NaCO 的混合溶液中离子浓度有如下关系:c(Na+)>c(CO2-)>c(ClO-)>c(OH-)
2 3 3C.等浓度的NaClO溶液和NaHCO 溶液中,水电离的c(OH-)前者小于后者
3
D.pH相等的溶液中,溶质浓度由大到小的顺序为:NaCO>NaClO>NaHCO >CHCOONa
2 3 3 3
【答案】A
【解析】A项,由于K (H CO)>K(HClO)>K (H CO),故NaClO溶液中通入少量CO,生成HClO和
1 2 3 2 2 3 2
NaHCO ,反应的离子方程式为ClO-+CO +H O=HClO+ HCO -,故A正确;B项,由于K(HClO)>
3 2 2 3
K (H CO),则等浓度的NaClO和NaCO 的混合溶液中,水解程度ClO-<CO2-,离子浓度有c(Na+)>
2 2 3 2 3 3
c(ClO-)>c(CO2-)>c(OH-),故B错误;C项,由于K (H CO)>K(HClO),则等浓度的NaClO溶液和
3 1 2 3
NaHCO 溶液中,水解程度ClO->HCO -,水解促进水的电离,则水电离的c(OH-)前者大于后者,故C错误;
3 3
D项,由于K(CHCOOH) >K (H CO)>K(HClO)>K (H CO),酸性越强离子的水解程度越小,即水解程
3 1 2 3 2 2 3
度CHCOO-<HCO -<ClO-<CO2-,则pH相等的溶液中,溶质浓度由大到小的顺序为CHCOONa>
3 3 3 3
NaHCO >NaClO>NaCO,故D错误;故选A。
3 2 3
3.(2021·四川成都市期末)室温下,①将浓度均为0.1mol·L-1的盐酸与氨水等体积混合,混合液pH
=a;②将浓度为bmol·L-1盐酸与0.3mol·L-1氨水等体积混合,混合液 (忽略溶液体积变化)。下列判断
错误的是( )
A.a<7 b<0.3
B.常温下氨水的电离平衡常数
C.②中混合液存在:c(NH +)+c(NH ·H O)+ c(Cl-)=0.3mol·L-1
4 3 2
D.将①与②混合液混合,则混合后溶液中存在:c(Cl-)>c(NH +)
4
【答案】C
【解析】A项,①将浓度均为0.1mol·L-1的盐酸与氨水等体积混合,二者恰好完全反应生成氯化铵和水,
氯化铵水解显酸性,故混合液pH =a<7;②将浓度为bmol·L-1盐酸与0.3mol·L-1氨水等体积混合,因该混合
液pH =7,故必须盐酸少量即b<0.3,A正确;B项,由题意列电荷守恒得:c(Cl-)+c(OH-) =c(H+)
+c(NH +),因室温下混合液pH =7,说明溶液显中性,c(H+)=c(OH-),所以c(Cl-)=c(NH +),因等体积混合故
4 4
c(Cl-)=c(NH +)= mol/L。常温下氨水中一水合氨的电离方程式为NH ·H O OH-+NH+,故其电离平衡
4 3 2 4常数 ,B正确;C项,②中混合液存在物料守恒c(NH +)
4
+c(NH ·H O)= , < ,故c(NH +)+c(NH ·H O)+
3 2 4 3 2
c(Cl-)≠0.3mol·L-1,C错误;D项,因①溶液显酸性,②溶液显中性,故将①与②混合液混合显酸性,
c(H+)>c(OH-),由电荷守恒得:c(Cl-)+c(OH-) =c(H+)+c(NH +),故c(Cl-)>c(NH +),D正确;故选C。
4 4
4.(2021·天津静海区月考)下列有关实验现象和解释或结论都正确的是( )
选项 实验操作 现象 解释或结论
A 将氯化铁溶液加热灼烧 有固体析出 该固体是氯化铁
氯化铜溶液中有氯化铁杂质,加入氧化
B 有红褐色物质析出 调节pH使铁离子水解平衡右移
铜除杂
C 将充满NO 的密闭玻璃球浸泡在热水中 红棕色变深 反应2NO NO 的 H>0
2 2 2 4
向1 mL 0.l mol/L的AgNO 溶液中加入
3 先生成白色沉淀,
D 4滴0.1 mol/L的NaCl溶液,再加10滴 K (AgI)<K (AgCl)
后产生黄色沉淀 sp sp
0.1 mol/L的NaI溶液,再振荡
【答案】B
【解析】A项,氯化铁水解生成氢氧化铁和氯化氢,氯化氢易挥发,故蒸干氯化铁溶液得氢氧化铁固
体,氢氧化铁受热易分解,灼烧得氧化铁,氯化铁溶液蒸干灼烧所得固体为氧化铁,A错误;B项,溶液
中的铁离子水解呈酸性,氧化铜消耗氢离子,调节pH使铁离子水解平衡右移,促进了的铁离子的水解,
最终铁离子转化成红褐色氢氧化铁沉淀,B正确;C.红棕色变深,说明升高温度,平衡移动,二氧化氮
的浓度增大,则说明反应2NO NO 的△H<0,C错误;D项,1 mL溶液约有20滴,向1 mL 0.l
2 2 4
mol/L的AgNO 溶液中加入4滴0.1 mol/L的NaCl溶液,再加10滴0.1 mol/L的NaI溶液,AgNO 是过量的,
3 3
不能确定是AgCl转化为AgI,所以不能比较K ,故D错误;故选B。
sp
5.(2021·四川成都市期末)25℃时,K (AgCl)= 1.56×10-10,K (Ag CrO)= 9.0×10-12。已知Ag CrO 沉
sp sp 2 4 2 4
呈显砖红色。下列说法正确的是( )
A.向含大量Ag CrO 和AgCl的悬浊液中加入少量水,c(Ag+)减小
2 4
B.向同浓度NaCrO 和NaCl的混合溶液中缓慢滴加AgNO 溶液,Ag CrO 先析出
2 4 3 2 4C.向Ag CrO 悬浊液中滴入饱和NaCl溶液,白色沉淀刚出现时,溶液中
2 4
D.用AgNO 标准溶液滴定NaCl溶液时,可用KCrO 溶液作指示剂
3 2 4
【答案】D
【解析】A项,向含大量Ag CrO 和AgCl的悬浊液中加入少量水后仍处于饱和状态,温度没有改变,
2 4
溶解度不变,故c(Ag+)不变,A错误;B项,析出沉淀时,AgCl溶液中c(Ag+)= ,Ag CrO 溶液中
2 4
c(Ag+)= ,因K (AgCl)= 1.56×10-10,K (Ag CrO)= 9.0×10-12,向同浓度NaCrO 和NaCl的
sp sp 2 4 2 4
混合溶液中缓慢滴加AgNO 溶液,析出AgCl所需的c(Ag+)小,故先析出AgCl,B错误;C项,向悬浊液
3
中滴入饱和NaCl溶液,白色沉淀刚出现时,溶液中
,C错误;D项,由B知先析出
AgCl,故用AgNO 标准溶液滴定 溶液时,可用KCrO 溶液作指示剂,当恰好开始出现砖红色沉淀
3 2 4
时,说明AgCl已沉淀完全即达到滴定终点,D正确;故选D。
6.(2021·河北高三零模)H PO 的电离是分步进行的,常温下Ka=7.6×10-3,Ka=6.3×10-8,
3 4 1 2
Ka=4.4×10-13。下列说法正确的是( )
3
A.浓度均为0.1 mol/L的NaOH溶液和HPO 溶液按照体积比2∶1混合,混合液的pH<7
3 4
B.NaHPO 溶液中,c(H+)+ c(HPO -)+c(HPO )= c(PO 3-)+c(OH-)
2 4 2 4 3 4 4
C.向0.1 mol/L的HPO 溶液中通入HCl气体(忽略溶液体积的变化),溶液pH=1时,溶液中大约有
3 4
7.1%的HPO 电离
3 4
D.在HPO 溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=11时,
3 4
c(PO 3-)>c(HPO 2-)
4 4
【答案】C
【解析】A项,浓度均为0.1 mol/L的NaOH溶液和HPO 溶液按照体积比2∶1混合,二者恰好反应
3 4
产生NaHPO ,在溶液中HPO 2-存在电离平衡:HPO 2- PO 3-+H+,也存在着水解平衡:HPO 2-+H O
2 4 4 4 4 4 2HPO -+OH-,电离平衡常数Ka=4.4×10-13,水解平衡常数K =
2 4 3 h2
=1.58×10-7>K =4.4×10-13,水解程度大于
a3
电离程度,因此溶液显碱性,pH>7,A错误;B项,在NaHPO 溶液中,根据质子守恒可得: c(H+)+
2 4
c(HPO -)+2c(HPO )= c(PO 3-)+c(OH-),B错误;C项,向0.1 mol/L的HPO 溶液中通入HCl气体(忽略溶液
2 4 3 4 4 3 4
体积的变化,溶液pH=1时,c(H+)=0.1 mol/L,假设电离的HPO 为x,根据电离平衡常数K =
3 4 a1
,解得x≈0.0071 mol/L,因此溶液中HPO 电离度
3 4
= =7.1%,C正确;D项,在HPO 溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH
3 4
增大,当溶液的pH=11时,c(H+)=10-11 mol/L,K = ,则
a3
,则c(PO 3-)<c(HPO 2-),D错误;故选C。
4 4
7.(2021·江苏高三零模)室温下,通过下列实验探究NaCO 溶液的性质。
2 3
实验 实验操作和现象
1 用pH试纸测定0.1 mol/L Na CO 溶液的pH,测得pH约为12
2 3
2 向0.1 mol/L Na CO 溶液中加入过量0.2 mol/L CaCl 溶液,产生白色沉淀
2 3 2
3 向0.1 mol/L Na CO 溶液中通入过量CO,测得溶液pH约为8
2 3 2
4 向0.1 mol/L Na CO 溶液中滴加几滴0.05 mol/L HCl,观察不到实验现象
2 3
下列有关说法正确的是( )
A.0.1 mol/L Na CO 溶液中存在c(OH-)=c(H+)+2c(H CO)+c(HCO -)
2 3 2 3 3
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO2-)0;升温有利于提高草酸的电离程度
2 2 4 2 4
B.草酸中的碳为+3价,具有较强的还原性△,可使酸性高锰酸钾溶液褪色
C.25℃时,KHC O 溶液呈弱酸性,有时用于清洗金属表面的锈迹
2 4
D.同浓度的KHC O 和KC O 混合溶液中:2c( H C O) +2c( HC O)+2c( C O2-) =3c(K+)
2 4 2 2 4 2 2 4 2 4 2 4
【答案】D
【解析】A项,升高温度,电离平衡正向进行,有利于提高草酸的电离度,A正确;B项,草酸中氢
元素为+1价,氧元素为-2价,所以碳元素为+3价,具有较强的还原性,可以与高锰酸钾反应使其褪色,B
正确;C项,25℃时,HC O-的水解平衡常数K = = =1.7×10-13< K ,草酸氢根的电离程度大
2 4 h a2
于水解程度,所以其呈弱酸性,可以用来清洗金属表面的锈迹,C正确;D项,根据物料守恒有,同浓度
的KHC O 和KC O 混合溶液中:3c(H C O)+3c(HC O)+3c(C O2-)=2c(K+),D错误;故选D。
2 4 2 2 4 2 2 4 2 4 2 4
10.(2021届·湖北省松滋市言程中学高三质检)有相同体积pH均为3的醋酸和盐酸,下列说法正确的
是( )
A.稀释10倍后,两者的pH变化醋酸大于盐酸
B.中和相同浓度的氢氧化钠溶液,消耗氢氧化钠的物质的量盐酸大于醋酸
C.加入一定量的锌粉,产生气体的体积相同,则醋酸一定过量
D.加入足量的锌粉,产生氢气的速率随时间的变化如图
【答案】C
【解析】A项,相同体积pH均为3的醋酸和盐酸,初始时氢离子浓度相同,醋酸为弱酸,加水稀释
促进醋酸的电离,将pH均为3的盐酸和醋酸溶液分别稀释10倍后,醋酸溶液的pH变化小,故A错误;B
项,盐酸是强酸不存在电离平衡,醋酸是弱酸,溶液中存在电离平衡,相同体积pH均为3的醋酸和盐酸
两种溶液总氢离子浓度相同,醋酸的浓度大于盐酸,加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积醋酸大于盐酸,故B错误;C项,相同体积pH均为3的醋酸和盐酸溶液的氢离子物质的量相等,
加入一定量的锌粉,醋酸溶液中存在电离平衡,反应后醋酸又电离出氢离子,则产生气体的体积相同,两
种溶液中消耗的氢离子物质的量相等,锌完全消耗说明醋酸过量,故C正确;D项,相同体积pH均为3
的醋酸和盐酸溶液中氢离子浓度相同,加入足量的锌粉,反应开始时反应速率相等,醋酸溶液中存在电离
平衡,反应后醋酸又电离出氢离子,因此产生的氢气的速率大于盐酸,反应后期强酸的反应速率下降得快,
最终生成氢气的体积小,故D错误;故选C。
11.(2021·宁夏银川市银川一中高三月考)已知pOH=-lgc(OH-),向20mL0.1mol·L-1的氨水中滴加未知
浓度的稀HSO ,测得混合溶液的温度、pOH随加入稀硫酸体积的变化如下图所示,下列说法不正确的是(
2 4
)
A.稀HSO 的物质的量浓度为0.05mol·L-1
2 4
B.当溶液中pH=pOH时,水的电离程度最小
C.a点时溶液中存在c(NH ·H O)+2c(OH-)=c(NH +)+2c(H+)
3 2 4
D.a、b、c 三点对应 NH +的水解平衡常数:K (b)>K (a)>K (c)
4 h h h
【答案】B
【解析】向20mL0.1mol•L-1的氨水中滴加未知浓度的稀HSO ,反应放热,溶液的温度升高,当二者
2 4
恰好完全反应时,放热最多,溶液的温度最高,所以硫酸的体积为20mL时,恰好完全反应。A项,有分
析可知:加入20ml硫酸与氨水恰好完全反应,硫酸是二元酸,一水合氨是一元碱,所以稀HSO 的物质
2 4
的量浓度为0.05mol·L-1 ,故A不选;B项,当溶液中pH=pOH时,溶液呈中性,水的电离既不促进又不
抑制,而不滴加硫酸时,溶液显碱性,抑制水的电离,当加入40ml硫酸时,酸过量,抑制水的电离,氨
水与硫酸恰好反应生成硫酸铵时水的电离程度最大,故B选;C项,a点时反应后溶质为一水合氨和硫酸
铵,且硫酸铵为一水合氨浓度的一半,有电荷守恒c(NH +)+c(H+)= c(OH-)+2c(SO 2-) 和物料守恒
4 4
4c(SO 2-)=c(NH +)+c(NH ·H O) 得c(NH ·H O)+2c(OH-)=c(NH +)+2c(H+) ,故C不选;D项,升高温度促
4 4 3 2 3 2 4
进铵根离子水解,水解常数增大,由图可知,温度:b>a>c ,则a、b、c 三点对应 NH +的水解平衡常
4
数:K (b)>K (a)>K (c),故D不选;故选B。
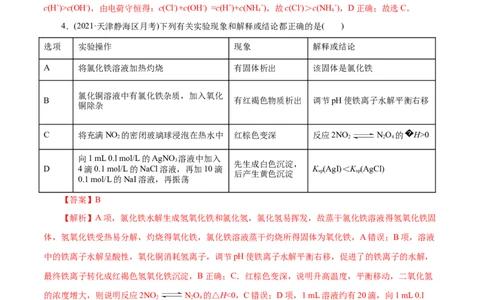
h h h12.(2021·陕西宝鸡市高三一模)常温下将NaOH溶液滴加到亚硒酸(H SeO) 溶液中,混合溶液的pH
2 3
与离子浓度变化的关系如图所示。下列叙述正确的是( )
A.曲线N表示pH与
B.图中a点对应溶液中: c (Na+) > c (HSeO -) + 2c (SeO 2-)
3 3
C.K (H SeO)与K HSeO) 之比为103
a1 2 3 a2( 2 3
D.NaHSeO 溶液中: c (HSeO-) > c (SeO 2-) > c (H SeO)
3 3 3 2 3
【答案】D
【解析】A项, = , = ,则pH相同时, = >
= ,根据图象可知,曲线M表示pH与 的关系,曲线N表示pH与
的变化关系,故A错误;B项,a点时pH=2.6,溶液显酸性,根据电荷守恒有:c (Na+) + c
(H+)= c (HSeO-) + 2c (SeO 2-)+c (OH-),由c (H+)> c (OH-),可知c (Na+) < c (HSeO -) + 2c (SeO 2-),故B错误;
3 3 3 3
C项,a点: =0,即 ,由 = 可知,Ka=c(H+)=10-2.6;b点
1
=0,即 ,由 = 可知,Ka=c(H+)=10-6.6;得
2
=104,故C错误;D项,由上面C选项分析可知,HSeO -的电离常数Ka=10-6.6,HSeO -的水解常数=
3 2 3<10-6.6,即HSeO -以电离为主,故NaHSeO 溶液中: c (HSeO-) > c (SeO 2-) > c (H SeO),故
3 3 3 3 2 3
D正确;故选D。
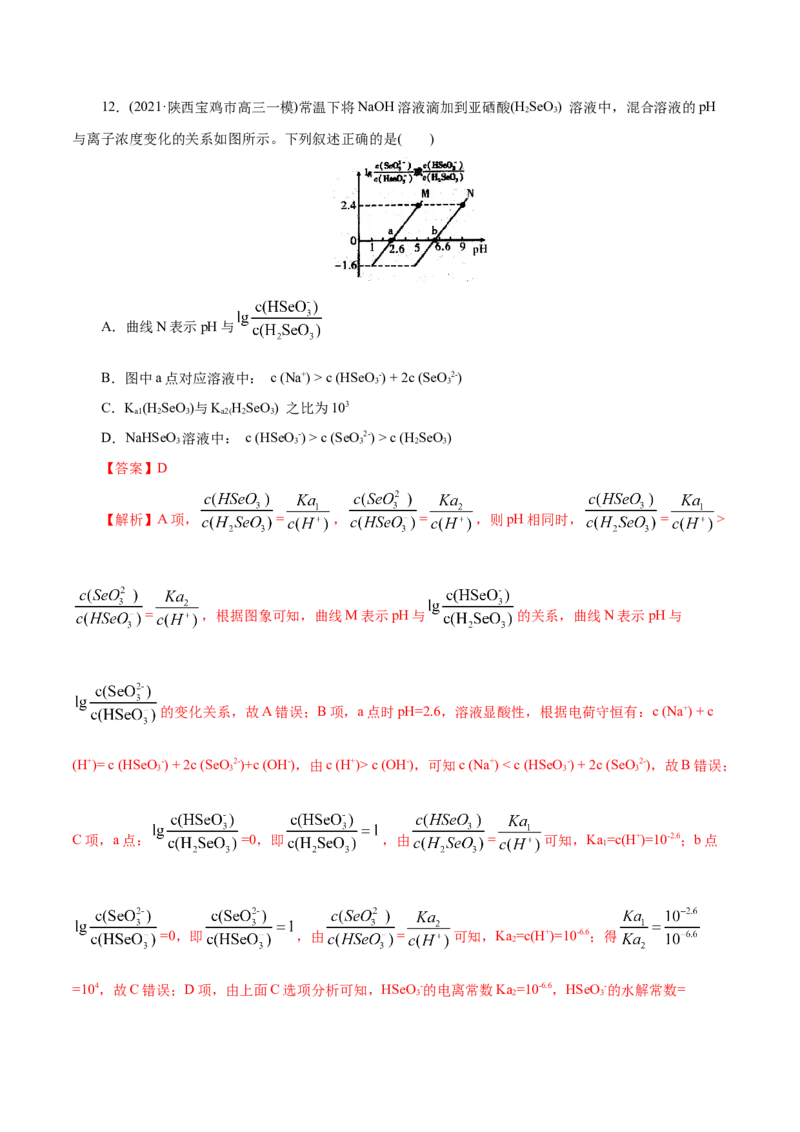
13.(2021·广东高三零模)水体中重金属铅的污染问题备受关注。溶液中Pb2+及其与OH- 形成的微粒的
浓度分数α随溶液pH变化的关系如图所示。已知NH ·H O 的K =1.74 ×10-5。向Pb(NO ) 溶液中滴加氨水,
3 2 b 3 2
关于该过程的说法正确的是( )
A.Pb2+的浓度分数先减小后增大
B.c(NO -)与c(Pb2+)的比值减小后增大, pH> 10后不变
3
C.pH=7时,存在的阳离子仅有Pb2+、Pb(OH)+和H+
D.溶液中Pb2+与Pb(OH) 浓度相等时,氨主要以NH +的形式存在
2 4
【答案】D
【解析】由图示可知,Pb2+与OH–依次形成Pd(OH)+、Pd(OH)、Pd(OH) -、Pd(OH)2-四种微粒。A项,
2 3 4
随着pH的增大,Pb2+的浓度分数逐渐减小,当pH=10时,Pb2+的浓度分数减小为0,A错误;B项,NO -
3
与Pb2+在同一溶液中,c(NO -)与c(Pb2+)的比值等于其物质的量之比,滴加氨水过程中,随着pH的增大,
3
n(Pb2+)逐渐减小,n(NO -)不变,n(NO -)与n(Pb2+)的比值增大,故c(NO -)与c(Pb2+)的比值增大,pH>10,
3 3 3
c(Pb2+)减小为0时,比值无意义,B错误;C项,当pH=7时,根据图示可知,溶液中存在的阳离子有
Pb2+、Pb(OH)+、H+以及NH +,C错误;D项,当溶液中Pb2+与Pb(OH) 浓度相等时,由图可知,此时溶液
4 2
pH约等于8,由NH ·H O电离常数K = =1.74 ×10-5,则 = =
3 2 b
=17.4,故溶液中氨主要以NH +形式存在,D正确;故答案选D。
4
14.(2021·山东烟台市高三期末)某二元酸HMO 在水中分两步电离:HMO =H++HMO -,HMO -
2 4 2 4 4 4H++MO 2-。常温下,向20 mL 0.1mol·Lˉ1NaHMO 溶液中滴入cmol·L-1 NaOH溶液,溶液温度与滴
4 4
入NaOH溶液体积关系如图。下列说法正确的是( )
A.该NaOH溶液pH=13
B.从G点到H点水的电离平衡正向移动
C.图像中E点对应的溶液中c(Na+)= c(HMO )+c(HMO -)+ c(MO 2-)
2 4 4 4
D.若F点对应的溶液pH=2,则MO 2-的水解平衡常数约为 5.4×10-13mol·L-1
4
【答案】A
【解析】A项,由HMO 在水中的电离方程式可知,第一步完全电离,第二步部分电离,由图可知,
2 4
向20 mL 0.1mol·Lˉ1NaHMO 溶液中滴入cmol·L-1 NaOH溶液,当加入20mLNaOH溶液时,溶液的温度最
4
高,此时恰好反应,则NaOH溶液的浓度也为0.1mol/L,故该NaOH溶液pH=13,故A正确;B项,由A
分析知,G点恰好反应生成NaMO ,继续加入NaOH溶液,水的电离程度减小,故从G点到H点水的电
2 4
离平衡逆向移动,故B错误;C项,图像中E点表示20 mL 0.1mol·Lˉ1NaHMO 溶液,由于HMO -不会水
4 4
解,则溶液中不存在HMO ,对应的溶液中c(Na+)=c(HMO -)+ c(MO 2-),故C错误;D项,F点对应加入
2 4 4 4
10mLNaOH溶液,此时溶液为等浓度的NaHMO 与NaMO 的混合溶液,对于MO 2-的水解反应MO 2-+H O
4 2 4 4 4 2
HMO -+OH- ,MO 2-的水解平衡常数为 ,此时,c(HMO -)≈c(MO 2-),则
4 4 4 4
MO 2-的水解平衡常数 ,故D错误;故选A。
4
15.(2021·甘肃白银市期末)向 溶液中缓慢滴加100 mL 盐酸,
溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和 未画出),已知:碳酸的电离平
衡常数 , ,下列说法错误的是( )A.滴加至A点时,
B.滴加至B点时,
C.滴加至C点时,
D.滴加至D点时,溶液的pH<7
【答案】C
【解析】A项,滴加至A点时,根据物料守恒知:n(K+)=2n(CO2-)+2n(HCO -)+2n(HCO)(此时无二氧
3 3 2 3
化碳生成),由图A点知n(Cl-)=n(CO2-)>n(HCO -), ,故A正确;B项,
3 3
, ,B点时,n(CO2-)=n(HCO -),
3 3
c(H+)=5.60×10-11, ,故B正确;C项,由C点知,
n(Cl-)>n(HCO -)>n(CO2-),此时加入n(HCl)=0.01 mol,此时溶质为KCl和KHCO ,且等浓度,由物料守恒
3 3 3
得:n(Cl-)=n(CO2-)+n(HCO -)+n(HCO),又因为n(HCO)>n(CO2-),所以 ,
3 3 2 3 2 3 3
故C错误;D项,D点时,n(Cl-)=0.02 mol,说明KCO+2HCl=2KCl+CO ↑+H O恰好完全反应,生成的二氧
2 3 2 2
化碳部分溶于水,则溶液的pH<7,故D正确;故选C。
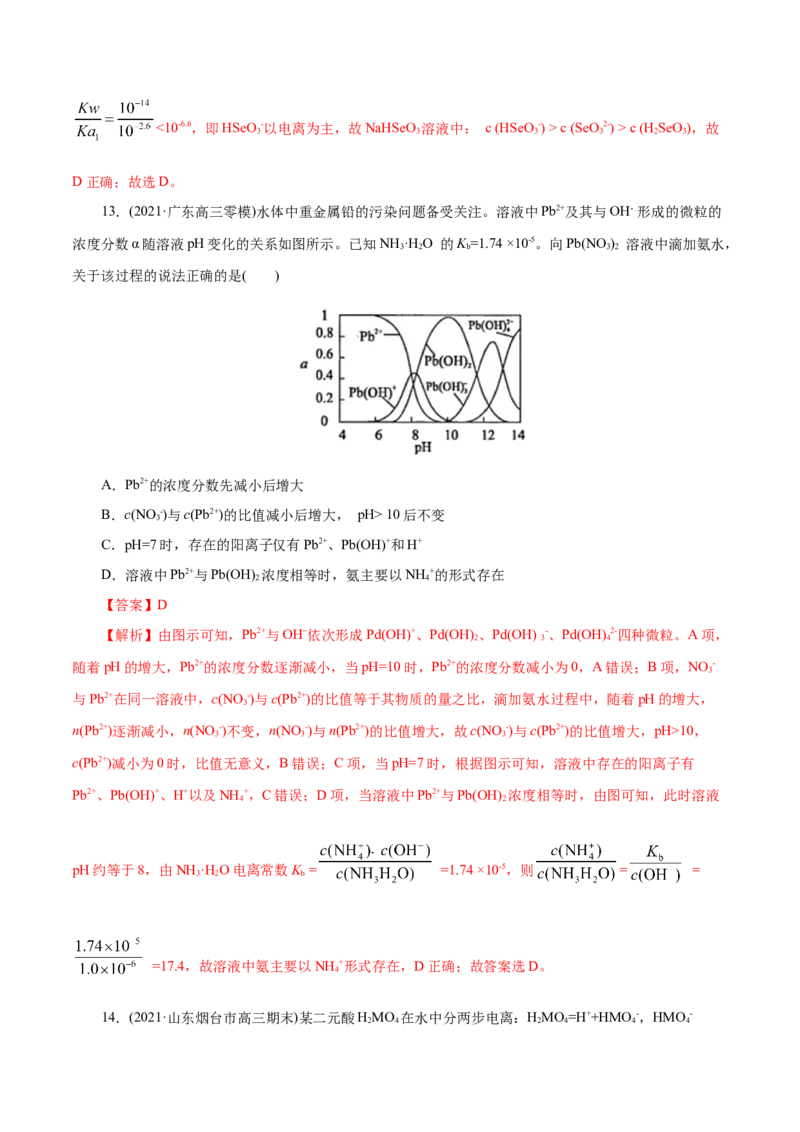
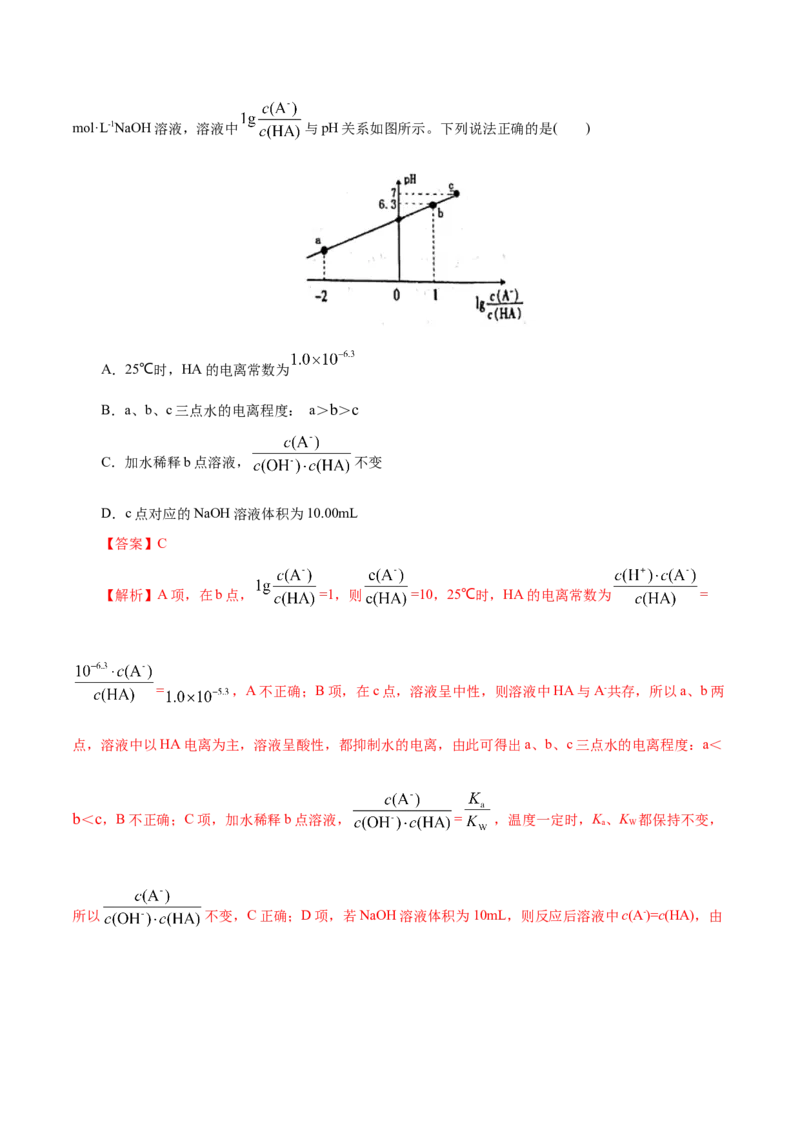
16.(2021·福建三明市高三期末)25℃时,在20 mL 0.1 mol·L-1一元弱酸HA溶液中滴加0.1mol·L-1NaOH溶液,溶液中 与pH关系如图所示。下列说法正确的是( )
A.25℃时,HA的电离常数为
B.a、b、c三点水的电离程度: a>b>c
C.加水稀释b点溶液, 不变
D.c点对应的NaOH溶液体积为10.00mL
【答案】C
【解析】A项,在b点, =1,则 =10,25℃时,HA的电离常数为 =
= ,A不正确;B项,在c点,溶液呈中性,则溶液中HA与A-共存,所以a、b两
点,溶液中以HA电离为主,溶液呈酸性,都抑制水的电离,由此可得出a、b、c三点水的电离程度:a<
b<c,B不正确;C项,加水稀释b点溶液, = ,温度一定时,K、K 都保持不变,
a W
所以 不变,C正确;D项,若NaOH溶液体积为10mL,则反应后溶液中c(A-)=c(HA),由=10-5.3,可求出c(H+)=10-5.3,则表明HA发生电离,而c点时pH=7,则应继续加入NaOH溶
液,所以c点对应的NaOH溶液体积应大于10.00mL,D不正确;故选C。
17.(2021·黑龙江牡丹江市牡丹江一中高三期末)25 ℃时,改变0.1 mol/L弱酸RCOOH溶液的pH,溶
液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知δ(RCOOH)= ],甲
酸(HCOOH)与丙酸(CHCHCOOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是( )
3 2
A.若弱酸pH增大是通过向弱酸中加入NaOH固体实现的,则图中M、N两点对应溶液中的c(Na+)相
等
B.对于甲酸和丙酸,当lg[c(RCOOH)/c(RCOO-)]>0时,溶液都为酸性
C.等浓度的HCOONa和CHCHCOONa两种溶液中的c(NaOH)相等
3 2
D.将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>
c(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
【答案】B
【解析】A项,当溶液中δ(RCOOH)=δ(RCOO-)时c(RCOOH)=c(RCOO-),K=
a
=c(H+)=10-pH,电离平衡常数越大,酸的酸性越强,根据图知:K(HCOOH)>K(CHCHCOOH),则酸性:
a a 3 2
HCOOH>CHCHCOOH,要使混合溶液中δ(RCOOH)=50%,混合溶液中酸的电离程度等于盐的水解程度,
3 2
酸性越强,加入的NaOH越多;故A错误;B项,当lg[c(RCOOH)/c(RCOO-)]>0时,c(RCOOH)>
c(RCOO-),即δ(RCOOH)>δ(RCOO-),根据图知,甲酸中M点前、丙酸中N 点前溶液都呈酸性,故B正
确;C项,等浓度的HCOONa和CHCHCOONa两种溶液中,水解程度:甲酸<丙酸,则CHCHCOONa
3 2 3 2
溶液中c(NaOH)越大,故C错误;D项,根据图知,K(HCOOH)=c(H+)=10-pH=10-3.75,则K (HCOO-)=
a h=10-10.25<K(HCOOH)=10-3.75,说明HCOOH电离程度大于HCOO-水解程度导致混合溶液呈酸性,
a
c(OH-)<c(H+),根据电荷守恒得c(Na+)<c(HCOO-),溶液中存在c(HCOO-)>c(Na+)>c(HCOOH)>c(H+)>
c(OH-),故D错误;故选B。
18.(2021·黑龙江牡丹江市牡丹江一中高三期末)常温下,二甲胺[(CH )NH·HO]是一元弱碱,其电离
3 2 2
常数K=1.6×10-4,10 mL c mol·L-1二甲胺溶液中滴加0.1 mo1·L-1盐酸,混合溶液的温度与盐酸体积的关系如
b
图所示。下列说法不正确的( )
A.二甲胺溶液的浓度为0.2 mol·L-1
B.在Y和Z点之间某点溶液pH=7
C.Y点存在:c(Cl-)>c[(CH )NH +]>c(H+)>c(OH-)
3 2 2
D.常温下,(CH)NH Cl水解常数K ≈6.25×10-11
3 2 2 h
【答案】B
【解析】A项,二甲胺与盐酸恰好完全中和时放出热量最多,溶液温度最高,即Y点表示酸碱恰好完
全反应,由反应方程式(CH)NH•H O+HCl=(CH )NH Cl+H O可知二甲胺溶液的浓度为0.2mol•L-1,故A正
3 2 2 3 2 2 2
确;B项,二甲胺是弱碱,Y点对应溶质是强酸弱碱盐,其溶液呈酸性,X点对应的溶液中
(CH)NH•H O、(CH)NH Cl的浓度相等,其混合溶液呈碱性,故中性点应在X点与Y点之间,故B错误;
3 2 2 3 2 2
C项,二甲胺是弱碱,Y点对应溶质是强酸弱碱盐,其溶液呈酸性,则Y点存在c(Cl-)>c[(CH )NH +]>
3 2 2
c(H+)>c(OH-),故C正确;D项,(CH)NH Cl水解常数K = = ≈6.25×10-11,故D正确;故选
3 2 2 h
B。
19.(2021·自贡市田家炳中学高三月考)常温下,用20 mL 0.1 mol·L-1 NaSO 溶液吸收SO 气体,吸收
2 3 2液的pH与lg 的关系如图所示。下列说法错误的是( )
A.b点对应的溶液中:c(Na+)>c(HSO -)=c(SO 2-)>c(OH-)>c(H+ )
3 3
B.c点对应的溶液中:c(Na+)=c(HSO -)+c(SO 2-)
3 3
C.常温下,HSO 第二步电离常数K =1.0×10-7.2
2 3 a2
D.在通入SO 气体的过程中,水的电离平衡逆向移动
2
【答案】B
【解析】A项,NaSO 溶液吸收SO 气体,发生反应:SO +Na SO +H O=2NaHSO ,b点对应的溶液
2 3 2 2 2 3 2 3
pH=7.2,lg =0,即溶液中c(OH-)>c(H+),c(HSO -)=c(SO 2-),结合电荷守恒:c(Na+)+ c(H+)=
3 3
c(HSO -)+2 c(SO 2-)+ c(OH-)知,c(Na+)>c(HSO -),A项正确;B项, pH=7.0,溶液呈中性,
3 3 3
c(OH-)=c(H+),依据电荷守恒:c(Na+)+ c(H+)= c(HSO -)+2 c(SO 2-)+ c(OH-),c(Na+)= c(HSO -)+2 c(SO 2-),
3 3 3 3
B项错误;C项, b点溶液pH=7.2,lg =0,即c(H+)=1.0×10-7.2,c(HSO -)= c(SO 2-),
3 3
,C项正确;D项, 由图可知,在通入SO 气体的过程中,溶液的酸性
2
不断增强,对水的电离抑制程度逐渐增大,故水的电离平衡逆向移动,D项正确;故选B。
20.(2021·山东潍坊市寿光现代中学高三月考)锰是重要的合金材料和催化剂,在工农业生产和科技领
域有广泛的用途。利用某工业废料[含MnO 、MnOOH、Zn(OH) 及少量Fe]制备Zn和MnO 的一种工艺流
2 2 2
程如图所示:已知:
①MnO能溶于酸,且Mn2+在酸性条件下比较稳定,pH高于5.5时易被O 氧化。
2
②室温下,K [Mn(OH) ]=10-13,K [Fe(OH) ]=10-38,K [Zn(OH) ]=10-17(当离子浓度≤10-5mol·L-1可认为
sp 2 sp 3 sp 2
沉淀完全)
下列说法错误的是( )
A.加入过量炭黑主要作用是将MnO 、MnOOH转化为MnO
2
B.“酸浸”时,不可以用浓盐酸代替稀硫酸
C.“净化”时,溶液中Mn2+、Zn2+的浓度约为0.1mol·L-1,调节pH的合理范围是3≤pH<8
D.“电解”时,阳极产物制得MnO ,阴极制得Zn,余下电解质溶液经处理可循环使用
2
【答案】C
【解析】“还原焙烧”时过量炭黑将废料[含MnO 、MnOOH、Zn(OH) 及少量Fe]中的MnO 、
2 2 2
MnOOH还原为MnO,Zn(OH) 受热分解产生ZnO,“还原焙烧后”得到含MnO、ZnO、Fe、炭黑的固体;
2
“酸浸”时硫酸和MnO、ZnO、Fe反应,过滤除去炭黑,滤渣1主要成分为炭黑,得到含Mn2+、Zn2+、
Fe2+、Fe3+、H+的滤液;“净化”时加合适的氧化剂将Fe2+氧化为Fe3+,再调pH到适当范围使Fe3+形成沉淀,
然后过滤除去,滤渣2主要成分为Fe(OH) ;通过“电解”阳极得到MnO ,阴极得到Zn。A项,从流程和
3 2
信息来看加入过量炭黑主要作用是将MnO 、MnOOH转化为MnO,A正确;B项,若“酸浸”时,用浓
2
盐酸代替稀硫酸,则溶液中含氯离子,电解时阳极产生氯气,不产生MnO ,因此“酸浸”时,不可以用
2
浓盐酸代替稀硫酸,B正确;C项,K [Fe(OH) ]=10-38,Fe3+完全沉淀时(Fe3+浓度≤10-5mol·L-1可认为沉淀
sp 3
完全),10-38≥10-5×c3(OH-),10-33≥c3(OH-),10-11 mol·L-1≥c(OH-),c(H+)≥10-3 mol·L-1,pH≥3,即Fe3+完全沉淀
的pH≥3;K [Mn(OH) ]=10-13,Mn2+开始沉淀时,10-13=0.1×c2(OH-),c2(OH-)=10-12,c(OH-)=10-6,pH=8;
sp 2
K [Zn(OH) ]=10-17,Zn2+开始沉淀时,10-17=0.1×c2(OH-),c2(OH-)=10-16,c(OH-)=10-8,pH=6;本题中,净化
sp 2
的目的是使Fe3+沉淀而除去,但不能使Zn2+、Mn2+形成沉淀,因此调节pH的合理范围是3≤pH<6,C错误;
D项,电解时,Mn2+在阳极失电子转化为MnO ,电极反应式为Mn2+-2e-+2H O=MnO +4H+,Zn2+在阴极得
2 2 2
电子转化为Zn,电极反应式为Zn2++2e-=Zn,因此阳极产生的H+和溶液中的硫酸根形成硫酸,硫酸经净化
处理可循环利用于“酸浸”,D正确。答案选C。
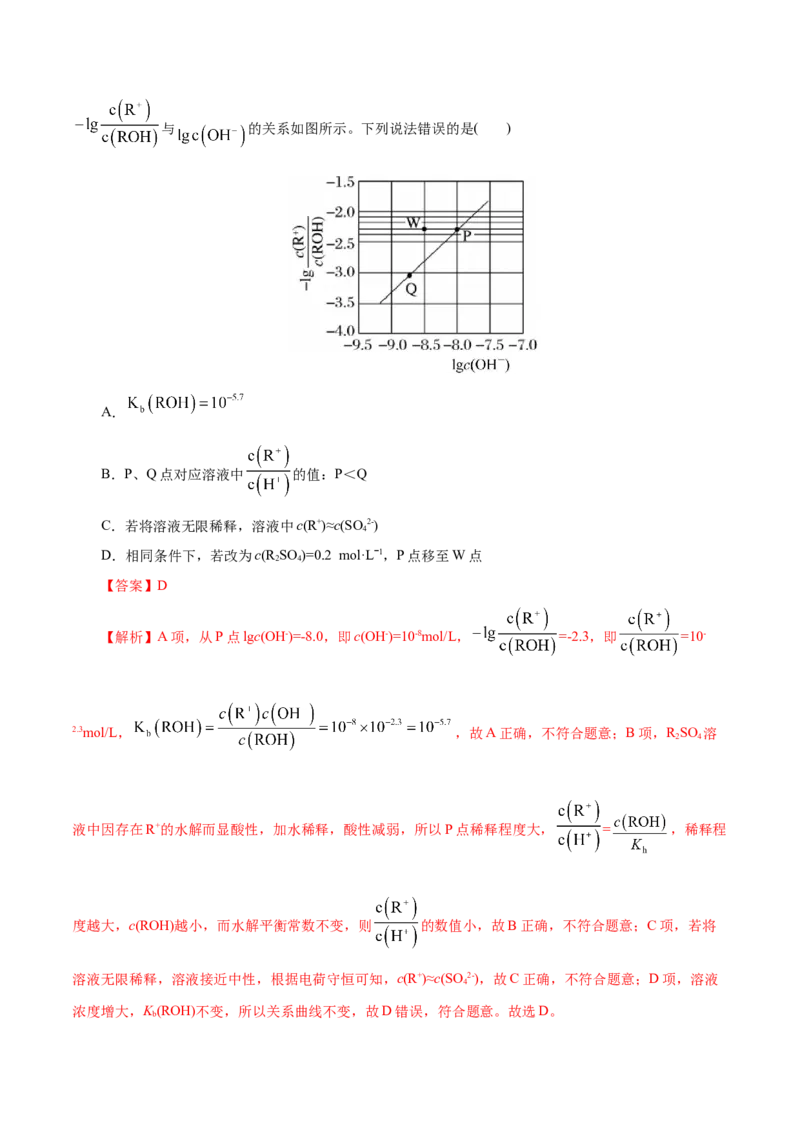
21.(2021·怀仁市第一中学校月考)25℃时,0.1 mol·Lˉ1R SO 溶液加水稀释,混合溶液中
2 4与 的关系如图所示。下列说法错误的是( )
A.
B.P、Q点对应溶液中 的值:P<Q
C.若将溶液无限稀释,溶液中c(R+)≈c(SO 2-)
4
D.相同条件下,若改为c(R SO )=0.2 mol·Lˉ1,P点移至W点
2 4
【答案】D
【解析】A项,从P点lgc(OH-)=-8.0,即c(OH-)=10-8mol/L, =-2.3,即 =10-
2.3mol/L, ,故A正确,不符合题意;B项,R SO 溶
2 4
液中因存在R+的水解而显酸性,加水稀释,酸性减弱,所以P点稀释程度大, = ,稀释程
度越大,c(ROH)越小,而水解平衡常数不变,则 的数值小,故B正确,不符合题意;C项,若将
溶液无限稀释,溶液接近中性,根据电荷守恒可知,c(R+)≈c(SO 2-),故C正确,不符合题意;D项,溶液
4
浓度增大,K (ROH)不变,所以关系曲线不变,故D错误,符合题意。故选D。
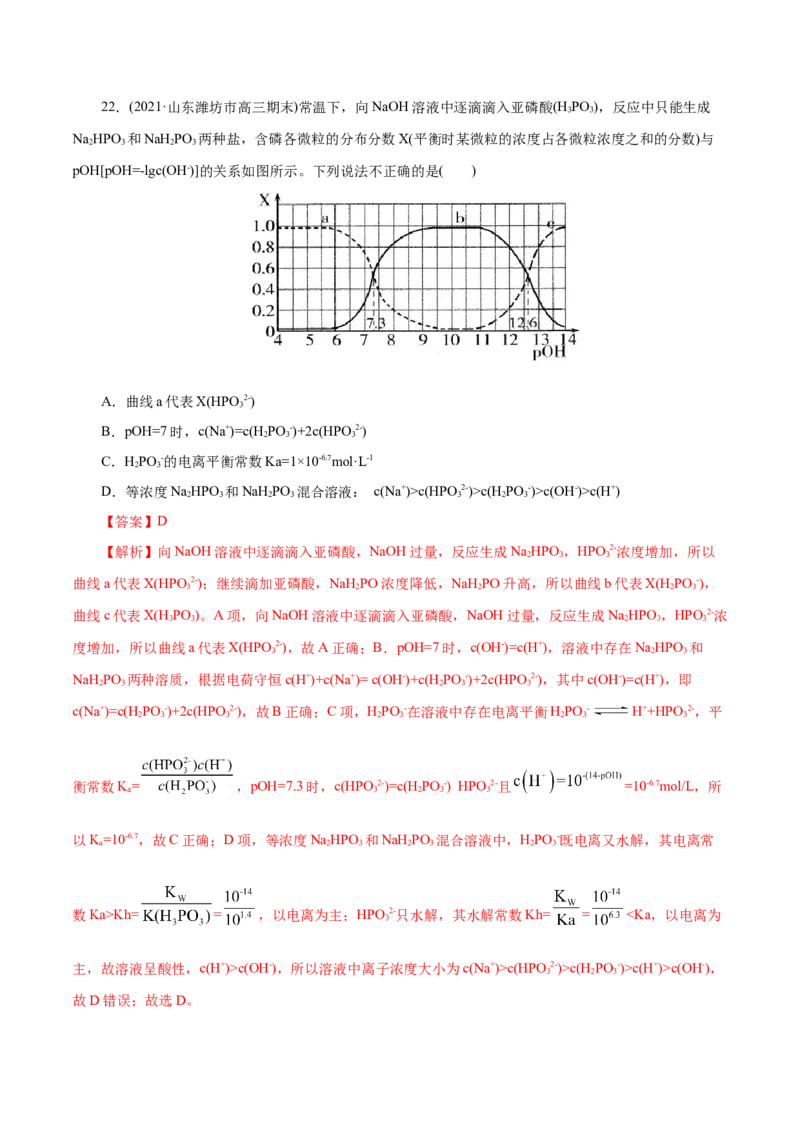
b22.(2021·山东潍坊市高三期末)常温下,向NaOH溶液中逐滴滴入亚磷酸(H PO ),反应中只能生成
3 3
NaHPO 和NaH PO 两种盐,含磷各微粒的分布分数X(平衡时某微粒的浓度占各微粒浓度之和的分数)与
2 3 2 3
pOH[pOH=-lgc(OH-)]的关系如图所示。下列说法不正确的是( )
A.曲线a代表X(HPO2-)
3
B.pOH=7时,c(Na+)=c(H PO -)+2c(HPO 2-)
2 3 3
C.HPO -的电离平衡常数Ka=1×10-6.7mol·L-1
2 3
D.等浓度NaHPO 和NaH PO 混合溶液: c(Na+)>c(HPO 2-)>c(H PO -)>c(OH-)>c(H+)
2 3 2 3 3 2 3
【答案】D
【解析】向NaOH溶液中逐滴滴入亚磷酸,NaOH过量,反应生成NaHPO ,HPO 2-浓度增加,所以
2 3 3
曲线a代表X(HPO2-);继续滴加亚磷酸,NaH PO浓度降低,NaH PO升高,所以曲线b代表X(H PO -),
3 2 2 2 3
曲线c代表X(H PO )。A项,向NaOH溶液中逐滴滴入亚磷酸,NaOH过量,反应生成NaHPO ,HPO 2-浓
3 3 2 3 3
度增加,所以曲线a代表X(HPO2-),故A正确;B.pOH=7时,c(OH-)=c(H+),溶液中存在NaHPO 和
3 2 3
NaH PO 两种溶质,根据电荷守恒c(H+)+c(Na+)= c(OH-)+c(H PO -)+2c(HPO 2-),其中c(OH-)=c(H+),即
2 3 2 3 3
c(Na+)=c(H PO -)+2c(HPO 2-),故B正确;C项,HPO -在溶液中存在电离平衡HPO - H++HPO 2-,平
2 3 3 2 3 2 3 3
衡常数K= ,pOH=7.3时,c(HPO 2-)=c(HPO -) HPO 2-且 =10-6.7mol/L,所
a 3 2 3 3
以K=10-6.7,故C正确;D项,等浓度NaHPO 和NaH PO 混合溶液中,HPO -既电离又水解,其电离常
a 2 3 2 3 2 3
数Ka>Kh= = ,以电离为主;HPO 2-只水解,其水解常数Kh= = c(OH-),所以溶液中离子浓度大小为c(Na+)>c(HPO 2-)>c(H PO -)>c(H+)>c(OH-),
3 2 3
故D错误;故选D。23.(2021·江苏扬州市高三期末)常温下,K (NH ·H O)=1.8×10-5,K (H CO)=4.2×10-7,
b 3 2 a1 2 3
K (H CO)=5.6×10-11。向20ml0.1mol·L-1NH HCO 溶液中加入NaOH固体并恢复至常温,理论上溶液中
a2 2 3 4 3
NH +、NH ·H O、HCO -、CO2-的变化如图所示(忽略溶液体积的变化)。下列说法正确的是( )
4 3 2 3 3
A.0.1mol·L-1NH HCO 溶液:c(NH +)>c(HCO)>c(HCO -)>c(NH ·H O)
4 3 4 2 3 3 3 2
B.0.1mol·L-1NH HCO 溶液:c(NH +)+c(NH·H O)+c(HCO -)+c(CO 2-)=0.2mol·L-1
4 3 4 3 2 3 3
C.曲线a表示的是c(NH +)的变化
4
D.M点时:c(CO2-)+c(HCO-)+c(OH-)=0.1mol·L-1+c(H+)
3 3
【答案】C
【解析】A项,0.1mol·L-1NH HCO 溶液中,NH ++H O NH ·H O+H+水解平衡常数K= =
4 3 4 2 3 2 1
= ,HCO -+H O HCO+OH-水解平衡常数K= = = 10-3,
3 2 2 3 2
K> K ,所以HCO -的水解程度大,则:c(NH +)>c(HCO -)>c(HCO)>c(NH ·H O),故A错误;B项,由物
2 1 3 4 3 2 3 3 2
料守恒可知c(NH +)+c(NH·H O) =0.1mol·L-1,c(HCO) +c(HCO -)+c(CO 2-)=0.1mol·L-1,所以c(NH +)
4 3 2 2 3 3 3 4
+c(NH·H O)+c(HCO -)+c(CO 2-)<0.2mol·L-1,故B错误;C项, NH HCO 中HCO -更易于OH-结合反应生
3 2 3 3 4 3 3
成CO2-,HCO -消耗的更快,所以曲线a表示的是c(NH +)的变化,曲线b表示的是c(HCO -)的变化,故C正
3 3 4 3
确;D项,M点时反应了0.002mol的NaOH,则溶液中c(Na+)= =0.1mol/L, NH HCO 与NaOH恰
4 3
好反应生成(NH )CO 和NaCO 溶液中存在Na+、 CO2-,HCO -、H+、NH +、OH- 所以电荷守恒为
4 2 3 2 3, 3 3 4 ,
2c(CO2-)+c(HCO-)+c(OH-)=c( Na+)+c(H+)+ c(NH +),又因c(Na+)=0.1mol/L,所以2c(CO2-)+c(HCO-)
3 3 4 3 3+c(OH-)=0.1mol·L-1+c(H+)+ c(NH +),故D错误。故选C。
4
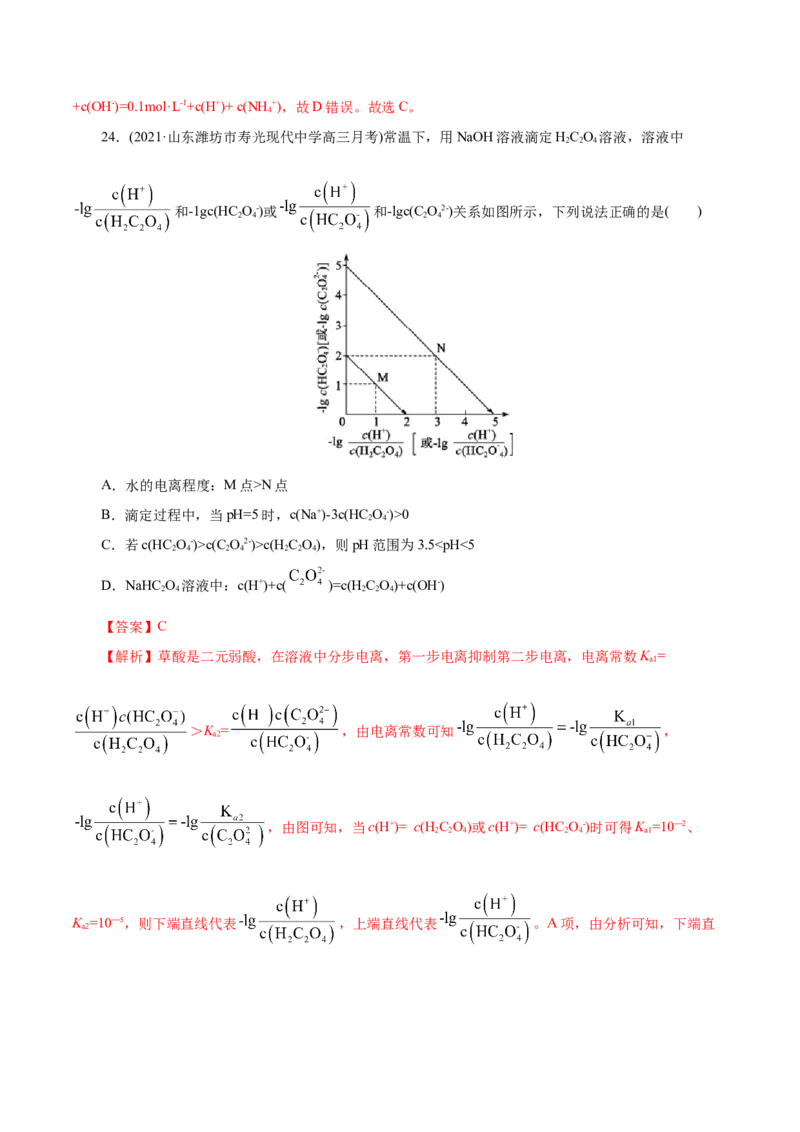
24.(2021·山东潍坊市寿光现代中学高三月考)常温下,用NaOH溶液滴定HC O 溶液,溶液中
2 2 4
和-1gc(HC O-)或 和-lgc(C O2-)关系如图所示,下列说法正确的是( )
2 4 2 4
A.水的电离程度:M点>N点
B.滴定过程中,当pH=5时,c(Na+)-3c(HC O-)>0
2 4
C.若c(HC O-)>c(C O2-)>c(H C O),则pH范围为3.5M点,故A错误;B项,当pH=5时,由K = =10—5可得
a2
c(HC O-)=c(C O2-),溶液中的电荷守恒关系为c(Na+)+ c(H+)= c(OH-)+ c(HC O-)+2c(C O2-),整合两式可
2 4 2 4 2 4 2 4
得c(Na+)-3c(HC O-)=c(OH-)—c(H+)<0,故B错误;C项,由c(HC O-)>c(C O2-)>c(H C O)可得
2 4 2 4 2 4 2 2 4
)> >1,由电离常数可得 )> >1,解不等式可知氢离子的范围为
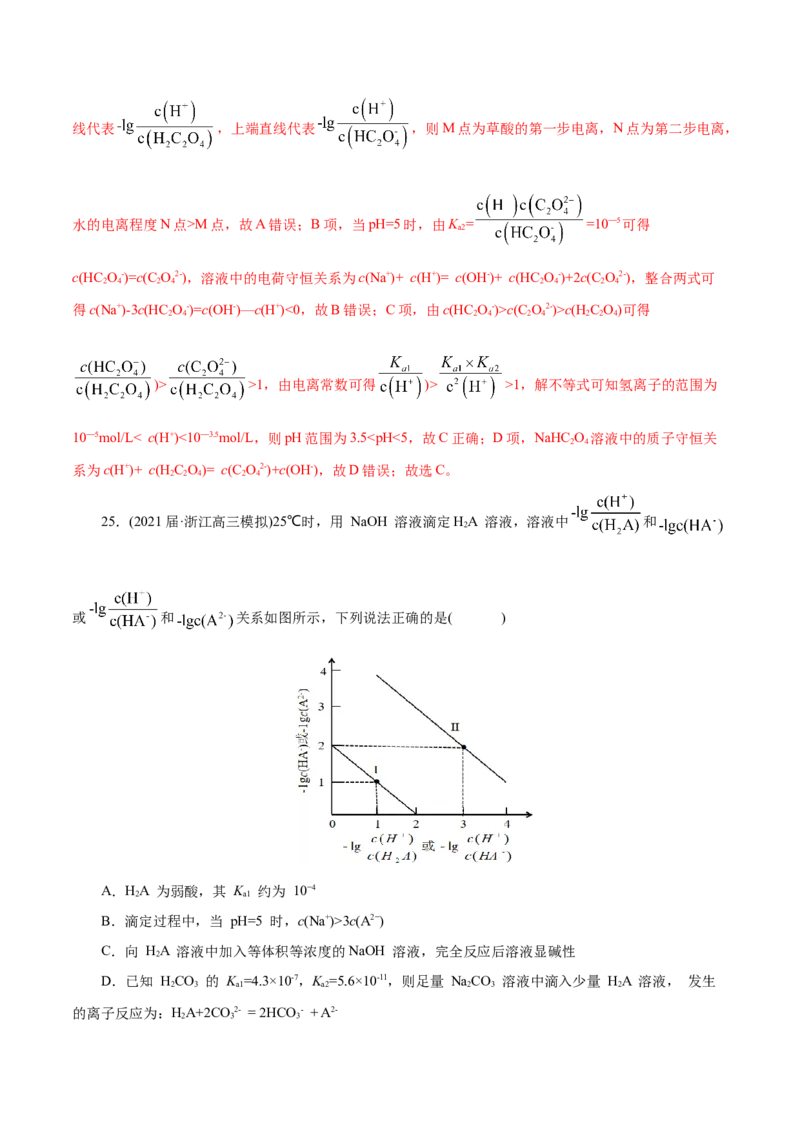
10—5mol/L< c(H+)<10—3.5mol/L,则pH范围为3.53c(A2−)
C.向 HA 溶液中加入等体积等浓度的NaOH 溶液,完全反应后溶液显碱性
2
D.已知 HCO 的 K =4.3×10-7,K =5.6×10-11,则足量 NaCO 溶液中滴入少量 HA 溶液, 发生
2 3 a1 a2 2 3 2
的离子反应为:HA+2CO2- = 2HCO - + A2-
2 3 3【答案】D
【解析】由图可知,HA 为二元弱酸,K = ,K = ,当 =0
2 a1 a2
时,溶液中 =— ,同理当 =0时, =— ,电离常数K >K ,由
a1 a2
图可知,曲线 I 表示 和 的关系,曲线 II 表示 和 的关系。A
项,由分析可知,HA 为二元弱酸,曲线 I 表示 和 的关系,当 =0时,
2
溶液中 =— ,则K 为10−2,故A 错误; B项,由图可知,当 =3时,
a1
=2,则K = =10-3×10-2=10-5,当 pH=5 时,溶液中c(HA- )=c(A2- ),由电荷守恒
a2
c(H+ ) + c (Na+ )═c (OH-)+ c (HA- )+2 c (A2- )可得c (H+ )+c(Na+ )═c(OH-)+3c(A2- ),则
c(Na+ )-3c(A2- )═c(OH-)-c(H+ )<0, c(Na+ )<3c(A2-),故B 错误;C项,向 HA 溶液中加入等体积等浓度
2
NaOH 溶液,完全反应后生成 NaHA 溶液,HA的二级电离常数K =10-5,A2-的二级水解常数K = =
2 a2 h2
=10-12< K ,则NaHA 溶液电离程度大于水解程度,溶液呈酸性,故C 错误;D项,由电离常数可
a2
知,酸的电离程度的大小顺序为HA>HA->H CO> HCO -,则过量 NaCO 溶液中与HA 溶液反应生成
2 2 3 3 2 3 2
NaHCO 和NaA,反应的离子方程式为. HA+2 CO2- = 2 HCO - + A2-,故D 正确;故选D。
3 2 2 3 3
二、非选择题26.一种利用钢铁厂烟灰(含Fe、Mn、SiO,少量的Al O、CaO及MgO)制备MnCO 的工艺流程如下:
2 2 3 3
已知25℃时,下列难溶物的溶度积常数:
难溶物 CaF MgF MnCO Mn(OH)
2 2 3 2
K 4.0×10-11 6.4×10-9 2.2×10-11 1.9×10-13
sp
回答下列问题:
(1)步骤(Ⅰ)浸渣的主要成分是______________(填化学式)。
(2)步骤(Ⅱ)加HO 溶液时反应的离子方程式为________________;
2 2
加氨水调节pH沉铁铝时,步骤(Ⅲ)应调节的pH适宜范围为____________。(部分金属离子开始沉淀与
沉淀完全的pH范围如下)
金属离子 Fe2+ Fe3+ Al3+ Mn2+ Mg2+
沉淀pH范围 7.6~9.6 2.7~3.7 3.4~5.2 8.3~9.3 9.6~11.1
(3)步骤(Ⅳ)用KF溶液沉钙镁时,要使c(Ca2+)、c(Mg2+)均小于1×10-6mol·L-1,则应控制反应液中
c(F-)>___________mol·L-1;反应MgF (s)+Ca2+ CaF (s)+Mg2+的平衡常数K=___________。
2 2
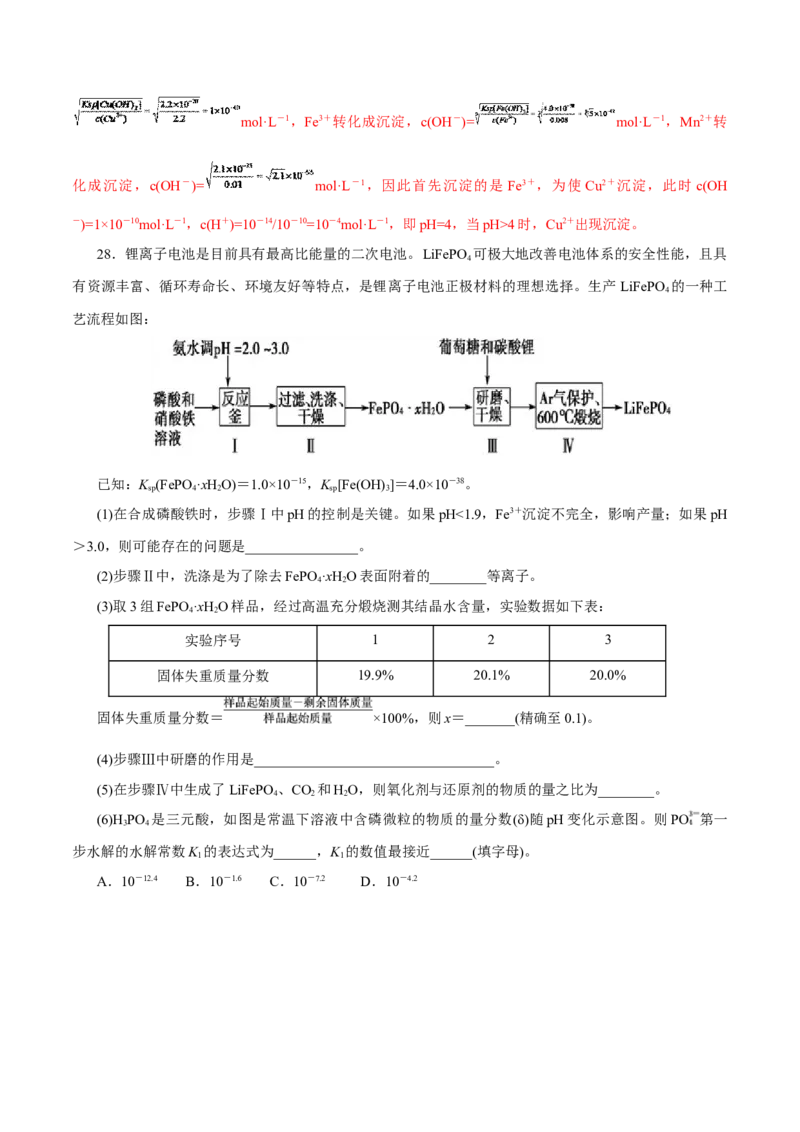
(4)步骤Ⅴ沉锰时,在60℃按投料比n[(NH )CO]/n(Mn2+)=2,溶液的pH对MnCO 产率的影响如图所
4 2 3 3
示;pH=7,按投料比n[(NH )CO]/n(Mn2+)=2,反应温度对MnCO 产率的影响如图所示。
4 2 3 3
①上图中,在pH<7.0时,pH越小产率____________(填“越高”或“越低”;在pH>7.0时,pH越大
产率越低且纯度也降低,其原因是___________________。②上图中,温度高于60℃时,温度越高产率越低且纯度也越低,主要原因是______________。
【答案】(1)SiO (2)2Fe2++H O+2H+-2Fe3++2H O 5.2~8.3
2 2 2 2
(3)0.08 160 (4)①越低 部分MnCO 转化为溶解度更小的Mn(OH)
3 2
②温度越高MnCO 水解程度越大[或温度升高,(NH )CO 和MnCO 也会热分解]
3 4 2 3 3
【解析】(1)步骤(Ⅰ)浸渣的主要成分是不与浓硫酸反应的酸性氧化物二氧化硅;(2)步骤(Ⅱ)加HO 溶
2 2
液时,双氧水将溶液中的亚铁离子氧化为铁离子,反应的离子方程式为2Fe2++H O+2H+-2Fe3++2H O;加入
2 2 2
氨水的目的是调节溶液pH,使溶液中铁离子和铝离子转化为氢氧化铁和氢氧化铝沉淀而除去,而锰离子不
能沉淀,由题给表格数据可知,应调节的pH适宜范围为5.2~8.3;(3)用KF溶液沉钙镁时,溶解度小的
CaF 沉淀先生成,MgF 沉淀后生成,则c(Mg2+)小于1×10-6mol·L-1时,溶液中c(F-)>
2 2
K 6.4×10−9
sp = =0.08mol/L;反应MgF (s)+Ca2+ CaF (s)+Mg2+的平衡常数K=
c(Mg2+) 1×10−6mol/L 2 2
c(Mg2+) c(Mg2+)c(F−) 6.4×10−9
= = =160; (4) ①由图可知,在60℃按投料比
c(Ca2+) c(Ca2+)c(F−) 4.0×10−11
n[(NH )CO]/n(Mn2+)=2时,在pH<7.0时,pH越小MnCO 产率越小;由表格所给溶度积可知,pH>7.0时,
4 2 3 3
溶液碱性增强, MnCO 部分会转化为溶解度更小的Mn(OH) ,导致产率和纯度降低;②由图可知,60℃
3 2
时,MnCO 产率最大,温度高于60℃时,温度升高MnCO 水解程度越大,(NH )CO 和MnCO 也会热分
3 3 4 2 3 3
解,导致产率和纯度降低。
27.铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含BeO:25%、
CuS:71%、少量FeS和SiO)中回收铍和铜两种金属的工艺流程如下:
2已知:I.铍、铝元素化学性质相似
II.常温下:Ksp[Cu(OH) ]=2.2×10-20、Ksp[Fe(OH) ]=4.0×10-38、Ksp[Mn(OH) ]=-2.1×10-13
2 3 2
(1)滤液A的主要成分除NaOH外,还有_____ (填化学式),写出反应I中含铍化合物与过量盐酸反应的
离子方程式_____________。
(2)①溶液C中含NaCl、BeCl 和少量HCl,为提纯BeCl ,选择最合理步骤顺序______。
2 2
a.加入过量的NaOH b.通入过量的CO c.加入过量的氨水
2
d.加入适量的HC1 e.过滤 f.洗涤
②从BeCl 溶液中得到BeCl 固体的操作是________________。
2 2
(3)①MnO 能将金属硫化物中的硫元素氧化为硫单质,写出反应 II中CuS 发生反应的化学方程式
2
______________。
②若用浓HNO 溶解金属硫化物,缺点是____________(任写一条)。
3
(4)溶液D中含c(Cu2+)=2.2mol/L、c(Fe3+)=0.008mol/L c(Mn2+)=0.01mol/L,逐滴加入稀氨水调节pH可依
次分离,首先沉淀的是___ (填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH值大于____。
【答案】(1)Na SiO、NaBeO(2分) BeO2-+4H+=Be2++2H O
2 3 2 2 2 2
(2)①cefd ②在氯化氢气流中蒸发结晶(或蒸发结晶时向溶液中持续通入氯化氢气体)
(3)①MnO +CuS+2H SO =S+MnSO +CuSO+2H O ②产生污染环境的气体
2 2 4 4 4 2
(3)Fe3+ 4
【解析】(1)旧铍铜原件的成分BeO、CuS、FeS、SiO ,根据信息I,BeO属于两性氧化物,CuS不与
2
氢氧化钠溶液反应,FeS不与氢氧化钠反应,SiO 属于酸性氧化物,能与氢氧化钠溶液反应,因此滤液A
2
中主要成分是NaOH、NaSiO 、NaBeO ;根据信息I,BeO -与过量盐酸反应生成氯化铍和水。其离子方
2 3 2 2 2
程式为BeO2-+4H+=Be2++2H O。(2)①利用Be元素、铝元素化学性质相似,向溶液C中先加入过量的氨
2 2
水,生成Be(OH) 沉淀,然后过滤、洗涤,再加入适量的HCl,生成BeCl ,合理步骤是cefd;②为了抑制
2 2
Be2+的水解,因此需要在HCl的氛围中对BeCl 溶液蒸发结晶;(3)①根据信息,CuS中S转化为S单质,
2
MnO 中 Mn 被 还 原 为 Mn2 + , 根 据 化 合 价 升 降 法 进 行 配 平 , 其 化 学 反 应 方 程 式 为
2
MnO +CuS+2H SO =S↓+MnSO +CuSO+2H O;②用浓硝酸作氧化剂,浓HNO 被还原成NO ,NO 有毒污
2 2 4 4 4 2 3 2 2
染环境;(4)三种金属阳离子出现沉淀,根据浓度商与 K 的关系,Cu2+转化成沉淀,c(OH-)=
spmol·L-1,Fe3+转化成沉淀,c(OH-)= mol·L-1,Mn2+转
化成沉淀,c(OH-)= mol·L-1,因此首先沉淀的是 Fe3+,为使 Cu2+沉淀,此时 c(OH
-)=1×10-10mol·L-1,c(H+)=10-14/10-10=10-4mol·L-1,即pH=4,当pH>4时,Cu2+出现沉淀。
28.锂离子电池是目前具有最高比能量的二次电池。LiFePO 可极大地改善电池体系的安全性能,且具
4
有资源丰富、循环寿命长、环境友好等特点,是锂离子电池正极材料的理想选择。生产 LiFePO 的一种工
4
艺流程如图:
已知:K (FePO ·xHO)=1.0×10-15,K [Fe(OH) ]=4.0×10-38。
sp 4 2 sp 3
(1)在合成磷酸铁时,步骤Ⅰ中pH的控制是关键。如果pH<1.9,Fe3+沉淀不完全,影响产量;如果pH
>3.0,则可能存在的问题是________________。
(2)步骤Ⅱ中,洗涤是为了除去FePO ·xHO表面附着的________等离子。
4 2
(3)取3组FePO ·xHO样品,经过高温充分煅烧测其结晶水含量,实验数据如下表:
4 2
实验序号 1 2 3
固体失重质量分数 19.9% 20.1% 20.0%
固体失重质量分数= ×100%,则x=_______(精确至0.1)。
(4)步骤Ⅲ中研磨的作用是__________________________________。
(5)在步骤Ⅳ中生成了LiFePO 、CO 和HO,则氧化剂与还原剂的物质的量之比为________。
4 2 2
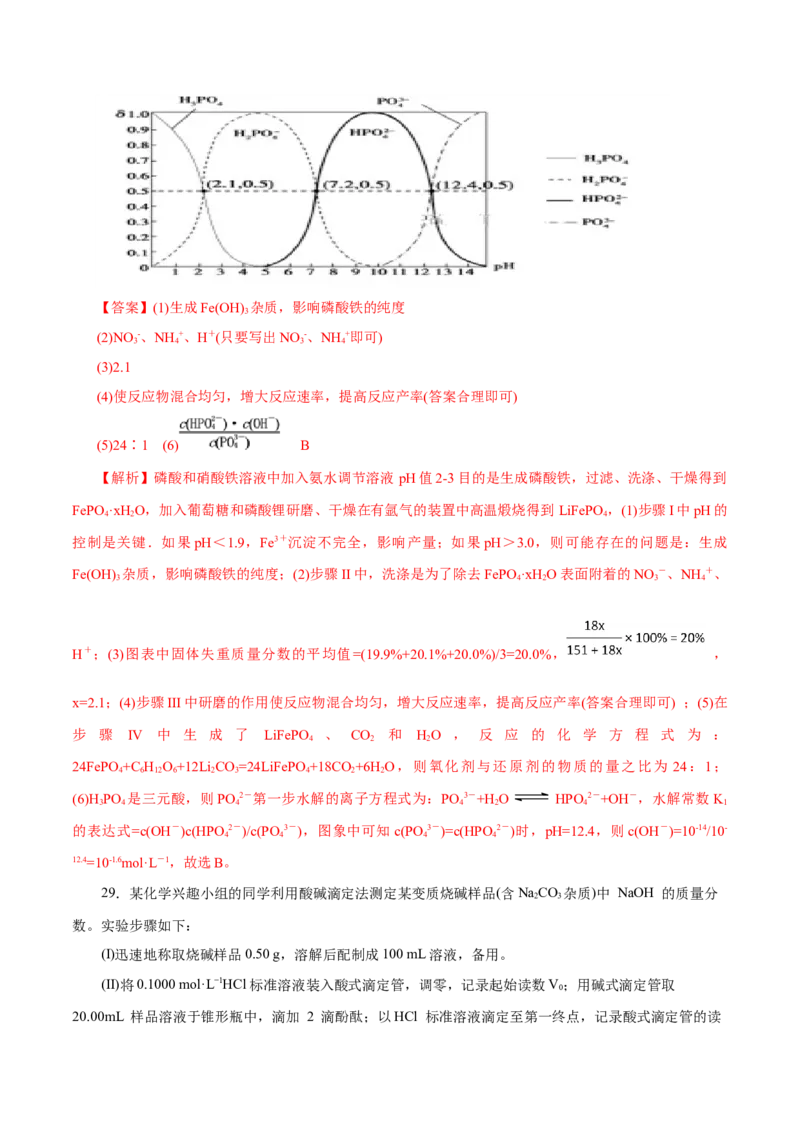
(6)H PO 是三元酸,如图是常温下溶液中含磷微粒的物质的量分数(δ)随pH变化示意图。则PO 第一
3 4
步水解的水解常数K 的表达式为______,K 的数值最接近______(填字母)。
1 1
A.10-12.4 B.10-1.6 C.10-7.2 D.10-4.2【答案】(1)生成Fe(OH) 杂质,影响磷酸铁的纯度
3
(2)NO -、NH +、H+(只要写出NO -、NH +即可)
3 4 3 4
(3)2.1
(4)使反应物混合均匀,增大反应速率,提高反应产率(答案合理即可)
(5)24∶1 (6) B
【解析】磷酸和硝酸铁溶液中加入氨水调节溶液 pH值2-3目的是生成磷酸铁,过滤、洗涤、干燥得到
FePO ·xH O,加入葡萄糖和磷酸锂研磨、干燥在有氩气的装置中高温煅烧得到 LiFePO ,(1)步骤I中pH的
4 2 4
控制是关键.如果pH<1.9,Fe3+沉淀不完全,影响产量;如果pH>3.0,则可能存在的问题是:生成
Fe(OH) 杂质,影响磷酸铁的纯度;(2)步骤II中,洗涤是为了除去FePO ·xH O表面附着的NO -、NH +、
3 4 2 3 4
H+;(3)图表中固体失重质量分数的平均值=(19.9%+20.1%+20.0%)/3=20.0%, ,
x=2.1;(4)步骤III中研磨的作用使反应物混合均匀,增大反应速率,提高反应产率(答案合理即可) ;(5)在
步 骤 IV 中 生 成 了 LiFePO 、 CO 和 HO , 反 应 的 化 学 方 程 式 为 :
4 2 2
24FePO +C H O+12Li CO=24LiFePO +18CO +6H O,则氧化剂与还原剂的物质的量之比为 24:1;
4 6 12 6 2 3 4 2 2
(6)H PO 是三元酸,则PO 2-第一步水解的离子方程式为:PO 3-+H O HPO 2-+OH-,水解常数K
3 4 4 4 2 4 1
的表达式=c(OH-)c(HPO 2-)/c(PO3-),图象中可知c(PO 3-)=c(HPO 2-)时,pH=12.4,则c(OH-)=10-14/10-
4 4 4 4
12.4=10-1.6mol·L-1,故选B。
29.某化学兴趣小组的同学利用酸碱滴定法测定某变质烧碱样品(含NaCO 杂质)中 NaOH 的质量分
2 3
数。实验步骤如下:
(I)迅速地称取烧碱样品0.50 g,溶解后配制成100 mL溶液,备用。
(II)将0.1000 mol·L−1HCl标准溶液装入酸式滴定管,调零,记录起始读数V;用碱式滴定管取
0
20.00mL 样品溶液于锥形瓶中,滴加 2 滴酚酞;以HCl 标准溶液滴定至第一终点,记录酸式滴定管的读数V;然后再向锥形瓶内滴加2滴甲基橙,继续用 HCl 标准溶液滴定至第二终点,记录酸式滴定管的读
1
数V。重复上述操作两次,记录数据如下:
2
实验序号 1 2 3
V/ mL 0.00 0.00 0.00
0
V/ mL 22.22 22.18 22.20
1
V/ mL 23.72 23.68 23.70
2
(1)步骤I中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和__。酸式滴定管用蒸馏水洗净后、装入标准
溶液并调零之前,应进行的操作是__。
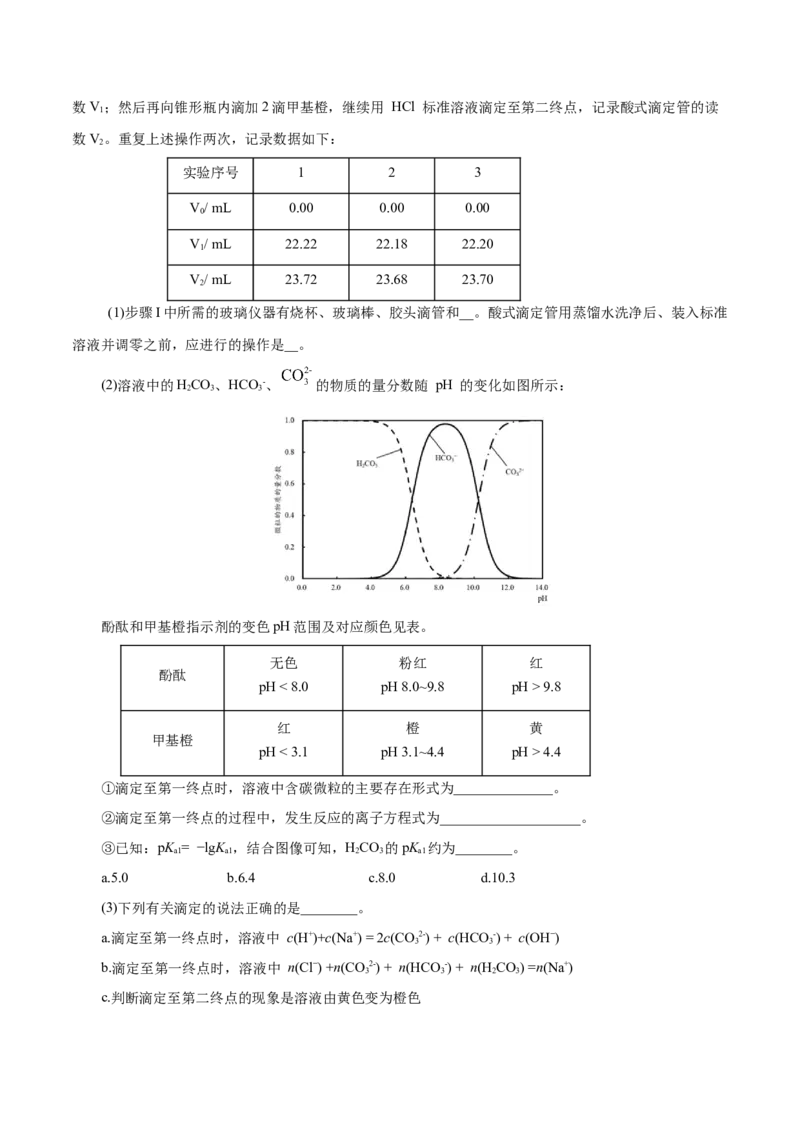
(2)溶液中的HCO、HCO-、 的物质的量分数随 pH 的变化如图所示:
2 3 3
酚酞和甲基橙指示剂的变色pH范围及对应颜色见表。
无色 粉红 红
酚酞
pH < 8.0 pH 8.0~9.8 pH > 9.8
红 橙 黄
甲基橙
pH < 3.1 pH 3.1~4.4 pH > 4.4
①滴定至第一终点时,溶液中含碳微粒的主要存在形式为______________。
②滴定至第一终点的过程中,发生反应的离子方程式为____________________。
③已知:pK = −lgK ,结合图像可知,HCO 的pK 约为________。
a1 a1 2 3 a1
a.5.0 b.6.4 c.8.0 d.10.3
(3)下列有关滴定的说法正确的是________。
a.滴定至第一终点时,溶液中 c(H+)+c(Na+) = 2c(CO2-) + c(HCO-) + c(OH−)
3 3
b.滴定至第一终点时,溶液中 n(Cl−) +n(CO2-) + n(HCO-) + n(H CO) =n(Na+)
3 3 2 3
c.判断滴定至第二终点的现象是溶液由黄色变为橙色d.记录酸式滴定管读数V 时,俯视标准液液面,会导致测得的NaOH质量分数偏低
1
(4)样品中NaOH的质量分数 (NaOH) =________%(计算结果保留小数点后 1 位)
【答案】(1)100mL容量瓶(量筒) 用标准盐酸溶液润洗酸式滴定管
(2)①HCO - ②H++OH-═H O H+ + CO2-= HCO - ③b
3 2 3 3
(3)bcd (4)84.1
【解析】(1)配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀,
用到的仪器:托盘天平、药匙、烧杯、玻璃棒、胶头滴管;还缺少的玻璃仪器:100mL容量瓶(量筒),酸
式滴定管用蒸馏水洗净后、装入标准溶液前,应进行的操作是:用HCl标准溶液润洗酸式滴定管;(2) ①
第一阶段滴定使用了酚酞做指示剂,故滴定到pH为8时,即为滴定终点,对照微粒分布图中可知,此时,
溶液中含碳微粒的主要存在形式为HCO -;②滴定至第一终点的过程中OH-和CO2-与盐酸反应分别生成水
3 3
和HCO -,故该过程中发生反应的离子方程式为H++OH-═H O,H+ + CO2-= HCO -;③根据电离平衡常数
3 2 3 3
表达式可知HCO 的K = 结合图像可知,当pH=6.4左右时,c(H CO) = c(HCO -),故
2 3 a1 2 3 3
HCO 的pK 约为6.4,故答案为b; (3) a项,滴定至第一终点时,溶液中的电荷守恒式为c(H+)+c(Na+) =
2 3 a1
2c(CO2-) + c(HCO -) +c(OH−)+c(Cl−),故a错误;b项,滴定至第一终点时,溶液中是氯化钠和碳酸氢钠的
3 3
混合溶液,故由物料守恒式:n(Cl−) +n(CO2-) + n(HCO -) +n(H CO) =n(Na+),故b正确;c项,根据图中可
3 3 2 3
知,碳酸氢根基本完全转化为碳酸时,pH大致为4,故滴定至第二终点的现象是溶液由黄色变为橙色,故
c正确;d项,记录酸式滴定管读数V 时,俯视标准液液面,记录盐酸溶液体积V 减小,计算得到碳酸钠
1 1
质量增大,氢氧化钠质量减小,质量分数减小,故d正确;故选bcd;(4)将0.1000mol/L HCl标准溶液装入
酸式滴定管,调零,记录起始读数V;用碱式滴定管取20.00 mL样品溶液于锥形瓶中,滴加2滴酚酞;以
0
HCl标准溶液滴定至第一终点(此时溶质为NaCl和NaHCO ),记录酸式滴定管的读数V,发生的反应为
3 1
NaOH+HCl=NaCl+H O,NaCO+HCl=NaHCO +NaCl,然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标
2 2 3 3
准溶液滴定至第二终点,发生的反应为:NaHCO +HCl=NaCl+H O+CO↑,记录酸式滴定管的读数V。重
3 2 2 2
复上述操作两次,记录数据如表,平均V= ,平均V=
1 2
,发生反应NaHCO +HCl=NaCl+H O+CO↑,消耗的盐酸溶液
3 2 2体积=23.70mL-22.20mL=1.50mL,结合反应过程计算样品中碳酸钠的质量=0.0015L×0.1mol/L×
=0.00075mol,得到样品中氢氧化钠的质量分数= 。