文档内容
选择题标准练(六)
1.2022年北京冬奥会被誉为科技奥运、绿色奥运,从清洁能源到环保材料,化学高科技所
起的作用功不可没。下列有关说法错误的是( )
A.二氧化碳跨临界直冷制冰技术环保节能、安全无毒
B.颁奖礼服内胆添加的石墨烯发热材料为有机高分子材料
C.滑雪服采用的剪切增稠流体材料可有效减小空气阻力
D.冬奥火炬“飞扬”外壳采用的是碳纤维与高性能树脂制成的新型复合材料
答案 B
解析 二氧化碳跨临界直冷制冰技术不需要发生化学反应,不会造成环境污染,故 A正确;
石墨烯属于碳单质,属于无机非金属材料,故B错误;增稠流体材料可有效减小空气阻力,
可制作滑雪服,故C正确;碳纤维与高性能树脂制成的火炬外壳是新型复合材料,具有耐
高温等性能,故D正确。
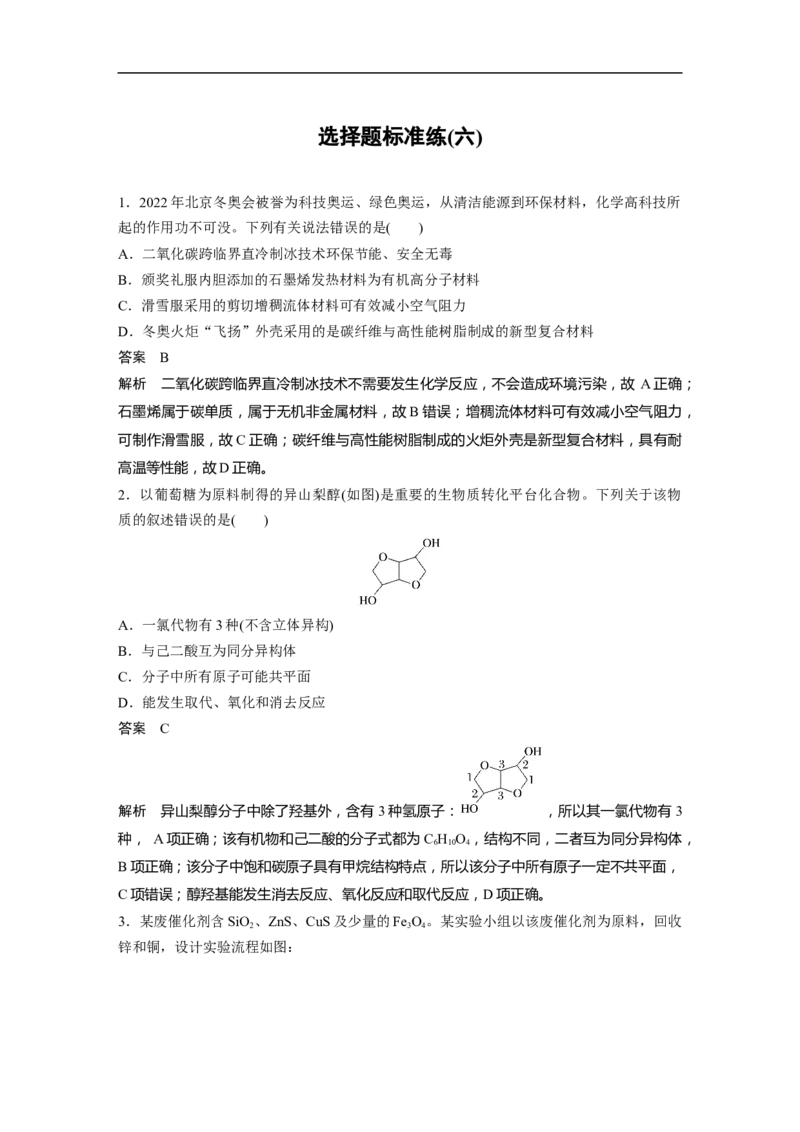
2.以葡萄糖为原料制得的异山梨醇(如图)是重要的生物质转化平台化合物。下列关于该物
质的叙述错误的是( )
A.一氯代物有3种(不含立体异构)
B.与己二酸互为同分异构体
C.分子中所有原子可能共平面
D.能发生取代、氧化和消去反应
答案 C
解析 异山梨醇分子中除了羟基外,含有3种氢原子: ,所以其一氯代物有3
种, A项正确;该有机物和己二酸的分子式都为C H O,结构不同,二者互为同分异构体,
6 10 4
B项正确;该分子中饱和碳原子具有甲烷结构特点,所以该分子中所有原子一定不共平面,
C项错误;醇羟基能发生消去反应、氧化反应和取代反应,D项正确。
3.某废催化剂含SiO 、ZnS、CuS及少量的Fe O 。某实验小组以该废催化剂为原料,回收
2 3 4
锌和铜,设计实验流程如图:下列说法不正确的是( )
A.步骤①操作中,生成的气体可用CuSO 溶液吸收
4
B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水
C.步骤②操作中,应先加1.0 mol·L-1 HSO ,然后不断搅拌下缓慢加入6% H O
2 4 2 2
D.滤渣1中含有SiO,滤渣2中含有S和SiO
2 2
答案 B
解析 废催化剂加入稀硫酸,第一次浸出主要发生反应:ZnS+HSO ===ZnSO +HS↑、
2 4 4 2
Fe O +4HSO ===FeSO +Fe (SO ) +4HO,过滤后滤液中含有ZnSO 、FeSO 、Fe (SO ) ,
3 4 2 4 4 2 4 3 2 4 4 2 4 3
浓缩结晶得到粗ZnSO·7H O,滤渣1中含有SiO 、CuS,向盛有滤渣1的反应器中加1.0
4 2 2
mol·
L-1 HSO 和6% H O 溶液,发生氧化还原反应,生成硫酸铜、硫,滤渣2含有硫和二氧化
2 4 2 2
硅,滤液含有硫酸铜,经浓缩结晶可得到粗硫酸铜晶体,以此解答该题。步骤①操作中生成
的气体为硫化氢,可与硫酸铜溶液反应生成硫化铜沉淀,则可用 CuSO 溶液吸收,故A正
4
确;滤液1中除含有Fe2+,还含有Fe3+,加入KSCN和新制的氯水不能检验,故B错误;
过氧化氢在加热条件下易发生分解,应先加入1.0 mol·L-1 HSO ,故C正确。
2 4
4.下列实验目的对应的方案设计、现象和结论都正确的是( )
选项 实验目的 方案设计 现象和结论
探究金属钠在氧
取少量固体粉末,加入 若无气体生成,则固体粉末为NaO;
2
A 气中燃烧所得固
2~3 mL蒸馏水 若有气体生成,则固体粉末为NaO
2 2
体粉末的成分
若溶液变为红色,说明样品已经变
探究 FeSO 固体 取少量待测样品溶于蒸
4
B 质;若溶液不变色,说明样品没有变
样品是否变质 馏水,滴加KSCN溶液
质
向KBr、KI混合溶液中
比较Cl 、Br 、I 溶液分层,下层呈紫红色,证明氧化
2 2 2
C 依次加入少量氯水和
的氧化性 性:Cl>Br >I
2 2 2
CCl ,振荡,静置
4
用 pH 计 测 定 pH :
比 较 HCO 与 pH:①>②,证明 HCO 酸性弱于
2 3 2 3
D ①NaHCO 溶液
3
CHCOOH的酸性 CHCOOH
3 3
②CHCOONa溶液
3
答案 B
解析 若Na没有完全反应,向固体粉末中加蒸馏水会产生H ,则若有气体生成,不能说明
2固体粉末为NaO ,A错误;KSCN溶液和Fe3+反应使溶液变为红色,因此,向样品溶液中
2 2
滴加KSCN溶液,若溶液变为红色,说明样品已经变质,若溶液不变色,说明样品没有变
质,B正确;向KBr、KI混合溶液中依次加入少量氯水和CCl ,振荡,由于I-的还原性比
4
Br-强,故少量氯水和KI反应,静置分层后,下层溶液呈紫红色,说明氧化性:Cl>I,不
2 2
能证明氧化性:Cl >Br ,C 错误;溶液浓度相同时,测得 pH:① NaHCO 溶液>
2 2 3
②CHCOONa溶液,可证明HCO 酸性弱于CHCOOH,D错误。
3 2 3 3
5.X、Y、Z、W为原子序数依次增大的短周期主族元素。已知X与Y形成的某一化合物易
生成二聚体(常温下为无色气体),Z的简单离子半径在其所在周期中最小,W原子的最外层
电子数是其他三种元素原子最外层电子数之和的。下列说法正确的是( )
A.X与Y形成的化合物均易溶于水
B.电负性:Z>Y>X
C.W的氢化物在其同族元素中的沸点最高
D.元素Y与W形成的化合物超过3种
答案 D
解析 短周期主族元素中X、Y可形成一种易生成二聚体分子的化合物,可推断X为N,Y
为O,X与Y形成的NO 可生成无色的NO 气体,Z的简单离子半径在其所在周期中最小,
2 2 4
可推断Z为Al,则W的最外层电子数为=7,W为Cl,据此分析解答。N与O形成的NO
不溶于水,A项错误;Cl(W)所在主族中的F元素的氢化物HF分子间有氢键,沸点高于其
他同主族元素的氢化物,C项错误;O与Cl形成的化合物有ClO、ClO 、ClO 、ClO 、
2 2 3 2 2 5
ClO 等,D项正确。
2 7
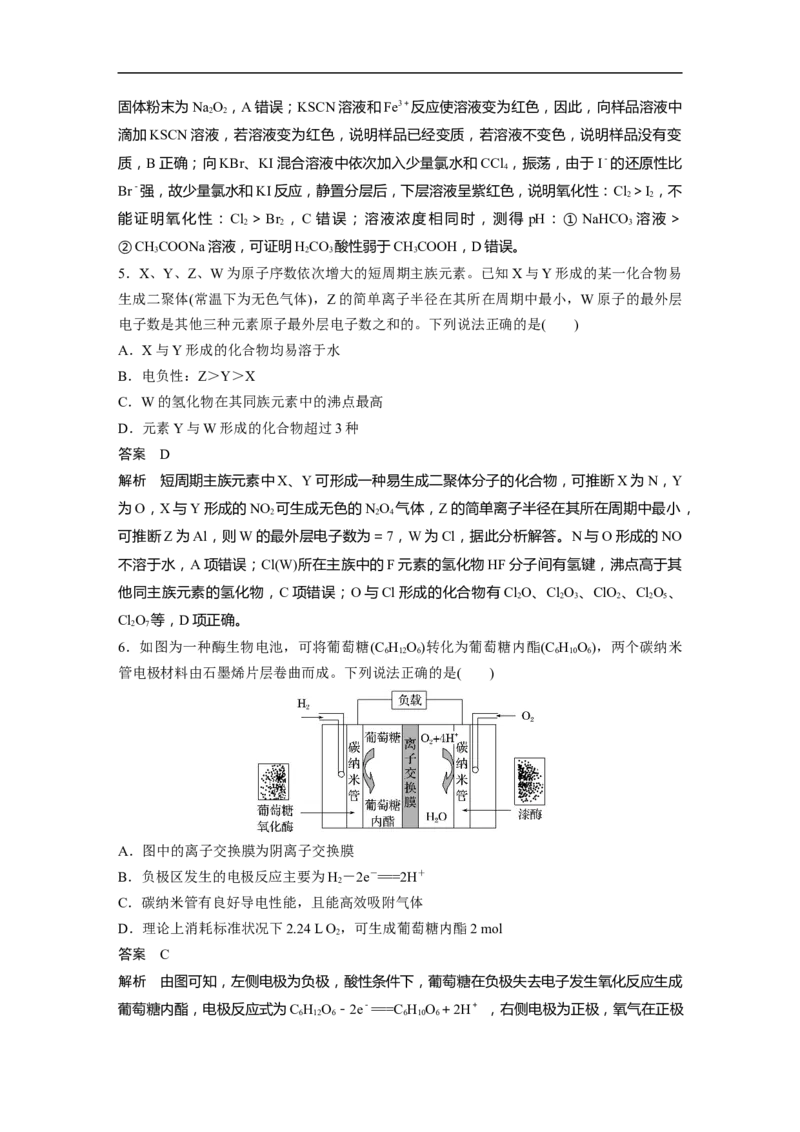
6.如图为一种酶生物电池,可将葡萄糖(C H O)转化为葡萄糖内酯(C H O),两个碳纳米
6 12 6 6 10 6
管电极材料由石墨烯片层卷曲而成。下列说法正确的是( )
A.图中的离子交换膜为阴离子交换膜
B.负极区发生的电极反应主要为H-2e-===2H+
2
C.碳纳米管有良好导电性能,且能高效吸附气体
D.理论上消耗标准状况下2.24 L O ,可生成葡萄糖内酯2 mol
2
答案 C
解析 由图可知,左侧电极为负极,酸性条件下,葡萄糖在负极失去电子发生氧化反应生成
葡萄糖内酯,电极反应式为C H O-2e-===C H O+2H+ ,右侧电极为正极,氧气在正极
6 12 6 6 10 6得到电子发生还原反应,负极生成的H+通过阳离子交换膜到正极参与反应,故A、B错误;
碳纳米管是常见的电极材料,有良好导电性能,且碳纳米管表面积大,能高效吸附气体,故
C正确;每消耗1 mol 葡萄糖,外电路中转移2 mol电子,消耗0.5 mol氧气,则理论上消
耗标准状况下2.24 L O ,可生成葡萄糖内酯0.2 mol,故D错误。
2
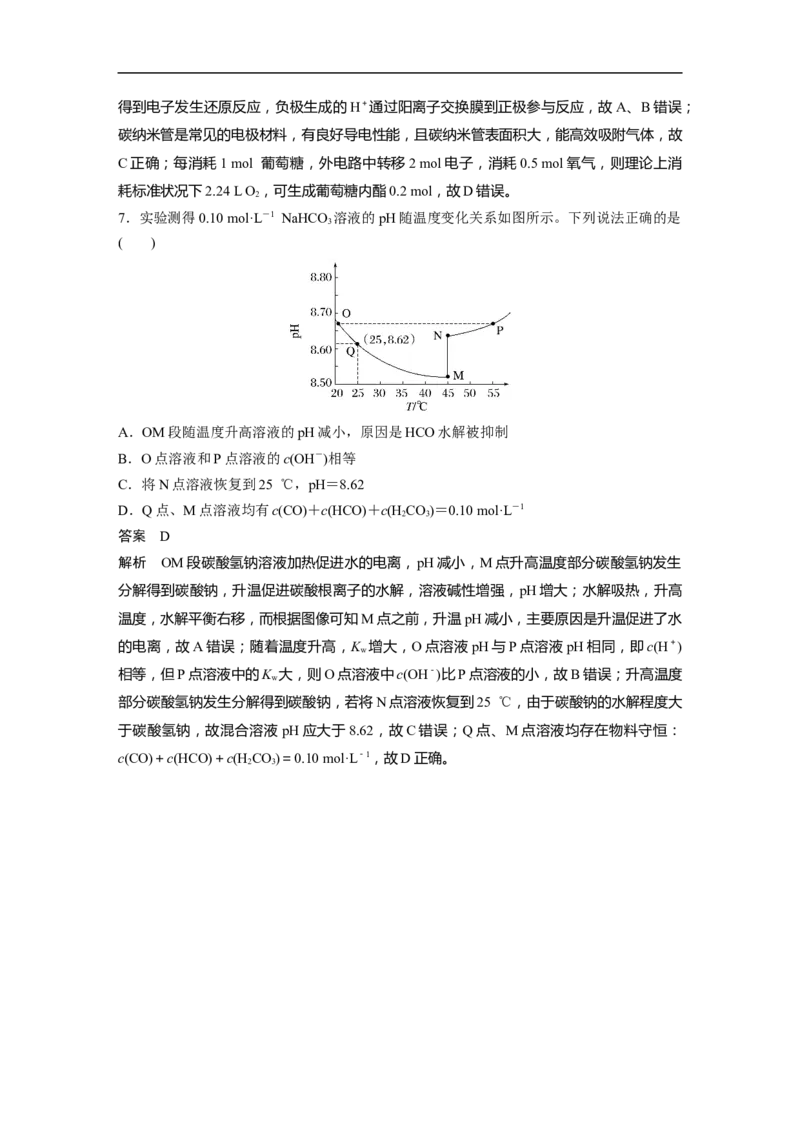
7.实验测得0.10 mol·L-1 NaHCO 溶液的pH随温度变化关系如图所示。下列说法正确的是
3
( )
A.OM段随温度升高溶液的pH减小,原因是HCO水解被抑制
B.O点溶液和P点溶液的c(OH-)相等
C.将N点溶液恢复到25 ℃,pH=8.62
D.Q点、M点溶液均有c(CO)+c(HCO)+c(H CO)=0.10 mol·L-1
2 3
答案 D
解析 OM段碳酸氢钠溶液加热促进水的电离,pH减小,M点升高温度部分碳酸氢钠发生
分解得到碳酸钠,升温促进碳酸根离子的水解,溶液碱性增强,pH增大;水解吸热,升高
温度,水解平衡右移,而根据图像可知M点之前,升温pH减小,主要原因是升温促进了水
的电离,故A错误;随着温度升高,K 增大,O点溶液pH与P点溶液pH相同,即c(H+)
w
相等,但P点溶液中的K 大,则O点溶液中c(OH-)比P点溶液的小,故B错误;升高温度
w
部分碳酸氢钠发生分解得到碳酸钠,若将N点溶液恢复到25 ℃,由于碳酸钠的水解程度大
于碳酸氢钠,故混合溶液 pH应大于8.62,故C错误;Q点、M点溶液均存在物料守恒:
c(CO)+c(HCO)+c(H CO)=0.10 mol·L-1,故D正确。
2 3