文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷03
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、文物保护中的化学知识(本题共18分)
铜锈为 Cu(OH)CO, 俗称铜绿,可溶于酸。出土铜器多带有铜锈。
2 2 3
1.《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。
“修旧如旧”是文物保护的主旨。(18分)
(1)请写出铜绿与盐酸反应的化学方程式
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu (OH) CO 和
2 2 3
Cu (OH) Cl。考古学家将铜锈分为无害锈和有密锈,结构如图所示:
2 2
① Cu (OH) CO 可否作无害锈,请解释原因。
2 2 3
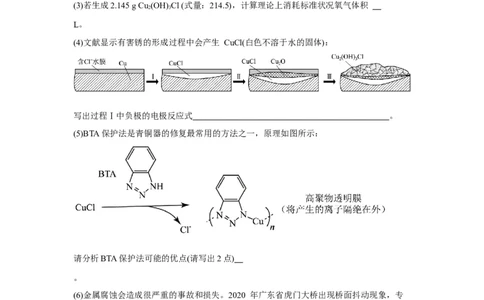
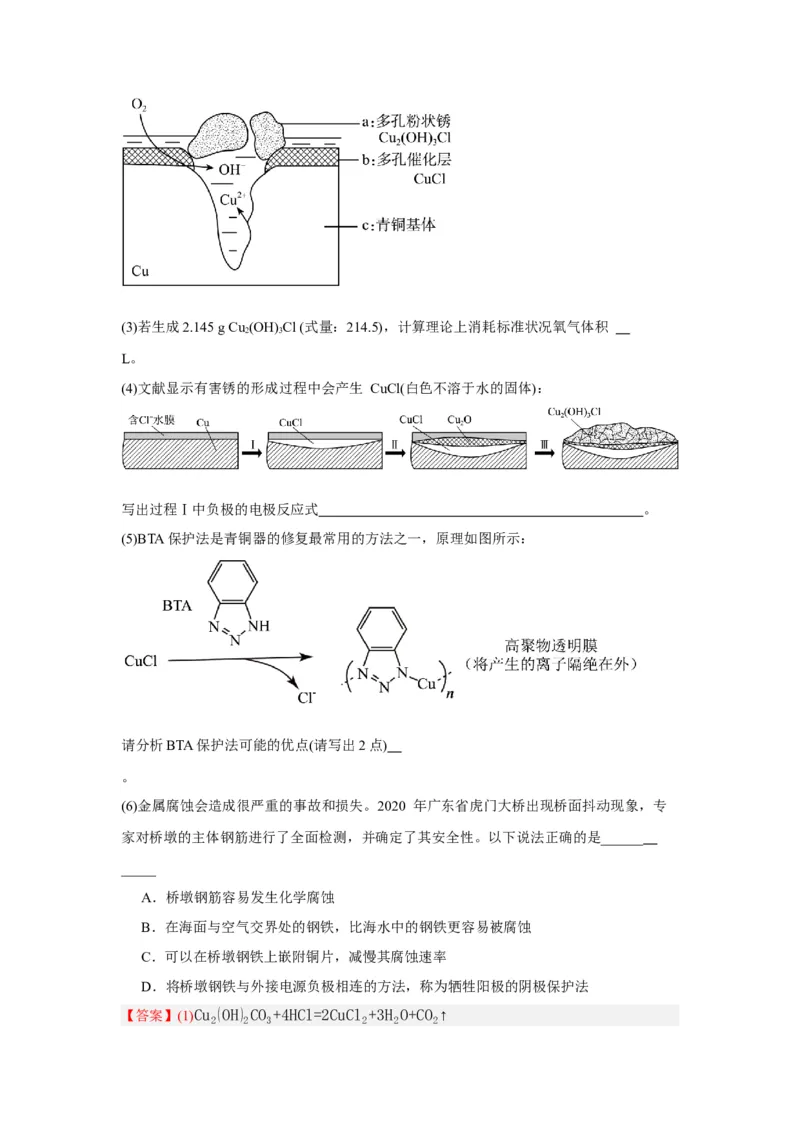
② 如图为青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu (OH) Cl的原理示
2
意图:(3)若生成2.145 g Cu (OH) Cl (式量:214.5),计算理论上消耗标准状况氧气体积
2 3
L。
(4)文献显示有害锈的形成过程中会产生 CuCl(白色不溶于水的固体):
写出过程Ⅰ中负极的电极反应式 。
(5)BTA保护法是青铜器的修复最常用的方法之一,原理如图所示:
请分析BTA保护法可能的优点(请写出2点)
。
(6)金属腐蚀会造成很严重的事故和损失。2020 年广东省虎门大桥出现桥面抖动现象,专
家对桥墩的主体钢筋进行了全面检测,并确定了其安全性。以下说法正确的是______
_____
A.桥墩钢筋容易发生化学腐蚀
B.在海面与空气交界处的钢铁,比海水中的钢铁更容易被腐蚀
C.可以在桥墩钢铁上嵌附铜片,减慢其腐蚀速率
D.将桥墩钢铁与外接电源负极相连的方法,称为牺牲阳极的阴极保护法
【答案】(1)Cu (OH) CO +4HCl=2CuCl +3H O+CO ↑
2 2 3 2 2 2(2)Cu (OH) CO 为致密的结构,可以防止铜的进一步锈蚀,故为无害锈
2 2 3
(3)0.224
(4)Cu-e-+Cl-=CuCl
(5)BTA能在青铜器表面形成一层致密的透明保护膜,能替换出锈层中的氯离子,能够高效
除去有害锈,不损害青铜器且使得青铜器得到保护
(6)B
【解析】(1)铜锈为Cu (OH) CO,由质量守恒定律可知,反应前后元素种类不变,和盐
2 2 3
酸反应生成氯化铜、水和二氧化碳,Cu (OH) CO +4HCl=2CuCl +3H O+CO ↑;
2 2 3 2 2 2
(2)①由图可知,Cu (OH) CO 为致密的结构,可以防止铜的进一步锈蚀,故为无害锈;
2 2 3
(3)若生成2.145 g Cu (OH) Cl (为0.01mol),反应中铜失去电子变为+2价铜、氧得到电子
2 3
转化为-2价氧,由电子守恒可知 ,则理论上消耗标准状况氧气
Cu (OH) Cl~4e-~O
2 3 2
0.01mol,体积为0.224L;
(4)Ⅰ中负极的电极反应为铜失去电子发生氧化反应和氯离子生成氯化亚铜,
Cu-e-+Cl-=CuCl;
(5)BTA能在青铜器表面形成一层致密的透明保护膜,能替换出锈层中的氯离子,能够
高效除去有害锈,不损害青铜器且使得青铜器得到保护;
(6)A.桥墩钢筋在水泥中密闭,不容易发生化学腐蚀,A错误;
B.在海面与空气交界处的钢铁,使得铁、氧气、水同时接触,故比海水中的钢铁更容易
被腐蚀,B正确;
C.铁比铜活泼,可以在桥墩钢铁上嵌附铜片,会使得铁做负极加速其腐蚀速率,C错误;
D.将桥墩钢铁与外接电源负极相连的方法,称为外接电源的阴极保护法,D错误;
故选B。
二、次氯酸钠处理氮氧化物等有害尾气 (本题共22分)
含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有NO等氮氧化物的尾气,
反应方程式如下:NaClO + NO + HO —— NaCl + HNO (未配平)。
2 3
2. 完成下列填空。(22分)
(1)氯在元素周期表中的位置是 ,其所在主族的元素中,
最高价氧化物对应的水化物酸性最强的是 (填化学式)。
(2)配平上述反应方程式 。每有0.3mol电子发生转移,可消耗标准状况下NO气体的体积约为 L。
(3)NaClO溶液中存在如下关系:c(OH-) c(HClO)(填“>”、“=”、或
“<”)。
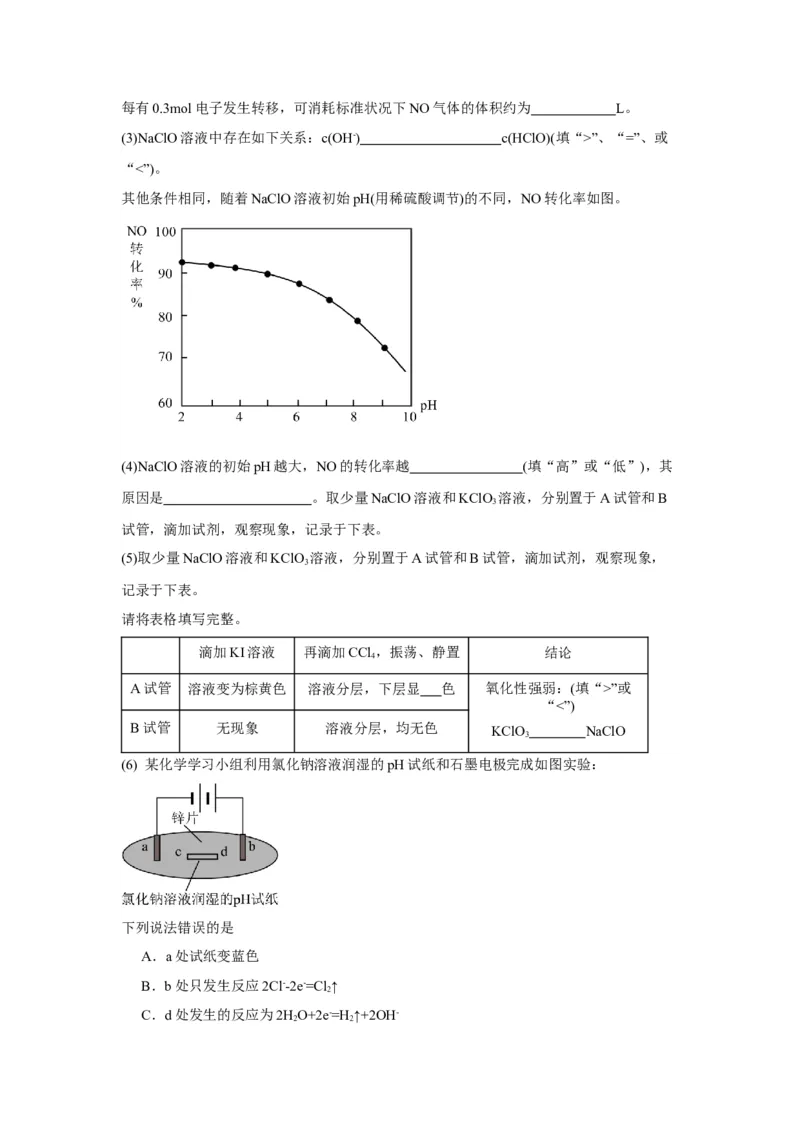
其他条件相同,随着NaClO溶液初始pH(用稀硫酸调节)的不同,NO转化率如图。
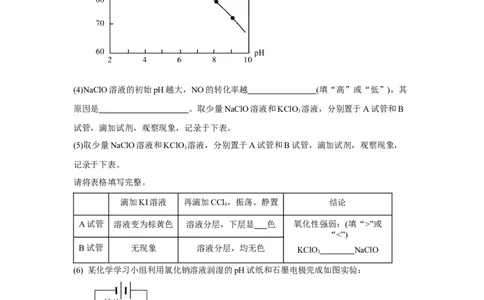
(4)NaClO溶液的初始pH越大,NO的转化率越 (填“高”或“低”),其
原因是 。取少量NaClO溶液和KClO 溶液,分别置于A试管和B
3
试管,滴加试剂,观察现象,记录于下表。
(5)取少量NaClO溶液和KClO 溶液,分别置于A试管和B试管,滴加试剂,观察现象,
3
记录于下表。
请将表格填写完整。
滴加KI溶液 再滴加CCl ,振荡、静置 结论
4
A试管 溶液变为棕黄色 溶液分层,下层显 色 氧化性强弱:(填“>”或
“<”)
B试管 无现象 溶液分层,均无色 KClO NaClO
3
(6) 某化学学习小组利用氯化钠溶液润湿的pH试纸和石墨电极完成如图实验:
下列说法错误的是
A.a处试纸变蓝色
B.b处只发生反应2Cl--2e-=Cl↑
2
C.d处发生的反应为2HO+2e-=H ↑+2OH-
2 2D.c极为阳极
【答案】(1) 第三周期第VIIA族 HClO
4
(2) 3NaClO + 2NO + H O=3NaCl +2HNO 2.24
2 3
(3)c(OH-)>c(HClO)
(4) 低 NaClO溶液中起氧化作用的主要是HClO;当溶液的pH越小,生成的
HClO浓度越大,氧化NO的能力越强,NO的去除率越高
(5) 紫 <
(6) B
【解析】(1)氯为17号元素,在元素周期表中的位置是第三周期第VIIA族;同主族由上
而下,金属性增强,非金属性变弱,非金属性越强,最高价氧化物对应水化物的酸性越强,
故其所在主族的元素中,氟没有正价,故最高价氧化物对应的水化物酸性最强的是
HClO;
4
(2)反应中氯元素化合价由+1变为-1降低、氮元素化合价由+2变为+5升高,根据电子守
恒、质量守恒可知,反应为3NaClO + 2NO + HO=3NaCl +2HNO ;电子转移为NO~3e-,
2 3
则每有0.3mol电子发生转移,可消耗标准状况下0.1mol,NO气体的体积约为2.24L;
(3)次氯酸根离子水解生成氢氧根离子和次氯酸,水也会电离出氢氧根离子,故
c(OH-)>c(HClO);
(4)由图可知,NaClO溶液的初始pH越大,NO的转化率越低,其原因是NaClO溶液中
起氧化作用的主要是HClO,当溶液的pH越小,生成的HClO浓度越大,氧化NO的能力
越强,NO的去除率越高;
(5)A试管中溶液变为棕黄色,说明次氯酸钠和碘化钾生成碘单质,碘单质被四氯化碳萃
取,有机层显紫色;B试管中溶液颜色为变化,说明氯酸钾和碘化钾不反应;根据氧化剂
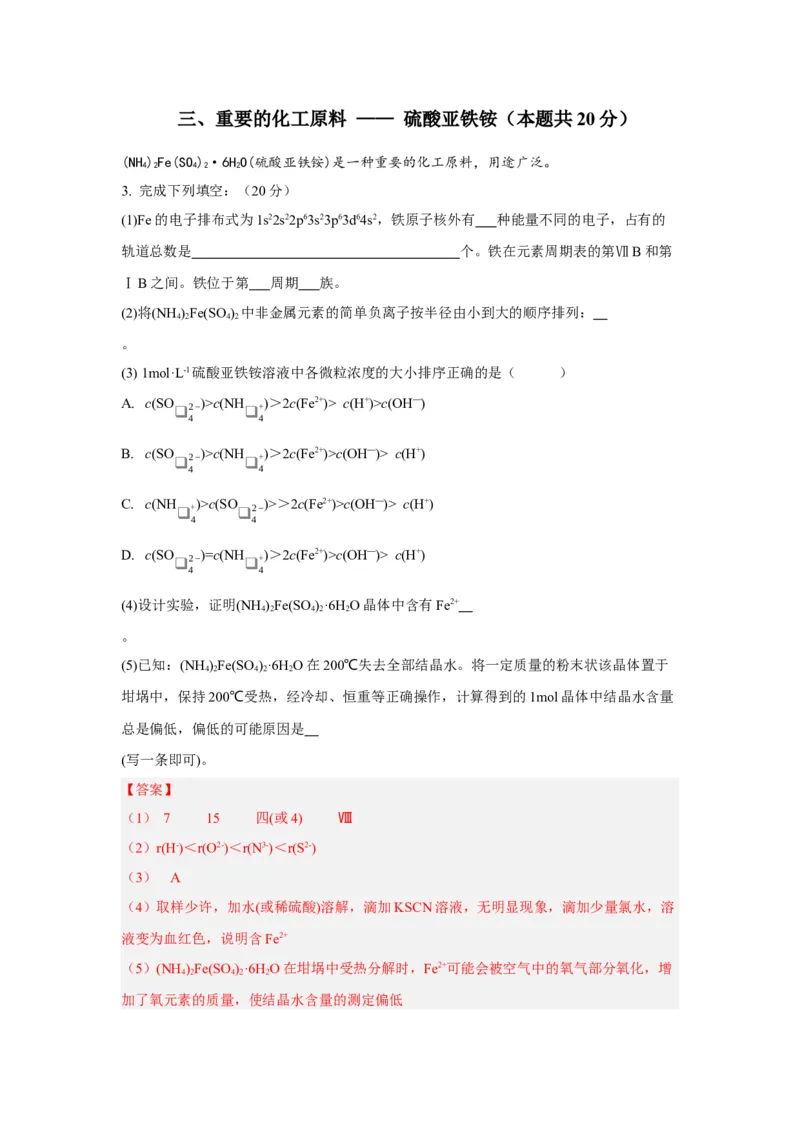
的氧化性大于氧化产物可知,氧化性强弱为:KClO3c(NH )>2c(Fe2+)> c(H+)>c(OH—)
2− +
❑ ❑
4 4
B. c(SO )>c(NH )>2c(Fe2+)>c(OH—)> c(H+)
2− +
❑ ❑
4 4
C. c(NH )>c(SO )>>2c(Fe2+)>c(OH—)> c(H+)
+ 2−
❑ ❑
4 4
D. c(SO )=c(NH )>2c(Fe2+)>c(OH—)> c(H+)
2− +
❑ ❑
4 4
(4)设计实验,证明(NH )Fe(SO )·6H O晶体中含有Fe2+
4 2 4 2 2
。
(5)已知:(NH )Fe(SO )·6H O在200℃失去全部结晶水。将一定质量的粉末状该晶体置于
4 2 4 2 2
坩埚中,保持200℃受热,经冷却、恒重等正确操作,计算得到的1mol晶体中结晶水含量
总是偏低,偏低的可能原因是
(写一条即可)。
【答案】
(1) 7 15 四(或4) Ⅷ
(2)r(H-)<r(O2-)<r(N3-)<r(S2-)
(3) A
(4)取样少许,加水(或稀硫酸)溶解,滴加KSCN溶液,无明显现象,滴加少量氯水,溶
液变为血红色,说明含Fe2+
(5)(NH )Fe(SO )·6H O在坩埚中受热分解时,Fe2+可能会被空气中的氧气部分氧化,增
4 2 4 2 2
加了氧元素的质量,使结晶水含量的测定偏低【解析】(1)电子能量由能层和能级共同决定,同一能级能量相同,铁原子核外有7个能级
填充电子,故有7种能量不同的电子;s能级有1个轨道,p能级有3个轨道,d能级有5
个轨道,根据铁原子的电子排布式知,1s~4s能级每个轨道都有电子填充,故共有15个轨
道有电子填充,占有的轨道总数为15个;铁元素价电子排布为:3d64s2,最高能层为第四
层,故位于第四周期,价电子共有8个,位于周期表的第8列,周期表中8、9、10三列合
称第Ⅷ族,即铁位于第四周期第Ⅷ族。
(2)四种非金属元素简单负离子分别为:H-、N3-、S2-、O2-,其中H-电子层为一层,半径最
小,S2-电子层为三层,半径最大,N3-、O2-电子层均为两层,但O的核电荷数大,对核外电
子引力强,故半径小,所以四种离子半径大小顺序为:r(H-)<r(O2-)<r(N3-)<r(S2-);
(3) 该溶液中硫酸根离子与铵根离子的物质的量最大,但是铵根离子将水解,且亚铁离子
亦水解,水解后溶液整体呈现碱性,因此c(SO )>c(NH )>2c(Fe2+)> c(H+)>c(OH—)
2− +
❑ ❑
4 4
(4)证明(NH )Fe(SO ) 中含有Fe2+,可以通过将Fe2+氧化为Fe3+检验,但需排除原有Fe3+干扰,
4 4 2
故应该先加KSCN,再氧化Fe2+,具体方案为:取样少许,加水(或稀硫酸)溶解,滴加
KSCN溶液,无明显现象,滴加少量氯水,溶液变为血红色,说明含Fe2+;
(5)由于样品中铁元素为二价,易被氧化,题目操作未说明隔绝空气,故会产生误差,即
(NH )Fe(SO )·6H O在坩埚中受热分解时,Fe2+可能会被空气中的氧气部分氧化,增加了氧
4 2 4 2 2
元素的质量,使结晶水含量的测定偏低。
四、 酸雨及其形成气体(本题共15分)
空气质量与我们的健康息息相关,目前我国通过监测6项污染物的百分比浓度来计算空气
质量指数(AQI),SO、NO 和CO是其中3项中的污染物。(15分)
2 2
4. 酸雨的形成可能由多种气体造成的,保护环境刻不容缓,工厂产生的有害气体必须经过
处理才可以排放至大气当中。
(1)上述3种气体直接排入空气后会引起酸雨的气体有 (填化学式)。
❑
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:SO (g)+NO (g) SO (g)+NO(g)
2 2 ⇌ 3
❑
❑ ❑
①若已知2SO (g)+O(g) 2SO (g) + Q 2NO(g)+O(g) 2NO (g) + Q
2 2 ⇌ 3 1 2 ⇌ 2 2
❑ ❑
❑
则SO (g)+NO (g) SO (g)+NO(g)+ Q , Q= kJ·mol-1。
2 2 ⇌ 3 3 3
❑
②一定温度下,向固定体积为2 L的密闭容器中充入SO 和NO 各1 mol,发生反应:
2 2❑
SO (g)+NO (g) SO (g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是 (选
2 2 ⇌ 3
❑
填序号)。
a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO 的同时消耗1 mol NO
3 2
(3)矿石燃料的燃烧是造成酸雨的主要因素之一 。而甲醇日趋成为重要的有机燃料,通常
❑
利用CO和H 合成甲醇,其反应的化学方程式为CO(g)+ 2H(g) CHOH(g)。今在一容
2 2 ⇌ 3
❑
积可变的密闭容器中,充有10 mol CO和20 mol H ,用于合成甲醇。CO的平衡转化率(α)
2
与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为 反应(填“放热”或“吸热”)。
②A、B、C三点的平衡常数K 、K 、K 的大小关系为 。
A B C
Q -Q
【答案】 SO 、NO 1 2 a 、d 放热 K =K >K
2 2 A B C
2
【解析】 、 和CO中,能和空气中的水蒸气反应的有 、 ,
(1)SO NO SO NO
2 2 2 2
SO +H O=H SO ,H SO 进一步被氧气氧化为硫酸,
2 2 2 3 2 3
3NO +H O=2HNO +NO,硫酸和硝酸融入雨水,形成酸雨,在空气中CO不能与水
2 2 3
反应,故答案为:SO 、NO ;
2 2
Ⅰ
(2) 2SO (g)+O (g)=2SO (g)+Q
2 2 3 1
Ⅱ
2NO(g)+O (g)=2NO (g)+Q
2 2 2
1
根据盖斯定律: ×(Ⅰ−Ⅱ)得:SO (g)+NO (g)=SO (g)+NO(g)+Q ,
2 2 2 3 3
Q −Q
Q = 1 2,
3 2
Q −Q
故答案为: 1 2;
2②a.在SO (g)+NO (g)=SO (g)+NO(g)反应中,反应前后的气体体积变化等于零,
2 2 3
即△V =0,无论是否平衡,体系内的压强永远不变;
a.左右气体总物质的量相同,压强不能说明反应以达到化学平衡,a错误;
b.只有NO 有颜色,气体的颜色不变,说明NO 的量不再发生变化,说明反应以达到化
2 2
学平衡,b正确;
c.NO的物质的量不变,说明反应以达到化学平衡,c正确;
d.生成SO 和消耗NO 描述的都是正反应,不能说明反应以达到化学平衡,d错误。
3 2
故答案为:ad;
从图上可见,在 时,随温度的升高CO的转化率越来越低,可见,升温时平衡向
(3)① P
2
逆向移动,据勒夏特列原理,正反应放热,故答案为:放热;
②化学平衡常数只受温度的影响,该反应放热,温度越高平衡逆向移动,K值减小,
故答案为:K =K >K 。
A B C
五、帕金森治疗药物盐酸罗替戈汀的合成(本题共25分)
盐酸罗替戈汀(G)是一种用于治疗帕金森病的药物,G的一种合成路线如图:(25分)
5. 回答下列问题:
(1)B的名称是3-甲氧基苯乙酰氯,则A的名称是 。
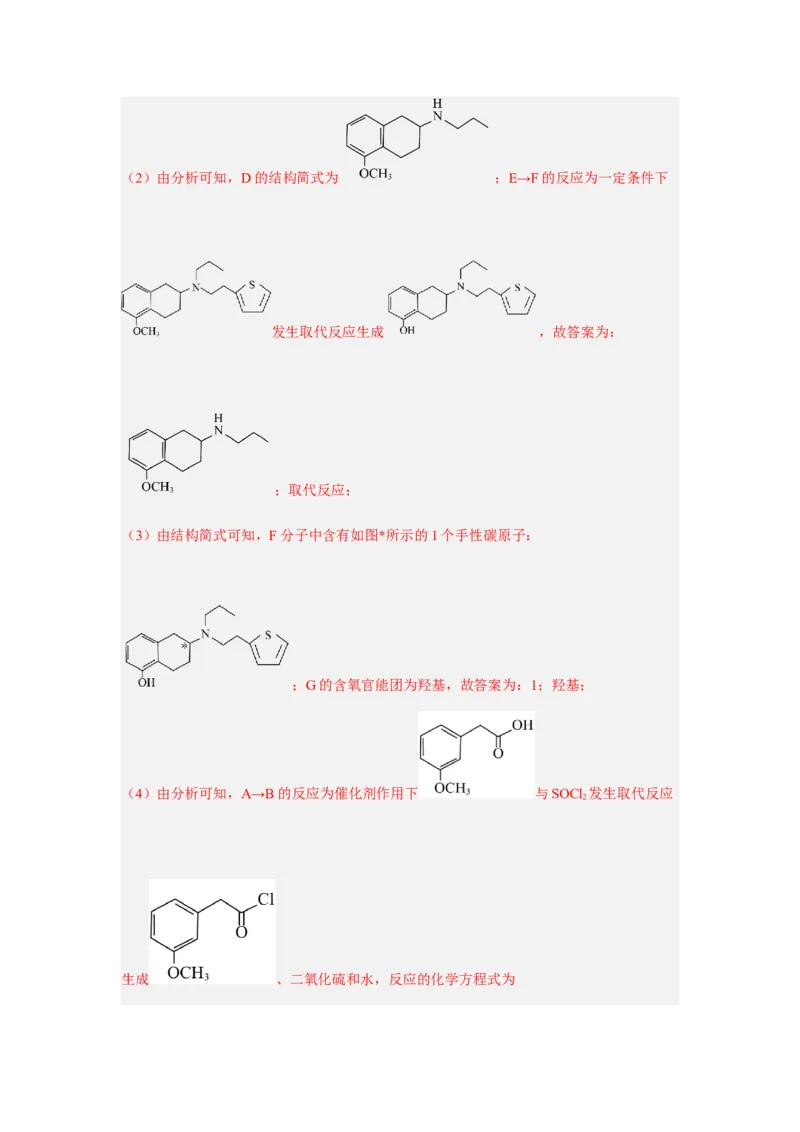
(2)D的结构简式为 ,E→F的反应类型是 。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳,F分子中有 个手性
碳,G的含氧官能团名称是 。
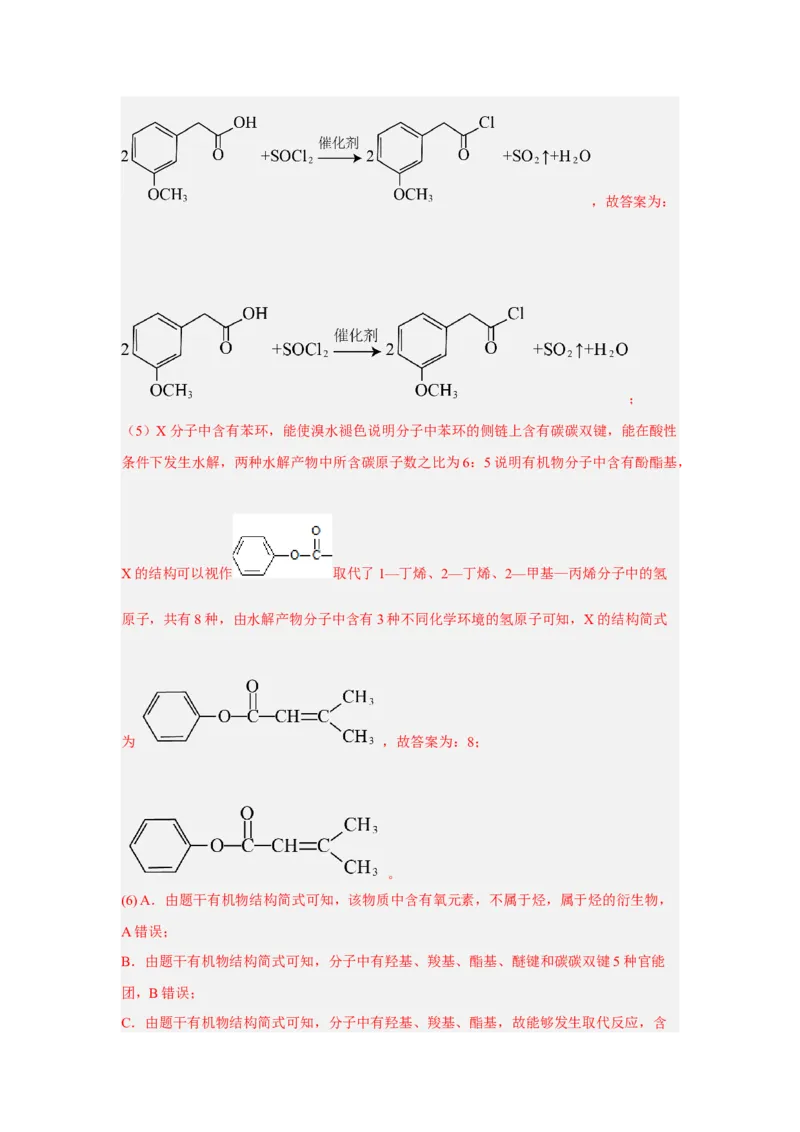
(4)A→B反应的化学方程式为 。
(5)C的同分异构体X同时满足下列条件,其结构有 种(不考虑立体异构)。
①含有苯环,能使溴水褪色;
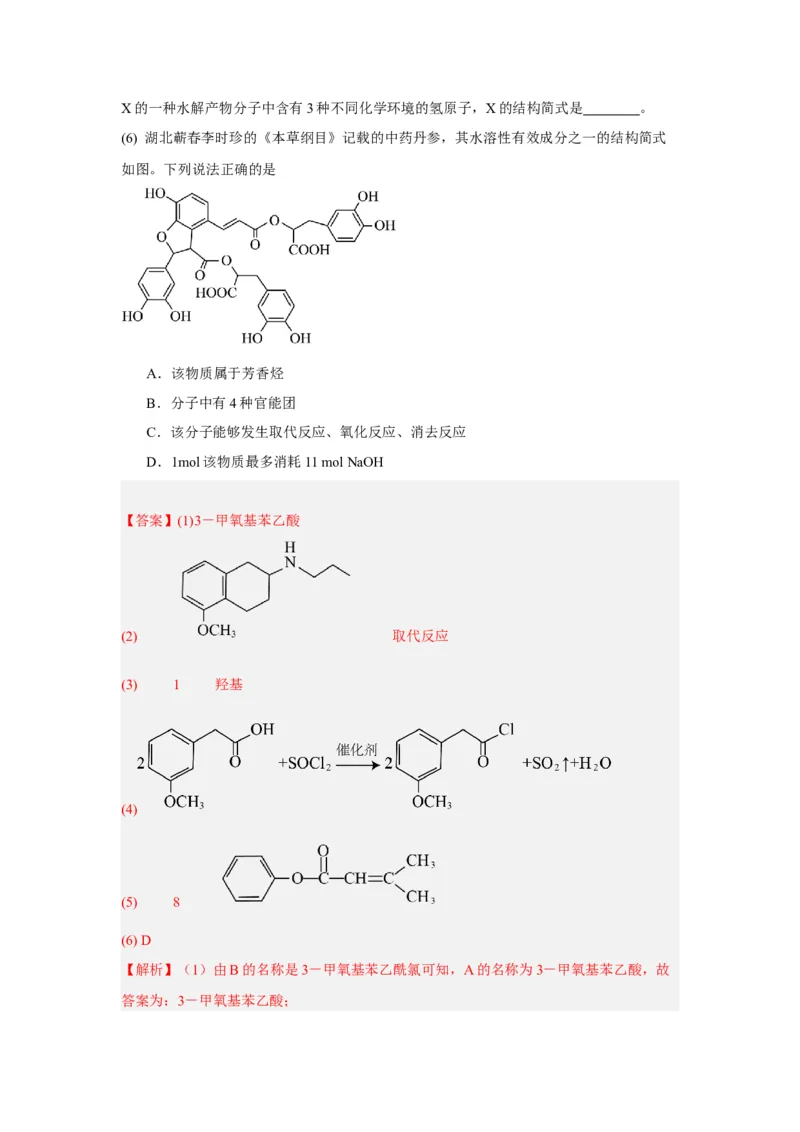
②能在酸性条件下发生水解,两种水解产物中所含碳原子数之比为6:5。X的一种水解产物分子中含有3种不同化学环境的氢原子,X的结构简式是 。
(6) 湖北蕲春李时珍的《本草纲目》记载的中药丹参,其水溶性有效成分之一的结构简式
如图。下列说法正确的是
A.该物质属于芳香烃
B.分子中有4种官能团
C.该分子能够发生取代反应、氧化反应、消去反应
D.1mol该物质最多消耗11 mol NaOH
【答案】(1)3-甲氧基苯乙酸
(2) 取代反应
(3) 1 羟基
(4)
(5) 8
(6) D
【解析】(1)由B的名称是3-甲氧基苯乙酰氯可知,A的名称为3-甲氧基苯乙酸,故
答案为:3-甲氧基苯乙酸;(2)由分析可知,D的结构简式为 ;E→F的反应为一定条件下
发生取代反应生成 ,故答案为:
;取代反应;
(3)由结构简式可知,F分子中含有如图*所示的1个手性碳原子:
;G的含氧官能团为羟基,故答案为:1;羟基;
(4)由分析可知,A→B的反应为催化剂作用下 与SOCl 发生取代反应
2
生成 、二氧化硫和水,反应的化学方程式为,故答案为:
;
(5)X分子中含有苯环,能使溴水褪色说明分子中苯环的侧链上含有碳碳双键,能在酸性
条件下发生水解,两种水解产物中所含碳原子数之比为6:5说明有机物分子中含有酚酯基,
X的结构可以视作 取代了1—丁烯、2—丁烯、2—甲基—丙烯分子中的氢
原子,共有8种,由水解产物分子中含有3种不同化学环境的氢原子可知,X的结构简式
为 ,故答案为:8;
。
(6) A.由题干有机物结构简式可知,该物质中含有氧元素,不属于烃,属于烃的衍生物,
A错误;
B.由题干有机物结构简式可知,分子中有羟基、羧基、酯基、醚键和碳碳双键5种官能
团,B错误;
C.由题干有机物结构简式可知,分子中有羟基、羧基、酯基,故能够发生取代反应,含有酚羟基和碳碳双键故能发生氧化反应,但不含醇羟基,故不能发生消去反应,C错误;
D.由题干有机物结构简式可知,分子中有7个羟基,2个羧基和2个醇酯基,故1mol该
物质最多消耗11 mol NaOH,D正确;
故答案为:D。