文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷03
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Ga 70
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.化学与生活密切相关。下列叙述正确的是
A.陶瓷坩埚和石英坩埚都是硅酸盐产品
B.乙醇、过氧化氢、次氯酸钠、 等消毒液均能将病毒氧化而达到消毒的目的
C.高分子材料聚氯乙烯广泛应用于食品包装材料
D.绿色化学是利用化学原理和技术手段,减少或消除产品在生产生活中涉及的有害物质
2.化学实验必须树立安全意识。下列说法错误的是
A.金属钠着火时,不能使用泡沫灭火器,应用超轻碳酸氢钾干粉灭火器扑灭
B.如不慎将碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸
C.有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
D.75%酒精免洗消毒喷雾存放处张贴 警示标识
3.下列关于 、 、 及 的叙述正确的是
A.都是共价化合物且常温下均为气体
B. 可用于制光导纤维,干冰可用于人工降雨
C.都是酸性氧化物,都能与强碱溶液反应
D.都能溶于水且与水反应生成相应的酸
4.氯气是一种重要的工业原料,工业上利用下列反应来检查氯气管道是否漏气:
。下列说法不正确的是
A.生成物 是离子晶体
B. 的结构式为 , 分子中含有 键和 键
C.可通过原电池将 与 反应的化学能转化为电能
D.该反应氧化剂和还原剂的物质的量之比为3:8
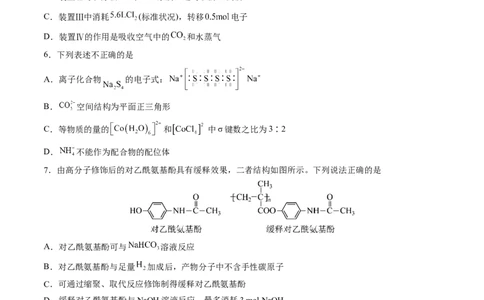
5.某校化学兴趣小组利用如图装置在实验室制备“84”消毒液,下列说法正确的是A.装置I中的 可以替换成
B.装置Ⅱ可以除去 中 杂质,还可以防止倒吸
C.装置Ⅲ中消耗 (标准状况),转移 电子
D.装置Ⅳ的作用是吸收空气中的 和水蒸气
6.下列表述不正确的是
A.离子化合物 的电子式:
B. 空间结构为平面正三角形
C.等物质的量的 和 中σ键数之比为3∶2
D. 不能作为配合物的配位体
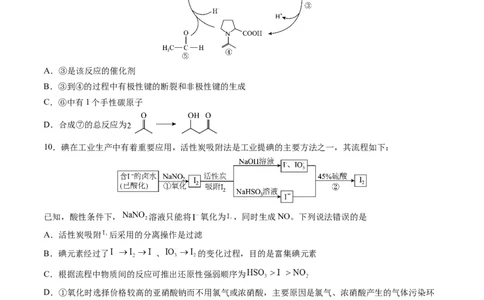
7.由高分子修饰后的对乙酰氨基酚具有缓释效果,二者结构如图所示。下列说法正确的是
A.对乙酰氨基酚可与 溶液反应
B.对乙酰氨基酚与足量 加成后,产物分子中不含手性碳原子
C.可通过缩聚、取代反应修饰制得缓释对乙酰氨基酚
D.缓释对乙酰氨基酚与NaOH溶液反应,最多消耗3 mol NaOH
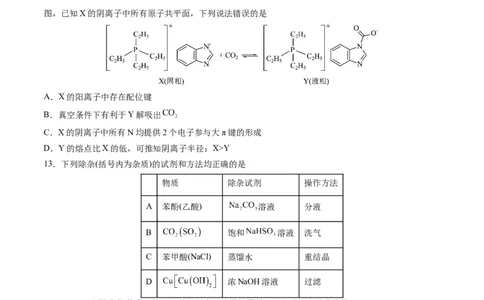
8.某离子液体结构如图,Q、R、T、X、Y和Z为原子序数依次增大的主族元素,基态T原子和Y原子最
外层均有两个单电子,Q、R、X和Z质子数均为奇数且和为22。下列说法错误的是
A.第一电离能:T<X<Y B.键长:T-Q>X-Q
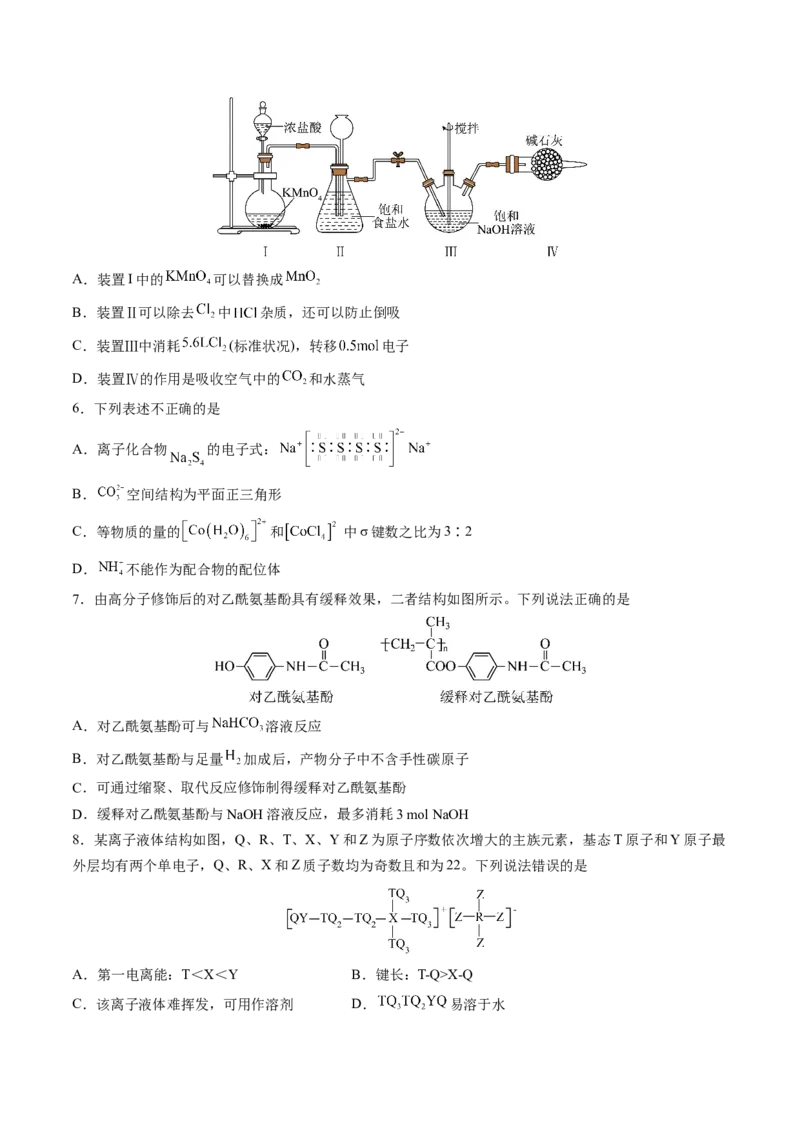
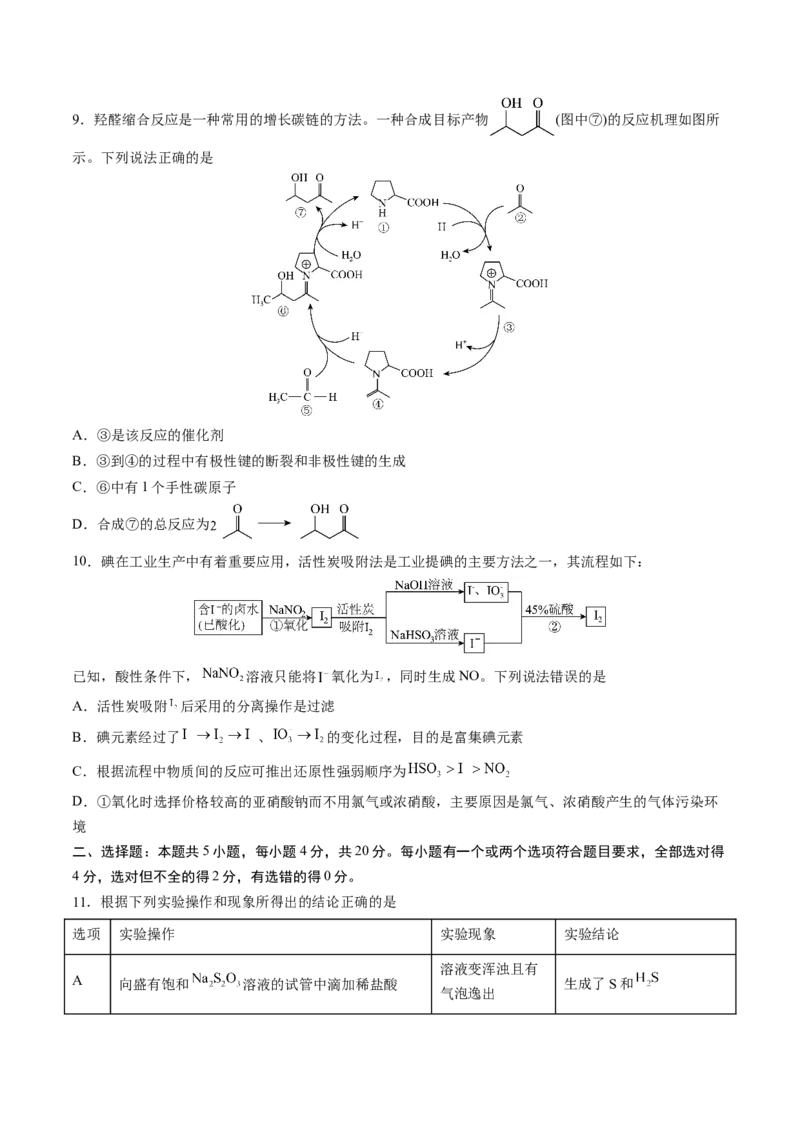
C.该离子液体难挥发,可用作溶剂 D. 易溶于水9.羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物 (图中⑦)的反应机理如图所
示。下列说法正确的是
A.③是该反应的催化剂
B.③到④的过程中有极性键的断裂和非极性键的生成
C.⑥中有1个手性碳原子
D.合成⑦的总反应为
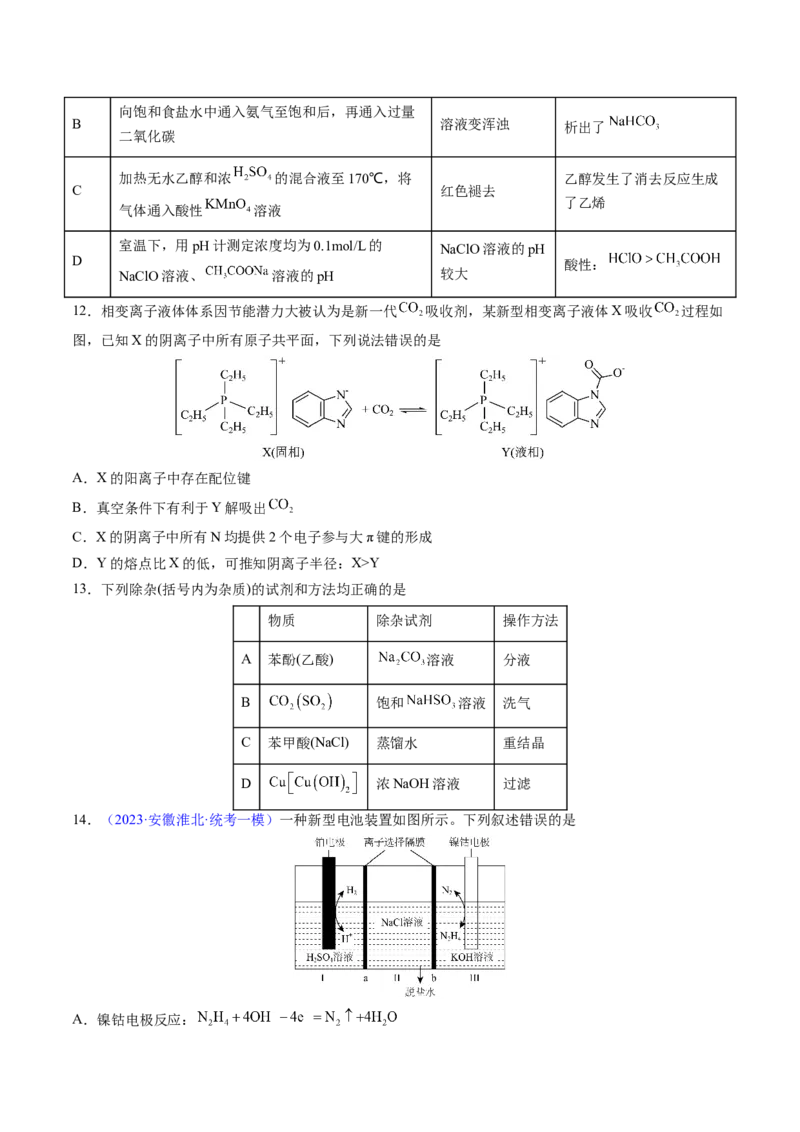
10.碘在工业生产中有着重要应用,活性炭吸附法是工业提碘的主要方法之一,其流程如下:
已知,酸性条件下, 溶液只能将 氧化为 ,同时生成NO。下列说法错误的是
A.活性炭吸附 后采用的分离操作是过滤
B.碘元素经过了 、 的变化过程,目的是富集碘元素
C.根据流程中物质间的反应可推出还原性强弱顺序为
D.①氧化时选择价格较高的亚硝酸钠而不用氯气或浓硝酸,主要原因是氯气、浓硝酸产生的气体污染环
境
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.根据下列实验操作和现象所得出的结论正确的是
选项 实验操作 实验现象 实验结论
溶液变浑浊且有
A 向盛有饱和 溶液的试管中滴加稀盐酸 生成了S和
气泡逸出向饱和食盐水中通入氨气至饱和后,再通入过量
B 溶液变浑浊 析出了
二氧化碳
加热无水乙醇和浓 的混合液至170℃,将 乙醇发生了消去反应生成
C 红色褪去
了乙烯
气体通入酸性 溶液
室温下,用pH计测定浓度均为0.1mol/L的 NaClO溶液的pH
D 酸性:
NaClO溶液、 溶液的pH 较大
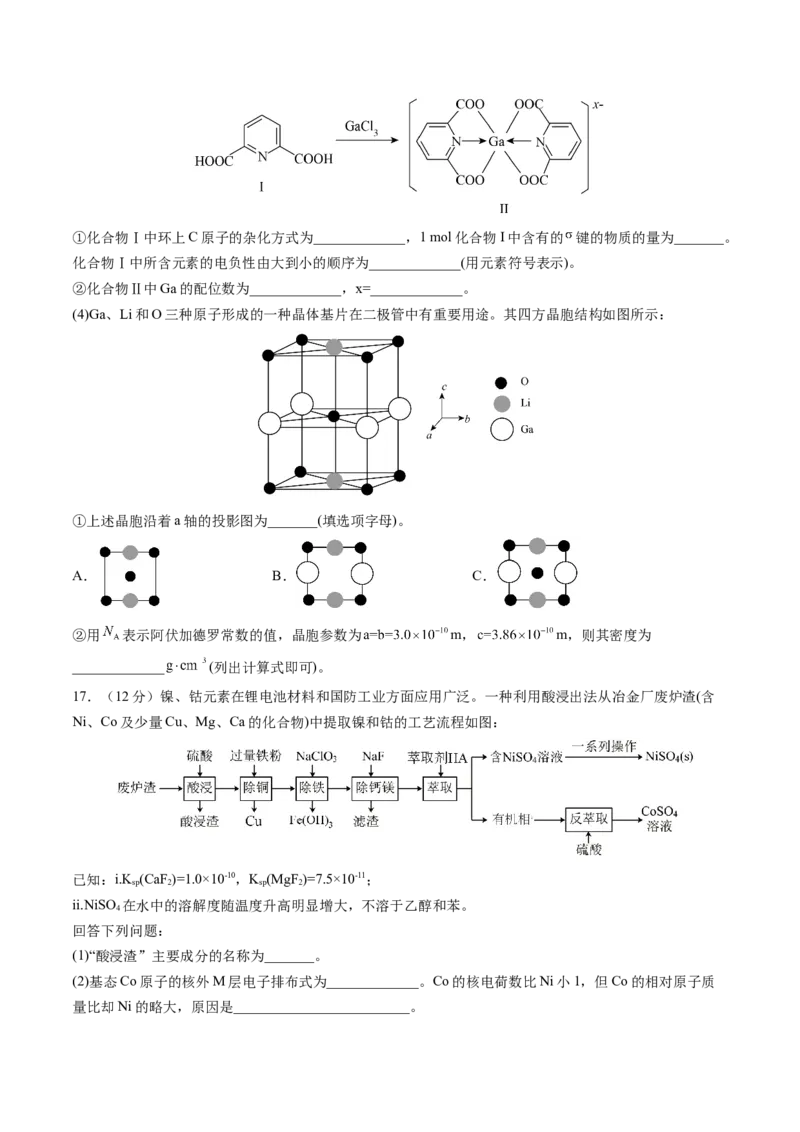
12.相变离子液体体系因节能潜力大被认为是新一代 吸收剂,某新型相变离子液体X吸收 过程如
图,已知X的阴离子中所有原子共平面,下列说法错误的是
A.X的阳离子中存在配位键
B.真空条件下有利于Y解吸出
C.X的阴离子中所有N均提供2个电子参与大π键的形成
D.Y的熔点比X的低,可推知阴离子半径:X>Y
13.下列除杂(括号内为杂质)的试剂和方法均正确的是
物质 除杂试剂 操作方法
A 苯酚(乙酸) 溶液 分液
B 饱和 溶液 洗气
C 苯甲酸(NaCl) 蒸馏水 重结晶
D 浓NaOH溶液 过滤
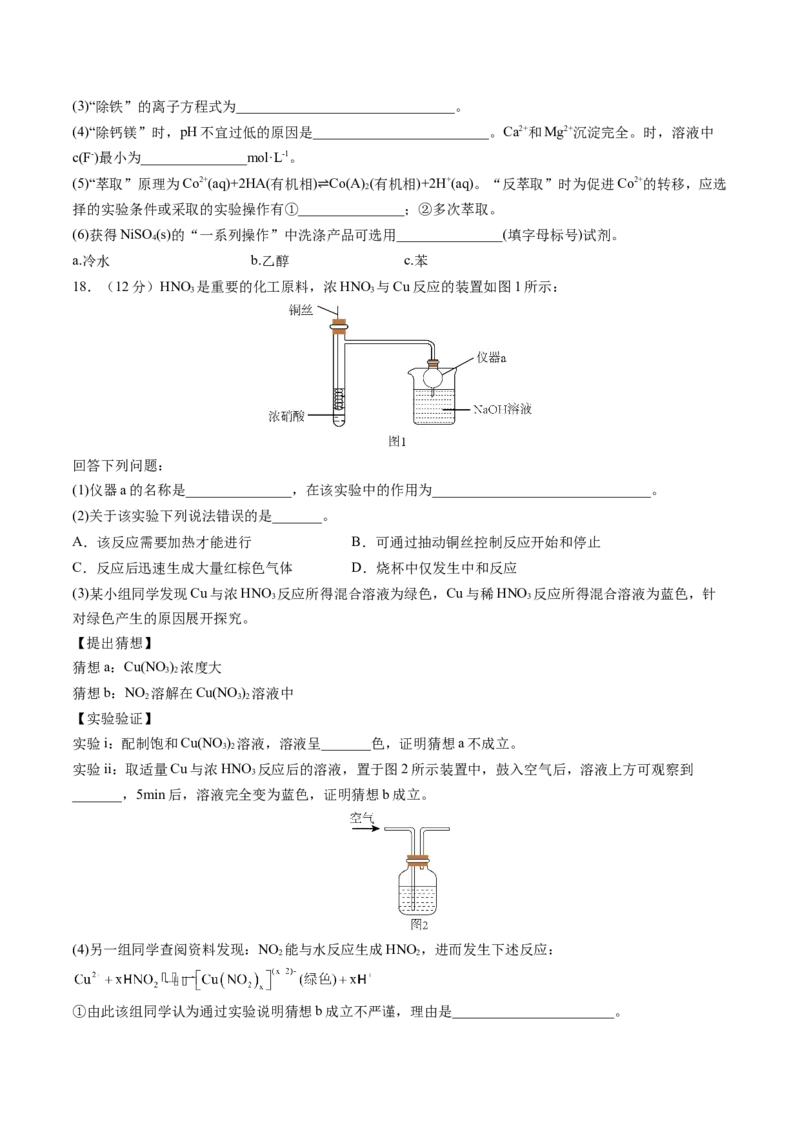
14.(2023·安徽淮北·统考一模)一种新型电池装置如图所示。下列叙述错误的是
A.镍钴电极反应:B.II区的 通过a交换膜向I区迁移, 通过b交换膜向III区迁移
C.该装置工作时总反应:
D.该装置工作时还利用了中和能
15.室温,向 和 的混合溶液中逐滴加入 溶液,溶液中 与 的变
化关系如图所示。下列说法正确的是
(已知: 的 、 分别为 、 ; )
A.a对应溶液的pH小于b
B.b对应溶液的
C.a→b变化过程中,溶液中的 减小
D.a对应的溶液中一定存在:
三、非选择题:本题共5小题,共60分。
16.(12分)镓及其化合物在合金工业、制药工业、电池工业有广泛的应用。回答下列问题:
(1)基态Ga原子的价层电子排布式为_______。
(2) 是一种温和的还原剂,其可由 和过量的LiH反应制得: 。
①已知 的熔点为77.9℃,LiCl的熔点为605℃,两者熔点差异较大的原因为___________________。
② 在270℃左右以二聚物存在,该二聚物的每个原子都满足8电子稳定结构,写出它的结构式:
___________________。
③ 的立体构型为_____________。
(3)一种含镓的药物合成方法如图所示:①化合物Ⅰ中环上C原子的杂化方式为_____________,1 mol化合物I中含有的 键的物质的量为_______。
化合物Ⅰ中所含元素的电负性由大到小的顺序为_____________(用元素符号表示)。
②化合物Ⅱ中Ga的配位数为_____________,x=_____________。
(4)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
①上述晶胞沿着a轴的投影图为_______(填选项字母)。
A. B. C.
②用 表示阿伏加德罗常数的值,晶胞参数为 m, m,则其密度为
_____________ (列出计算式即可)。
17.(12分)镍、钴元素在锂电池材料和国防工业方面应用广泛。一种利用酸浸出法从冶金厂废炉渣(含
Ni、Co及少量Cu、Mg、Ca的化合物)中提取镍和钴的工艺流程如图:
已知:i.K (CaF )=1.0×10-10,K (MgF )=7.5×10-11;
sp 2 sp 2
ii.NiSO 在水中的溶解度随温度升高明显增大,不溶于乙醇和苯。
4
回答下列问题:
(1)“酸浸渣”主要成分的名称为_______。
(2)基态Co原子的核外M层电子排布式为_____________。Co的核电荷数比Ni小1,但Co的相对原子质
量比却Ni的略大,原因是_________________________。(3)“除铁”的离子方程式为_______________________________。
(4)“除钙镁”时,pH不宜过低的原因是_________________________。Ca2+和Mg2+沉淀完全。时,溶液中
c(F-)最小为_______________mol·L-1。
(5)“萃取”原理为Co2+(aq)+2HA(有机相) Co(A) (有机相)+2H+(aq)。“反萃取”时为促进Co2+的转移,应选
2
择的实验条件或采取的实验操作有①_______________;②多次萃取。
⇌
(6)获得NiSO (s)的“一系列操作”中洗涤产品可选用_______________(填字母标号)试剂。
4
a.冷水 b.乙醇 c.苯
18.(12分)HNO 是重要的化工原料,浓HNO 与Cu反应的装置如图1所示:
3 3
回答下列问题:
(1)仪器a的名称是_______________,在该实验中的作用为_______________________________。
(2)关于该实验下列说法错误的是_______。
A.该反应需要加热才能进行 B.可通过抽动铜丝控制反应开始和停止
C.反应后迅速生成大量红棕色气体 D.烧杯中仅发生中和反应
(3)某小组同学发现Cu与浓HNO 反应所得混合溶液为绿色,Cu与稀HNO 反应所得混合溶液为蓝色,针
3 3
对绿色产生的原因展开探究。
【提出猜想】
猜想a:Cu(NO ) 浓度大
3 2
猜想b:NO 溶解在Cu(NO ) 溶液中
2 3 2
【实验验证】
实验i:配制饱和Cu(NO ) 溶液,溶液呈_______色,证明猜想a不成立。
3 2
实验ii:取适量Cu与浓HNO 反应后的溶液,置于图2所示装置中,鼓入空气后,溶液上方可观察到
3
_______,5min后,溶液完全变为蓝色,证明猜想b成立。
(4)另一组同学查阅资料发现:NO 能与水反应生成HNO,进而发生下述反应:
2 2
①由此该组同学认为通过实验说明猜想b成立不严谨,理由是_______________________。②写出NO 与水反应生成HNO 的化学方程式_______________________________。
2 2
③该组同学改进后设计了新的实验:
实验iii:取适量Cu与浓HNO 反应后的溶液,置于图2所示装置中,鼓入氮气后,溶液上方现象与实验ii
3
相同,但5min后,溶液仍为绿色。对比实验ii与实验iii,可推测Cu(NO ) 溶液为绿色的原因主要是
3 2
_______________________________________________________。
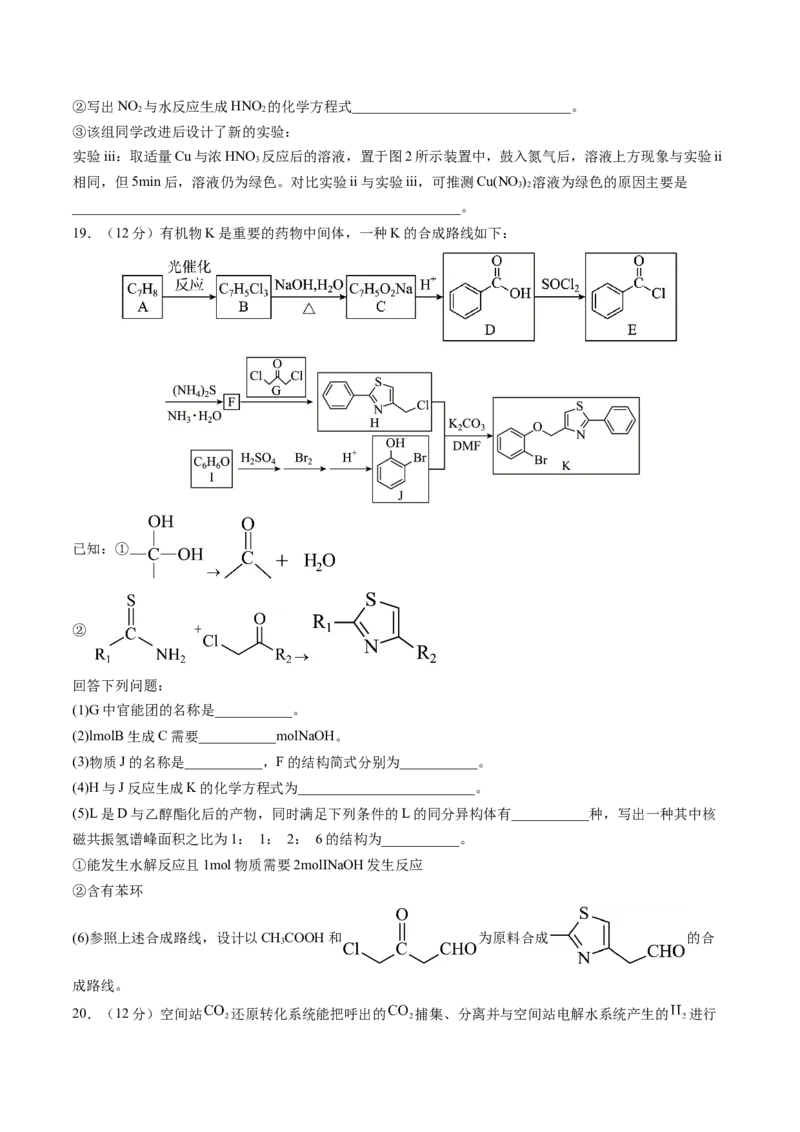
19.(12分)有机物K是重要的药物中间体,一种K的合成路线如下:
已知:①
② +
回答下列问题:
(1)G中官能团的名称是___________。
(2)lmolB生成C需要___________molNaOH。
(3)物质J的名称是___________,F的结构简式分别为___________。
(4)H与J反应生成K的化学方程式为_________________________。
(5)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有___________种,写出一种其中核
磁共振氢谱峰面积之比为1: 1: 2: 6的结构为___________。
①能发生水解反应且1mol物质需要2molINaOH发生反应
②含有苯环
(6)参照上述合成路线,设计以CHCOOH和 为原料合成 的合
3
成路线。
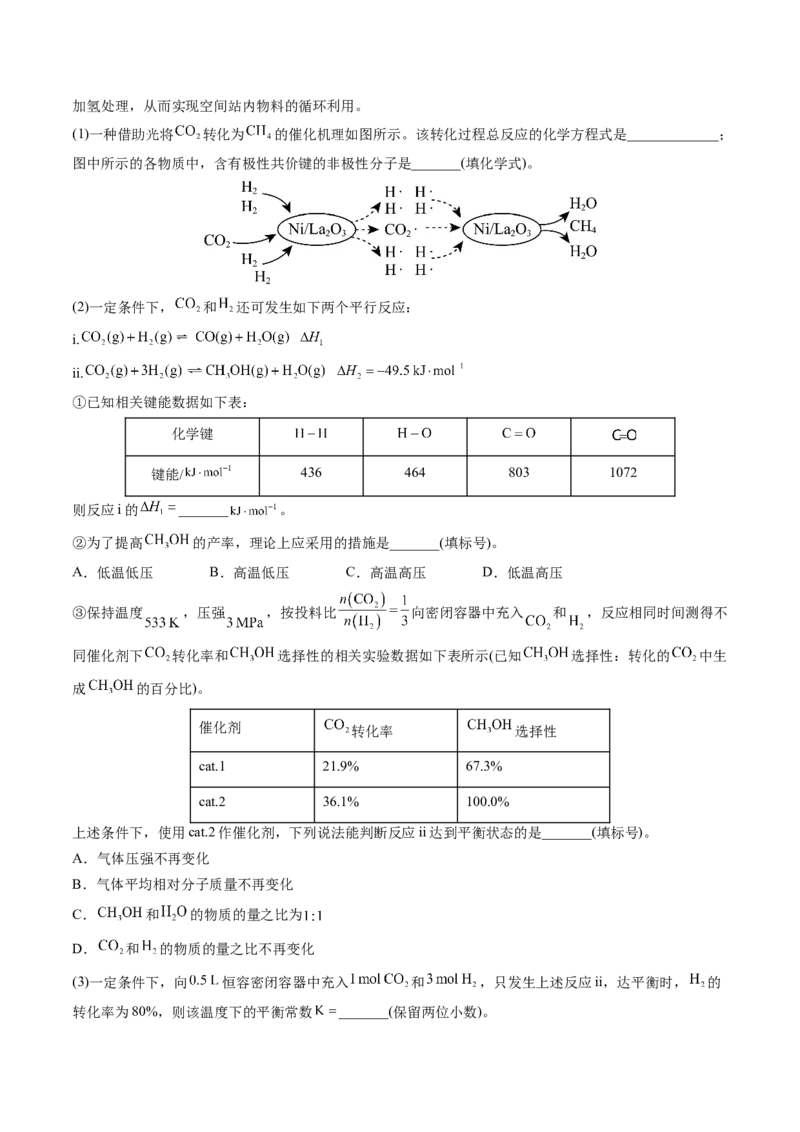
20.(12分)空间站 还原转化系统能把呼出的 捕集、分离并与空间站电解水系统产生的 进行加氢处理,从而实现空间站内物料的循环利用。
(1)一种借助光将 转化为 的催化机理如图所示。该转化过程总反应的化学方程式是_____________;
图中所示的各物质中,含有极性共价键的非极性分子是_______(填化学式)。
(2)一定条件下, 和 还可发生如下两个平行反应:
i.
ii.
①已知相关键能数据如下表:
化学键
键能/ 436 464 803 1072
则反应i的 _______ 。
②为了提高 的产率,理论上应采用的措施是_______(填标号)。
A.低温低压 B.高温低压 C.高温高压 D.低温高压
③保持温度 ,压强 ,按投料比 向密闭容器中充入 和 ,反应相同时间测得不
同催化剂下 转化率和 选择性的相关实验数据如下表所示(已知 选择性:转化的 中生
成 的百分比)。
催化剂 转化率 选择性
cat.1 21.9% 67.3%
cat.2 36.1% 100.0%
上述条件下,使用cat.2作催化剂,下列说法能判断反应ii达到平衡状态的是_______(填标号)。
A.气体压强不再变化
B.气体平均相对分子质量不再变化
C. 和 的物质的量之比为
D. 和 的物质的量之比不再变化
(3)一定条件下,向 恒容密闭容器中充入 和 ,只发生上述反应ii,达平衡时, 的
转化率为80%,则该温度下的平衡常数 _______(保留两位小数)。(4)若恒容密闭容器中只发生上述反应i,在进气比 不同、温度不同时,测得相应的 平衡
转化率如图所示。则B和D两点的温度 _______ (填“<”,“>”,或“=”),其原因是_______。