文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(浙江专用)
黄金卷03
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32
Cl 35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Br 80 Ag 108 Ba 137
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.下列物质中属于难溶于水的碱性氧化物的是( )
A.SiO B.Fe O C.CuO D.Al O
2 3 4 2 3
2.下列化学用语表示正确的是( )
A.中子数为76 的碘原子:
B.乙烷的球棍模型:
C.2−丁烯的结构简式:CH=CHCH=CH
2 2
D.用电子式表示 NaO的形成过程:
2
3.NaSiO 应用广泛,下列说法不正确的是( )
2 3
A.Si元素位于周期表p区 B. NaSiO 属于强电解质
2 3
C.NaSiO 的水溶液俗称水玻璃 D.存放 NaSiO 溶液的试剂瓶可以用玻璃塞
2 3 2 3
4.物质的性质决定用途,下列两者关系对应不正确的是( )
A.铝合金质量轻、强度大,可用作制造飞机和宇宙飞船的材料
B.FeCl 溶液呈酸性,可腐蚀覆铜板制作印刷电路板
3
C.CuS、HgS极难溶,可用NaS作沉淀剂除去废水中的Cu2+和Hg2+
2
D.碳化硅硬度大,可用作砂纸、砂轮的磨料
5.下列实验装置能达到相应实验目的的是( )
选项 A B C D实验
装置
关闭a、打开
实验 验证牺牲阳极法 验证MnO 是HO
制备并收集氨气 2 2 2 b,可检查装
目的 保护铁 分解的催化剂
置的气密性
6.制取乙炔时,常用CuSO 溶液除去乙炔中的杂质。反应为:
4
①HS+CuSO= CuS↓+H SO
2 4 2 4
②24CuSO +11PH +12H O=8CuP↓+3H PO +24H SO
4 3 2 3 3 4 2 4
下列分析正确的是( )
A.在燃料电池中,通入C H 一极为正极
2 2
B.依据反应①可推出氢硫酸为二元强酸
C.反应②中若1.2mol CuSO 发生反应,被氧化的PH 为0.156mol
4 3
D.CuP既是氧化产物,也是还原产物
3
7.N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.铁与水蒸气反应后,固体质量增加了3.2g,则电子转移的数目为0.4N
A
B.1L0.1mol/L K CrO 溶液中,CrO2-的数目为0.1N
2 2 7 2 7 A
C.10g14N16O 和16O 混合气体中含有的质子数为5N
2 2 A
D.3.2gN H 中含有的共价键的数目为0.5N
2 4 A
8.下列说法不正确的是( )
A.甘油醛是最简单的醛糖,存在对映异构体
B.蛋白质溶液中加入少量的硫酸铵溶液产生白色沉淀,加水后溶解
C.核酸是由核苷酸单体缩聚形成的生物大分子,其单体水解得到核苷和磷酸
D.在酸催化下,等物质的量的苯酚和甲醛反应得到线型结构酚醛树脂
9.下列离子方程式书写正确的是
A.NaHCO 溶液的水解:HCO -+H O CO2-+H O+
3 3 2 3 3
B.向Al (SO ) 溶液中滴加NaCO 溶液:2Al3++3CO 2-=Al(CO)↓
2 4 3 2 3 3 2 3 3
C.向Fe (SO ) 溶液中通入足量HS:2Fe3++S2-=2Fe2++S↓
2 4 3 2
D.向Ca(ClO) 溶液中通入少量SO :Ca2++3ClO-+SO+H O=Cl-+CaSO↓+2HClO
2 2 2 2 4
10.一种高分子化合物W的合成路线如图(图中 表示链延长):下列说法不正确的是( )
A.化合物Y中最多18个原子共平面
B.化合物Z的核磁共振氢谱有3组峰
C.高分子化合物W具有网状结构
D.X、Y、Z通过缩聚反应合成高分子化合物W
11.下X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的2p轨道上有两个未成对电子,Z
最高能级电子数是总电子数的一半,M是同周期主族元素中原子半径最大的,Q与Z的某种化合物可作为
新型自来水消毒剂。下列说法不正确的是( )
A.第一电离能:Y>X>Z>M
B.X的氢化物沸点可能高于Z的氢化物
C.X、Z与M三种元素形成的化合物中可能含有非极性共价键
D.最高价氧化物对应水化物的酸性:Q>Y
12.用钛铁矿(主要成分为FeTiO,含有少量MgO、SiO 等杂质)制备LiFePO 的工艺流程如图所示:
3 2 4
已知:
钛铁矿经盐酸浸取后钛主要以TiOCl 2-形式存在, , 。
4
下列说法不正确的是( )
A.滤液①中含有Fe2+、Mg2+
B.相同温度下溶解度:Mg(PO )>FePO
3 4 2 4
C.煅烧的主要反应为2FePO + LiCO+H C O 2LiFePO +3CO ↑+H O↑
4 2 3 2 2 4 4 2 2
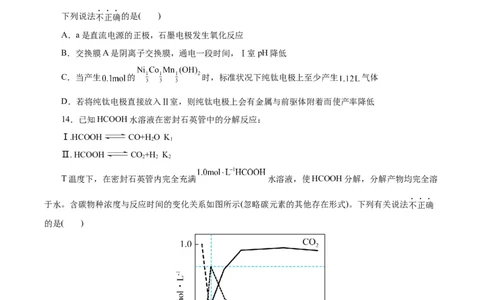
D.为保证水解过滤时能完全除钛,需调pH至溶液呈碱性13.电解硫酸钠溶液制取电池正极材料 的前驱体 ,其工作原理如图
所示:
下列说法不正确的是( )
A.a是直流电源的正极,石墨电极发生氧化反应
B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低
C.当产生 的 时,标准状况下纯钛电极上至少产生 气体
D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低
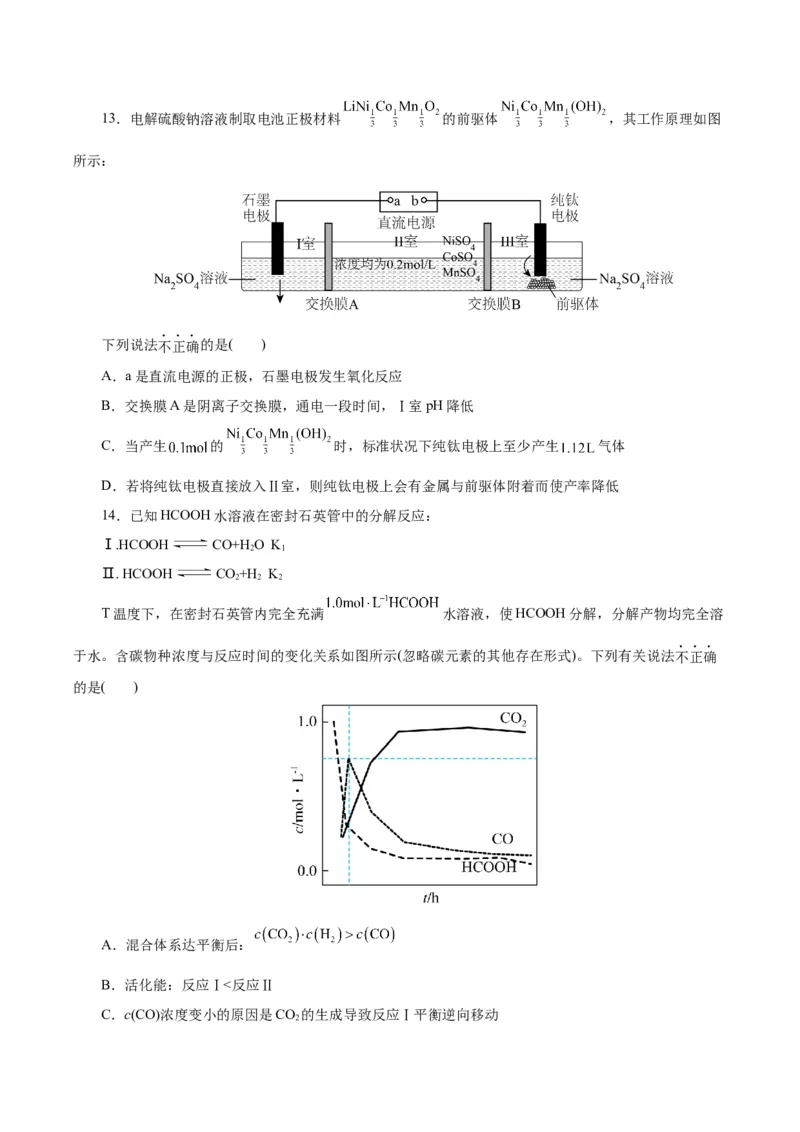
14.已知HCOOH水溶液在密封石英管中的分解反应:
Ⅰ.HCOOH CO+HO K
2 1
Ⅱ. HCOOH CO+H K
2 2 2
T温度下,在密封石英管内完全充满 水溶液,使HCOOH分解,分解产物均完全溶
于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列有关说法不正确
的是( )
A.混合体系达平衡后:
B.活化能:反应Ⅰ<反应Ⅱ
C.c(CO)浓度变小的原因是CO 的生成导致反应Ⅰ平衡逆向移动
2D.c(HCOOH)可降为0
15.苯酚是重要的化工原料,将废水中的苯酚富集并加入NaCO;转化为苯酚钠,再通入CO,可进
2 3 2
一步分离回收。已知:K(C HOH)=1.0×10-10,K (H CO)=4.5×10-7,K (H CO)=4.7×10-11。下列说法正确的
a 6 5 a1 2 3 a2 2 3
是( )
A.NaCO;也可用NaOH或NaHCO 替代
2 3 3
B.2HCO - HCO+CO 2-的平衡常数K约为9.57×103
3 2 3 3
C.转化反应中若c(Na+)=2c(C HO-)+ 2c(C HOH),此时溶液中c(HCO -)>c(C HO-)
6 5 6 5 3 6 5
D.当通入CO 至溶液pH=10时,溶液中的C HONa完全转化为C HOH
2 6 5 6 5
16.探究氮及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案 现象 结论
一段时间后,前者有气体产 稀硝酸的氧化性强
A 常温下,将Fe片分别插入稀硝酸和浓硝酸中
生,后者无明显现象 于浓硝酸
Fe(NO ) 晶体已氧
B 将Fe(NO ) 样品溶于稀硫酸后,滴加KSCN溶液 溶液变红 3 2
3 2 化变质
向两个同规格烧瓶中分别装入同比例的NO 和 一段时间后,两烧瓶内颜色 NO →NO 的转化
C 2 2 2 4
NO 气体,并分别浸泡于热水和冷水中 深浅不同 存在限度
2 4
试管底部固体消失,试管口 NH Cl固体受热易
D 将盛有NH Cl固体的试管加热 4
4 有晶体凝结 升华
第Ⅱ卷
二、非选择题:共5题,共52分。
17.(10分)氮化铝晶体为共价晶体,是一种新型的无机非金属材料,有其重大用途。
(1)某一种制取方法是Al O+C+N →AlN+CO (未配平)。
2 3 2
①每个N 中含 _______ 个 键,碳单质常见的是金刚石、石墨,其碳原子通常依次采用 _______ 、
2
_______ 杂化;
②碳单质与生石灰在高温下生成电石与CO,CaC 晶体属于含离子键和 _______(填非极性或极性)共
2
价键的离子晶体,而CO与CO 比较,CO中C-O键更短,其主要原因是 _______ 。
2
(2) AlN也可由(CH) Al和NH 在一定条件下制取,该反应的化学方程式是 _______(可以不写反应
3 3 3
条件),氨属于含极性共价键的 _______(填非极性或极性)分子。
(3)已知 晶胞如图所示:①空心球(原子)半径大于黑心球(原子)半径,空心球代表的是 _______(写名称)原子,理由是 (空心球)
_______ (黑心球)[填写某一种原子 的原子半径 的单质通常不形成共价晶体];
②设N 为阿伏加德罗常数的值,晶胞的边长 ,则 的晶体密度为_______ g· cm-3。
A
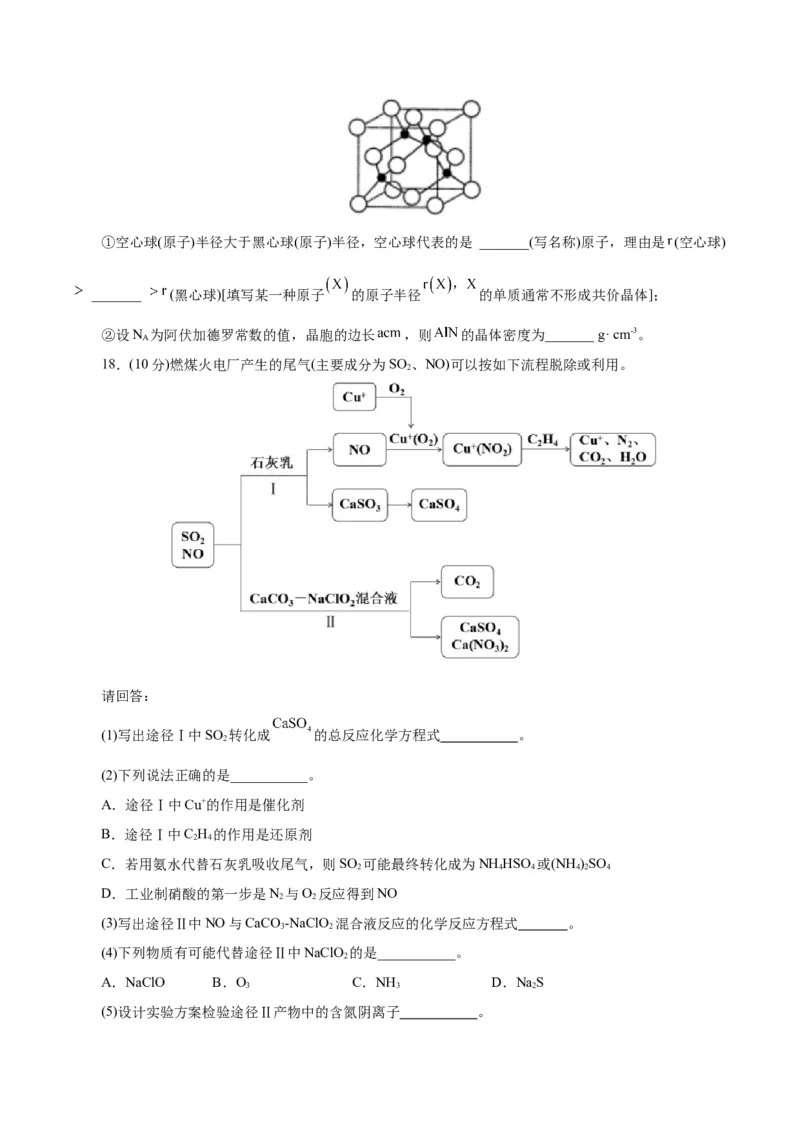
18.(10分)燃煤火电厂产生的尾气(主要成分为SO 、NO)可以按如下流程脱除或利用。
2
请回答:
(1)写出途径Ⅰ中SO 转化成 的总反应化学方程式 。
2
(2)下列说法正确的是___________。
A.途径Ⅰ中Cu+的作用是催化剂
B.途径Ⅰ中C H 的作用是还原剂
2 4
C.若用氨水代替石灰乳吸收尾气,则SO 可能最终转化成为NH HSO 或(NH )SO
2 4 4 4 2 4
D.工业制硝酸的第一步是N 与O 反应得到NO
2 2
(3)写出途径Ⅱ中NO与CaCO -NaClO 混合液反应的化学反应方程式 。
3 2
(4)下列物质有可能代替途径Ⅱ中NaClO 的是___________。
2
A.NaClO B.O C.NH D.NaS
3 3 2
(5)设计实验方案检验途径Ⅱ产物中的含氮阴离子 。19.(10分)丙烯是一种重要的化工原料,其主要产品聚丙烯是生产口罩喷溶布的原料。铬基催化剂下
丙烷生产丙烯相关主要反应有:
Ⅰ.C H(g) C H(g)+H(g) ΔH =+124.14kJ·mol−1
3 8 3 6 2 1
Ⅱ.C H(g) C H(g)+CH(g)
3 8 2 4 4
Ⅲ.C H(g) 3(s)+4H(g)
3 8 2
请回答:
(1)已知键能: , 。C=C的键能与C-C的键能相差约
kJ/mol。
(2)600℃时,容器压强恒为P,铬基催化剂下两个密闭容器中分别按下表投料发生反应:
容器 C H/mol CO/mol N/mol
3 8 2 2
A 1 0 10
B 1 2 8
①容器B生成C H 的反应流程如下:
3 6
下列有关说法正确的是 。
A.原料气中通入N 可提高C H 的平衡转化率
2 3 8
B.升高温度,一定能提高的C H 平衡产率
3 6
C.过程1产生C H 的量大于过程2和过程3产生的C H
3 6 3 6
D.在铬基催化剂中适当加入CaO可促进过程2平衡正移而提高C H 的平衡转化率
3 8
②若容器A中只发生反应Ⅰ和反应Ⅱ,C H 的平衡转化率为 ,C H 的选择性(选择性
3 8 3 6
)为w,计算反应Ⅰ的平衡常数 。(用平衡分压代替
平衡浓度计算,分压=总压×物质的量分数)。
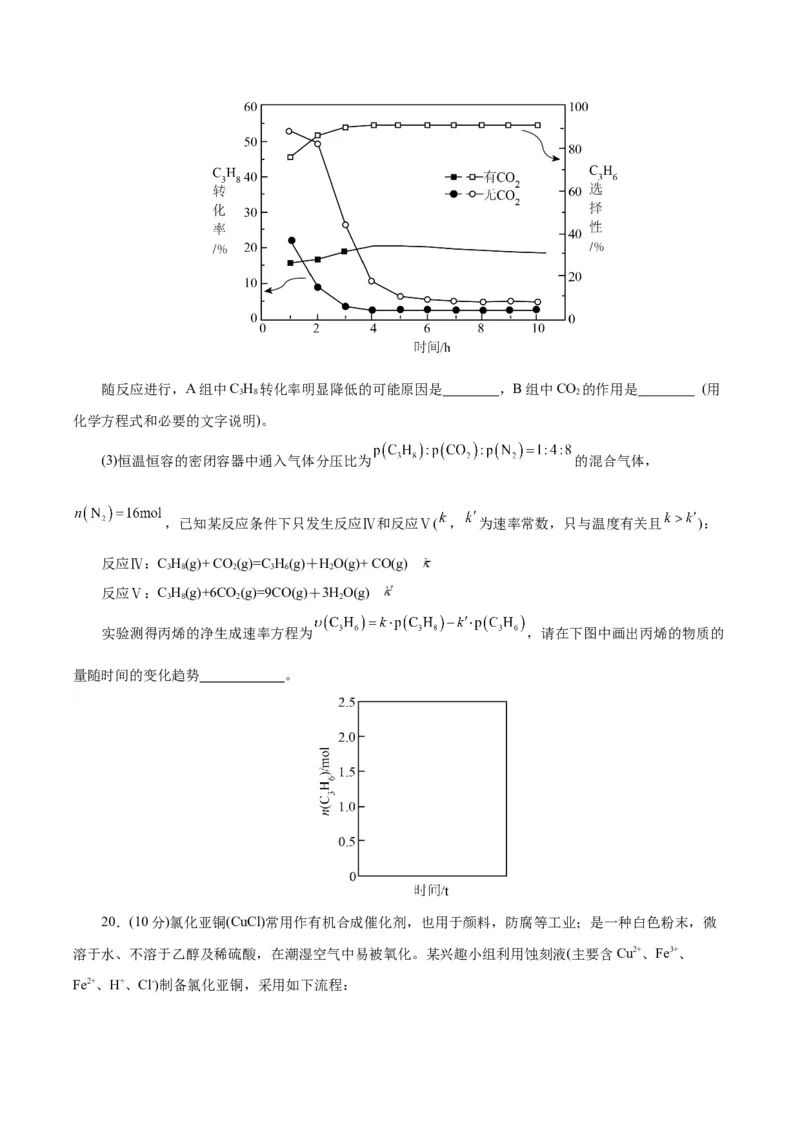
③按照容器A和容器B的气体组分比,将两组气体按相同流速分别通过催化剂固定床反应器,C H 的
3 8
转化率和C H 的选择性随时间变化如图所示:
3 6随反应进行,A组中C H 转化率明显降低的可能原因是 ,B组中CO 的作用是 (用
3 8 2
化学方程式和必要的文字说明)。
(3)恒温恒容的密闭容器中通入气体分压比为 的混合气体,
,已知某反应条件下只发生反应Ⅳ和反应Ⅴ( , 为速率常数,只与温度有关且 ):
反应Ⅳ:C H(g)+ CO (g)=C H(g)+HO(g)+ CO(g)
3 8 2 3 6 2
反应Ⅴ:C H(g)+6CO (g)=9CO(g)+3HO(g)
3 8 2 2
实验测得丙烯的净生成速率方程为 ,请在下图中画出丙烯的物质的
量随时间的变化趋势 。
20.(10分)氯化亚铜(CuCl)常用作有机合成催化剂,也用于颜料,防腐等工业;是一种白色粉末,微
溶于水、不溶于乙醇及稀硫酸,在潮湿空气中易被氧化。某兴趣小组利用蚀刻液(主要含Cu2+、Fe3+、
Fe2+、H+、Cl-)制备氯化亚铜,采用如下流程:已知:
①
②Cu++2SO2-= [Cu(SO )]3-
3 3 2
(1)步骤Ⅰ发生反应的离子方程式 。
(2)下列说法正确的是___________。
A.步骤Ⅰ,可以用KMnO 溶液代替双氧水
4
B.步骤Ⅱ,试剂X可以是CuO、CuCO、Cu(OH) 等物质
3 2
C.步骤Ⅲ,混合液中NaCO 的作用是及时除去反应过程中产生的 ,避免产生SO
2 3 2
D.步骤Ⅳ,为了防止CuCl被氧化,可用SO 水溶液洗涤
2
(3)步骤Ⅲ在如图所示装置中进行,仪器a的名称是 ;你认为恒压漏斗中所装试剂是
,理由是 。
(4)准确称取所制备的氯化亚铜样品0.50g,将其置于过量的FeCl 溶液中,待样品完全溶解后过滤,用
3
蒸馏水洗涤烧杯、玻璃棒及滤渣2~3次,将滤液及洗涤液一并转移到瓶中,加入指示剂2滴,立即用
0.20mol/L Ce(SO ) 标准溶液滴至终点,消耗Ce(SO) 标准溶液24.00mL,样品中CuCl的质量分数为
4 2 4 2
%(已知: ,且杂质不参与反应)。
21.(12分)某研究小组按下列路线合成降压药尼卡地平。已知:
(1)化合物C中含氧官能团的名称为硝基、 。
(2)写出B→C的化学方程式 。
(3)下列说法正确的是___________。
A.A→B的反应类型为取代反应
B.1molE与足量H 反应,最多可消耗2molH
2 2
C.1molF与足量NaOH溶液反应,最多可消耗3molNaOH
D.尼卡地平的分子式为C H NO
26 27 3 6
(4)化合物G的结构简式为 。
(5)设计以CHOH、CHCHO为原料合成E( )的合成路线(用流程图表示,无机试剂任
3 3
选) 。
(6)写出同时符合下列条件的化合物B的同分异构体的结构简式 。
①分子中含 (结构与苯相似),无其他环;
②能发生银镜反应;
③1H-NMR谱检测表明:分子中有3种不同化学环境的氢原子。