文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖北专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 O 16 S 32 Cu 64 Se 79 Te 128
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.制造大飞机是一项重要的国家大项目。下列与飞机制造有关的说法正确的是
A.制造飞机用的金属材料都是合金,合金的熔点比成分金属高,硬度大
B.飞机壳用铝合金而不用不锈钢是因为铝合金耐腐蚀性强
C.油管用硅橡胶比普通橡胶耐腐蚀
D.航空玻璃是由无机硅酸盐玻璃与有机透明材料复合而成的,硅酸盐玻璃、水玻璃、石英玻璃、有
机玻璃都含有相同成分
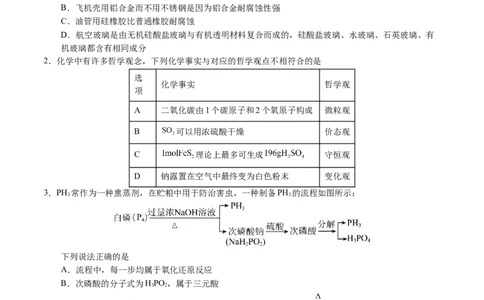
2.化学中有许多哲学观念,下列化学事实与对应的哲学观点不相符合的是
选
化学事实 哲学观
项
A 二氧化碳由1个碳原子和2个氧原子构成 微粒观
B 可以用浓硫酸干燥 价态观
C 理论上最多可生成 守恒观
D 钠露置在空气中最终变为白色粉末 变化观
3.PH 常作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备PH 的流程如图所示:
3 3
下列说法正确的是
A.流程中,每一步均属于氧化还原反应
B.次磷酸的分子式为HPO ,属于三元酸
3 2
C.白磷与浓NaOH溶液反应的化学方程式为:P+3NaOH(浓)+3H O PH ↑+3NaHPO
4 2 3 2 2
D.理论上,1 mol白磷可生产2.0 mol PH
3
4.抗生素克拉维酸的结构简式如图所示,下列关于克拉维酸的说法不正确的是
A.存在顺反异构和对映异构
B.含有5种官能团C.可形成分子内氢键和分子间氢键
D.最多可与3 molNaOH反应
5.下列叙述正确的是
A.HBrO的结构式为:H-Br-O
B.醋酸的电离方程式为:CHCOOH+H O CHCOO-+H O+
3 2 3 3
C.基态Si原子的价层电子的轨道表示式:
D.NH 的VSEPR模型:
3
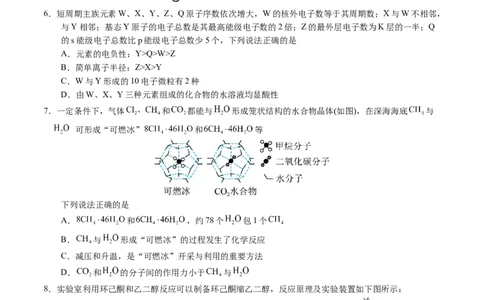
6.短周期主族元素W、X、Y、Z、Q原子序数依次增大,W的核外电子数等于其周期数;X与W不相邻,
与Y相邻;基态Y原子的电子总数是其最高能级电子数的2倍;Z的最外层电子数为K层的一半;Q
的s能级电子总数比p能级电子总数少5个,下列说法正确的是
A.元素的电负性:Y>Q>W>Z
B.简单离子半径:Z>X>Y
C.W与Y形成的10电子微粒有2种
D.由W、X、Y三种元素组成的化合物的水溶液均显酸性
7.一定条件下,气体 和 都能与 形成笼状结构的水合物晶体(如图),在深海海底 与
可形成“可燃冰” 和 等
下列说法正确的是
A. 和 ,约78个 包1个
B. 与 形成“可燃冰”的过程发生了化学反应
C.减压和升温,是“可燃冰”开采与利用的重要方法
D. 和 的分子间的作用力小于 与
8.实验室利用环己酮和乙二醇反应可以制备环己酮缩乙二醇,反应原理及实验装置如下图所示:
下列有关说法错误的是
A.冷凝管可改用球形冷凝管
B.当观察到分水器中苯层液面高于支管口时,必须打开旋塞B将水放出C.反应中加入苯的作用是作反应溶剂,同时与水形成共沸物便于蒸出水
D.当分水器中水层不再增多,说明制备实验已完成
9.下列关于物质结构的说法错误的是
A.邻羟基苯甲醛的沸点高于对羟基苯甲醛
B.HO的键角小于NH 的键角
2 3
C.通过X射线衍射可获得青蒿素的分子结构
D.O 分子为极性分子,分子中的共价键是极性键
3
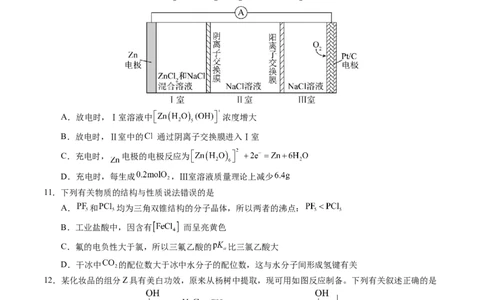
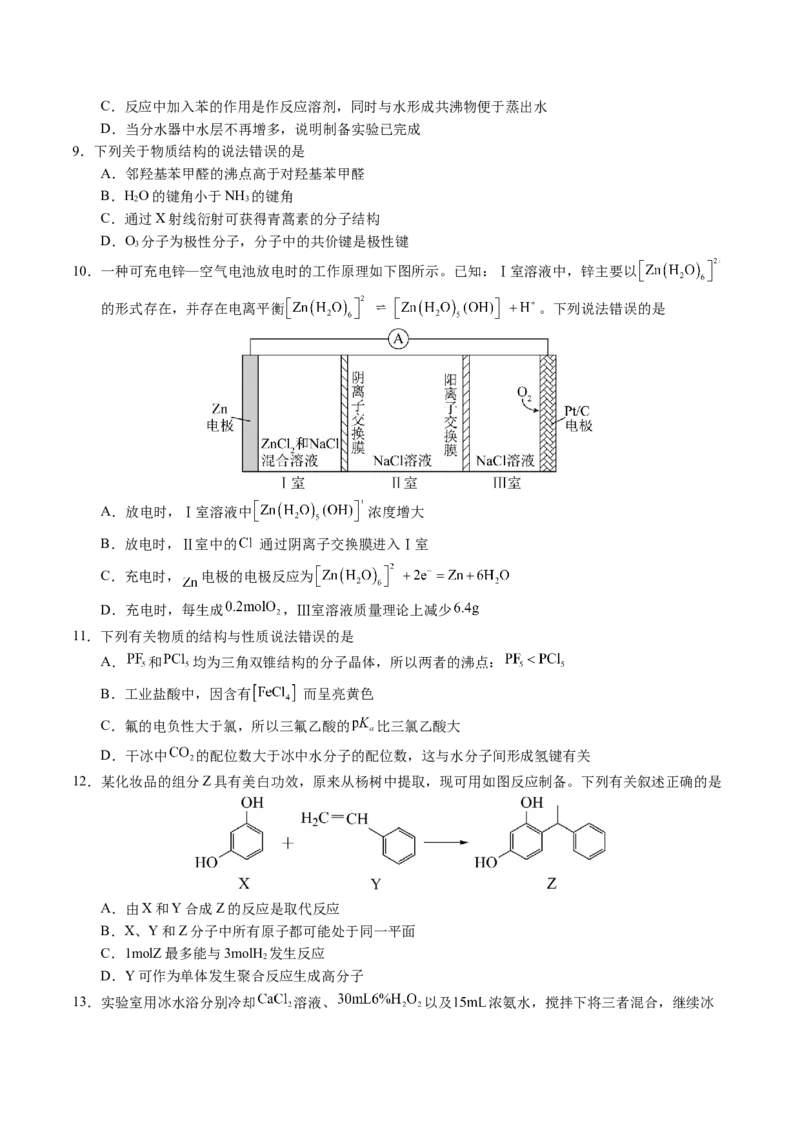
10.一种可充电锌—空气电池放电时的工作原理如下图所示。已知:Ⅰ室溶液中,锌主要以
的形式存在,并存在电离平衡 。下列说法错误的是
A.放电时,Ⅰ室溶液中 浓度增大
B.放电时,Ⅱ室中的 通过阴离子交换膜进入Ⅰ室
C.充电时, 电极的电极反应为
D.充电时,每生成 ,Ⅲ室溶液质量理论上减少
11.下列有关物质的结构与性质说法错误的是
A. 和 均为三角双锥结构的分子晶体,所以两者的沸点:
B.工业盐酸中,因含有 而呈亮黄色
C.氟的电负性大于氯,所以三氟乙酸的 比三氯乙酸大
D.干冰中 的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关
12.某化妆品的组分Z具有美白功效,原来从杨树中提取,现可用如图反应制备。下列有关叙述正确的是
A.由X和Y合成Z的反应是取代反应
B.X、Y和Z分子中所有原子都可能处于同一平面
C.1molZ最多能与3molH 发生反应
2
D.Y可作为单体发生聚合反应生成高分子
13.实验室用冰水浴分别冷却 溶液、 以及 浓氨水,搅拌下将三者混合,继续冰水浴 ,待溶液中不再有固体析出后,经“一系列操作”得到含 固体混合物。将所得固体置
于试管中加热,发生反应: ,利用下列装置可测量 的产率,下列有关说
法正确的是
A. 中阳离子和阴离子的个数比为
B.一系列操作中包括“蒸发结晶”
C.制备 的化学方程式为
D.反应结束后,J、K两管液面的差值即为氧气的体积
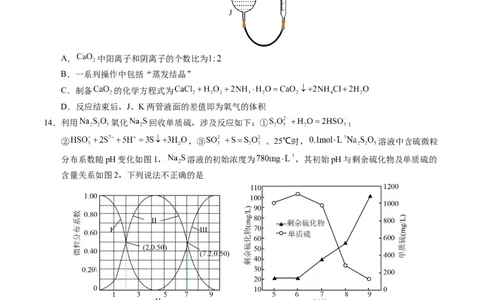
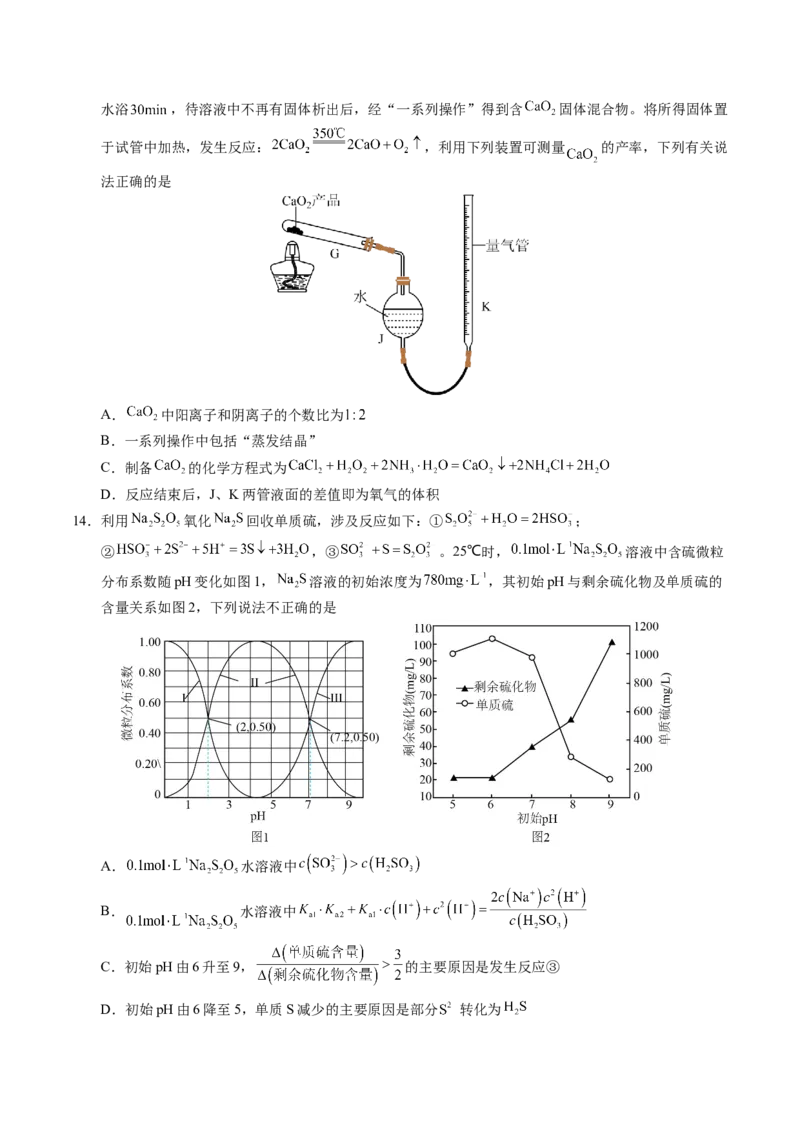
14.利用 氧化 回收单质硫,涉及反应如下:① ;
② ,③ 。25℃时, 溶液中含硫微粒
分布系数随pH变化如图1, 溶液的初始浓度为 ,其初始pH与剩余硫化物及单质硫的
含量关系如图2,下列说法不正确的是
A. 水溶液中
B. 水溶液中
C.初始pH由6升至9, 的主要原因是发生反应③
D.初始pH由6降至5,单质S减少的主要原因是部分 转化为15.钠硒电池是一类以单质硒或含硒化合物为正极、金属钠为负极的新型电池,具有能量密度大、导电率
高、成本低等优点。以 填充碳纳米管作为正极材料的一种钠硒电池工作原理如图所示,充放电
过程中正极材料立方晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个 晶胞中 个数为
B.放电时,正极的电极反应式为
C.充电时外电路中转移1mol电子,两极质量变化差为23g
D.在 晶胞结构中,晶胞参数为a pm,则其密度为
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
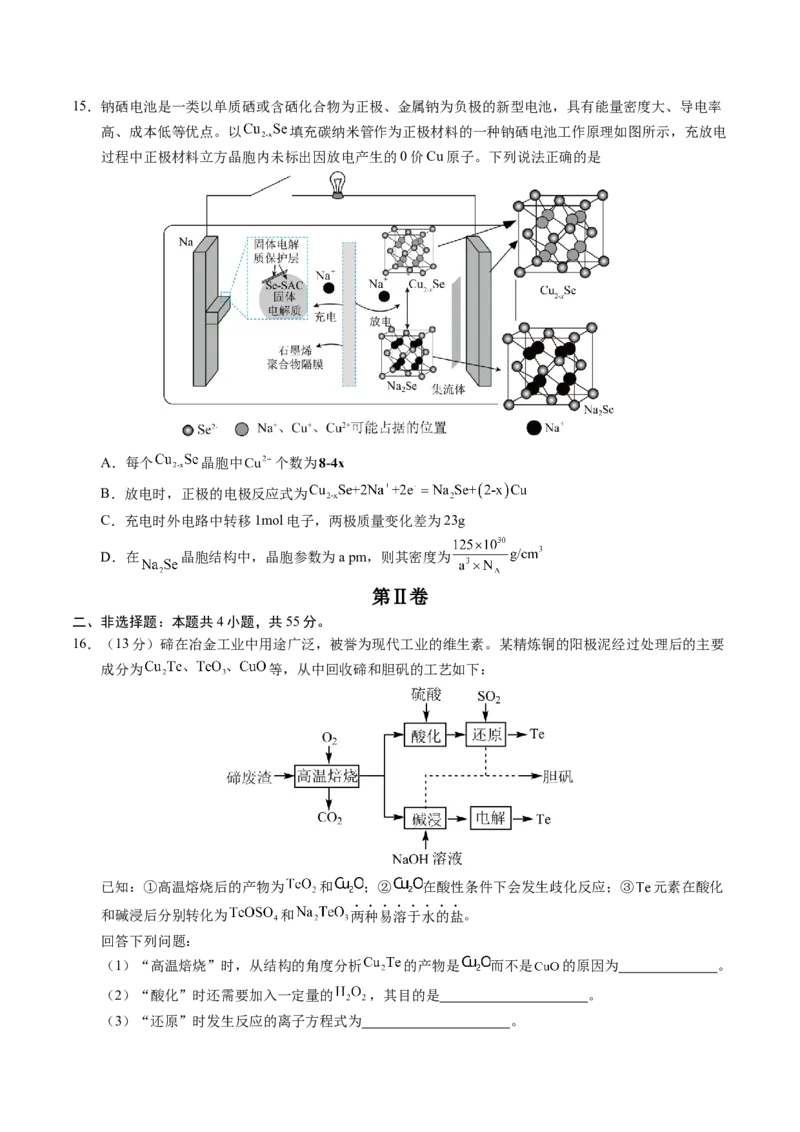
16.(13分)碲在冶金工业中用途广泛,被誉为现代工业的维生素。某精炼铜的阳极泥经过处理后的主要
成分为 等,从中回收碲和胆矾的工艺如下:
已知:①高温熔烧后的产物为 和 ;② 在酸性条件下会发生歧化反应;③ 元素在酸化
和碱浸后分别转化为 和 两种易溶于水的盐。
回答下列问题:
(1)“高温焙烧”时,从结构的角度分析 的产物是 而不是 的原因为 。
(2)“酸化”时还需要加入一定量的 ,其目的是 。
(3)“还原”时发生反应的离子方程式为 。(4)碱浸后铜元素的存在形式为 (写化学式)。
(5)“电解”制 的原理如图,其中N与电源的 (填“正极”或“负极”)相连:与M相
连的惰性电极上发生电极反应式为 。
(6)胆矾的结构如图所示。下列说法正确的是___________。
A.胆矾晶体中含有离子键、配位键、氢键等化学键
B.胆矾属于离子晶体
C. 的空间结构为正四面体形
D.电负性O>S,第一电离能
(7) 的立方晶胞结构如图。其中 的配位数为 ;已知晶胞边长为 , 为阿
伏伽德罗常数的值,则该晶体的密度为 (列出计算式即可)。
17.(13分)化合物X是一种香豆素衍生物,可以用作香料,其合成路线如下:
已知:①
② +
③④分子式: ; ;
(1)A所含官能团的名称是 。
(2)B生成C反应的化学方程式是 。
(3)碳酸乙烯酯 中碳原子杂化方式为 ,每个分子中含 个 键。
(4)题目中涉及的物质中互为同分异构体的是 (用结构简式表示)。
(5)X与足量NaOH溶液共热的化学方程式是 。
(6)E可以经多步反应合成F,请写出一条可能的合成路线(用结构简式表示有机物,用箭头表示转化
关系,箭头上注明试剂和反应条件) 。
18.(14分)胆矾(CuSO ·5H O)具有催吐、祛腐、解毒、治风痰壅塞等功效,易溶于水、甘油和甲醇,不
4 2
溶于乙醇。实验室用铜粉、稀硫酸和过氧化氢制取胆矾,装置如图:
实验步骤:
Ⅰ.按照上图装置组装好仪器,在三颈烧瓶中加入6.4g铜粉和稀硫酸(铜粉和硫酸的物质的量之比为
1∶1.3),再通过滴液漏斗加入一定量的HO 溶液,启动磁力搅拌器,维持温度30~40℃。当反应完全
2 2
后,静置3min。
Ⅱ.将上述溶液转移至仪器a中,蒸发浓缩,当加热至有晶膜出现时,即可冷却结晶,析出胆矾晶体,
经过一系列操作后,称量产品质量为23.2g。
(1)步骤I中采用的最佳加热方式为 ;反应温度不能超过40℃的原因是
;反应过程中有气泡产生且生成气泡的速率越来越快的原因是 。
(2)该实验制取硫酸铜的化学方程式为 。
(3)步骤Ⅱ中的仪器a是 (选填下列仪器字母标号),铜粉和硫酸物质的量比小于理论值的
原因是 。
(4)反应完全后通过注射器取样于点滴板上,加入4滴淀粉碘化钾检测液,混合溶液迅速变蓝,
(填“能”或“不能”)证明过氧化氢过量,原因是 。
(5)本实验的产率为 。
(6)本实验产品质量低于理论值的原因可能是 (任写一点)。
19.(15分)通过苯和环己烷之间的可逆反应可实现氢能的储存和释放,反应的热化学方程式为:(g)+3H(g) (g) H。
2 1
(1)氢化焓是指一种不饱和有机化合物变为完全饱和有机物时反应过程的焓变。已知:
⇌ △
CH=CH (g)+H(g) CH-CH(g) H=—136kJ•mol-1,据此估算苯的氢化焓△H=
2 2 2 3 3 2 1
kJ•mol-1,实测苯的氢化焓大得多,原因是 。
⇌ △
(2)保持总压为pkpa,测得反应达到平衡时w[w= ]随温度、苯氢比[
]变化的图像如图:
①图中曲线a、b、c中,苯氢比最大的为 ,判断的理由是 。
②a为苯氢比1:2时的变化曲线,曲线上M、N对应的苯的平衡体积分数:M N(填
“>”、“=”、“<”)。
③实际加氢工艺中常通入适量水蒸气。若按n(C H):n(H ):n(H O)=1:3:1混合反应气体,并控制
6 6 2 2
体系总压为35kPa,4.0s后测得HO的分压为10kPa,则0~4.0sC H 消耗的平均反应速率为
2 6 6
kPa•s-1。
(3)苯转化为环己烷存在副反应: (g) (g) H=16.8kJ•mol-1
①温度下,该反应平衡常数为K,则环己烷的平衡转化率为 。
△
⇌
②为了降低甲基环戊烷的百分含量,可以采取的措施是 、
(写出两种)。