文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷04
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.化学作为一门基础学科在生产、生活中起到了重要的作用。下列有关说法中正确的是
A.载人飞船上的太阳能电池板能实现将化学能直接转化为电能
B.铁制品表面镀上铜保护层,是利用牺牲阳极法
C.煤的干馏、气化与石油的分馏、裂化均属于化学变化
D.我国发射的“北斗组网卫星”所使用的碳纤维,是一种新型无机非金属材料
2.下列化学用语表示不正确的是
A.用电子式表示 形成:
B.基态锗原子的简化电子排布式:
C.氯仿的球棍模型:
D.聚氯乙烯的结构简式:
3. 为阿伏加德罗常数的值。下列说法中,正确的是
A.标准状况下,22.4L己烷的氢原子数约为
B.密闭容器中23g 与 的混合气体中氮原子数为
C.过氧化钠与水反应时,生成0.1mol 转移的电子数为
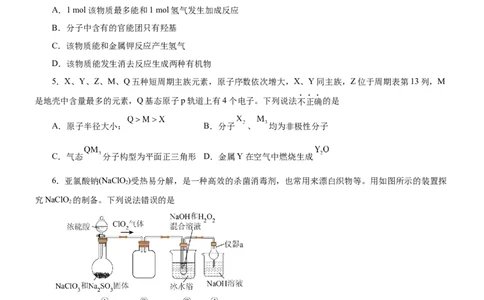
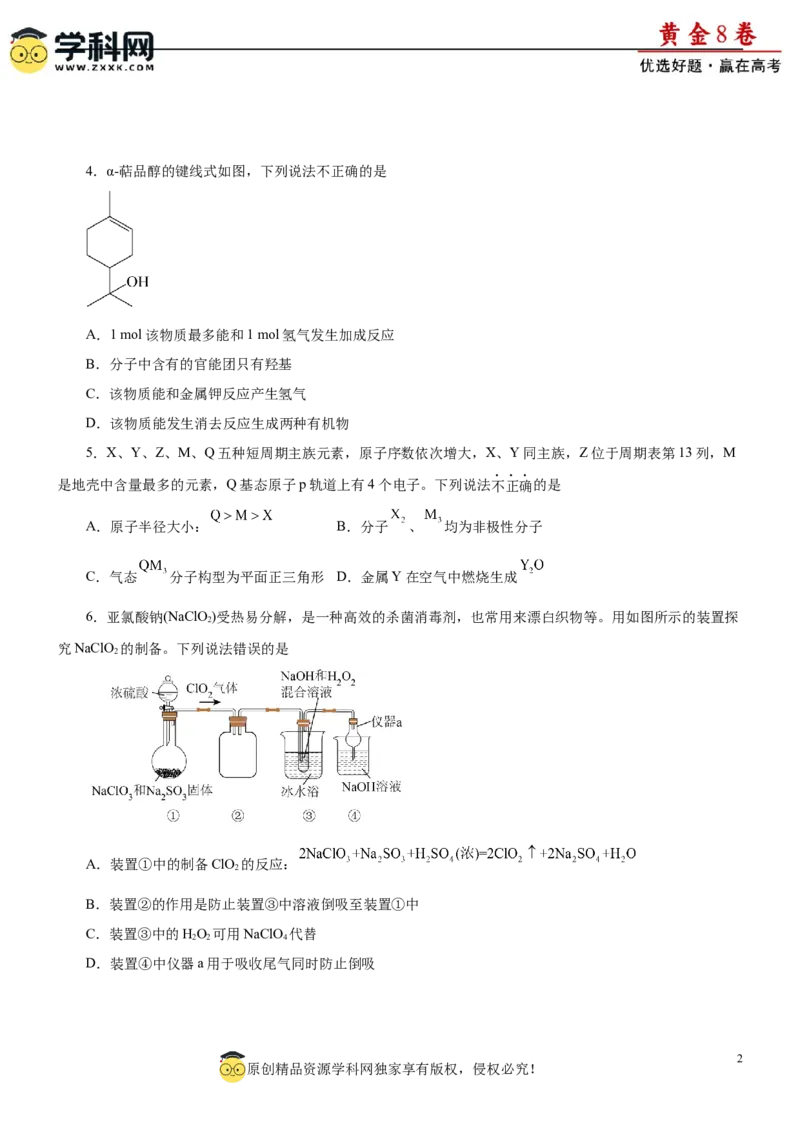
D.1L 的 溶液中 和 离子数之和为4.α-萜品醇的键线式如图,下列说法不正确的是
A.1 mol该物质最多能和1 mol氢气发生加成反应
B.分子中含有的官能团只有羟基
C.该物质能和金属钾反应产生氢气
D.该物质能发生消去反应生成两种有机物
5.X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大,X、Y同主族,Z位于周期表第13列,M
是地壳中含量最多的元素,Q基态原子p轨道上有4个电子。下列说法不正确的是
A.原子半径大小: B.分子 、 均为非极性分子
C.气态 分子构型为平面正三角形 D.金属Y在空气中燃烧生成
6.亚氯酸钠(NaClO)受热易分解,是一种高效的杀菌消毒剂,也常用来漂白织物等。用如图所示的装置探
2
究NaClO 的制备。下列说法错误的是
2
A.装置①中的制备ClO 的反应:
2
B.装置②的作用是防止装置③中溶液倒吸至装置①中
C.装置③中的HO 可用NaClO 代替
2 2 4
D.装置④中仪器a用于吸收尾气同时防止倒吸
2
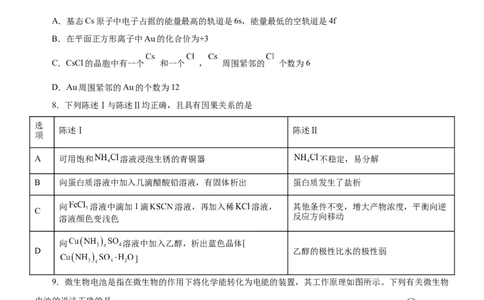
原创精品资源学科网独家享有版权,侵权必究!7.已知CsAuCl 的结构不能表示为 ,实际上可看作一种阳离子和两种阴离子按照个数比为2:
3
1:1形成的,这两种阴离子形状分别是直线形和平面正方形,已知Au的晶胞如图所示,下列有关说法不正确
的是
A.基态Cs原子中电子占据的能量最高的轨道是6s,能量最低的空轨道是4f
B.在平面正方形离子中Au的化合价为+3
C.CsCl的晶胞中有一个 和一个 , 周围紧邻的 个数为6
D.Au周围紧邻的Au的个数为12
8.下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A 可用饱和 溶液浸泡生锈的青铜器 不稳定,易分解
B 向蛋白质溶液中加入几滴醋酸铅溶液,有固体析出 蛋白质发生了盐析
向 溶液中滴加1滴 溶液,再加入稀 溶液, 其他条件不变,增大产物浓度,平衡向逆
C
反应方向移动
溶液颜色变浅色
向 溶液中加入乙醇,析出蓝色晶体[
D 乙醇的极性比水的极性弱
]
9.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物
电池的说法正确的是
A.该装置是原电池,b极是负极
B.该电池工作时,应选用质子交换膜
C.该电池工作时,电子从a经电流表A流向b,离子从右经交换
膜向左迁移
D.电极a反应:(C H O)-24e-+7H O=6CO↑+24H+
6 10 5 n 2 2
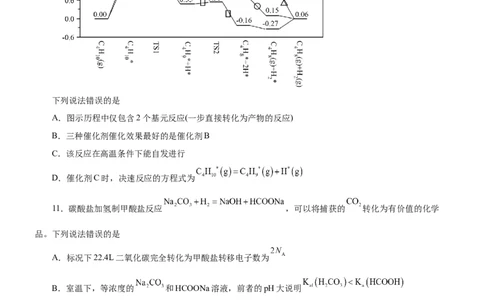
10.丁烯是石油化工基础原料,在石油化工烯烃原料中地位仅次于乙烯和丙烯,我国科学家研究不同催化
剂下丁烷脱氢制丁烯,催化反应历程如图所示[注:标*的物质表示吸附在催化剂上的中间产物, 表示1个 个 的能量)]:
下列说法错误的是
A.图示历程中仅包含2个基元反应(一步直接转化为产物的反应)
B.三种催化剂催化效果最好的是催化剂B
C.该反应在高温条件下能自发进行
D.催化剂C时,决速反应的方程式为
11.碳酸盐加氢制甲酸盐反应 ,可以将捕获的 转化为有价值的化学
品。下列说法错误的是
A.标况下22.4L二氧化碳完全转化为甲酸盐转移电子数为
B.室温下,等浓度的 和HCOONa溶液,前者的pH大说明
C.该工艺中NaOH可以循环利用
D.碳酸钠溶液中含碳元素微粒浓度顺序为
4
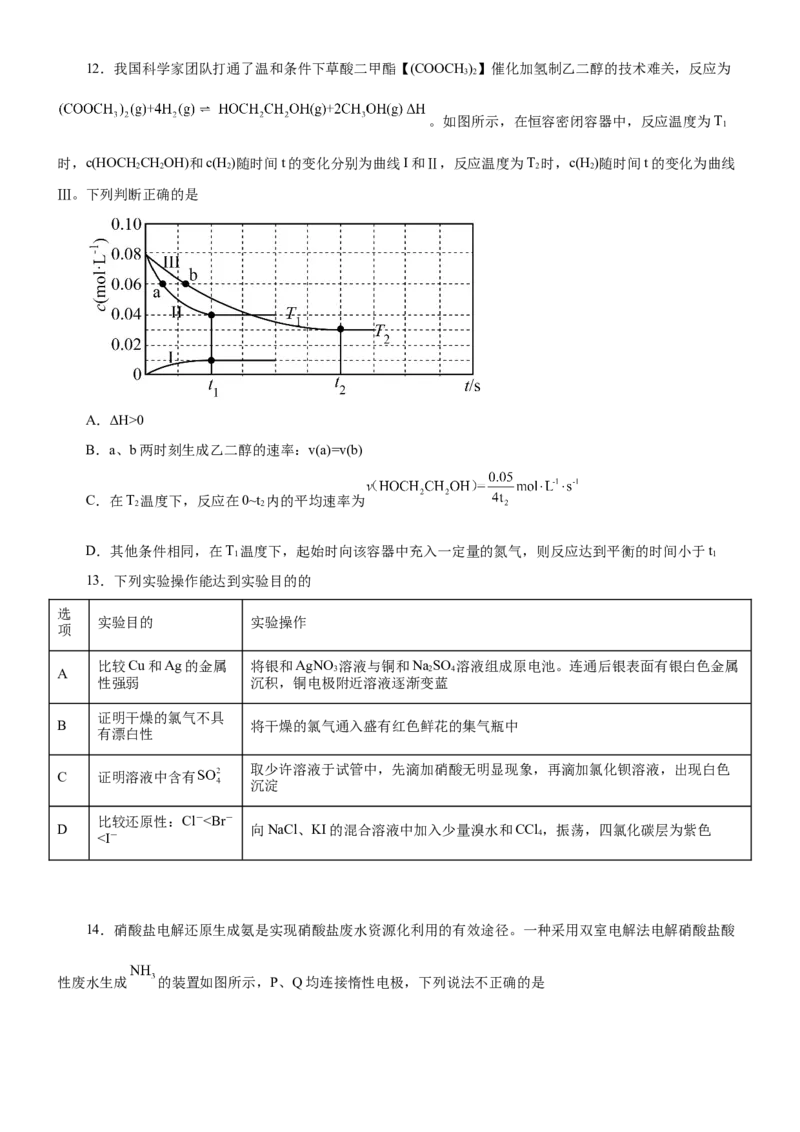
原创精品资源学科网独家享有版权,侵权必究!12.我国科学家团队打通了温和条件下草酸二甲酯【(COOCH )】催化加氢制乙二醇的技术难关,反应为
3 2
。如图所示,在恒容密闭容器中,反应温度为T
1
时,c(HOCH CHOH)和c(H)随时间t的变化分别为曲线I和Ⅱ,反应温度为T 时,c(H)随时间t的变化为曲线
2 2 2 2 2
Ⅲ。下列判断正确的是
A.ΔH>0
B.a、b两时刻生成乙二醇的速率:v(a)=v(b)
C.在T 温度下,反应在0~t 内的平均速率为
2 2
D.其他条件相同,在T 温度下,起始时向该容器中充入一定量的氮气,则反应达到平衡的时间小于t
1 1
13.下列实验操作能达到实验目的的
选
实验目的 实验操作
项
比较Cu和Ag的金属 将银和AgNO 溶液与铜和NaSO 溶液组成原电池。连通后银表面有银白色金属
A 3 2 4
性强弱 沉积,铜电极附近溶液逐渐变蓝
证明干燥的氯气不具
B 将干燥的氯气通入盛有红色鲜花的集气瓶中
有漂白性
取少许溶液于试管中,先滴加硝酸无明显现象,再滴加氯化钡溶液,出现白色
C 证明溶液中含有
沉淀
比较还原性:Cl-”或“<”)
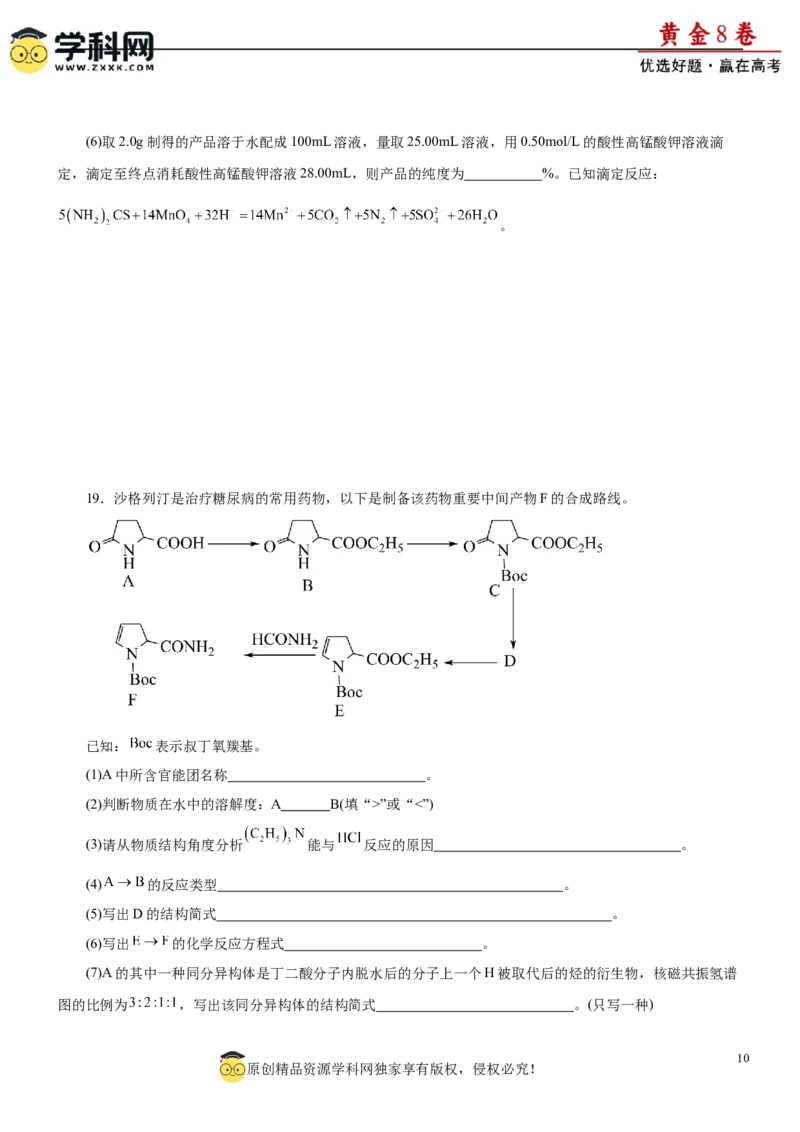
(3)请从物质结构角度分析 能与 反应的原因 。
(4) 的反应类型 。
(5)写出D的结构简式 。
(6)写出 的化学反应方程式 。
(7)A的其中一种同分异构体是丁二酸分子内脱水后的分子上一个H被取代后的烃的衍生物,核磁共振氢谱
图的比例为 ,写出该同分异构体的结构简式 。(只写一种)
10
原创精品资源学科网独家享有版权,侵权必究!